Page 1

InflateFX™ Fracture M708348B168 Rev. B
Management Inflatable Bone
Tamp (Sizes 10/3 and 15/3)
Important Information on the InateFX™ Fracture Management Inatable Bone Tamp
Important Information sur le dispositif gonflable de plombage osseux pour gestion des fractures InflateFX™
Información Importante Sobre el impactor óseo hinchable para el tratamiento de fracturas InflateFX™
Wichtige Informationen Zum InflateFX™ insufflierbaren Frakturmanagement-Knochenstopfen
Importanti Informazioni sull’impattatore osseo gonfiabile per la gestione delle fratture InflateFX™
Belangrijke Informatie Over de InflateFX™ vulbare bot-stopper voor fractuurmanagement
Vigtige Oplysninger Om InflateFX™ inflaterbart knogleindlæg til frakturbehandling
Viktig Information Om InflateFX™ Frakturbehandling med uppblåsbar benballong
Viktig Informasjon Om InflateFX™ inflaterbar bentamper for frakturbehandling
ΣΗΜΑΝΤΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ πληρούενο βύσα οστών για την αντιετώπιση καταγάτων InflateFX™
INFORMAŢII IMPORTANTE PRIVIND dispozitivul de plombare osoasă pentru gestionarea fracturilor InflateFX™
2013-06-19
Medtronic Australasia Pty Ltd Medtronic Sofamor Danek USA, Inc. Medtronic B.V.
97 Waterloo Rd 1800 Pyramid Place Earl Bakkenstraat 10
North Ryde, NSW 2113 Memphis, TN 38132 6422 PJ Heerlen
Australia Telephone 800 933 2635 (In U.S.A.) The Netherlands
901 396 3133 (Outside U.S.A.) Tel: + 31 45 566 80 00
Fax 901 396 0356
ENGLISH
INDICATIONS FOR USE
The InflateFX™ Fracture Management Inflatable Bone Tamp (IBT) is intended to be used as a conventional bone tamp for the reduction of fractures and/or creation of a void in cancellous
bone in the hand, tibia, radius, and calcaneus.
DEVICE DESCRIPTION
See Figure 1.
1. Cap
2. Stylet
3. Stylet Port
4. Inflation Port
5. Color Coded Band
6. Exit Marker Band
7. Insertion Sleeve
8. Radiopaque Markers
9. Inflatable Component
• The Inflatable Component of the IBT is designed to compress cancellous bone and/or move cortical bone as it inflates. The Inflatable Component of the IBT is near the distal tip of
the device as shown in Figure 1.
• The shaft contains two non-communicating lumens. The outer lumen is used for IBT inflation, and the central lumen contains a removable stiffening Stylet for IBT insertion.
• The proximal end of the shaft has a side-arm adapter. The Inflation Port of the adapter is contiguous with the outer lumen. The Stylet Port is contiguous with the inner lumen and
contains the stiffening Stylet. The Stylet has a Cap at its proximal end for optional removal.
• The Color Coded Band, located just distal to the side-arm adapter, indicates the balloon size (i.e., a yellow band for 10/3 size, and a black band for 15/3 size).
• The Exit Marker Band located on the outer lumen is used during IBT insertion.
• Radiopaque Markers located at the distal and proximal end of the deflated working surface allow fluoroscopic visualization of the deflated IBT during positioning.
CONTRAINDICATIONS
• Bleeding disorder or treatment that increases the chance of excessive bleeding.
• In the presence of active or incompletely treated infection at the site where the bone void filler is to be applied.
• Any known severe allergy to contrast material and bone void filler.
• If the patient has a confirmed pregnancy.
WARNINGS
• Breakage of the device may require intervention or retrieval.
• Do not use this product after the expiration (use-by) date printed on the package. The device may not be safe or effective beyond its expiration (use-by) date.
• The Inflatable Component may fail due to sharp bony spicules or surgical instruments.
• Inflating the IBT beyond the maximum inflation volume may cause the balloon to rupture before reaching the maximum inflation pressure.
• Inflating the IBT beyond the maximum inflation pressure may cause the balloon to rupture before reaching the maximum inflation volume.
• Never use air or gaseous materials to inflate the balloon.
PRECAUTIONS
• The Inflatable Bone Tamp is a single use device intended to contact body tissues. Do not reuse, reprocess, or resterilize. Reusing these devices carries the risk of contamination and
may cause patient infection or cross-infection, regardless of the cleaning and resterilization methods. There is also an increased risk of the deterioration of the device performance
due to the reprocessing steps, which may lead to patient injury or death.
• It is important to read the Instructions For Use and these precautions carefully prior to device operation.
• Use the IBT prior to the use-by date noted on the package.
• Do not use if package is opened or damaged because product integrity, including sterility, may be compromised.
• Do not use damaged products. Before use, inspect the IBT and packaging to verify that no damage has occurred.
• Prior to use, the IBT should be examined to verify functionality and ensure that its size is suitable for the specific procedure for which it is to be used.
• Do not use this product if you have not been properly trained. The IBT should only be used by physicians who are trained in the techniques of bone tamp use. Physicians using the
devices should be familiar with the physiology and pathology of the selected anatomy.
• The IBT should be manipulated only while under fluoroscopic observation with radiographic equipment that provides high quality images.
• The IBT should only be inflated using an Inflation Syringe with a minimum of 14ml volume capacity.
• Only inflate the IBT with liquid contrast medium: a 60% solution is recommended. Follow manufacturer’s instructions for contrast medium indications, usage, and cautions.
• Do not use air or other gas to inflate the IBT.
• The inflation characteristics of the IBT are altered by inflation inside bone.
• Reconditioning, refurbishing, repair, modification, or resterilization of the device to enable further use is expressly prohibited.
• Any surgery has risks; however, using the balloon in the treatment of these fractures does not increase these risks from a clinical standpoint compared to the traditional methods
of elevating the depressed bone fragments. These risks include:
o Failure to properly reduce the fracture fragments.
o Delayed union and non-union.
o Infection.
o Neurovascular injury or compartment syndrome leading to loss of function or amputation.
NOTE: A Kyphon® branded inflation syringe provides superior volume control compared to other inflating systems, such as a standard syringe, and is required for inflation of the IBT. Follow
the manufacturer’s Instructions for Use of a Kyphon® branded inflation syringe. The Kyphon® Locking Syringe is packaged with a Kyphon® branded inflation syringe.
ADVERSE EVENTS
Adverse events potentially associated with use of the IBT include serious events, which although rare, can be fatal.
Adverse events include:
• Embolism of fat, thrombus or other materials resulting in symptomatic pulmonary embolism or other clinical sequelae.
• Rupture with fragmentation of the inflatable portion of the IBT resulting in retention of a fragment within the affected region.
• Rupture of the IBT causing contrast medium exposure, possibly resulting in an allergic reaction or anaphylaxis.
• Deep or superficial wound infection.
• Bleeding or hematoma.
DIRECTIONS FOR USE
CAUTION: Follow the manufacturer’s Instructions for Use of a Kyphon® branded inflation syringe.
CAUTION: Contrast media may have different viscosity and precipitation levels that may cause slower inflation and deflation times. For this reason, the use of 60% contrast medium
is recommended.
1. Twist Cap on Stylet Port to tighten Stylet on IBT. Push plunger all the way into the Kyphon® Locking Syringe. Attach the Kyphon® Locking Syringe to Inflation Port on IBT.
2. Pull the Kyphon® Locking Syringe plunger back. Turn plunger to lock it in position on the last slot in syringe.
3. Detach the Kyphon® Locking Syringe from IBT.
4. Attach connecting port on Kyphon® branded inflation syringe tubing to Inflation Port on IBT. The system is now prepared and ready to use.
USE OF THE IBT
1. Select IBT size based on site and treatment goal. Figure 1 and Table 1 define the inflated diameter (D) and inflated length (L) of the IBTs in 37°C water at inflation volume increments
to the maximum inflation volume.
2. These dimensions may vary during product use due to local variation in bone structure.
Table 1 - IBT Inflated Dimensions (in 37°C water)
Model Number E103A Inflated Dimensions
Size 10/3 Volume Avg Diameter (D1, D2) Length (L)
Max. Inflation Volume 4ml 2ml 12.9mm 14.7mm
Max. Inflation Pressure 400psi (27atm) 4ml 17.2mm 19.1mm
Model Number E153A Inflated Dimensions
Size 15/3 Volume Avg Diameter (D1, D2) Length (L)
Max. Inflation Volume 4ml 2ml 12.1mm 17.4mm
Max. Inflation Pressure 400psi (27 atm) 4ml 16mm 22.1mm
IBT INSERTION
1. An access channel is required for IBT placement.
2. Follow the Instructions for Use for the chosen bone access tools to create an access channel into the bone.
3. Remove Insertion Sleeve prior to use.
NOTE: The distal tip of the deflated IBT has reached the distal end of the cannula when the Exit Marker on the outer lumen of the IBT enters the proximal end of the cannula.
4. Place the deflated IBT into the access channel and position it under image guidance using the Radiopaque Markers. A gentle twisting motion with the forward push can aid insertion.
5. While holding the IBT in place, inflate to 44psi (3atm) to secure IBT in position. Remove the Stylet, if desired.
IBT INFLATION
1. Inflate the IBT under continuous image guidance. Use the lateral view to monitor distance from the anterior and lateral cortex. Use the AP view to monitor the lateral cortices.
2. If continuous imaging is not used, increase the volume in small increments (0.25 – 0.5ml). Assess tamp position in lateral and AP views before proceeding to further volume increase.
3. Stop when treatment goal is achieved or any part of the IBT inflated length contacts cortical bone or maximum inflation volume and/or maximum inflation pressure is attained
(See Table 1).
IBT REMOVAL
CAUTION: Do not withdraw the IBT unless the Inflatable Component is fully deflated. Never withdraw the IBT against resistance. Determine the cause of resistance under fluoroscopy
and take the necessary remedial actions.
Use a Kyphon® branded inflation syringe to evacuate the contrast medium from the IBT until the balloon is completely deflated. Remove the IBT from the bone through the cannula
with a gentle twisting motion.
• If there is resistance, connect a 30ml syringe to the Inflation Port. Pull the syringe plunger back to the “30ml” mark to create a vacuum. Resume the IBT removal.
• Confirm entry of the inflatable portion of the IBT into the cannula. If the Inflatable Component does not move into the cannula, advance the cannula over the IBT to the proximal
Radiopaque Marker. Following cannula advancement, withdraw the IBT through the cannula. If resistance is noted, remove IBT and cannula simultaneously.
STERILIZATION
Sterilized with irradiation.
HOW SUPPLIED
The IBTs are supplied sterile in a peel-open package. In the event of damage to the sterile packaging, do not use and notify the manufacturer.
MATERIALS NOT SUPPLIED
• Kyphon® branded inflation syringe with Kyphon® Locking Syringe
• Contrast Medium (60%)
• Small Bowl
NOTE: Kyphon® branded inflation syringe with Kyphon® Locking Syringe is available from Medtronic.
STORAGE
IBTs should be stored in their original shipping materials. Proper care should be taken to ensure IBTs will not be damaged. Store in a cool dry place.
LIMITATION OF LIABILITY
MEDTRONIC WILL NOT BE RESPONSIBLE FOR ANY DIRECT, INDIRECT, INCIDENTAL, CONSEQUENTIAL, OR EXEMPLARY DAMAGES RESULTING FROM REUSE OF THE InflateFX™ FRACTURE
MANAGEMENT INFLATABLE BONE TAMPS.
IN NO EVENT SHALL MEDTRONIC BE LIABLE FOR ANY DIRECT, INDIRECT, INCIDENTAL, CONSEQUENTIAL, OR EXEMPLARY DAMAGES ARISING OUT OF OR IN CONNECTION WITH THE InflateFX™
FRACTURE MANAGEMENT INFLATABLE BONE TAMPS, BASED UPON BREACH OF CONTRACT (INCLUDING BREACH OF WARRANTY).
REQUESTS FOR INFORMATION
For further information, contact Customer Service.
© 2013 Medtronic Sofamor Danek USA, Inc. All rights reserved.
FraNçaIS
INDICATIONS D’USAGE
Le dispositif gonflable de plombage osseux pour gestion des fractures (Inflatable Bone Tamp, IBT) InflateFX™ est destiné à être utilisé comme un plombage osseux classique pour la
réduction de fractures et/ou la création d’une cavité dans l’os spongieux de la main, du tibia, du radius et du calcanéus.
DESCRIPTION DES DISPOSITIFS
Voir la figure 1.
1. Capuchon
2. Stylet
3. Raccord du stylet
4. Raccord de gonflage
5. Bague codée couleur
6. Bague-repère de sortie
7. Manchon d’insertion
8. Marqueurs radio-opaques
9. Composant gonflable
• Le composant gonflable du dispositif IBT est conçu en vue de comprimer l’os spongieux et/ou de déplacer l’os cortical pendant le gonflage du dispositif. Le composant gonflable du
dispositif IBT se trouve près de son extrémité distale, ainsi qu’il est illustré à la Figure 1.
• La tige du dispositif renferme deux lumières non communicantes. La lumière externe est utilisée pour gonfler le dispositif IBT et la lumière centrale contient un stylet de support
amovible servant à insérer le dispositif IBT.
• L’extrémité proximale de la tige est équipée d’un adaptateur latéral. Le raccord de gonflage de l’adaptateur est contigu à la lumière externe. Le raccord du stylet est contigu à la
lumière interne et contient le stylet de support. Le stylet est équipé d’un capuchon à son extrémité proximale pour un retrait éventuel.
• La bague codée couleur, située juste en aval de l’adaptateur latéral, indique la taille du ballonnet (une bague jaune pour la taille 10/3 et une bague noire pour la taille 15/3).
• La bague-repère de sortie, se trouvant sur la lumière externe, est utilisée lors de l’insertion du dispositif IBT.
• Des marqueurs radio-opaques, se trouvant aux extrémités distale et proximale de la surface de travail dégonflée, permettent de visualiser le dispositif IBT dégonflé sous radioscopie
au cours de sa mise en place.
CONTREINDICATIONS
• Trouble hémorragique ou traitement augmentant le risque d’un saignement excessif.
• Présence d’une infection active ou partiellement traitée au niveau du site d’application du produit de comblement osseux.
• Toute allergie sévère connue au produit de contraste ou le produit de comblement osseux.
• Grossesse confirmée chez la patiente.
AVERTISSEMENTS
• La rupture du dispositif peut nécessiter son retrait ou une intervention chirurgicale.
• Ne pas utiliser ce produit après la date de péremption (Utiliser avant le) indiquée sur l’emballage. La sécurité ou l’efficacité du produit risque d’être compromise après la date de
péremption (Utiliser avant le).
• Le composant gonflable risque de ne pas fonctionner correctement en raison d’un contact avec des esquilles ou des instruments chirurgicaux tranchants.
• Un gonflage du dispositif IBT au-delà du volume de gonflage maximal risque de provoquer la rupture du ballonnet avant que la pression de gonflage maximale ne soit atteinte.
• Un gonflage du dispositif IBT au-delà de la pression de gonflage maximale risque de provoquer la rupture du ballonnet avant que le volume de gonflage maximal ne soit atteinte.
• Ne jamais utiliser d’air ou de produits gazeux pour gonfler le ballonnet.
PRÉCAUTIONS
• Le dispositif gonflable de plombage osseux est un dispositif à usage unique prévu pour être en contact avec les tissus corporels. Ne pas réutiliser, retraiter ni restériliser. La réutilisation
de ces dispositifs pose un risque de contamination et peut provoquer une infection ou une infection croisée chez le patient, quelles que soient les méthodes de nettoyage et de
restérilisation utilisées. Il existe également une augmentation du risque de détérioration des performances du dispositif en raison des étapes de retraitements, ce qui pourrait
causer des lésions ou le décès du patient.
• Avant d’utiliser le dispositif, il est important de lire attentivement ce mode d’emploi et les précautions.
• Utiliser le dispositif IBT avant la date de péremption indiquée sur l’emballage.
• Ne pas utiliser si l’emballage est ouvert ou endommagé car l’intégrité du produit, notamment sa stérilité, risque d’être compromise.
• Ne pas utiliser de produits endommagés. Avant de l’utiliser, examiner le dispositif IBT et son emballage pour vérifier qu’ils n’ont pas été endommagés.
• Avant de l’utiliser, examiner le dispositif IBT pour vérifier son bon fonctionnement et s’assurer qu’il a la taille adéquate pour la procédure spécifique prévue.
• N’utilisez pas ce produit si vous n’avez pas reçu la formation adéquate. Le dispositif IBT ne doit être utilisé que par des médecins ayant reçu la formation nécessaire à l’utilisation des
dispositifs de plombage osseux. Les médecins utilisant ces dispositifs doivent avoir de bonnes connaissances de la physiologie et de la pathologie du site anatomique sélectionné.
• Le dispositif IBT ne doit être manipulé que sous contrôle radioscopique avec un équipement radiographique donnant des images de haute qualité.
• Le dispositif IBT ne doit être gonflé qu’à l’aide d’une seringue de gonflage pouvant contenir un volume minimum de 14 ml.
• Ne gonfler le dispositif IBT qu’avec un produit de contraste liquide. il est recommandé d’utiliser une solution à 60 %. Suivre les instructions du fabricant concernant les indications,
l’utilisation et les mises en garde relatives au produit de contraste.
• Ne jamais utiliser d’air ou de produits gazeux pour gonfler le dispositif IBT.
• Les caractéristiques de gonflage du dispositif IBT sont différentes lorsque le dispositif est gonflé à l’intérieur de l’os.
• Il est expressément interdit de procéder au reconditionnement, à la remise à neuf, à des réparations, à une modification ou à la restérilisation du dispositif en vue de prolonger son utilisation.
• Toute intervention chirurgicale comporte des risques ; toutefois, d’un point de vue clinique, l’utilisation du ballonnet lors du traitement de ces fractures n’accroît pas ces risques par
rapport aux techniques traditionnelles d’élévation de fragments osseux enfoncés. Ces risques incluent :
o Réduction insuffisante des fragments de fracture.
o Fusion retardée ou absence de fusion.
o Infection.
o Blessure neurovasculaire ou syndrome des loges provoquant une perte de fusion ou amputation.
REMARQUE : La seringue de gonflage Kyphon® offre un contrôle du volume supérieur à celui d’autres systèmes de gonflage, comme une seringue normale, et est nécessaire pour
gonfler le dispositif IBT. Suivre les instructions du fabricant en ce qui concerne l’utilisation de la seringue de gonflage Kyphon®. La seringue à verrouillage Kyphon® est conditionnée
avec une seringue de gonflage de marque Kyphon®.
ÉVÉNEMENTS INDÉSIRABLES
Les événements indésirables pouvant accompagner l’utilisation du dispositif IBT incluent des événements graves qui, bien qu’ils soient rares, peuvent fatals.
Les événements indésirables incluent :
• Embolie graisseuse, de thrombus ou d’autre matériau produisant une embolie pulmonaire symptomatique ou d’autres séquelles cliniques.
• Rupture avec fragmentation de la partie gonflable du dispositif IBT, conduisant à la rétention d’un fragment au sein de la région affectée.
• Rupture du dispositif IBT entraînant l’exposition du produit de contraste, produisant potentiellement une réaction allergique ou anaphylactique.
• Infection profonde ou superficielle de plaie.
• Saignement ou hématome.
DIRECTIVES D’UTILISATION
ATTENTION : Suivre les instructions du fabricant en ce qui concerne l’utilisation de la seringue de gonflage Kyphon®.
ATTENTION : Les produits de contraste peuvent avoir des viscosités et des niveaux de précipitation différents, ce qui peut engendrer des temps de gonflage et de dégonflage plus lents.
Pour cette raison, il est recommandé d’utiliser un produit de contraste à 60 %.
1. Visser le capuchon du raccord du stylet pour fixer le stylet sur le dispositif IBT. Enfoncer le piston complètement à l’intérieur de la seringue à verrouillage Kyphon®. Connecter la
seringue à verrouillage Kyphon® au raccord de gonflage sur le dispositif IBT.
2. Tirer sur le piston de la seringue à verrouillage Kyphon®. Tourner le piston pour le bloquer en position sur la dernière encoche de la seringue.
3. Déconnecter la seringue à verrouillage Kyphon® du dispositif IBT.
4. Connecter le raccord de connexion sur la tubulure de la seringue de gonflage Kyphon® ™ au raccord de gonflage sur le dispositif IBT. Le système est maintenant préparé et prêt à l’usage.
UTILISATION DU DISPOSITIF IBT
1. Sélectionner la taille du dispositif IBT en fonction du site et de l’objectif thérapeutique. La figure 1 et le tableau 1 indiquent le diamètre gonflé (D) et la longueur gonflée (L) des
dispositifs IBT dans de l’eau à 37 °C et des incréments de volume de gonflage jusqu’au volume de gonflage maximal.
2. Ces dimensions peuvent varier au cours de l’utilisation du produit en fonction des différences locales de structure osseuse.
Tableau 1 – Dimensions du dispositif IBT gonflé (dans de l’eau à 37 °C)
Numéro de modèle E103A Dimensions du dispositif gonflé
Taille 10/3 Volume Diamètre moyen (D1, D2) Longueur (L)
Volume maxi.de gonflage 4 ml 2 ml 12,9 mm 14,7 mm
Pression maxi. de gonflage 27 atm 4 ml 17,2 mm 19,1 mm
Numéro de modèle E153A Dimensions du dispositif gonflé
Taille 15/3 Volume Diamètre moyen (D1, D2) Longueur (L)
Volume maxi.de gonflage 4 ml 2 ml 12,1 mm 17,4 mm
Pression maxi. de gonflage 27 atm 4 ml 16 mm 22,1 mm
Tärkeää Tietoa täytettävästä InflateFX™-luuntiivistimestä murtumien hoitoon
Ões Importantes Sobre o calcador de osso insuflável InflateFX™ para tratamento de fracturas
Informaç
DŮLEŽITÉ INFORMACE O nafukovací kostní ucpávce InflateFX™ pro ošetření fraktur
Oluline Teave luumurru ravi täidetava luutampooni InflateFX™ kohta
Fontos Információ Az InflateFX™ töréskezelő felfújható csonttömörítő eszközről
īga Informācija Par InflateFX™ piepildāmo kaulu spiedi lūzumu ārstēšanai
Svar
Svarbi Informacija Apie slėginį kaulo užpildymo įtaisą „InflateFX™“, skirtą lūžiams gydyti
WAŻNA INFORMACJA O napełnianym balonie ortopedycznym do leczenia złamań InflateFX™
DÔLEŽITÉ INFORMÁCIE o nafukovacej kostnej ubíjačke InflateFX™ na liečbu zlomenín
InflateFX™ Kırık Yönetimi Şişirilebilir Kemik Tamponu Hakkinda Önemli Bilgi
POMEMBNE INFORMACIJE O polnljivem kostnem tamponu za oskrbo zlomov InflateFX™
AUSTRALIAN SPONSOR:
Important Information on the InflateFX™ Fracture
Management Inflatable Bone Tamp (Sizes 10/3 and 15/3)
CAUTION: Federal (USA) law restricts this device to sale by or on the order of a physician.
Important Information sur le dispositif gonflable de plombage
osseux pour gestion des fractures InflateFX™ (Tailles 10/3 et 15/3)
ATTENTION : La législation fédérale des États-Unis n’autorise la vente de ce dispositif que par un médecin ou sur prescription médicale.
0123
EC REP
INSERTION DU DISPOSITIF IBT
1. Il est nécessaire d’établir un canal d’accès pour mettre le dispositif IBT en place.
2. Suivre le mode d’emploi des instruments d’accès à l’os sélectionnés pour établir le canal d’accès dans l’os.
3. Retirer le manchon d’insertion avant usage.
REMARQUE : L’extrémité distale du dispositif IBT dégonflé a atteint l’extrémité distale de la canule lorsque le repère de sortie se trouvant sur la lumière externe du dispositif IBT pénètre
dans l’extrémité proximale de la canule.
4. Placer le dispositif IBT dégonflé dans le canal d’accès et ajuster sa position sous contrôle par imagerie à l’aide des marqueurs radio-opaques. On peut faire pivoter doucement le
dispositif tout en le poussant vers l’avant afin de faciliter son insertion.
5. Tout en maintenant le dispositif IBT, le fixer en place en le gonflant à 0,3 MPa (3 atm). Retirer éventuellement le stylet.
GONFLAGE DU DISPOSITIF IBT
1. Gonfler le dispositif IBT sous contrôle continu par imagerie. Utiliser la vue latérale pour vérifier la distance par rapport au cortex antérieur et latéral. Utiliser la vue AP (antéropostérieure) pour surveiller les corticales latérales.
2. Si l’imagerie en continu n’est pas utilisée, augmenter le volume par petits incréments (0,25 à 0,5 ml). Évaluer la position du dispositif en vues latérale et AP avant de continuer à
augmenter le volume.
3. Arrêter lorsque l’objectif thérapeutique est atteint ou lorsqu’une partie de la longueur du dispositif IBT gonflé entre en contact avec l’os cortical ou lorsque le volume et/ou la pression
maximum de gonflage ont été atteints (voir le Tableau 1).
RETRAIT DU DISPOSITIF IBT
ATTENTION : Ne pas retirer le dispositif IBT sans dégonfler complètement son composant gonflable. Ne jamais retirer le dispositif IBT en cas de résistance. Déterminer la cause de la
résistance sous observation radioscopique et remédier à la situation.
Utiliser une seringue de gonflage de marque Kyphon® pour retirer le produit de contraste du dispositif IBT jusqu’à ce que le ballonnet soit complètement dégonflé. Retirer le dispositif
IBT de l’os par la canule en le faisant lentement pivoter sur son axe.
• En cas de résistance, connecter une seringue de 30 ml au raccord de gonflage. Tirer sur le piston de la seringue jusqu’au repère « 30 ml » de façon à créer un vide. Essayer à nouveau
de retirer le dispositif IBT.
• Vérifier l’entrée de la partie gonflable du dispositif IBT dans la canule. Si le composant gonflable n’entre pas dans la canule, faire avancer la canule sur le dispositif IBT jusqu’au niveau
du marqueur radio-opaque proximal. Une fois la canule avancée, retirer le dispositif IBT par la canule. En cas de résistance, retirer simultanément le dispositif IBT et la canule.
STÉRILISATION
Stérilisé par rayonnement.
PRÉSENTATION
Les systèmes IBT sont fournis stériles dans un emballage pelable. Si l’emballage stérile est endommagé, ne pas utiliser le dispositif et avertir le fabricant.
MATÉRIEL NON FOURNI
• Seringue de gonflage de marque Kyphon® avec seringue à verrouillage Kyphon®
• Produit de contraste (à 60 %)
• Petit bol
REMARQUE : La seringue de gonflage de marque Kyphon® avec seringue à verrouillage Kyphon® est disponible auprès de Medtronic.
STOCKAGE
Les dispositifs IBT doivent être conservés dans leur emballage d’expédition d’origine. Prendre les précautions nécessaires pour s’assurer que les dispositifs IBT ne seront pas endommagés
Conserver au sec dans un lieu frais.
LIMITE DE RESPONSABILITÉ
EN AUCUN CAS MEDTRONIC NE PEUT ETRE TENU RESPONSABLE DE TOUT DOMMAGE DIRECT, INDIRECT, ACCIDENTEL, SECONDAIRE OU EXEMPLAIRE RESULTANT D’UNE REUTILISATION DES
DISPOSITIFS GONFLABLES OSSEUX POUR GESTION DES FRACTURES InflateFX™.
EN AUCUN CAS MEDTRONIC NE POURRA ÊTRE TENUE RESPONSABLE DE TOUT DOMMAGE DIRECT, INDIRECT, ACCIDENTEL, SECONDAIRE OU EXEMPLAIRE DÛ OU LIÉ AUX DISPOSITIFS GONFLABLES
DE PLOMBAGE OSSEUX POUR GESTION DE FRACTURES InflateFX™, SUR LA BASE D’UNE RUPTURE DE CONTRAT (Y COMPRIS UNE VIOLATION DE LA GARANTIE).
DEMANDES D’INFORMATIONS
Pour des informations complémentaires, contacter le service clientèle.
©2013 Medtronic Sofamor Danek USA, Inc. Tous droits réservés.
ESpañoL
INDICACIONES
El impactor óseo hinchable (Inflatable Bone Tamp, IBT) para el tratamiento de fracturas InflateFX™ está concebido para utilizarse como un impactor óseo convencional para la reducción
de fracturas y la creación de un espacio en el hueso esponjoso de la mano, la tibia, el radio y el calcáneo.
DESCRIPCIÓN DEL DISPOSITIVO
Consulte la figura 1.
1. Tapa
2. Estilete
3. Conector del estilete
4. Conector de hinchado
5. Banda cromocodificada
6. Banda marcadora de salida
7. Manguito de inserción
8. Marcadores radiopacos
9. Componente hinchable
• El componente hinchable del IBT está diseñado para comprimir el hueso esponjoso y mover el hueso cortical a medida que se hincha. El componente hinchable del IBT se halla cerca
de la punta distal del dispositivo, tal y como muestra la figura 1.
• El cuerpo contiene dos luces que no se comunican. La luz exterior se utiliza para hinchar el IBT, y la central contiene un estilete rígido y extraíble para insertar el IBT.
• El extremo proximal del cuerpo tiene un adaptador de brazo lateral. El conector de hinchado del adaptador está contiguo a la luz externa. El conector del estilete está contiguo a la
luz interna y contiene el estilete rígido. El estilete tiene una tapa en su extremo proximal para extraerlo si así se desea.
• La banda cromocodificada, situada distal al adaptador de brazo lateral, indica el tamaño del balón (p. ej., la banda amarilla indica el tamaño 10/3 y la negra, el tamaño 15/3).
• La banda marcadora de salida, situada sobre la luz exterior se emplea durante la inserción del IBT.
• Los marcadores radiopacos, situados en los extremos distal y proximal de la superficie de trabajo deshinchada permiten visualizar mediante fluoroscopia el IBT sin hinchar durante
su colocación.
CONTRAINDICACIONES
• Trastorno hemorrágico o tratamiento que aumente el riesgo de hemorragia excesiva.
• Presencia de infección activa o no completamente tratada en el lugar de aplicación del relleno para espacios óseos.
• Hipersensibilidad grave conocida al material de contraste o al relleno para espacios óseos.
• Paciente con embarazo confirmado.
ATENCIÓN: La ley federal (EE. UU.) permite la venta de este dispositivo únicamente a médicos o por prescripción facultativa.
ADVERTENCIAS
• La rotura del producto puede requerir intervención quirúrgica o extracción.
• No utilice este producto después de la fecha de caducidad impresa en el envase. Es posible que el dispositivo no sea seguro o eficaz después de su fecha de caducidad.
• El componente hinchable puede fallar debido a los instrumentos quirúrgicos o a la presencia de espículas óseas afiladas.
• Si se supera el volumen máximo de hinchado del IBT al hincharlo, el balón podría romperse antes de alcanzar la presión máxima de hinchado.
• Si se supera la presión máxima de hinchado del IBT al hincharlo, el balón podría romperse antes de alcanzar el volumen máximo de hinchado.
• Nunca utilice aire ni materiales gaseosos para hinchar el balón.
PRECAUCIONES
• El impactor óseo hinchable es un dispositivo para un solo uso, concebido para entrar en contacto con los tejidos del cuerpo. No lo vuelva a utilizar, procesar ni esterilizar. La
reutilización de estos dispositivos conlleva riesgo de contaminación y puede provocar la infección cruzada o infección del paciente, independientemente de los métodos de limpieza
y de reesterilización utilizados. También hay un mayor riesgo de deterioro de la eficacia del dispositivo debido a los pasos del reprocesamiento, lo que puede provocar lesiones en
el paciente o la muerte de éste.
• Es importante leer atentamente las Instrucciones de uso y estas precauciones antes de utilizar el dispositivo.
• Emplee el IBT antes de la fecha de caducidad indicada en el envase.
• No utilice el producto si el envase está abierto o dañado, ya que esto podría afectar a su integridad, en particular a su esterilidad.
• No utilice productos dañados. Antes del uso, compruebe que el IBT y el envase no estén dañados.
• Antes del uso, es preciso examinar el IBT a fin de verificar su funcionalidad y garantizar que su tamaño es apto para el procedimiento en el cual será utilizado.
• No utilice este producto si no ha recibido la formación adecuada para utilizarlo. Únicamente médicos formados en las técnicas de uso de impactores óseos deben emplear el IBT.
Los médicos que utilicen los dispositivos deberán estar familiarizados con la fisiología y patología de la anatomía seleccionada.
• El IBT debe ser manipulado exclusivamente bajo observación fluoroscópica con equipo radiográfico capaz de proporcionar imágenes de alta calidad.
• El IBT debe ser hinchado únicamente con una jeringa de hinchado que tenga una capacidad mínima de 14 ml.
• Hinche el IBT únicamente con medio de contraste líquido: se recomienda una solución al 60 %. Siga las instrucciones del fabricante respecto a las indicaciones, utilización y
precauciones pertinentes al medio de contraste.
• No utilice aire ni otros gases para hinchar el IBT.
• Las características de hinchado del IBT se alteran como consecuencia del hinchado intraóseo.
• Se prohíbe expresamente reacondicionar, restaurar, reparar, modificar o volver a esterilizar el dispositivo para seguir utilizándolo.
• Cualquier cirugía tiene riesgos; no obstante, el uso del balón para el tratamiento de estas fracturas no aumenta dichos riesgos desde el punto de vista clínico, en comparación con
los métodos tradicionales de elevación de los fragmentos óseos hundidos. Estos riesgos incluyen:
o Fracaso en el intento de reducir correctamente los fragmentos de la fractura.
o Unión retardada o falta de unión.
o Infección.
o Lesión neurovascular o síndrome compartimental que ocasione la pérdida de función o la amputación.
NOTA: La jeringa de hinchado Kyphon® proporciona un control de volumen superior en comparación con otros sistemas de hinchado, como una jeringa estándar, y es necesaria para
el hinchado del IBT. Siga las instrucciones de uso del fabricante de la jeringa de hinchado Kyphon®. La jeringa de bloqueo Kyphon® está envasada con la jeringa de hinchado Kyphon®.
REACCIONES ADVERSAS
Las reacciones adversas potencialmente asociadas al uso del IBT incluyen reacciones graves que, a pesar de ser raras, pueden ser mortales.
Las reacciones adversas incluyen:
• Embolia grasa, trombos u otros materiales que ocasionen una embolia pulmonar sintomática u otras secuelas clínicas.
• Rotura con fragmentación de la parte hinchable del IBT que provoca la retención de un fragmento en la zona afectada.
• Exposición del paciente al medio de contraste como consecuencia de la rotura del IBT y posible reacción alérgica o anafiláctica.
• Infección profunda o superficial de la herida quirúrgica.
• Hemorragia o hematoma.
MODO DE EMPLEO
ATENCIÓN: Siga las instrucciones de uso del fabricante de la jeringa de hinchado Kyphon®.
ATENCIÓN: Las diferentes viscosidades y niveles de precipitación de los medios de contraste podrían prolongar los tiempos de hinchado y deshinchado. Por esta razón, se recomienda
utilizar un medio de contraste al 60 %.
1. Gire la tapa del conector del estilete para apretar el estilete al IBT. Empuje el émbolo hasta el fondo de la jeringa de bloqueo Kyphon®. Conecte la jeringa de bloqueo Kyphon® al
conector de hinchado del IBT.
2. Tire del émbolo de la jeringa de bloqueo Kyphon® hacia fuera. Gire el émbolo para fijarlo en su posición en la última ranura de la jeringa.
3. Desconecte la jeringa de bloqueo Kyphon® del IBT.
4. Acople el conector del tubo de la jeringa de hinchado Kyphon® al conector de hinchado del IBT. Con esto el sistema queda preparado y listo para utilizarse.
UTILIZACIÓN DEL IBT
1. Seleccione el tamaño del IBT según la zona de tratamiento y el objetivo terapéutico. En la figura 1 y la tabla 1 se define el diámetro (D) y la longitud (L) del IBT hinchado en agua a
37 ºC en incrementos hasta el volumen máximo de hinchado.
2. Estas dimensiones pueden variar durante el uso del producto, debido a variaciones locales en la estructura ósea.
Tabla 1 – Dimensiones del IBT hinchado (en agua a 37 ºC)
Modelo E103A Dimensiones del dispositivo hinchado
Tamaño 10/3 Volumen Diámetro medio (D1, D2) Longitud (L)
Volumen máx. de hinchado 4 ml 2 ml 12,9 mm 14,7 mm
Presión máx. de hinchado 27 atm 4 ml 17,2 mm 19,1 mm
Modelo E153A Dimensiones del dispositivo hinchado
Tamaño 15/3 Volumen Diámetro medio (D1, D2) Longitud (L)
Volumen máx. de hinchado 4 ml 2 ml 12,1 mm 17,4 mm
Presión máx. de hinchado 27 atm 4 ml 16 mm 22,1 mm
INSERCIÓN DEL IBT
1. La colocación del IBT requiere la creación de un canal de acceso.
2. Siga las instrucciones de uso de los instrumentos de acceso óseo elegidos para crear un canal de acceso al interior del hueso.
3. Retire el manguito de inserción antes del uso.
NOTA: La punta distal del IBT deshinchado habrá llegado al extremo distal de la cánula cuando el marcador de salida en la luz exterior del IBT entre en el extremo proximal de la cánula.
4. Sitúe el IBT deshinchado en el canal de acceso y colóquelo con ayuda de técnicas de imagen y el uso de los marcadores radiopacos. Se puede facilitar la inserción con una torsión
suave sobre el dispositivo mientras se empuja hacia adelante.
5. Mientras sujeta el IBT en su lugar, hinche hasta 0,3 MPa (3 atm) para afianzar el IBT en dicha posición. Extraiga el estilete, si lo desea.
HINCHADO DEL IBT
1. Hinche el IBT con la ayuda de una técnica de imagen continua. Utilice la vista lateral para vigilar la distancia desde el córtex anterior y lateral. Utilice la vista anteroposterior (AP)
para vigilar los córtex laterales.
2. Si no utiliza una técnica de imagen continua, aumente el volumen en pequeños incrementos (0,25-0,5 ml). Evalúe la posición del impactor mediante las vistas lateral y AP antes
de proceder a un mayor aumento del volumen.
3. Deténgase cuando se logre el objetivo terapéutico o cualquier parte de la longitud del IBT hinchado entre en contacto con el hueso cortical o se haya alcanzado el volumen o la
presión de hinchado máximos (consulte la tabla 1).
EXTRACCIÓN DEL IBT
ATENCIÓN: No extraiga el IBT a menos que el componente hinchable esté totalmente deshinchado. Tampoco intente extraer el IBT si percibe resistencia. Determine el origen de la
resistencia mediante fluoroscopia y tome las medidas necesarias para remediar la situación.
Desbloquee la jeringa de hinchado Kyphon® y evacue el medio de contraste del IBT hasta que el balón se deshinche por completo. Retire el IBT del hueso a través de la cánula mediante
un suave movimiento de torsión.
• Si nota resistencia, conecte una jeringa de 30 ml al conector de hinchado. Tire del émbolo de la jeringa hasta la marca «30ml» para crear un vacío. Reanude la extracción del IBT.
• Confirme la entrada de la parte hinchable del IBT al interior de la cánula. Si el componente hinchable no entra en la cánula, haga avanzar la cánula sobre el IBT hasta el marcador
radiopaco proximal. Tras avanzar la cánula, retire el IBT a través de ella. Si detecta resistencia, retire el IBT y la cánula a la vez.
ESTERILIZACIÓN
Esterilizado con radiación.
PRESENTACIÓN
Los IBT se suministran estériles en un envase pelable. En caso de que el envase estéril se haya dañado, no utilice el producto y avise al fabricante.
MATERIALES NO SUMINISTRADOS
• Jeringa de hinchado Kyphon® con jeringa de bloqueo Kyphon®
• Medio de contraste (60 %)
• Cuenco pequeño
NOTA: La jeringa de hinchado Kyphon® con jeringa de bloqueo Kyphon® está disponible a través de Medtronic.
ALMACENAMIENTO
Los IBT deben ser almacenados en sus materiales de embalaje originales. Deben tomarse las precauciones adecuadas para impedir que los IBT se dañen. Consérvese en lugar fresco y seco.
LIMITACIÓN DE RESPONSABILIDADES
MEDTRONIC NO SE HACE RESPONSABLE DE NINGÚN DAÑO DIRECTO, INDIRECTO, INCIDENTAL, RESULTANTE O EJEMPLAR DERIVADO DE LA REUTILIZACIÓN DE LOS IMPACTORES ÓSEOS
HINCHABLES PARA EL TRATAMIENTO DE FRACTURAS InflateFX™.
MEDTRONIC NO SE RESPONSABILIZARÁ, EN NINGUNA CIRCUNSTANCIA, DE NINGÚN DAÑO DIRECTO, INDIRECTO, FORTUITO, RESULTANTE O EJEMPLAR ORIGINADO POR LOS IMPACTORES
ÓSEOS HINCHABLES PARA EL TRATAMIENTO DE FRACTURAS InflateFX™ O RELACIONADO CON SU USO SOBRE LA BASE DEL INCUMPLIMIENTO DE CONTRATO (INCLUIDO EL INCUMPLIMIENTO
DE LA GARANTÍA).
SOLICITUD DE INFORMACIÓN
Para obtener más información, póngase en contacto con el departamento de atención al cliente.
©2013 Medtronic Sofamor Danek USA, Inc. Reservados todos los derechos.
DEUTSCH
INDIKATIONEN
Der InflateFX™ insufflierbare Frakturmanagement-Knochenstopfen (Inflatable Bone Tamp, IBT) dient zur Verwendung als konventioneller Knochenstopfen zur Reduzierung von Frakturen
und/oder zur Herstellung eines Hohlraums in der Knochenspongiosa der Hand, Tibia, des Radius und Calcaneus.
PRODUKTBESCHREIBUNG
Siehe Abbildung 1.
1. Kappe
2. Mandrin
3. Mandrinöffnung
4. Insufflationsanschluss
5. Farbkodiertes Band
6. Austrittsmarkierungsband
7. Einführhülse
8. Röntgendichte Markierungen
9. Insufflationselement
• Das Insufflationselement des IBT-Instruments ist so ausgelegt, dass bei der Insufflation spongiöser Knochen komprimiert und/oder kortikaler Knochen verschoben wird. Das
Insufflationselement des IBT-Instruments befindet sich nahe der distalen Spitze der Vorrichtung (siehe Abbildung 1).
• Der Schaft enthält zwei voneinander getrennte Lumen. Das äußere Lumen wird für die IBT-Insufflation verwendet und das zentrale Lumen enthält einen entfernbaren
Versteifungsmandrin für die Einführung des IBT-Instruments.
• Das proximale Ende des Schafts weist einen Adapter-Seitenarm auf. Der Insufflationsanschluss des Adapters ist mit dem äußeren Lumen verbunden. Die Mandrinöffnung ist mit
dem inneren Lumen verbunden und enthält den Versteifungsmandrin. Zur wahlweisen Entfernung des Mandrins ist er am proximalen Ende mit einer Kappe versehen.
• Das farbcodierte Band, das sich unmittelbar distal vom Adapter-Seitenarm befindet, zeigt die Ballongröße an (d.h. ein gelbes Band für Größe 10/3 und ein schwarzes Band für
Größe 15/3).
• Das Austrittsmarkierungsband am äußeren Lumen wird zum Einführen des IBT-Instruments verwendet.
• Röntgendichte Markierungen am distalen und proximalen Ende der desufflierten Nutzfläche ermöglichen die fluoroskopische Visualisierung des desufflierten IBT bei der Positionierung.
KONTRAINDIKATIONEN
• Blutungsstörungen oder Therapie, die das Risiko für starke Blutungen erhöhen.
• Vorliegen einer aktiven oder unvollständig behandelten Infektion an der Stelle, an der das Knochenfüllmaterial appliziert werden soll.
• Bekannte schwere Allergie gegen Kontrastmittel und Knochenfüllmaterial.
• Bei Patientinnen mit nachgewiesener Schwangerschaft.
ACHTUNG: Nach US-amerikanischem Recht darf diese Vorrichtung nur von einem Arzt bzw. auf ärztliche Anordnung verkauft werden.
WARNHINWEISE
• Bei einem Bruch des Produkts kann eine chirurgische Intervention bzw. ein Entfernen erforderlich werden.
• Das vorliegende Produkt nicht nach dem auf der Packung aufgedruckten Verfallsdatum verwenden. Das Instrument ist nach seinem Verfallsdatum möglicherweise nicht mehr
sicher oder wirksam.
• Das Insufflationselement kann durch scharfe Knochensplitter oder durch chirurgische Instrumente seine Funktionsfähigkeit verlieren.
• Eine Insufflation des IBT-Instruments über das maximale Insufflationsvolumen könnte dazu führen, dass der Ballon reißt, bevor der maximale Insufflationsdruck erreicht wird.
• Eine Insufflation des IBT-Instruments über den maximalen Insufflationsdruck könnte dazu führen, dass der Ballon reißt, bevor das maximale Insufflationsvolumen erreicht wird.
• Zum Insufflieren des Ballons keinesfalls Luft oder gasförmige Materialien verwenden.
VORSICHTSHINWEISE
• Der insufflierbare Knochenstopfen ist ein Einwegprodukt, das zum Kontakt mit Körpergeweben vorgesehen ist. Nicht erneut verwenden, erneut aufbereiten oder resterilisieren.
Bei erneuter Verwendung dieser Instrumente besteht das Risiko einer Kontamination und Infektion bzw. Kreuzinfektion des Patienten, unabhängig von den Reinigungs- und
Resterilisationsmethoden. Die Schritte einer Aufbereitung bewirken auch ein erhöhtes Risiko einer Leistungsminderung des Instruments, was zu Verletzungen und sogar zum Tod
des Patienten führen kann.
• Vor Gebrauch des Instruments müssen die Gebrauchsanweisung und diese Vorsichtshinweise sorgfältig durchgelesen werden.
• Das IBT-Instrument vor dem auf der Packung angegebenen Verfallsdatum verwenden.
• Nicht verwenden, wenn die Packung geöffnet oder beschädigt ist, da die Unversehrtheit sowie die Sterilität des Produkts beeinträchtigt sein können.
• Beschädigte Produkte nicht verwenden. Vor Gebrauch sicherstellen, dass das IBT-Instrument und die Verpackung keine Beschädigung aufweisen.
• Das IBT-Instrument vor dem Gebrauch in Hinblick auf seine Funktionstüchtigkeit überprüfen und sicherstellen, dass die Größe für das vorgesehene spezifische Verfahren geeignet
ist.
• Dieses Produkt darf nur nach entsprechender Schulung benutzt werden. Das IBT-Instrument darf nur von Ärzten verwendet werden, die in den Anwendungstechniken von
Knochenstopfen geschult sind. Ärzte, die diese Instrumente verwenden, müssen mit der Physiologie und Pathologie der gewählten anatomischen Region vertraut sein.
• Das IBT-Instrument sollte nur unter Durchleuchtungskontrolle, mit einem Röntgengerät, das hohe Bildqualität gewährleistet, verwendet werden.
• Zum Insufflieren des IBT-Instruments ausschließlich eine Insufflationsspritze mit einer Volumenkapazität von mindestens 14 ml verwenden.
• Zum Insufflieren des IBT-Instruments nur flüssige Kontrastmittel verwenden: 60%ige Lösung wird empfohlen. Die Herstelleranweisungen zum Kontrastmittel bezüglich Indikationen,
Anwendung und Vorsichtsmaßnahmen beachten.
• Zum Insufflieren des IBT-Instruments keine Luft oder andere Gase verwenden.
• Die Insufflationseigenschaften des IBT-Instruments sind bei der Insufflation in einem Knochen verändert.
• Die Wiederinstandsetzung, Wiederaufbereitung, Reparatur, Modifizierung oder Resterilisation der Vorrichtung zum Zwecke der weiteren Verwendung ist ausdrücklich untersagt.
• Jede Operation hat Risiken; vom klinischen Standpunkt aus und im Vergleich zu herkömmlichen Impressionsfraktur-Hebemethoden erhöht die Verwendung des Ballons bei der
Behandlung dieser Frakturen diese Risiken allerdings nicht. Zu diesen Risiken zählen:
o Unzureichende Frakturfragmentreduktion.
o Verzögerte Vereinigung und Nichtvereinigung.
o Infektion.
o Neurovaskuläre Verletzung oder Kompartmentsyndrom mit folglichem Funktionsverlust oder folglicher Amputation.
HINWEIS: Eine Insufflationsspritze der Marke Kyphon® bietet eine bessere Volumenkontrolle als andere Insufflationssysteme (wie z.B. eine Standardspritze) und muss bei Insufflation
des IBT-Instruments verwendet werden. Die Gebrauchsanweisung des Herstellers der Insufflationsspritze der Marke Kyphon® befolgen. Die Kyphon® Spritze mit Sperrmechanismus
befindet sich in derselben Packung wie die Insufflationsspritze der Marke Kyphon®.
UNERWÜNSCHTE EREIGNISSE
Zu unerwünschten Ereignissen, die möglicherweise mit der Verwendung des IBT-Instruments in Verbindung gebracht werden können, zählen schwerwiegende Ereignisse, die zwar
selten sind, aber zum Tod führen können.
Zu unerwünschten Ereignissen zählen:
• Verschleppung von Fett, eines Thrombus oder anderen Materialien, die zu einer symptomatischen Lungenembolie oder anderen klinischen Folgen führen kann.
• Ruptur mit Zerfall des insufflierbaren IBT-Teils, was zur Retention eines Fragments im betroffenen Bereich führt.
• IBT-Ruptur mit Kontrastmittelexposition, was zu einer allergischen Reaktion bzw. Anaphylaxie führen kann.
• Tiefe oder oberflächliche Wundinfektion.
• Blutung oder Hämatom.
GEBRAUCHSANWEISUNG
ACHTUNG: Die Gebrauchsanweisung des Herstellers der Insufflationsspritze der Marke Kyphon® befolgen.
ACHTUNG: Kontrastmittel können sich in ihrer Viskosität und den Ausfällungsschwellen unterscheiden und dadurch zu Verzögerungen bei der Insufflation und Desufflation führen. Aus
diesem Grund wird die Verwendung eines 60%igen Kontrastmittels empfohlen.
1. Durch Drehen der Kappe auf der Mandrinöffnung den Mandrin fest am IBT-Instrument anbringen. Den Kolben vollständig in die Kyphon® Spritze mit Sperrmechanismus drücken.
Die Kyphon® Spritze mit Sperrmechanismus an den Insufflationsanschluss auf dem IBT-Instrument anschließen.
2. Den Kolben der Kyphon® Spritze mit Sperrmechanismus zurückziehen. Den Kolben drehen, um seine Position im letzten Spalt in der Spritze zu sperren.
3. Die Kyphon® Spritze mit Sperrmechanismus vom IBT-Instrument abnehmen.
4. Die verbindende Öffnung auf dem Schlauch der Insufflationsspritze der Marke Kyphon® an den Insufflationsanschluss auf dem IBT-Instrument anschließen. Das System ist nun
vorbereitet und einsatzbereit.
ANWENDUNG DES IBTINSTRUMENTS
1. Die für den Behandlungsbereich und das Behandlungsziel geeignete IBT-Größe wählen. In Abbildung 1 und Tabelle 1 werden die Durchmesser (D) und Längen (L) bei Insufflation
der IBT-Instrumente in Wasser mit einer Temperatur von 37 °C schrittweise bis zum maximalen Insufflationsvolumen angegeben.
2. Diese Abmessungen können während der Anwendung des Produkts aufgrund lokal unterschiedlicher Knochenstrukturen schwanken.
Información Importante Sobre el impactor óseo hinchable para el
tratamiento de fracturas InflateFX™ (Tamaños 10/3 y 15/3)
Wichtige Informationen Zum InflateFX™ insufflierbaren
Frakturmanagement-Knochenstopfen (Größen 10/3 und 15/3)
Tabelle 1 – IBT-Abmessungen in insuffliertem Zustand (in Wasser mit einer Temperatur von 37 °C)
Modellnummer E103A Abmessungen in insuffliertem Zustand
Größe 10/3 Volumen Durchschn. Durchmesser (D1, D2) Länge (L)
Max. Insufflationsvolumen 4 ml 2 ml 12,9 mm 14,7 mm
Max. Insufflationsdruck 27 atm 4 ml 17,2 mm 19,1 mm
Modellnummer E153A Abmessungen in insuffliertem Zustand
Größe 15/3 Volumen Durchschn. Durchmesser (D1, D2) Länge (L)
Max. Insufflationsvolumen 4 ml 2 ml 12,1 mm 17,4 mm
Max. Insufflationsdruck 27 atm 4 ml 16 mm 22,1 mm
EINFÜHRUNG DES IBTINSTRUMENTS
1. Für die Platzierung des IBT-Instruments ist ein Zugangskanal erforderlich.
2. Bei Herstellung eines Zugangskanals in den Knochen die Gebrauchsanweisungen für die gewählten Knochenzugangsinstrumente befolgen.
3. Vor dem Gebrauch die Einführhülse entfernen.
HINWEIS: Die distale Spitze des desufflierten IBT-Instruments hat das distale Ende der Kanüle erreicht, sobald die Austrittsmarkierung am äußeren Lumen des IBT-Instruments in
das proximale Ende der Kanüle eintritt.
4. Das desufflierte IBT-Instrument in den Zugangskanal einbringen und anhand der röntgendichten Markierungen unter Durchleuchtungskontrolle positionieren. Behutsames Drehen
beim Vorschieben kann das Einführen erleichtern.
5. Das IBT-Instrument in Position halten und durch Insufflation auf 3 atm in der gewünschten Stellung fixieren. Den Mandrin nach Bedarf entfernen.
INSUFFLATION DES IBTINSTRUMENTS
1. Das IBT-Instrument unter ständiger Durchleuchtungskontrolle insufflieren. Die Distanz zum anterioren und lateralen Kortex in lateraler Perspektive überwachen. Die lateralen
Kortizes in der AP-Perspektive überwachen.
2. Wenn keine Dauerbildgebung durchgeführt wird, das Volumen in kleinen Schritten (0,25 – 0,5 ml) erhöhen. Vor weiteren Volumenerhöhungen die Stopfenposition in lateraler
und AP-Perspektive beurteilen.
3. Den Vorgang beenden, sobald das Behandlungsziel erreicht ist oder ein Teil der insufflierten Länge des IBT-Instruments kortikalen Knochen berührt oder das maximale
Insufflationsvolumen und/oder der maximale Insufflationsdruck erreicht ist (siehe Tabelle 1).
ENTFERNUNG DES IBTINSTRUMENTS
ACHTUNG: Das IBT-Instrument erst dann zurückziehen, wenn das Insufflationselement vollständig desuffliert ist. Das IBT-Instrument niemals gegen Widerstand zurückziehen. Die
Ursache des Widerstands durch Durchleuchtungskontrolle ermitteln und alle erforderlichen Abhilfemaßnahmen treffen.
Mithilfe einer Insufflationsspritze der Marke Kyphon® das Kontrastmittel aus dem IBT-Instrument herausziehen, bis der Ballon vollständig desuffliert ist. Das IBT-Instrument mit einer
behutsamen Drehbewegung durch die Kanüle aus dem Knochen entfernen.
• Bei Widerstand eine 30-ml-Spritze an den Insufflationsanschluss anschließen. Den Kolben der Spritze bis zur Marke „30ml“ zurückziehen, um Unterdruck zu erzeugen. Mit der
Entfernung des IBT-Instruments fortfahren.
• Den Eintritt des insufflierbaren Teils des IBT-Instruments in die Kanüle sicherstellen. Sollte sich das Insufflationselement nicht in die Kanüle einbringen lassen, muss die Kanüle über
das IBT-Instrument bis zur proximalen röntgendichten Markierung vorgeschoben werden. Nach Vorschieben der Kanüle das IBT-Instrument durch die Kanüle hindurch herausziehen.
Bei spürbarem Widerstand das IBT-Instrument und die Kanüle gleichzeitig entfernen.
STERILISATION
Sterilisiert mittels Bestrahlung.
LIEFERFORM
Die IBT-Instrumente werden steril in einer Aufreißpackung geliefert. Bei Beschädigung der Sterilverpackung das Produkt nicht verwenden und den Hersteller benachrichtigen.
NICHT IM LIEFERUMFANG ENTHALTENE MATERIALIEN
• Insufflationsspritze der Marke Kyphon® mit Kyphon® Spritze mit Sperrmechanismus
• Kontrastmittel (60%)
• Kleine Schale
HINWEIS: Die Insufflationsspritze der Marke Kyphon® mit Kyphon® Spritze mit Sperrmechanismus ist bei Medtronic erhältlich.
AUFBEWAHRUNG
Die IBT-Instrumente sollten in den Original-Versandmaterialien aufbewahrt werden. Es ist sorgfältig darauf zu achten, dass die IBT-Instrumente nicht beschädigt werden. Kühl und
trocken aufbewahren.
HAFTUNGSBESCHRÄNKUNGEN
MEDTRONIC HAFTET NICHT FÜR UNMITTELBARE, MITTELBARE, ZUFÄLLIGE, FOLGE- ODER EXEMPLARISCHE SCHÄDEN, DIE SICH AUS DER WIEDERVERWENDUNG DER InflateFX™
INSUFFLIERBAREN FRAKTURMANAGEMENT-KNOCHENSTOPFEN ERGEBEN.
MEDTRONIC HAFTET UNTER KEINEN UMSTÄNDEN FÜR UNMITTELBARE, MITTELBARE, ZUFÄLLIGE, FOLGE- ODER EXEMPLARISCHE SCHÄDEN, DIE SICH AUS DER VERWENDUNG VON ODER IN
VERBINDUNG MIT DEN InflateFX™ INSUFFLIERBAREN FRAKTURMANAGEMENT-KNOCHENSTOPFEN INFOLGE VON VERTRAGSBRUCH (EINSCHLIESSLICH GARANTIEVERLETZUNG) ERGEBEN.
ANFRAGEN
Für weitere Informationen bitte den Kundendienst kontaktieren.
© 2013 Medtronic Sofamor Danek USA, Inc. Alle Rechte vorbehalten.
ITaLIaNo
INDICAZIONI PER L’USO
L’impattatore osseo gonfiabile (IBT, Inflatable Bone Tamp) per la gestione delle fratture InflateFX™ è previsto per l’uso come impattatore convenzionale per la riduzione delle fratture
e/o la creazione di cavità nell’osso spugnoso della mano, della tibia, del radio e del calcagno.
DESCRIZIONE DEL DISPOSITIVO
Vedere la Figura 1.
1. Cappuccio
2. Mandrino
3. Porta per il mandrino
4. Porta per il gonfiaggio
5. Striscia con codifica a colori
6. Indicatore di uscita
7. Guaina di inserimento
8. Contrassegni radiopachi
9. Componente gonfiabile
• Il componente gonfiabile dell’IBT è stato progettato per comprimere l’osso spugnoso e/o spostare l’osso corticale durante il gonfiaggio. Il componente gonfiabile dell’IBT si trova
vicino alla punta distale del dispositivo come illustrato nella Figura 1.
• Lo stelo contiene due lumi non comunicanti. Il lume esterno viene utilizzato per il gonfiaggio dell’IBT, mentre il lume centrale contiene un mandrino di rinforzo rimovibile per
l’inserimento dell’IBT.
• L’estremità prossimale dello stelo è munita di un adattatore laterale. La porta per il gonfiaggio dell’adattatore è contigua al lume esterno. La porta per il mandrino è contigua al
lume interno e contiene il mandrino di rinforzo. Sull’estremità prossimale del mandrino si trova un cappuccio che può essere usato per rimuovere il mandrino stesso, se lo si desidera.
• La striscia con codifica a colori, situata in posizione immediatamente distale rispetto all’adattatore laterale, indica la dimensione del palloncino (una striscia gialla per la misura
10/3 e una striscia nera per la misura 15/3).
• L’indicatore di uscita situato sul lume esterno viene utilizzato durante l’inserimento dell’IBT.
• I contrassegni radiopachi presenti sull’estremità distale e prossimale della superficie utile del dispositivo sgonfio consentono la visualizzazione tramite fluoroscopia dell’IBT sgonfio
durante il posizionamento.
CONTROINDICAZIONI
• Disturbi emorragici o trattamento in grado di aumentare la probabilità di sanguinamento eccessivo.
• Presenza di infezione attiva o irrisolta nel sito di applicazione previsto per il riempitivo di cavità ossee.
• Qualsiasi allergia grave nota al materiale di contrasto e al riempitivo per cavità ossee.
• Gravidanza confermata.
ATTENZIONE - La legge federale degli Stati Uniti limita la vendita di questo dispositivo ai medici o su presentazione di prescrizione medica.
AVVERTENZE
• La rottura del dispositivo può richiedere un intervento chirurgico o di recupero.
• Non utilizzare il prodotto dopo la data di scadenza (Utilizzare entro) indicata sulla confezione. Dopo tale data (Utilizzare entro), il prodotto può risultare non sicuro o inefficace.
• Il componente gonfiabile potrebbe cedere a causa di frammenti ossei o di strumenti chirurgici appuntiti.
• Il gonfiaggio dell’IBT oltre il volume massimo di gonfiaggio può causare la rottura del palloncino prima del raggiungimento della pressione massima di gonfiaggio.
• Il gonfiaggio dell’IBT oltre la pressione massima di gonfiaggio può causare la rottura del palloncino prima del raggiungimento del volume massimo di gonfiaggio.
• Non usare mai aria o sostanze gassose per il gonfiaggio del palloncino.
PRECAUZIONI
• L’impattatore osseo gonfiabile è un dispositivo monouso previsto per il contatto con i tessuti corporei. Non riutilizzare, ricondizionare o risterilizzare. Il riutilizzo di questi dispositivi
comporta il rischio di contaminazione e può causare infezione del paziente o infezione crociata, indipendentemente dai metodi di pulizia e risterilizzazione. Esiste anche un aumentato
rischio di deterioramento delle prestazioni del dispositivo a causa delle operazioni di ritrattamento, con conseguenti lesioni o decesso del paziente.
• Prima di utilizzare il dispositivo, è importante leggere attentamente le istruzioni per l’uso e i presenti avvisi.
• Usare l’IBT prima della data di scadenza indicata sulla confezione.
• Non usare il prodotto se la confezione è aperta o danneggiata; l’integrità del prodotto, inclusa la sterilità, potrebbe essere stata compromessa.
• Non utilizzare prodotti danneggiati. Prima dell’uso, esaminare l’IBT e la sua confezione per accertarsi che non abbiano subito danni.
• Prima dell’uso, l’IBT va esaminato per confermarne la funzionalità e per accertare l’idoneità della misura scelta per la procedura specifica nella quale si intende utilizzarlo.
• Non utilizzare il presente prodotto senza avere ricevuto un adeguato addestramento al suo impiego. L’IBT va usato esclusivamente da medici debitamente addestrati alle tecniche
di utilizzo degli espansori ossei. I medici che si avvalgono di questi dispositivi devono avere dimestichezza con la fisiologia e la patologia dell’anatomia interessata.
• L’IBT va utilizzato esclusivamente sotto osservazione fluoroscopica con apparecchiature radiologiche in grado di generare immagini di alta qualità.
• L’IBT va gonfiato unicamente mediante una apposita siringa di gonfiaggio con una capacità minima di 14 ml.
• Gonfiare l’IBT esclusivamente con mezzo di contrasto liquido: si consiglia di usare una soluzione al 60%. Per le indicazioni, l’impiego e le precauzioni relative al mezzo di contrasto,
attenersi alle istruzioni per l’uso fornite dalla casa produttrice.
• Per il gonfiaggio dell’IBT non usare aria o altro gas.
• Le caratteristiche di gonfiaggio dell’IBT risultano alterate a seguito del suo gonfiaggio all’interno dell’osso.
• Il ricondizionamento, la rimessa a nuovo, la riparazione, la modifica o la risterilizzazione dei dispositivi volti a consentirne l’ulteriore utilizzo sono esplicitamente vietati.
• Qualsiasi intervento chirurgico comporta dei rischi; dal punto di vista clinico, tuttavia, l’impiego del palloncino nel trattamento di queste fratture non aumenta tali rischi rispetto
ai metodi tradizionali che prevedono il sollevamento dei frammenti ossei compressi. Questi rischi includono i seguenti.
o Mancata riduzione corretta dei frammenti della frattura.
o Unione ritardata e mancata unione.
o Infezione.
o Lesioni neurovascolari o sindrome compartimentale con conseguente perdita della funzionalità o amputazione.
NOTA - La siringa di gonfiaggio Kyphon® fornisce un maggiore controllo del volume rispetto ad altri sistemi di gonfiaggio, come le siringhe standard, e pertanto il suo uso è essenziale
per il gonfiaggio dell’IBT. Per l’impiego della siringa di gonfiaggio Kyphon® attenersi alle istruzioni per l’uso fornite dalla casa produttrice. La siringa di bloccaggio Kyphon® è fornita
in dotazione alla siringa di gonfiaggio Kyphon®.
EVENTI INDESIDERATI
Gli eventi indesiderati potenzialmente associati all’uso dell’IBT includono eventi gravi che, sebbene rari, possono risultare fatali. Gli eventi indesiderati includono i seguenti.
• Embolia lipidica, trombo o altro materiale, con conseguente embolia polmonare sintomatica o altra conseguenza clinica.
• Rottura con frammentazione della sezione gonfiabile dell’IBT con conseguente ritenzione di un frammento all’interno della regione interessata.
• Rottura dell’IBT con conseguente esposizione al mezzo di contrasto e quindi possibile reazione allergica o anafilattica.
• Infezione profonda o superficiale dell’incisione.
• Emorragia o ematoma.
ISTRUZIONI PER L’USO
ATTENZIONE - Per l’impiego della siringa di gonfiaggio Kyphon® attenersi alle istruzioni per l’uso fornite dalla casa produttrice.
ATTENZIONE - I mezzi di contrasto possono avere viscosità diverse e livelli di precipitazione diversi che potrebbero rallentare i tempi di gonfiaggio e sgonfiaggio. Per questa ragione
si consiglia di usare il mezzo di contrasto al 60%.
1. Avvitare il cappuccio sulla porta per il mandrino per fissare il mandrino all’IBT. Spingere fino in fondo lo stantuffo della siringa di bloccaggio Kyphon®. Fissare la siringa di bloccaggio
Kyphon® alla porta per il gonfiaggio dell’IBT.
2. Tirare indietro lo stantuffo della siringa di bloccaggio Kyphon®. Far ruotare lo stantuffo per bloccarlo in posizione sull’ultima fessura della siringa.
3. Staccare la siringa di bloccaggio Kyphon® dall’IBT.
4. Fissare la porta per il collegamento della cannula della siringa di gonfiaggio Kyphon® alla porta per il gonfiaggio dell’IBT. Il sistema è ora pronto per l’uso.
USO DELL’IBT
1. Selezionare la misura dell’IBT in base al sito e all’obiettivo del trattamento. La Figura 1 e la Tabella 1 definiscono il diametro (D) e la lunghezza (L) dopo il gonfiaggio degli IBT in
acqua a 37 °C, in incrementi del volume fino al volume di gonfiaggio massimo.
2. Queste dimensioni possono variare durante l’uso del prodotto a causa delle variazioni individuali della struttura ossea.
Tabella 1 – Dimensioni dell’IBT gonfio (in acqua a 37 °C)
Numero di modello E103A Dimensioni gonfio
Misura 10/3 Volume Diametro medio (D1, D2) Lunghezza (L)
Volume massimo di gonfiaggio 4 ml 2 ml 12,9 mm 14,7 mm
Pressione massima di gonfiaggio 27 atm 4 ml 17,2 mm 19,1 mm
Numero di modello E153A Dimensioni gonfio
Misura 15/3 Volume Diametro medio (D1, D2) Lunghezza (L)
Volume massimo di gonfiaggio 4 ml 2 ml 12,1 mm 17,4 mm
Pressione massima di gonfiaggio 27 atm 4 ml 16 mm 22,1 mm
INSERIMENTO DELL’IBT
1. È necessario creare un canale di accesso per posizionare l’IBT.
2. Attenersi alle istruzioni per l’uso degli strumenti per accesso osseo selezionati per creare un canale di accesso all’osso.
3. Prima dell’uso, rimuovere la guaina di inserimento.
NOTA - La punta distale dell’IBT sgonfio ha raggiunto l’estremità distale della cannula quando l’indicatore di uscita sul lume esterno dell’IBT entra nell’estremità prossimale della cannula.
4. Inserire l’IBT sgonfio nel canale di accesso e posizionarlo sotto osservazione guidata da immagini utilizzando come riferimento i contrassegni radiopachi. Un delicato movimento
di torsione con una spinta in avanti può facilitare l’inserimento.
5. Mantenendo fermo l’IBT, gonfiarlo a 0,3 MPa (3 atm) per fissarlo in posizione. Volendo, si può rimuovere il mandrino.
GONFIAGGIO DELL’IBT
1. Gonfiare l’IBT sotto continua osservazione mediante immagini. Utilizzare la vista laterale per monitorare la distanza dalla corteccia anteriore e da quella laterale. Utilizzare la vista
anteroposteriore per monitorare le cortecce laterali.
2. Se non si utilizza il monitoraggio continuo mediante imaging, aumentare il volume in piccoli incrementi (0,25-0,5 ml). Valutare la posizione dell’espansore nelle viste laterale e
anteroposteriore prima di procedere con un ulteriore aumento di volume.
3. Interrompere il gonfiaggio quando si raggiunge l’obiettivo del trattamento, cioè quando qualsiasi parte della lunghezza dell’IBT gonfio è a contatto con l’osso corticale, oppure
quando sono stati raggiunti il volume massimo e/o la pressione massima di gonfiaggio (vedere la Tabella 1).
RIMOZIONE DELL’IBT
ATTENZIONE - Non ritirare l’IBT prima di aver sgonfiato completamente il componente gonfiabile. Non ritirare l’IBT se si avverte resistenza. Determinare la causa della resistenza
mediante fluoroscopia e intervenire con le misure necessarie.
Usare la siringa di gonfiaggio Kyphon® per evacuare il mezzo di contrasto dall’IBT finché il palloncino non è completamente sgonfio. Rimuovere l’IBT dall’osso attraverso la cannula
con un delicato movimento di torsione.
• Se si incontra resistenza, fissare una siringa da 30 ml alla porta per il gonfiaggio. Tirare lo stantuffo della siringa fino al contrassegno “30ml” per creare il vuoto. Riprendere la
rimozione dell’IBT.
• Confermare che la porzione gonfiabile dell’IBT sia entrata nella cannula. Se il componente gonfiabile non entra nella cannula, fare avanzare la cannula sull’IBT fino al contrassegno
radiopaco prossimale. Dopo l’avanzamento della cannula, ritirare l’IBT attraverso la cannula stessa. Se si avverte resistenza, rimuovere l’IBT e la cannula simultaneamente.
STERILIZZAZIONE
Sterilizzato mediante irradiazione.
CONFEZIONAMENTO
Gli IBT sono forniti sterili in una confezione con apertura a strappo. In caso di danni alla confezione sterile, non usare il dispositivo e notificare la casa produttrice.
MATERIALI NON FORNITI
• Siringa di gonfiaggio Kyphon® con siringa di bloccaggio Kyphon®
• Mezzo di contrasto al 60%
• Vaschetta piccola
NOTA - La siringa di gonfiaggio Kyphon® con la siringa di bloccaggio Kyphon® sono disponibili presso Medtronic.
CONSERVAZIONE
Gli IBT vanno conservati nei materiali di imballaggio originali. Prendere tutte le opportune precauzioni per evitare che gli IBT vengano danneggiati. Conservare in luogo fresco e asciutto.
LIMITAZIONE DI RESPONSABILITÀ
MEDTRONIC NON SI RITERRÀ RESPONSABILE DI ALCUN DANNO DIRETTO, INDIRETTO, FORTUITO, CONSEGUENTE O PUNITIVO , DERIVANTE DAL RIUTILIZZO DEGLI IMPATTATORI OSSEI
GONFIABILI PER LA GESTIONE DELLE FRATTURE InflateFX™.
IN NESSUN CASO MEDTRONIC SARÀ RITENUTA RESPONSABILE DI QUALSIASI DANNO DIRETTO, INDIRETTO, FORTUITO, CONSEGUENTE O PUNITIVO CHE INSORGA O SIA CONNESSO AGLI
IMPATTATORI OSSEI GONFIABILI PER LA GESTIONE DELLE FRATTURE InflateFX™ E CONSEGUENTE AD UNA VIOLAZIONE CONTRATTUALE (INCLUSO L’INADEMPIMENTO DELLA GARANZIA).
RICHIESTA DI INFORMAZIONI
Per ulteriori informazioni, rivolgersi a Customer Service.
© 2013 Medtronic Sofamor Danek USA, Inc. Tutti i diritti riservati.
NEDErLaNDS
INDICATIES VOOR GEBRUIK
De InflateFX™ vulbare bot-stopper voor fractuurmanagement (Inflatable Bone Tamp; IBT) wordt gebruikt als conventionele bot-stopper om fracturen te zetten en/of om een holte in
het spongieuze bot van de hand, tibia, radius of calcaneus te vormen.
BESCHRIJVING VAN HET INSTRUMENT
Zie afbeelding 1.
1. Dop
2. Stilet
3. Stiletpoort
4. Vulpoort
5. Band met kleurcode
6. Uitgangsmarkering
7. Inbrenghuls
8. Radiopake markeringen
9. Vulbaar deel
• Het vulbare deel van de IBT is zo ontworpen dat het naarmate het wordt gevuld spongieus bot samendrukt en/of corticaal bot verschuift. Het vulbare deel van de IBT bevindt zich
bij de distale tip van het apparaat, zoals in afbeelding 1 te zien is.
• De schacht bevat twee niet met elkaar communicerende lumina. Het buitenlumen wordt gebruikt om de IBT te vullen en het binnenlumen bevat een verwijderbaar verstevigend
stilet voor het inbrengen van de IBT.
• Het proximale uiteinde van de schacht is voorzien van een zijarmadapter. De vulpoort van de adapter grenst aan het buitenlumen. De stiletpoort grenst aan het binnenlumen en
bevat het verstevigende stilet. Het stilet is voorzien van een dop aan het proximale uiteinde voor optionele verwijdering.
• De band met kleurcode, die zich net distaal van de zijarmadapter bevindt, geeft de ballonmaat aan (namelijk een gele band voor maat 10/3 en een zwarte band voor maat 15/3).
• De uitgangsmarkering op het buitenlumen wordt gebruikt bij het inbrengen van de IBT.
• Met behulp van de radiopake markeringen die zich aan het distale en proximale uiteinde van het lege werkoppervlak bevinden, kan de lege IBT onder fluoroscopische beeldvorming
in de juiste positie worden gebracht.
CONTRAINDICATIES
• Bloedingsstoornis of een behandeling die de kans op overmatig bloeden doet toenemen.
• Aanwezigheid van actieve of onvolledig behandelde infectie op de plaats waar het botholtevulmiddel moet worden aangebracht.
• Elke bekende ernstige allergie tegen contrastmiddel en botholtevulmiddel.
• Bevestigde zwangerschap.
OPGELET: Volgens de federale wetgeving van de Verenigde Staten mag dit instrument uitsluitend door of op voorschrift van een arts worden verkocht.
WAARSCHUWINGEN
• Breken van het instrument kan interventie of verwijdering noodzakelijk maken.
• Dit product niet gebruiken na de uiterste gebruiksdatum die op de verpakking staat gedrukt. Het kan zijn dat het instrument na de uiterste gebruiksdatum niet meer veilig of
effectief is.
• Het is mogelijk dat het vulbare deel van de IBT defect raakt door scherpe botuitsteeksels of chirurgische instrumenten.
• De ballon kan scheuren voordat de maximale vuldruk is bereikt als de IBT voorbij het maximale vulvolume wordt gevuld.
• De ballon kan scheuren voordat het maximale vulvolume is bereikt als de IBT voorbij de maximale vuldruk wordt gevuld.
• Gebruik nooit lucht of gasachtige materialen om de ballon te vullen.
VOORZORGSMAATREGELEN
• De vulbare bot-stopper is een voor eenmalig gebruik bestemd instrument dat in aanraking komt met lichaamsweefsels. Niet opnieuw gebruiken, opnieuw verwerken of opnieuw
steriliseren. Hergebruik van deze apparaten draagt het risico van besmetting met zich mee en kan infectie of kruisinfectie van de patiënt veroorzaken, ongeacht de reinigings- en
hersterilisatiemethoden. Er is ook een verhoogde kans op verslechtering van de prestatie van het instrument als gevolg van herbewerkingsstappen, wat tot letsel bij de patiënt of
tot overlijden kan leiden.
• Het is belangrijk om de Gebruiksaanwijzing en deze voorzorgsmaatregelen zorgvuldig te lezen voordat u het instrument bedient.
• Gebruik de IBT vóór de op de verpakking vermelde uiterste gebruiksdatum.
• Niet gebruiken als de verpakking geopend of beschadigd is, omdat de integriteit van het product, inclusief de steriliteit, dan mogelijk niet meer intact is.
• Gebruik geen beschadigde producten. Inspecteer vóór gebruik de IBT en de verpakking om er zeker van te zijn dat er geen beschadiging is.
• Vóór gebruik dient te worden onderzocht of de IBT goed werkt en of de maat geschikt is voor de specifieke ingreep waarvoor de IBT gebruikt zal worden.
• Gebruik dit product niet als u niet goed in het gebruik ervan getraind bent. De IBT mag uitsluitend worden gebruikt door artsen die getraind zijn in de techniek van het gebruik
van bot-stoppers. Artsen die dit instrument gebruiken, dienen vertrouwd te zijn met de fysiologie en pathologie van de geselecteerde anatomische structuur.
• De IBT mag uitsluitend gemanipuleerd worden onder doorlichting met radiografische apparatuur die beelden van hoge kwaliteit geeft.
• De IBT mag uitsluitend worden gevuld met een vulspuit met een minimale inhoud van 14 ml.
• Vul de IBT uitsluitend met een vloeibaar contrastmiddel; een 60% oplossing wordt aanbevolen. Volg de aanwijzingen van de fabrikant voor indicaties en voorzorgsmaatregelen
inzake contrastmiddelen en het gebruik ervan.
• Gebruik nooit lucht of ander gas om de IBT te vullen.
• De vulkenmerken van de IBT zijn bij vullen in bot niet dezelfde.
• Het is uitdrukkelijk verboden om dit instrument te herconditioneren, te reviseren, te repareren, te modificeren of opnieuw te steriliseren om het langer te gebruiken.
• Aan elke operatie zijn risico’s verbonden; klinisch gezien vormt het gebruik van de ballon bij de behandeling van deze fracturen echter geen hoger risico in vergelijking met
traditionele methoden om ingedrukte botfragmenten omhoog te brengen. Deze risico’s omvatten:
o De fractuurfragmenten niet naar behoren kunnen zetten.
o Vertraagde botheling en niet-helende fractuur.
o Infectie.
o Neurovasculair letsel of compartimentsyndroom met als gevolg verlies van functie of amputatie.
NB: Een vulspuit van het merk Kyphon® verschaft superieur volumebeheersing vergeleken met andere vulsystemen zoals een standaardspuit en is vereist voor vullen van de IBT. Volg
de aanwijzingen van de fabrikant voor het gebruik van een vulspuit van het merk Kyphon®. De Kyphon® vergrendelbare injectiespuit is verpakt met de vulspuit met het merk Kyphon®.
ONGEWENSTE VOORVALLEN
Ongewenste voorvallen die mogelijk samenhangen met het gebruik van de IBT zijn onder meer ernstige voorvallen, die, hoewel zeldzaam, fataal kunnen zijn.
Ongewenste voorvallen zijn onder meer:
• Vetembolie, trombus of ander materiaal dat tot symptomatische longembolie of andere klinische complicaties leidt.
• Ruptuur met fragmentering van het vulbare deel van de IBT, waardoor een fragment in het getroffen gebied blijft zitten.
• Ruptuur van de IBT met blootstelling aan contrastmiddel, wat mogelijk tot een allergische reactie of anafylaxie leidt.
• Diepe of oppervlakkige wondinfectie.
• Bloeding of hematoom.
GEBRUIKSAANWIJZING
OPGELET: Volg de aanwijzingen van de fabrikant voor het gebruik van een vulspuit van het merk Kyphon®.
OPGELET: De viscositeit en precipitatie van contrastmiddelen kan verschillen, waardoor de vul- en leeglooptijden langzamer kunnen zijn. Om deze reden wordt gebruik van een
contrastmiddel van 60% aanbevolen.
1. Draai aan de dop op de stiletpoort om het stilet op de IBT vast te zetten. Duw de zuiger volledig in de Kyphon® vergrendelbare spuit. Bevestig de Kyphon® vergrendelbare spuit
aan de vulpoort op de IBT.
Importanti Informazioni sull’impattatore osseo gonfiabile
per la gestione delle fratture InflateFX™ (Misure 10/3 e 15/3)
Belangrijke Informatie Over de InflateFX™ vulbare bot-stopper
voor fractuurmanagement (maten 10/3 en 15/3)
2. Trek de zuiger van de Kyphon® vergrendelbare spuit naar achteren. Draai de zuiger om deze vast te zetten in de laatste sleuf in de spuit.
3. Maak de Kyphon® vergrendelbare spuit los van de IBT.
4. Bevestig de aansluitpoort op de slang van de vulspuit van het merk Kyphon® aan de vulpoort op de IBT. Het systeem is nu gereed voor gebruik.
GEBRUIK VAN DE IBT
1. Kies de IBT-maat op basis van de plaats en het doel van de behandeling. Afbeelding 1 en tabel 1 preciseren de diameter (D) en de lengte (L) van de gevulde IBT’s in water van 37
°C in vulvolumestappen tot het maximale vulvolume.
2. Deze afmetingen kunnen tijdens gebruik van het product variëren wegens plaatselijke variaties in de botstructuur.
Tabel 1 – afmetingen gevulde IBT (in water van 37 °C)
Modelnummer E103A Afmetingen in gevulde staat
Maat 10/3 Volume Gem diameter (D1, D2) Lengte (L)
Max. vulvolume 4 ml 2 ml 12,9 mm 14,7 mm
Max. vuldruk 27 atm 4 ml 17,2 mm 19,1 mm
Modelnummer E153A Afmetingen in gevulde staat
Maat 15/3 Volume Gem diameter (D1, D2) Lengte (L)
Max. vulvolume 4 ml 2 ml 12,1 mm 17,4 mm
Max. vuldruk 27 atm 4 ml 16 mm 22,1 mm
IBT INBRENGEN
1. Voor de plaatsing van de IBT is een toegangskanaal vereist.
2. Volg de gebruiksaanwijzing voor de gekozen instrumenten voor bottoegang om een toegangskanaal in het bot te maken.
3. Verwijder de inbrenghuls vóór gebruik.
NB: De distale tip van de lege IBT heeft het distale uiteinde van de canule bereikt als de uitgangsmarkering op het buitenlumen van de IBT het proximale uiteinde van de canule binnengaat.
4. Plaats de lege IBT in het toegangskanaal en breng deze onder beeldvorming in de juiste positie met behulp van de radiopake markeringen. Licht draaien bij het vooruitduwen kan
het inbrengen vergemakkelijken.
5. Terwijl u de IBT op zijn plaats houdt, vult u de IBT tot 0,3 MPa (3 atm.) om de IBT vast te zetten. Verwijder desgewenst het stilet.
IBT VULLEN
1. Vul de IBT onder continue beeldvorming. Gebruik het zijaanzicht om de afstand tot de voorste en de laterale cortex te bewaken. Gebruik het AP-aanzicht (anteroposterieure aanzicht)
om de laterale cortices te bewaken.
2. Als er geen continue beeldvorming wordt gebruikt, verhoogt u het volume in kleine stappen (0,25-0,5 ml). Beoordeel de positie van de stopper aan de hand van het zijaanzicht en
AP-aanzicht voordat u het volume verder verhoogt.
3. Stop wanneer het doel van de behandeling is bereikt, een deel van het gevulde gedeelte van de IBT het corticale bot raakt of het maximale vulvolume en/of de maximale vuldruk
is bereikt (zie tabel 1).
IBT VERWIJDEREN
OPGELET: Trek de IBT pas terug als het opblaasbare deel volledig is geleegd. Trek de IBT nooit terug als u weerstand ondervindt. Bepaal de oorzaak van de weerstand onder doorlichting
en neem de nodige maatregelen om het probleem te verhelpen.
Verwijder met een vulspuit van het merk Kyphon® het contrastmiddel uit de IBT totdat de ballon helemaal leeg is. Verwijder de IBT via de canule uit het bot met een lichte draaibeweging.
• Als er weerstand optreedt, sluit u een spuit van 30 ml aan op de vulpoort. Trek de zuiger van de injectiespuit terug naar het merkteken voor 30 ml om een vacuüm te trekken. Ga
verder met het verwijderen van de IBT.
• Controleer of het vulbare deel van de IBT in de canule is binnengegaan. Als het vulbare deel niet in de canule gaat, voert u de canule op over de IBT tot de proximale radiopake
markering. Na het opvoeren van de canule trekt u de IBT door de canule terug. Als u weerstand ondervindt, verwijdert u de IBT en de canule gelijktijdig.
STERILISATIE
Gesteriliseerd met bestraling.
WIJZE VAN LEVERING
De IBT’s worden steriel in een opentrekbare verpakking geleverd. Gebruik het instrument niet indien de steriele verpakking beschadigd is; waarschuw in dat geval de fabrikant.
NIETBIJGELEVERDE MATERIALEN
• Vulspuit van het merk Kyphon® met Kyphon® vergrendelbare injectiespuit
• Contrastmiddel (60%)
• Kleine kom
NB: De vulspuit van het merk Kyphon® met Kyphon® vergrendelbare injectiespuit is verkrijgbaar bij Medtronic.
OPSLAG
De IBT’s moeten in de oorspronkelijke verpakking worden bewaard. Er moeten adequate maatregelen worden getroffen om te verzekeren dat de IBT’s geen schade oplopen. Droog
en koel bewaren.
BEPERKING VAN AANSPRAKELIJKHEID
MEDTRONIC IS NIET VERANTWOORDELIJK VOOR DIRECTE, INDIRECTE OF INCIDENTELE SCHADE, GEVOLGSCHADE OF SMARTENGELD VOORTVLOEIEND UIT HERGEBRUIK VAN DE InflateFX™
VULBARE BOT-STOPPERS VOOR FRACTUURMANAGEMENT.
IN GEEN GEVAL IS MEDTRONIC AANSPRAKELIJK VOOR DIRECTE, INDIRECTE, INCIDENTELE, SPECIALE OF GEVOLGSCHADE VOORTVLOEIEND UIT OF IN VERBAND MET DE InflateFX™ VULBARE
BOT-STOPPERS VOOR FRACTUURMANAGEMENT, GEBASEERD OP CONTRACTBREUK (WAARONDER GARANTIEBREUK).
VERZOEK OM INFORMATIE
Voor nadere informatie neemt u contact op met de klantenservice.
©2013 Medtronic Sofamor Danek USA, Inc. Alle rechten voorbehouden.
DaNSK
BRUGSINDIKATIONER
InflateFX™ inflaterbart knogleindlæg til frakturbehandling (IBT) er beregnet til at blive anvendt som et traditionelt knogleindlæg til reduktion af frakturer og/eller oprettelse af et
hulrum i spongiosa i hånd, tibia, radius og calcaneous.
BESKRIVELSE AF ANORDNINGEN
Se figur 1.
1. Hætte
2. Stilet
3. Stiletport
4. Inflationsport
5. Farvekodet bånd
6. Udgangsmarkørbånd
7. Indføringshylster
8. Røntgenfaste markører
9. Oppustelig del
• Den oppustelige del af IBT er udformet til at komprimere spongiosa og/eller flytte kortikal knogle, mens den pustes op. Den oppustelige del af IBT findes nær den distale spids på
anordningen, som vist i figur 1.
• Skaftet indeholder to lumen, der ikke har forbindelse med hinanden. Det ydre lumen bruges til oppustning af IBT, og det centrale lumen indeholder en aftagelig, afstivende stilet
til indføring af IBT.
• Skaftets proksimale ende har en sidearmsadapter. Adapterens inflationsport grænser op til det ydre lumen. Stiletporten grænser op til det indre lumen og indeholder den afstivende
stilet. Stiletten har en hætte ved dens proksimale ende, som kan fjernes efter ønske.
• Det farvekodede bånd, der sidder lige distalt for sidearmsadapteren, angiver ballonens størrelse (dvs. gult bånd for størrelse 10/3 og et sort bånd for størrelse 15/3).
• Udgangsmarkørbåndet, der sidder på det ydre lumen, bruges under indføring af IBT.
• Røntgenfaste markører anbragt på den distale og proksimale ende af den deflaterede arbejdsoverflade, giver mulighed for fluoroskopisk visualisering af det deflaterede IBT under
positionering.
KONTRAINDIKATIONER
• Blødningsforstyrrelse eller behandling, der øger risikoen for overdreven blødning.
• Ved forekomst af aktiv eller ufuldstændig behandling af infektion på det sted, hvor knoglehulrumsfilleren skal anvendes.
• En hvilken som helst kendt svær allergi over for kontrastmateriale og knoglehulrumsfiller.
• Hvis patienten er konstateret gravid.
FORSIGTIG: I henhold til forbundslovgivningen i USA må denne anordning kun sælges af eller efter anvisning fra en læge.
ADVARSLER
• Hvis anordningen brækker, kan det kræve kirurgisk intervention eller fjernelse.
• Dette produkt må ikke anvendes efter udløbsdatoen (anvendes inden), der er trykt på emballagen. Anordningen kan være usikker eller ineffektiv efter udløbsdatoen (anvendes
inden).
• Den oppustelige komponent kan svigte på grund af små skarpe knoglefremspring eller kirurgiske instrumenter.
• Oppustning af IBT ud over den maksimale oppustningsvolumen kan forårsage, at ballonen springer, før den når det maksimale inflationstryk.
• Oppustning af IBT ud over det maksimale inflationstryk kan forårsage, at ballonen springer, før den når den maksimale oppustningsvolumen.
• Der må aldrig anvendes luft eller gasholdige materialer til at puste ballonen op.
FORHOLDSREGLER
• Det inflaterbare knogleindlæg er en engangsanordning, der er beregnet til kontakt med kropsvæv. Må ikke genbruges, genforarbejdes eller resteriliseres. Genbrug af disse anordninger
indebærer risiko for kontamination og kan forårsage infektion hos patienten eller krydsinfektion, uanset de anvendte rengørings- og resteriliseringsmetoder. Genbehandling
indebærer også øget risiko for forringelse af anordningens ydeevne, hvilket kan resultere i patientskade eller død.
• Det er vigtigt at læse brugsanvisningen og disse forholdsregler omhyggeligt, inden anordningen anvendes.
• Anvend IBT inden udløbsdatoen angivet på emballagen.
• Må ikke anvendes, hvis emballagen er åbnet eller beskadiget, fordi produktets integritet, herunder steriliteten, kan være kompromitteret.
• Beskadigede produkter må ikke anvendes. Undersøg IBT og emballagen inden brug for at sikre, at de ikke er blevet beskadiget.
• Inden brug bør IBT undersøges for at bekræfte funktionaliteten og for at sikre, at størrelsen er passende til den særlige procedure, den skal anvendes til.
• Du må ikke anvende dette produkt, hvis du ikke er korrekt uddannet. IBT bør kun anvendes af læger, som er uddannet i brug af knogleindlæg. Læger, som anvender anordningerne,
bør være fortrolige med de fysiologiske og patologiske karakteristika af den valgte anatomi.
• IBT bør kun manipuleres under fluoroskopisk opsyn med røntgenologisk udstyr, der giver billeder af høj kvalitet.
• IBT bør kun inflateres med en inflationssprøjte med en minimumskapacitet på 14 ml.
• IBT må kun inflateres med flydende kontraststof: der anbefales en 60 % opløsning. Følg producentens anvisninger for kontraststof mht. indikationer, anvendelse og forsigtighedsregler.
• Benyt ikke luft eller nogen anden gasart til inflation af IBT.
• Inflationsegenskaberne for IBT ændres ved inflation inde i knoglen.
• Ombygning, renovering, reparation, modificering eller resterilisering af anordningen for at muliggøre yderligere anvendelse er udtrykkeligt forbudt.
• Ethvert kirurgisk indgreb har risici, dog gælder, at brug af ballonen til behandlingen af disse frakturer ikke øger disse risici fra et klinisk synspunkt sammenlignet med traditionelle
elevationsmetoder til nedtrykte knoglefragmenter. Disse risici omfatter:
o Frakturfragmenterne bliver ikke reduceret rigtigt.
o Forsinket heling og ikke ikke-heling.
o Infektion.
o Neurovaskulær læsion eller hulrumssyndrom, der fører til funktionstab eller amputation.
BEMÆRK: En inflationssprøjte af mærket Kyphon® giver en suveræn mængdekontrol sammenlignet med andre inflationssystemer, som for eksempel en standardsprøjte, og er påkrævet
til oppustning af IBT. Følg producentens brugsanvisning til en inflationssprøjte af mærket Kyphon ®. Kyphon ® låsesprøjte er pakket med en inflationssprøjte af mærket Kyphon ®.
KOMPLIKATIONER
Komplikationer, der er potentielt forbundet med anvendelse af IBT omfatter alvorlige hændelser, som til trods for at de er sjældne kan være fatale.
Komplikationer omfatter:
• Fedtemboli, trombe eller andre materialer, der resulterer i symptomatisk lungeemboli eller andre kliniske følgetilstande.
• Ruptur med fragmentation af den oppustelige del af IBT, hvilket fører til retention af et fragment i det berørte område.
• Ruptur af IBT, der forårsager eksponering for kontraststof, som muligvis kan resultere i en allergisk reaktion eller anafylaksi.
• Dyb eller overfladisk sårinfektion.
• Blødning eller hæmatom.
BRUGSANVISNING
FORSIGTIG: Følg producentens brugsanvisning til en inflationssprøjte af mærket Kyphon ®.
FORSIGTIG: Kontraststoffer kan have forskellige viskositets- og udfældningsniveauer, som kan bevirke langsommere inflations- og deflationstider. Af denne årsag anbefales brug
af 60 % kontraststof.
1. Drej hætten på stiletåbningen for at fastgøre stiletten på IBT. Tryk stemplet hele vejen ind i Kyphon ® låsesprøjten. Sæt Kyphon ® låsesprøjten på inflationsporten på IBT.
2. Træk Kyphon ® låsesprøjtens stempel tilbage. Drej stemplet for at låse det i position på den sidste rille i sprøjten.
3. Afmonter Kyphon ® låsesprøjten fra IBT.
4. Tilslut forbindelsesporten på inflationssprøjteslangen af mærket Kyphon ® til inflationsporten på IBT. Systemet er nu forberedt og klar til brug.
BRUG AF IBT
1. Vælg størrelse af IBT baseret på stedet og formålet med behandlingen. Figur 1 og tabel 1 definerer den inflaterede diameter (D) og den inflaterede længde (L) af IBT i 37 °C varmt
vand ved stigninger i inflationsvolumen til den maksimale inflationsvolumen.
2. Disse dimensioner kan variere under brug af produktet på grund af lokale forskelle i knoglestrukturen.
Tabel 1 – IBT inflaterede dimensioner (i 37 °C varmt vand)
Modelnummer E103A Inflaterede dimensioner
Størrelse 10/3 Volumen Gennemsnitlig diameter (D1, D2) Længde (L)
Maks. inflationsvolumen 4 ml 2 ml 12,9 mm 14,7 mm
Maks. inflationstryk 27 ATM 4 ml 17,2 mm 19,1 mm
Modelnummer E153A Inflaterede dimensioner
Størrelse 15/3 Volumen Gennemsnitlig diameter (D1, D2) Længde (L)
Maks. inflationsvolumen 4 ml 2 ml 12,1 mm 17,4 mm
Maks. inflationstryk 27 ATM 4 ml 16 mm 22,1 mm
INDFØRING AF IBT
1. Der kræves en adgangskanal ved placering af IBT.
2. Følg brugsanvisningen til det valgte knogleadgangsudstyr for at skabe en adgangskanal i knoglen.
3. Fjern indføringshylstret inden brug.
BEMÆRK: Den distale spids på det deflaterede IBT har nået den distale ende af kanylen, når udgangsmarkøren på IBTs ydre lumen føres ind i kanylens proksimale ende.
4. Anbring det deflaterede IBT i adgangskanalen, og positionér det under billedovervågning ved hjælp af de røntgenfaste markører. En forsigtig drejende bevægelse, mens der skubbes
fremad, kan hjælpe ved indføringen.
5. Mens IBT holdes på plads, inflateres den til 3 ATM (0,3 MPa) for at sikre IBT forsvarligt i position. Fjern stiletten, hvis det ønskes.
INFLATION AF IBT
1. Inflatér IBT under kontinuerlig billedovervågning. Benyt det laterale billede til at overvåge afstanden fra den anteriore og laterale cortex. Benyt AP (anteroposterior)-billedet til at
overvåge de laterale cortex.
2. Hvis der ikke anvendes kontinuerlig billedovervågning, øges volumen med små stigninger (0,25-0,5 ml). Vurdér knogleindlæggets position i det laterale billede og AP-billedet,
inden der fortsættes med yderligere volumenøgning.
3. Stop, når behandlingsmålet er nået, eller enhver del af den inflaterede længde af IBT berører cortikal knogle eller maksimal inflationsvolumen, og/eller maksimalt inflationstryk
er opnået (Se tabel 1).
FJERNELSE AF IBT
FORSIGTIG: Træk ikke IBT ud, medmindre den inflaterbare komponent er helt deflateret. Træk aldrig IBT ud, hvis der er modstand. Afgør årsagen til modstand under fluoroskopi, og
foretag de nødvendige foranstaltninger til afhjælpning.
Brug en inflationssprøjte af mærket Kyphon® til at tømme kontraststoffet fra IBT, indtil ballonen er helt deflateret. Fjern IBT fra knoglen gennem kanylen med en forsigtig drejende bevægelse.
• Hvis der er modstand, tilsluttes en 30 ml sprøjte til inflationsporten. Træk sprøjtestemplet tilbage til ”30ml”-mærket for at skabe et vakuum. Genoptag fjernelse af IBT.
• Bekræft, at den inflaterbare del af IBT er ført ind i kanylen. Hvis ikke den inflaterbare del føres ind i kanylen, skal kanylen føres frem over IBT til den proksimale røntgenfaste markør.
Efter fremføring af kanylen trækkes IBT tilbage gennem kanylen. Hvis der bemærkes modstand, fjernes IBT og kanylen samtidigt.
STERILISATION
Steriliseret med bestråling.
LEVERING
IBT leveres sterilt i en emballage, der kan skrælles af. I tilfælde af beskadigelse af den sterile emballage må indholdet ikke bruges, og producenten skal underrettes.
MATERIALER, SOM IKKE MEDFØLGER
• Inflationssprøjte af mærket Kyphon® med Kyphon® låsesprøjte
• Kontraststof (60 %)
• Lille skål
BEMÆRK: Inflationssprøjte af mærket Kyphon® med Kyphon® låsesprøjte kan fås hos Medtronic.
OPBEVARING
IBT bør opbevares i den oprindelige emballage. Det bør omhyggeligt sikres, at IBT ikke beskadiges. Opbevares på et køligt, tørt sted.
ANSVARSBEGRÆNSNING
MEDTRONIC ER IKKE ANSVARLIG FOR NOGEN DIREKTE, INDIREKTE, RESULTERENDE ELLER EKSEMPLARISKE BESKADIGELSER, DER ER FORÅRSAGET AF GENBRUG AF InflateFX™ INFLATERBARE
KNOGLEINDLÆG TIL FRAKTURBEHANDLING.
PÅ INTET TIDSPUNKT VIL MEDITRONIC VÆRE ANSVARLIG FOR NOGEN DIREKTE, INDIREKTE ELLER RESULTERENDE ELLER EKSEMPLARISKE BESKADIGELSER, DER ER OPSTÅET SOM FØLGE AF
ELLER I FORBINDELSE MED InflateFX™ INFLATERBARE KNOGLEINDLÆG TIL FRAKTURBEHANDLING, DER SKYLDES KONTRAKTBRUD (HERUNDER GARANTIBRUD).
YDERLIGERE OPLYSNINGER
Yderligere oplysninger kan fås ved at rette henvendelse til kundeservice.
©2013 Medtronic Sofamor Danek USA, Inc. Alle rettigheder forbeholdes.
SVENSKa
INDIKATIONER
InflateFX™ Frakturbehandling med uppblåsbar benballong (IBT) är avsedd att användas som konventionell benballong för att minska frakturer och/eller för att skapa ett tomrum i det
spongiösa benet i handen, tibia, radius och kalkaneus.
PRODUKTBESKRIVNING
Se figur 1.
1. Lock
2. Mandräng
3. Mandrängport
4. Uppblåsningsport
5. Band med färgkod
6. Utträdesmarkör
7. Införingshylsa
8. Röntgentäta markeringar
9. Fyllningsbar komponent
• Den fyllningsbara delen av IBT är avsedd att komprimera spongiös benvävnad och/eller flytta på kortikalt ben allt eftersom delen fylls. IBT:s fyllningsbara komponent är belägen
nära anordningens distala spets enligt figur 1.
• Skaftet innehåller två icke-kommunicerande lumen. Det yttre lumen används för uppblåsning av IBT och den centrala lumen innehåller en borttagbar förstyvningsmandräng för
införande av IBT.
• Skaftets proximala ände har en sidoarmsadapter. Adapterns uppblåsningsport gränsar till det yttre lumen. Mandrängporten gränsar till den inre lumen och innehåller
förstyvningsmandrängen. Mandrängens proximala ände har ett lock som kan tas bort, om så önskas.
• Det färgkodade bandet som sitter alldeles distalt om sidoarmsadaptern anger ballongstorleken (dvs. ett gult band för storlek 10/3 och ett svart band för storlek 15/3).
• Utträdesmarkören på det yttre lumen används under IBT-införing.
• Röntgentäta markeringar vid den distala och proximala änden av den icke fyllda arbetsytan möjliggör fluoroskopisk visualisering av den icke fyllda IBT under placeringen.
KONTRAINDIKATIONER
• Blödningsrubbningar eller behandling som ökar risken för kraftiga blödningar.
• Vid aktiv eller ofullbordad behandling av infektion vid det ställe där benutfyllnaden ska appliceras.
• Känd allvarlig allergi mot kontrastmaterial och benutfyllnad.
• Patienten är bekräftat gravid.
VIKTIGT! Enligt federal lagstiftning (USA) får detta instrument endast säljas av läkare eller på läkares ordination.
VARNINGAR
• Om anordningen går sönder kan kirurgiskt ingrepp eller hämtning krävas.
• Produkten får inte användas efter det utgångsdatum som finns tryckt på förpackningen. Anordningen är eventuellt inte säker eller effektiv efter dess utgångsdatum.
• Den fyllningsbara delen kan förlora sin funktion på grund av benflisor eller kirurgiska instrument.
• Om IBT fylls till mer än den maximala uppblåsningsvolymen kan ballongen spricka innan den når det maximala uppblåsningstrycket.
• Om IBT fylls till mer än den maximala uppblåsningstrycket kan ballongen spricka innan den når det maximala uppblåsningsvolymen.
• Använd aldrig gas eller gasliknande material för att fylla ballongen.
FÖRSIKTIGHETSÅTGÄRDER
• Den uppblåsbara benballongen är en anordning för engångsbruk avsedd att komma i kontakt med kroppsvävnad. Får inte återanvändas, ombearbetas eller omsteriliseras.
Återanvändning av instrumenten medför risk för kontamination och kan orsaka infektion eller korsinfektion hos patienten, oavsett rengörings- och omsteriliseringsmetoder. Det
finns även en ökad risk för försämring av anordningens prestanda på grund av ombehandlingsåtgärder, som kan orsaka skada eller dödsfall hos patienten.
• Det är viktigt att noga läsa igenom bruksanvisningen och dessa försiktighetsåtgärder före användning av anordningen.
• Använd IBT före den sista förbrukningsdag som står på förpackningen.
• Får inte användas om förpackningen har öppnats eller skadats eftersom produktens integritet, inklusive sterilitet, kan ha försämrats.
• Använd inte skadade produkter. Före användning skall du undersöka IBT och förpackningen och bekräfta att skador inte har uppstått.
• Före användning skall du undersöka IBT och bekräfta dess funktionsduglighet samt säkerställa att storleken är lämplig för det specifika förfarande som instrumentet skall användas
i.
• Använd inte produkten om du inte har rätt utbildning för dess användning. IBT bör endast användas av läkare som är utbildade i benballongteknik. Läkare som använder instrumenten
bör känna till den utvalda anatomins fysiologi och patologi.
• IBT bör endast manövreras under fluoroskopisk observation med radiografisk utrustning som ger bilder av hög kvalitet.
• IBT bör endast blåsas upp med en uppblåsningsspruta med minst 14 ml volymkapacitet.
• Fyll endast IBT med flytande kontrastmedel: en 60-procentig lösning rekommenderas. Följ tillverkarens instruktioner för indikationer, användning och varningar för kontrastmedlet.
• Använd inte luft eller annan gas för att fylla IBT.
• IBT:s uppblåsningsegenskaper förändras vid fyllning inuti ben.
• Renovering, reparation, ändring eller omsterilisering av instrumentet för att möjliggöra ytterligare användning är uttryckligen förbjudet.
• All kirurgi utgör risker. Användning av ballongen vid behandling av de här frakturerna innebär emellertid ingen ökning av riskerna ur en klinisk synvinkel jämfört med traditionella
metoder för att höja nedtryckta benfragment. Dessa risker inkluderar:
o Misslyckad minskning av frakturfragmenten.
o Fördröjd hopläkning eller avsaknad hopläkning.
o Infektion.
o Neurovaskulär skada eller kompartmentsyndrom som leder till funktionsförlust eller amputation.
OBS! Kyphon®uppblåsningsspruta ger bättre volymkontroll jämfört med andra uppblåsningssystem, såsom en vanlig spruta, och krävs för att blåsa upp IBT. Följ tillverkarens instruktioner
för användning av en Kyphon® uppblåsningsspruta. Kyphon® låsningsspruta förpackas tillsammans med en Kyphon® uppblåsningsspruta.
BIVERKNINGAR
Biverkningar som potentiellt förknippas med användning av IBT inklusive allvarliga händelser som, även om de är sällsynta, kan leda till döden.
Biverkningar inkluderar:
• Embolier av fett, koagel och andra material, vilka resulterar i symtomatiska lungembolier eller andra kliniska följdtillstånd.
• Ruptur med fragmentering av den fyllningsbara delen av IBT, som resulterar i retention av ett fragment i det berörda området.
• Ruptur av IBT som orsakar att kontrastmedel exponeras och eventuellt resulterar i en allergisk reaktion eller anafylaxi.
• Djup eller ytlig sårinfektion.
• Blödning eller hematom.
BRUKSANVISNING
VIKTIGT! Följ tillverkarens instruktioner för användning av en Kyphon® uppblåsningsspruta.
VIKTIGT! Kontrastmedel kan ha olika viskositets- och utfällningsnivåer vilket kan orsaka längre uppblåsnings- och tömningstider. Av denna anledning rekommenderas 60 % kontrastmedel.
1. Vrid på locket på mandrängporten för att dra åt mandrängen på IBT. Tryck in kolven i Kyphon® låsningsspruta så långt det går. Fäst Kyphon® låsningsspruta vid uppblåsningsporten
på IBT.
Vigtige Oplysninger Om InflateFX™ inflaterbart knogleindlæg
til frakturbehandling (størrelse 10/3 og 15/3)
Viktig Information Om InflateFX™ Frakturbehandling med
uppblåsbar benballong (Storlekar 10/3 och 15/3)
2. Dra tillbaka kolven på Kyphon® låsningsspruta. Vrid kolven så att den låses fast på plats i sprutans sista spår.
3. Koppla bort Kyphon® låsningsspruta från IBT.
4. Anslut anslutningsporten på Kyphon® uppblåsningssprutans slang till på IBT. Systemet har nu förberetts och är färdigt att användas.
ANVÄNDA IBT
1. Välj storlek på IBT efter användningsställe och behandlingssyfte. I figur 1 och tabell 1 anges diametern (D) i fyllt tillstånd och längden (L) i fyllt tillstånd för IBT i 37 °C vatten vid
ökande uppblåsningsvolymer upp till den maximala uppblåsningsvolymen.
2. Dessa dimensioner kan variera vid användning av produkten på grund av variationer i benstruktur.
Tabell 1 – IBT Storlek i fyllt tillstånd (i 37 °C vatten)
Modellnummer E103A Storlek i fyllt tillstånd
Storlek 10/3 Volym Genomsn. diameter (D1, D2) Längd (L)
Max. uppblåsningsvolym 4 ml 2 ml 12,9 mm 14,7 mm
Max. uppblåsningstryck 27 atm 4 ml 17,2 mm 19,1 mm
Modellnummer E153A Storlek i fyllt tillstånd
Storlek 15/3 Volym Genomsn. diameter (D1, D2) Längd (L)
Max. uppblåsningsvolym 4 ml 2 ml 12,1 mm 17,4 mm
Max. uppblåsningstryck 27 atm 4 ml 16 mm 22,1 mm
IBTINFÖRING
1. En åtkomstkanal krävs för IBT-placering.
2. Följ bruksanvisningen för valt benåtkomstinstrument för att skapa en åtkomstkanal in i benet.
3. Ta bort införingshylsan före användning.
OBS! Den distala spetsen på den tömda IBT har nått kanylens distala ände när utträdesmarkören på IBT:s ytterlumen kommer in i den proximala änden av kanylen.
4. Placera den tömda IBT i åtkomstkanalen och placera den i läge under bildledning med användning av de röntgentäta markeringarna. En lätt vridande rörelse under framåtskjutningen
kan underlätta införingen.
5. Håll IBT på plats och utvidga ballongen till 0,3 MPa (3 atm) för att hålla IBT på plats. Avlägsna mandrängen om så önskas.
IBTFYLLNING
1. Fyll IBT under kontinuerlig bildledning. Använd sidovyn för att kontrollera avståndet från anterior och lateral cortex. Använd den anteroposteriora vyn (AP-vyn) för att övervaka
laterala barkar.
2. Om kontinuerlig röntgengenomlysning inte används skall volymen ökas i små steg (0,25-0,5 ml). Bedöm packarballongens läge i lateral vy och i AP-vy före ytterligare volymökning.
3. Avbryt när behandlingsmålet har uppnåtts, dvs. när någon del av IBT:s uppblåsta längd kommer i kontakt med kortikalt ben eller när maximal uppblåsningsvolym och/eller maximalt
uppblåsningstryck har uppnåtts (se tabell 1).
AVLÄGSNANDE AV IBT
VIKTIGT! Dra inte tillbaka IBT innan den uppblåsbara komponenten är fullständigt tömd. Dra aldrig tillbaka IBT vid motstånd. Ta reda på orsaken till motståndet med fluoroskopi och
vidtag nödvändiga åtgärder.
Använd en Kyphon® uppblåsningsspruta och töm ut kontrastmedlet från IBT tills ballongen är helt tömd. Avlägsna IBT från benet genom kanylen med en lätt vridrörelse.
• Om det uppstår motstånd ska en 30 ml spruta anslutas till uppblåsningsporten. Dra tillbaka sprutans kolv till 30 ml markeringen så att vakuum skapas. Fortsätt med att ta bort IBT.
• Bekräfta att den uppblåsbara delen av IBT har förts in i kanylen. Om den uppblåsbara komponenten inte går in i kanylen förs kanylen fram över IBT till den proximala röntgentäta
markören. När kanylen har förts fram skall IBT dras tillbaka genom kanylen. Om motstånd märks skall IBT och kanyl avlägsnas samtidigt.
STERILISERING
Steriliserad med strålning.
LEVERANSFORM
IBT:erna levereras steril i en peel open-förpackning. Informera tillverkaren om sterilförpackningen är skadad. Använd ej skadade produkter.
ICKE MEDFÖLJANDE MATERIAL
• Kyphon® uppblåsningsspruta med Kyphon® låsningsspruta
• Kontrastmedel (60 %)
• Liten skål
OBS! Kyphon® uppblåsningsspruta med Kyphon® låsningsspruta levereras av Medtronic LLC.
FÖRVARING
IBT:er bör förvaras i det ursprungliga leveransmaterialet. Lämplig försiktighet bör iakttas för att säkerställa att IBT:er inte skadas. Förvaras svalt och torrt.
ANSVARSBEGRÄNSNING
MEDTRONIC ÄR INTE ANSVARIGT FÖR DIREKTA, INDIREKTA, OFÖRUTSEDDA ELLER EFTERFÖLJANDE SKADOR, ELLER FÖR SKADESTÅND I AVSKRÄCKANDE SYFTE FÖR SKADOR SOM UPPSTÅR
VID ÅTERANVÄNDNING AV InflateFX™ FRAKTURBEHANDLING MED UPPBLÅSBARA BALLONGER.
UNDER INGA OMSTÄNDIGHETER ÄR MEDTRONIC ANSVARIGT FÖR DIREKTA, INDIREKTA, OFÖRUTSEDDA, EFTERFÖLJANDE ELLER FÖR SKADESTÅND I AVSKRÄCKANDE SYFTE, SOM UPPSTÅR
GENOM, ELLER I SAMBAND MED InflateFX™ FRAKTURBEHANDLING MED UPPBLÅSBARA BALLONGER, BASERAT PÅ KONTRAKTSBROTT (INKLUSIVE GARANTIBROTT).
BEGÄRAN OM INFORMATION
För mer information, kontakta kundtjänst.
©2013 Medtronic Sofamor Danek USA, Inc. Med ensamrätt.
NorSK
INDIKASJONER FOR BRUK
InflateFX™ inflaterbar bentamper for frakturbehandling (IBT) er tiltenkt for bruk som en konvensjonell bentamper for å redusere frakturer og/eller danne et hulrom i spongiøst ben i
manus, tibia, radius og calcaneum.
BESKRIVELSE AV ENHETEN
Se figur 1.
1. Hette
2. Stilett
3. Stilettport
4. Inflasjonsport
5. Fargekodet bånd
6. Utløpsmarkørbånd
7. Innføringshylse
8. Røntgentette markører
9. Inflaterbar komponent
• Den inflaterbare komponenten i bentamperen er laget for å presse sammen spongiøst ben og/eller bevege på kortikalt ben mens den inflateres. Den inflaterbare komponenten i
bentamperen sitter nær den distale spissen på enheten som vist i figur 1.
• Skaftet inneholder to ikke-forbundne lumen. Det ytre lumen brukes til inflatering av bentamperen, og det sentrale lumen inneholder en avtakbar avstivningsstilett til innsetting
av bentamperen.
• Den proksimale enden av skaftet har en sidearmsadapter. Inflasjonsporten i adapteren grenser opp til det ytre lumen. Stilettporten grenser opp til det indre lumen og inneholder
avstivningsstiletten. Stiletten har en hette på den proksimale enden som kan fjernes.
• Det fargekodede båndet som sitter like distalt for sidearmsadapteren, angir ballongstørrelsen (dvs. et gult bånd for 10/3-størrelsen og et svart bånd for 15/3- størrelsen).
• Utløpsmarkørbåndet sitter på det ytre lumen og brukes ved innsetting av bentamperen.
• De røntgentette markørene på den distale og proksimale enden av den deflaterte arbeidsflaten gjør det mulig å se den deflaterte bentamperen når den plasseres ved hjelp av
gjennomlysning.
KONTRAINDIKASJONER
• Blødningsforstyrrelse eller behandling som øker faren for kraftig blødning.
• Ved en aktiv eller ufullstendig behandlet infeksjon på stedet hvor fyllmaterialet for benhulrom skal påføres.
• Eventuell kjent kraftig allergi overfor kontrastmiddel og fyllmateriale for benhulrom.
• Det er bekreftet at pasienten er gravid.
OBS! Ifølge føderale lover i USA må dette produktet kun selges av leger eller etter anvisning av leger.
ADVARSLER
• Brudd på utstyret kan føre til kirurgisk intervensjon eller uthenting.
• Ikke bruk dette produktet etter utløpsdatoen (brukes innen) som er trykt på pakken. Enheten er muligens verken sikker eller effektiv etter utløpsdatoen (brukes innen).
• Den inflaterbare komponenten kan svikte på grunn av skarpe benspisser eller kirurgiske instrumenter.
• Hvis den inflaterbare bentamperen inflateres med mer enn maksimalt inflateringsvolum, kan det føre til at ballongen revner før maksimalt inflateringstrykk nås.
• Hvis den inflaterbare bentamperen inflateres med mer enn maksimalt inflateringstrykk, kan det føre til at ballongen revner før maksimalt inflateringsvolum nås.
• Bruk aldri luft eller gass til å inflatere ballongen.
FORHOLDSREGLER
• Den inflaterbare bentamperen er en enhet for engangsbruk som er tiltenkt for kontakt med kroppsvev. Må ikke gjenbrukes, reprosesseres eller resteriliseres. Gjenbruk av disse
enhetene innebærer en risiko for kontaminasjon og kan forårsake pasientinfeksjon eller kryssinfeksjon, uansett hvilken rengjørings- og resteriliseringsmetode som brukes. Det er
også en økt risiko for at anordningens ytelse reduseres som følge av trinnene som inngår i bearbeidingen for gjenbruk, noe som kan medføre skade eller død for pasienten.
• Det er viktig å lese bruksanvisningen og disse forholdsreglene nøye før enheten tas i bruk.
• Bruk bentamperen før brukes innen-datoen som er angitt på pakken.
• Skal ikke brukes hvis pakken er åpnet eller skadet, da dette kan tyde på at produktet ikke er sterilt eller at det ikke er intakt.
• Skadde produkter skal ikke brukes. Før bentamperen tas i bruk, skal den, samt emballasjen, inspiseres for eventuelle skader.
• Før bentamperen tas i bruk, må den kontrolleres med hensyn til funksjonalitet og for å sikre at størrelsen passer til den spesifikke prosedyren den er tiltenkt.
• Ikke bruk dette produktet hvis du ikke har fått relevant opplæring. Bentamperen skal kun brukes av leger som har erfaring med bentamperteknikker. Leger som bruker utstyret,
skal ha inngående kjennskap til fysiologien og patologien til den aktuelle anatomien.
• Bentamperen skal kun brukes ved hjelp av gjennomlysning med radiografisk utstyr som gir høy bildekvalitet.
• Bentamperen skal kun inflateres ved hjelp av en inflasjonssprøyte med minimum 14 ml volumkapasitet.
• Bare inflater bentamperen med flytende kontrastmiddel: En løsning på 60 % anbefales. Følg produsentens instruksjoner når det gjelder indikasjoner for kontrastmiddel, bruk og
forholdsregler.
• Bruk aldri luft eller gass til å inflatere bentamperen.
• Inflateringsegenskapene til bentamperen endres ved inflatering inne i benet.
• Det er spesielt forbudt å rekondisjonere, pusse opp, reparere, endre eller resterilisere instrumentet.
• Ethvert inngrep medfører risikoer; fra et klinisk ståsted øker imidlertid ikke disse risikoene når ballongen brukes til behandling av disse frakturene sammenlignet med tradisjonelle
metoder for å heve de senkede benfragmentene. Disse risikoene omfatter:
o Manglende evne til å redusere frakturfragmentene ordentlig.
o Forsinket eller manglende sammenføyning.
o Infeksjon.
o Nevrovaskulær skade eller kompartmentsyndrom som fører til funksjonstap eller amputasjon.
MERKNAD: En Kyphon®-merket inflasjonssprøyte gir overlegen volumkontroll sammenlignet med andre inflasjonssystemer, for eksempel en standardsprøyte, og er påkrevd til inflatering
av bentamperen. Følg produsentens bruksanvisning for en Kyphon®-merket inflasjonssprøyte. Kyphon®-låsesprøyten er pakket sammen med en Kyphon®-merket inflasjonssprøyte.
UØNSKEDE HENDELSER
Uønskede hendelser som potensielt er knyttet til bruken av den inflaterbare bentamperen, omfatter alvorlige hendelser. Selv om disse sjelden oppstår, kan de være dødelige. Uønskede
hendelser omfatter:
• Emboli forårsaket av fett, trombe eller andre materialer som resulterer i symptomatisk lungeemboli eller andre kliniske sekveler.
• Ruptur med fragmentering av den inflaterbare bentamperens inflaterbare del, som fører til at et fragment blir sittende fast inne i det berørte området.
• Ruptur av bentamperen som forårsaker eksponering for kontrastmidlet, noe som kan føre til en allergisk reaksjon eller anafylaksi.
• Dyp eller overfladisk sårinfeksjon.
• Blødning eller hematom.
BRUKSANVISNING
OBS! Følg produsentens bruksanvisning for en Kyphon®-merket inflasjonssprøyte.
OBS! Kontrastmidler kan ha varierende viskositet og presipitasjonsnivåer som kan føre til langsommere inflatering og deflatering. Av denne grunn anbefales bruk av 60 % kontrastmiddel.
1. Vri hetten på stilettporten for å stramme stiletten på bentamperen. Skyv stemplet helt inn i Kyphon®-låsesprøyten. Fest Kyphon®-låsesprøyte til inflasjonsporten på bentamperen.
2. Trekk tilbake stemplet i Kyphon®-låsesprøyten. Drei på stemplet slik at det låses på plass i det siste sporet på sprøyten.
3. Koble Kyphon®-låsesprøyte fra bentamperen.
4. Fest tilkoblingsporten på den Kyphon®-merkede inflasjonssprøyteslangen til inflasjonsporten på bentamperen. Systemet er nå klargjort og klart til bruk.
BRUK AV BENTAMPEREN
1. Velg bentamperstørrelse basert på stedet og målet for behandlingen. Figur 1 og tabell 1 angir den inflaterte diameteren (D) og den inflaterte lengden (L) til inflaterbare bentampere
i vann på 37 °C i volumtrinn opp til maksimum inflatert volum.
2. Disse dimensjonene kan variere med bruken av produktet på grunn av lokale variasjoner i benstrukturen.
Tabell 1 – Inflaterte dimensjoner (i vann på 37 °C)
Modellnummer E103A Inflaterte dimensjoner
Størrelse 10/3 Volum Gj.snittlig diameter
(D1, D2) Lengde (L)
Maks. inflasjonsvolum 4 ml 2 ml 12,9 mm 14,7 mm
Maks. inflasjonstrykk 27 atm 4 ml 17,2 mm 19,1 mm
Modellnummer E153A Inflaterte dimensjoner
Størrelse 15/3 Volum Gj.snittlig diameter
(D1, D2) Lengde (L)
Maks. inflasjonsvolum 4 ml 2 ml 12,1 mm 17,4 mm
Maks. inflasjonstrykk 27 atm 4 ml 16 mm 22,1 mm
SETTE INN BENTAMPEREN
1. Det kreves en tilgangskanal for plassering av bentamperen.
2. Følg bruksanvisningen for de valgte bentilgangsverktøyene for å lage en tilgangskanal inn i benet.
3. Fjern innføringshylsen før bruk.
MERKNAD: Den distale spissen på den deflaterte bentamperen har nådd den distale enden på kanylen når utløpsmarkøren på bentamperens ytre lumen kommer inn i den proksimale
enden på kanylen.
4. Plasser den deflaterte bentamperen i tilgangskanalen og plasser den under bildeveiledning ved bruk av de røntgentette markørene. En forsiktig skrubevegelse samtidig med
skyving framover kan gjøre innsettingen enklere.
5. Hold bentamperen på plass og inflater til 0,3 MPa (3 atm) for å feste bentamperen på riktig sted. Fjern stiletten etter ønske.
INFLATERE BENTAMPEREN
1. Inflater bentamperen under kontinuerlig bildeveiledning. Bruk lateral visning for å overvåke avstanden fra anterior og lateral cortex. Bruk AP-visning (anterior-posterior) for å
overvåke laterale cortices.
2. Hvis det ikke benyttes kontinuerlig avbildning, må volumet økes i små inkrementer (0,25–0,5 ml). Vurder bentamperposisjonen ved lateral- og AP-visning før volumet økes
ytterligere.
3. Stopp når målet for behandlingen er nådd eller noen del av bentamperens inflaterte lengde kommer i kontakt med kortikalbenet eller maksimalt inflasjonsvolum og/eller maksimalt
inflasjonstrykk er nådd (se tabell 1).
FJERNE BENTAMPEREN
OBS! Ikke trekk ut den inflaterbare bentamperen hvis ikke den inflaterbare komponenten er helt tømt. Bentamperen må aldri trekkes ut hvis det oppstår motstand. Fastslå årsaken til
motstanden ved hjelp av gjennomlysning og ta nødvendige forholdsregler.
Bruk en Kyphon®-merket inflasjonssprøyte for å tømme ut kontrastmiddelet fra bentamperen inntil ballongen er helt deflatert. Fjern bentamperen fra benet gjennom kanylen med
en forsiktig skrubevegelse.
• Hvis det finnes motstand, kobler du en 30 ml sprøyte til inflasjonsporten. Trekk sprøytestempelet tilbake til «30ml»-merket for å danne et vakuum. Fortsett å fjerne bentamperen.
• Bekreft at den inflaterbare delen av bentamperen har kommet inn i kanylen. Hvis de inflaterbare komponentene ikke kommer inn i kanylen, føres kanylen over bentamperen til den
proksimale røntgentette markøren. Mens kanylen føres fram, trekkes bentamperen tilbake gjennom kanylen. Hvis det oppstår motstand, fjernes bentamperen og kanylen samtidig.
STERILISERING
Sterilisert med bestråling.
LEVERINGSMÅTE
Bentamperne leveres sterile i en peel-open-pakke. Ved eventuell skade på den sterile emballasjen, skal produktet ikke brukes og produsenten underrettes.
UTSTYR SOM IKKE FØLGER MED I PAKKEN
• Kyphon®-merket inflasjonssprøyte med Kyphon® låsesprøyte
• Kontrastmiddel (60 %)
• Liten skål
MERKNAD: Kyphon®-merket inflasjonssprøyte med Kyphon® låsesprøyte er tilgjengelig fra Medtronic.
OPPBEVARING
Bentampere skal oppbevares i originalemballasjen. Vær nøye med å påse at bentamperne ikke vil bli skadet. Oppbevares tørt og kjølig.
ANSVARSBEGRENSNING
MEDTRONIC ER IKKE ANSVARLIG FOR NOEN DIREKTE, INDIREKTE, TILFELDIGE ELLER FØLGEMESSIGE SKADER ELLER STRAFFEERSTATNINGER SOM OPPSTÅR FRA GJENBRUK AV InflateFX™
INFLATERBARE BENTAMPERE FOR FRAKTURBEHANDLING.
UNDER INGEN OMSTENDIGHET SKAL MEDTRONIC VÆRE ANSVARLIG FOR NOEN DIREKTE, INDIREKTE, TILFELDIGE ELLER FØLGEMESSIGE SKADER ELLER STRAFFEERSTATNINGER SOM OPPSTÅR
FRA, ELLER I FORBINDELSE MED, InflateFX™ INFLATERBARE BENTAMPERE FOR FRAKTURBEHANDLING, BASERT PÅ KONTRAKTBRUDD (INKLUDERT GARANTIBRUDD).
ANMODNING OM INFORMASJON
For mer informasjon ber vi deg kontakte kundeservice.
©2013 Medtronic Sofamor Danek USA, Inc. Ettertrykk forbudt.
SUoMI
KÄYTTÖAIHEET
Täytettävä InflateFX™-luuntiivistin murtumien hoitoon (IBT) on tarkoitettu käytettäväksi tavanomaisena luuntiivistimenä murtumien reduktiossa ja/tai onteloiden muodostamisessa
käden, sääriluun, värttinäluun ja kantaluun hohkaluuhun.
INSTRUMENTIN KUVAUS
Katso kuvaa 1.
1. Hattu
2. Mandriini
3. Mandriiniportti
4. Täyttöportti
5. Värikoodattu rengas
6. Poistumismerkkirengas
7. Sisäänvientiholkki
8. Röntgenpositiiviset merkit
9. Täytettävä osa
• Täytettävän luuntiivistimen täytettävä osa on tarkoitettu tiivistämään hohkaluuta ja/tai siirtämään kortikaaliluuta laajetessaan. Luuntiivistimen täytettävä osa on lähellä välineen
distaalikärkeä kuvan 1 osoittamalla tavalla.
• Varressa on kaksi erillistä luumenia. Ulompaa luumenia käytetään luuntiivistimen täyttämiseen ja keskellä olevassa luumenissa on irrotettava jäykistävä mandriini luuntiivistimen
sisäänvientiä varten.
• Varren proksimaalipäässä on sivuhaaraliitin. Liittimen täyttöportti on yhteydessä ulompaan luumeniin. Mandriiniportti on yhteydessä sisäluumeniin ja sen sisällä on jäykistävä
mandriini. Mandriinin proksimaalipäässä on hattu mahdollista poistamista varten.
• Värikoodattu rengas, joka sijaitsee hieman distaalisesti sivuhaaraliittimestä, osoittaa pallon kokoa (ts. keltainen rengas: koko 10/3, musta rengas: koko 15/3).
• Ulomman luumenin poistumismerkkirengasta käytetään luuntiivistimen sisäänviennin yhteydessä.
• Tyhjennetyn työskentelypinnan distaali- ja proksimaalipäissä sijaitsevien röntgenpositiivisten merkkien avulla tyhjennettyä luuntiivistintä voidaan tarkkailla läpivalaisussa sitä
sijoitettaessa.
VASTAAIHEET
• verenvuotohäiriö tai hoito, joka lisää liiallisen verenvuodon mahdollisuutta
• aktiivinen tai osaksi hoitamaton infektio kohdassa, johon luuaukon täyttöainetta on tarkoitus laittaa
• mikä tahansa voimakas allergia varjoaineelle tai luuaukon täyttöaineelle
• potilaan on todettu olevan raskaana
HUOMIO: Yhdysvaltain lain mukaan tämän tuotteen saa myydä ainoastaan lääkäri tai lääkärin määräyksestä.
VAROITUKSET
• Jos väline rikkoutuu, voidaan joutua tekemään leikkaus tai poistamaan väline.
• Tuotetta ei saa käyttää pakkaukseen merkityn viimeisen käyttöpäivän jälkeen. Väline ei ehkä ole turvallinen tai tehokas enää viimeisen käyttöpäivän jälkeen.
• Täytettävä osa voi pettää terävien luuspikuloiden tai kirurgisten instrumenttien vaikutuksesta.
• Luuntiivistimen täyttäminen yli sen enimmäistäyttötilavuuden voi saada pallon puhkeamaan, ennen kuin se saavuttaa enimmäistäyttöpaineensa.
• Luuntiivistimen täyttäminen yli sen enimmäistäyttöpaineen voi saada pallon puhkeamaan, ennen kuin se saavuttaa enimmäistäyttötilavuutensa.
• Älä koskaan käytä ilmaa tai kaasumaisia aineita pallon täyttämiseen.
VAROTOIMET
• Täytettävä luuntiivistin on kertakäyttöinen, kudoskontaktiin tarkoitettu väline. Ei saa käyttää uudelleen, prosessoida uudelleen tai steriloida uudelleen. Näiden välineiden
uudelleenkäyttäminen sisältää kontaminaatioriskin ja voi aiheuttaa potilasinfektion tai sairaalainfektion puhdistus- ja uudelleensterilointimenetelmistä riippumatta. Lisäksi
uudelleenkäsittelyn vaiheet saattavat heikentää välineen toimintaa, mistä voi olla seurauksena potilaan vahingoittuminen tai kuolema.
• On tärkeää lukea huolellisesti käyttöohjeet ja nämä varotoimet ennen laitteen käyttämistä.
• Täytettävää luuntiivistintä ei saa käyttää pakkaukseen merkityn viimeisen käyttöpäivän jälkeen.
• Ei saa käyttää, jos pakkaus on avattu tai vaurioitunut, koska tuotteen koskemattomuus, steriiliys mukaan lukien, on saattanut vaarantua.
• Vaurioituneita tuotteita ei saa käyttää. Tarkasta täytettävä luuntiivistin ja sen pakkaus ennen käyttöä vaurioiden varalta.
• Ennen täytettävän luuntiivistimen käyttöä on tarkastettava sen toimivuus ja varmistettava, että sen koko on sopiva tehtävään toimenpiteeseen.
• Tätä tuotetta ei saa käyttää ilman asianmukaista koulutusta. Täytettävää luuntiivistintä saavat käyttää vain lääkärit, jotka ovat saaneet tarvittavaa tekniikkaa koskevan koulutuksen.
Välineitä käyttävien lääkäreiden on tunnettava hoitokohteen fysiologia ja patologia.
• Täytettävää luuntiivistintä saa käsitellä vain läpivalaisussa röntgenlaitteilla, joilla saadaan hyvälaatuisia kuvia.
• Täytettävän luuntiivistimen saa täyttää vain tilavuuskapasiteetiltaan vähintään 14 ml:n täyttöruiskulla.
• Täytettävän luuntiivistimen saa täyttää vain nestemäisellä varjoaineella. 60-prosenttisen liuoksen käyttöä suositellaan. Noudata valmistajan antamia varjoaineen käyttöaiheita,
käyttöä ja varotoimia koskevia ohjeita.
• Älä täytä luuntiivistintä ilmalla tai muulla kaasulla.
• Täytettävän luuntiivistimen täyttöominaisuudet muuttuvat, kun sitä täytetään luun sisällä.
• Välineen kunnostaminen, korjaaminen, muuntelu tai uudelleensterilointi jatkokäyttöä ajatellen on nimenomaisesti kielletty.
• Kaikkiin leikkauksiin liittyy riskejä, mutta pallon käyttö näiden murtumien hoidossa ei lisää näitä riskejä kliiniseltä kannalta katsottuna verrattuna perinteisiin menetelmiin, joissa
nostetaan painuneita luunsiruja. Näitä riskejä ovat mm.:
o murtumafragmenttien asianmukaisen reponoinnin epäonnistuminen
o viivästynyt luutuminen tai luutumattomuus
o infektio
o neurovaskulaarinen vaurio tai lihasaitio-oireyhtymä, joka johtaa toiminnan menetykseen tai amputaatioon
HUOMAUTUS: Kyphon®-merkkisessä täyttöruiskussa on erinomaiset tilavuuden hallintaominaisuudet muihin täyttöjärjestelmiin, kuten tavallisiin ruiskuihin, verrattuna, ja täytettävän
luuntiivistimen saa täyttää ainoastaan sitä käyttäen. Noudata valmistajan antamia Kyphon®-merkkisen täyttöruiskun käyttöohjeita. Lukittuva Kyphon®-merkkinen ruisku on pakattu
yhteen Kyphon®-merkkisen täyttöruiskun kanssa.
HAITTAVAIKUTUKSET
Täytettävän luuntiivistimen käyttöön mahdollisesti liittyviin haittavaikutuksiin kuuluu vakavia vaikutuksia, jotka ovat tosin harvinaisia mutta mahdollisesti hengenvaarallisia.
Haittavaikutuksia ovat mm.:
• rasvan, trombin tai muun materiaalin aiheuttama embolia ja siitä seuraava symptomaattinen keuhkoveritulppa tai muut kliiniset jälkitilat
• täytettävän luuntiivistimen täytettävän osan puhkeaminen ja pirstoutuminen ja sen seurauksena palasen jääminen vaikutusalueelle
• luuntiivistimen puhkeamisen aiheuttama varjoaineelle altistuminen ja sen seurauksena mahdollisesti allerginen reaktio tai anafylaksia
• syvän tai pintahaavan infektio
• verenvuoto tai hematooma
KÄYTTÖOHJEET
HUOMIO: Noudata valmistajan antamia Kyphon®-merkkisen täyttöruiskun käyttöohjeita.
Viktig Informasjon Om InflateFX™ inflaterbar bentamper
for frakturbehandling (størrelse 10/3 og 15/3)
Tärkeää Tietoa täytettävästä InflateFX™-luuntiivistimestä
murtumien hoitoon (koot 10/3 ja 15/3)
HUOMIO: Varjoaineiden viskositeetti ja saostumisominaisuudet saattavat poiketa toisistaan, mikä voi pidentää täyttö- ja tyhjennysaikoja. Tästä syystä 60-prosenttisen varjoaineen
käyttö on suositeltavaa.
1. Kierrä mandriiniportin hattua kiristääksesi mandriinin täytettävään luuntiivistimeen. Työnnä mäntä kokonaan lukittuvaan Kyphon®-ruiskuun. Kiinnitä lukittuva Kyphon®-ruisku
täytettävän luuntiivistimen täyttöporttiin.
2. Vedä lukittuvan Kyphon®-ruiskun mäntä taakse. Lukitse mäntä paikalleen ruiskun viimeiseen koloon mäntää kiertämällä.
3. Irrota lukittuva Kyphon®-ruisku täytettävästä luuntiivistimestä.
4. Kiinnitä Kyphon®-merkkisen täyttöruiskun letkun liitäntäportti täytettävän luuntiivistimen täyttöporttiin. Järjestelmä on nyt valmisteltu ja käyttövalmis.
TÄYTETTÄVÄN LUUNTIIVISTIMEN KÄYTTÖ
1. Valitse täytettävän luuntiivistimen koko käyttökohteen ja hoidon tarkoituksen mukaan. Kuvassa 1 ja taulukossa 1 ilmoitetaan täytettävien luuntiivistimien läpimitta täytettynä
(D) ja pituus täytettynä (L) 37-asteisessa vedessä täyttötilavuusvälein enimmäistilavuuteen saakka.
2. Nämä mitat voivat vaihdella tuotteen käytön aikana luun rakenteen paikallisten vaihtelujen mukaan.
Taulukko 1 – Täytetyn luuntiivistimen mitat (37-asteisessa vedessä)
Mallinumero E103A Mitat täytettynä
Koko 10/3 Tilavuus Keskimääräinen läpimitta (D1, D2) Pituus (L)
Suurin täyttötilavuus 4 ml 2 ml 12,9 mm 14,7 mm
Suurin täyttöpaine 27 atm 4 ml 17,2 mm 19,1 mm
Mallinumero E153A Mitat täytettynä
Koko 15/3 Tilavuus Keskimääräinen läpimitta (D1, D2) Pituus (L)
Suurin täyttötilavuus 4 ml 2 ml 12,1 mm 17,4 mm
Suurin täyttöpaine 27 atm 4 ml 16 mm 22,1 mm
LUUNTIIVISTIMEN ASETUS
1. Luuntiivistimen asetukseen tarvitaan sisäänvientikanava.
2. Tee luuhun sisäänvientikanava valitun luunavausvälineen käyttöohjeiden mukaisesti.
3. Poista sisäänvientiholkki ennen käyttöä.
HUOMAUTUS: Tyhjennetyn luuntiivistimen distaalikärki on saavuttanut kanyylin distaalipään, kun luuntiivistimen ulomman luumenin poistumismerkki menee kanyylin
proksimaalipäähän.
4. Aseta tyhjennetty täytettävä luuntiivistin sisäänvientikanavaan ja sijoita se oikeaan kohtaan läpivalaisussa röntgenpositiivisten merkkien avulla. Pieni kiertoliike eteenpäin
työnnettäessä voi auttaa sisäänvientiä.
5. Pidä täytettävää luuntiivistintä paikallaan ja kiinnitä täytettävä luuntiivistin haluttuun kohtaan täyttämällä se 0,3 MPa:n (3 atm) paineeseen. Poista mandriini haluttaessa.
LUUNTIIVISTIMEN TÄYTTÄMINEN
1. Täytä täytettävä luuntiivistin jatkuvassa läpivalaisutarkkailussa. Tarkkaile sen etäisyyttä anteriorisesta ja lateraalisesta korteksista lateraalikuvassa. Tarkkaile lateraalisia kortekseja
AP-projektiossa (AP = anteroposteriorinen).
2. Jos jatkuvaa läpivalaisua ei käytetä, lisää tilavuutta vähitellen (0,25–0,5 ml kerrallaan). Määritä tiivistimen asento lateraali- ja AP-projektiosta ennen tilavuuden lisäämistä edelleen.
3. Lopeta täyttö, kun hoidon tavoite on saavutettu tai mikä tahansa osa täytettävän luuntiivistimen täyttöpituudesta koskettaa luun korteksia tai saavutetaan suurin täyttötilavuus
ja/tai suurin täyttöpaine (katso taulukkoa 1).
LUUNTIIVISTIMEN POISTAMINEN
HUOMIO: Luuntiivistintä ei saa vetää pois, ellei täytettävää osaa ole tyhjennetty kokonaan. Luuntiivistintä ei saa koskaan vetää pois, jos tuntuu vastusta. Määritä vastuksen syy
läpivalaisussa ja poista se asianmukaisesti.
Käytä Kyphon®-merkkistä täyttöruiskua ja poista varjoainetta täytettävästä luuntiivistimestä, kunnes pallo on aivan tyhjä. Poista luuntiivistin luusta kanyyliä pitkin kääntämällä
sitä varovasti.
• Jos tuntuu vastusta, liitä 30 ml:n ruisku täyttöporttiin. Aikaansaa tyhjiö vetämällä ruiskun mäntä taaksepäin ”30ml”-merkin kohdalle. Jatka luuntiivistimen poistamista.
• Varmista, että täytettävän luuntiivistimen laajennettava osa on kanyylissä. Jos täytettävä osa ei vetäydy kanyyliin, vie kanyyli luuntiivistintä pitkin proksimaalisen röntgenpositiivisen
merkin kohdalle. Kun olet siirtänyt kanyylin eteenpäin, vedä tiivistin pois kanyylin läpi. Jos tunnet vastusta, poista tiivistin ja kanyyli samanaikaisesti.
STERILOINTI
Steriloitu säteilyttämällä.
TOIMITUSTAPA
Täytettävät luuntiivistimet toimitetaan steriileinä repäisypakkauksessa. Jos steriili pakkaus on vaurioitunut, älä käytä tuotetta vaan ilmoita asiasta valmistajalle.
MATERIAALIT, JOTKA EIVÄT SISÄLLY TOIMITUKSEEN
• Kyphon®-merkkinen täyttöruisku ja lukittuva Kyphon®-ruisku
• Varjoaine (60-pros.)
• Pieni astia
HUOMAUTUS: Kyphon®-merkkinen täyttöruisku ja lukittuva Kyphon®-ruisku ovat tilattavissa Medtronicilta.
SÄILYTYS
Täytettävät luuntiivistimet on säilytettävä alkuperäisissä pakkauksissa. Täytettäviä luuntiivistimiä on käsiteltävä huolellisesti niiden vaurioitumisen estämiseksi. Säilytettävä viileässä
ja kuivassa paikassa.
TAKUUN RAJOITUSLAUSEKE
MEDTRONIC EI OLE VASTUUSSA MISTÄÄN SUORISTA, EPÄSUORISTA, SATUNNAISISTA, VÄLILLISISTÄ TAI RANGAISTUSLUONTEISISTA VAHINGOISTA/VAHINGONKORVAUKSISTA, JOTKA JOHTUVAT
TÄYTETTÄVIEN, MURTUMIEN HOITOON TARKOITETTUJEN InflateFX™-LUUNTIIVISTIMEN UUDELLEENKÄYTÖSTÄ.
MEDTRONIC EI OLE MISSÄÄN TAPAUKSESSA VASTUUSSA MISTÄÄN TÄYTETTÄVISTÄ, MURTUMIEN HOITOON TARKOITETUISTA InflateFX™-LUUNTIIVISTIMISTÄ JOHTUVISTA TAI NIIHIN LIITTYVISTÄ
SUORISTA, EPÄSUORISTA, SATUNNAISISTA, VÄLILLISISTÄ TAI RANGAISTUSLUONTEISISTA VAHINGOISTA/VAHINGONKORVAUKSISTA VÄITETYN SOPIMUKSEN RIKKOMISEN (MUKAAN LUKIEN
TAKUUSOPIMUKSEN RIKKOMISEN) PERUSTEELLA.
YHTEYSTIEDOT LISÄTIETOJEN SAAMISTA VARTEN
Lisätietoja saa ottamalla yhteyttä asiakaspalveluun.
© 2013 Medtronic Sofamor Danek USA, Inc. Kaikki oikeudet pidätetään.
ΕΛΛΗΝΙΚΑ
ΕΝΕΙΞΕΙΣ ΧΡΗΣΗΣ
Το πληρούμενο βύσμα οστών (IBT) για την αντιμετώπιση καταγμάτων InflateFX™ προορίζεται για χρήση ως συμβατικό βύσμα οστών για την ανάταξη καταγμάτων ή/και τη δημιουργία
κενού σε σπογγώδες οστό στο άκρο χέρι, την κνήμη, την κερκίδα και την πτέρνα.
ΠΕΡΙΓΡΑΦΗ ΣΥΣΚΕΥΗΣ
Βλέπε εικόνα 1.
1. Πώμα
2. Στειλεός
3. Θύρα στειλεού
4. Θύρα διόγκωσης
5. Ταινία με χρωματική κωδικοποίηση
6. Ταινία δείκτη εξόδου
7. Περίβλημα εισαγωγής
8. Ακτινοσκιεροί δείκτες
9. Πληρούμενο εξάρτημα
• Το πληρούμενο εξάρτημα του IBT έχει σχεδιαστεί για τη συμπίεση σπογγώδους οστού ή/και για τη μετακίνηση φλοιώδους οστού καθώς πληρώνεται. Το πληρούμενο εξάρτημα του
IBT βρίσκεται κοντά στο περιφερικό άκρο της συσκευής, όπως φαίνεται στην εικόνα 1.
• Ο άξονας περιέχει δύο αυλούς που δεν επικοινωνούν μεταξύ τους. Ο εξωτερικός αυλός χρησιμοποιείται για τη διόγκωση του IBT και ο κεντρικός αυλός περιέχει έναν αφαιρούμενο
ενισχυτικό στειλεό για εισαγωγή του IBT.
• Το εγγύς άκρο του άξονα φέρει έναν προσαρμογέα πλευρικού βραχίονα. Η θύρα διόγκωσης του προσαρμογέα είναι παρακείμενη στον εξωτερικό αυλό. Η θύρα του στειλεού είναι
παρακείμενη με τον εσωτερικό αυλό και περιέχει τον ενισχυτικό στειλεό. Ο στειλεός φέρει ένα πώμα στο εγγύς άκρο του για προαιρετική αφαίρεση.
• Η χρωματικά κωδικοποιημένη ταινία, που βρίσκεται μόλις περιφερικότερα του προσαρμογέα πλευρικού βραχίονα, υποδεικνύει το μέγεθος του μπαλονιού (δηλαδή κίτρινη ταινία
για μέγεθος 10/3 και μαύρη ταινία για μέγεθος 15/3).
• Η ταινία δείκτη εξόδου που βρίσκεται στον εξωτερικό αυλό χρησιμοποιείται κατά τη διάρκεια της εισαγωγής του IBT.
• Ακτινοσκιεροί δείκτες, που βρίσκονται στο περιφερικό και το εγγύς άκρο της ξεφουσκωμένης επιφάνειας εργασίας, επιτρέπουν την ακτινοσκοπική απεικόνιση του ξεφουσκωμένου
IBT κατά τη διάρκεια της τοποθέτησης.
ΑΝΤΕΝΕΙΞΕΙΣ
• Αιμορραγική διαταραχή ή θεραπεία που αυξάνει την πιθανότητα υπερβολικής αιμορραγίας.
• Παρουσία ενεργού ή ατελώς θεραπευθείσας λοίμωξης στη θέση όπου πρόκειται να εφαρμοστεί το υλικό πλήρωσης οστικών κενών.
• Οποιαδήποτε γνωστή σοβαρή αλλεργία στο σκιαγραφικό μέσο και το υλικό πλήρωσης οστικών κενών.
• Σε ασθενή με επιβεβαιωμένη εγκυμοσύνη.
ΠΡΟΣΟΧΗ: Η ομοσπονδιακή νομοθεσία (των Η.Π.Α.) επιτρέπει την πώληση της συσκευής αυτής μόνον σε ιατρό ή κατόπιν εντολής ιατρού.
ΠΡΟΕΙΟΠΟΙΗΣΕΙΣ
• Η θραύση της συσκευής ενδέχεται να απαιτήσει παρέμβαση ή ανάκτηση.
• Μη χρησιμοποιείτε αυτό το προϊόν μετά την ημερομηνία λήξης που είναι τυπωμένη στη συσκευασία. Η συσκευή ενδέχεται να μην είναι ασφαλής ή αποτελεσματική μετά την παρέλευση
της ημερομηνίας λήξης της.
• Το πληρούμενο εξάρτημα μπορεί να αστοχήσει λόγω αιχμηρών οστικών παρασχίδων ή χειρουργικών εργαλείων.
• Διόγκωση του IBT πέραν του μέγιστου όγκου πλήρωσης μπορεί να προκαλέσει ρήξη του μπαλονιού πριν από την επίτευξη της μέγιστης πίεσης πλήρωσης.
• Διόγκωση του IBT πέραν της μέγιστης πίεσης πλήρωσης μπορεί να προκαλέσει ρήξη του μπαλονιού πριν από την επίτευξη του μέγιστου όγκου πλήρωσης.
• Μη χρησιμοποιείτε ποτέ αέρα ή αέρια υλικά για την πλήρωση του μπαλονιού.
ΠΡΟΦΥΛΑΞΕΙΣ
• Το πληρούμενο βύσμα οστών είναι συσκευή μίας χρήσης που προορίζεται για να έρχεται σε επαφή με σωματικούς ιστούς. Μην τις επαναχρησιμοποιείτε και μην τις υποβάλλετε σε
νέα επεξεργασία ή νέα αποστείρωση. Η επαναχρησιμοποίηση αυτών των συσκευών ενέχει τον κίνδυνο μόλυνσης και μπορεί να προκαλέσει λοίμωξη ή ετερολοίμωξη, ανεξάρτητα
από τις μεθόδους καθαρισμού και νέας αποστείρωσης. Υπάρχει επίσης αυξημένος κίνδυνος μείωσης της απόδοσης της συσκευής λόγω των βημάτων επεξεργασίας εκ νέου, η οποία
μπορεί να οδηγήσει σε τραυματισμό ή θάνατο του ασθενούς.
• Είναι σημαντικό να διαβάσετε τις οδηγίες χρήσης και αυτές τις προφυλάξεις προτού χρησιμοποιήσετε τη συσκευή.
• Χρησιμοποιήστε το IBT πριν από την ημερομηνία λήξης που αναγράφεται στη συσκευασία.
• Μη χρησιμοποιείτε τη συσκευασία εάν έχει ανοιχτεί ή υποστεί ζημιά επειδή ενδέχεται να έχει διακυβευθεί η ακεραιότητα του προϊόντος, συμπεριλαμβανομένης της στειρότητάς του.
• Μη χρησιμοποιείτε προϊόντα που έχουν υποστεί ζημιά. Πριν τη χρήση, επιθεωρήστε το IBT και τη συσκευασία του για να βεβαιωθείτε ότι δεν έχει προκληθεί ζημιά.
• Πριν από τη χρήση, το IBT θα πρέπει να εξεταστεί προκειμένου να επιβεβαιωθεί η λειτουργικότητά του και ότι το μέγεθός του είναι κατάλληλο για τη συγκεκριμένη διαδικασία για
την οποία προορίζεται να χρησιμοποιηθεί.
• Μη χρησιμοποιείτε το προϊόν αυτό εάν δεν έχετε εκπαιδευτεί κατάλληλα. Το IBT θα πρέπει να χρησιμοποιείται μόνον από ιατρούς που είναι εκπαιδευμένοι σε τεχνικές χρήσης οστικού
βύσματος. Οι ιατροί που χρησιμοποιούν τις συσκευές θα πρέπει να γνωρίζουν τη φυσιολογία και την παθολογία της επιλεγμένης ανατομικής δομής.
• Ο χειρισμός του IBT θα πρέπει να γίνεται μόνον υπό ακτινοσκοπική παρατήρηση με ακτινολογικό εξοπλισμό που παρέχει εικόνες υψηλής ποιότητας.
• Το IBT θα πρέπει να πληρώνεται μόνο χρησιμοποιώντας μια σύριγγα πλήρωσης ελάχιστης χωρητικότητας 14 ml.
• Πληρώνετε το IBT μόνο με υγρό σκιαγραφικό μέσο: συνιστάται διάλυμα 60%. Ακολουθήστε τις οδηγίες του κατασκευαστή σχετικά με τις ενδείξεις, τη χρήση και τις συστάσεις προσοχής
για το σκιαγραφικό μέσο.
• Μη χρησιμοποιείτε αέρα ή άλλο αέριο για να πληρώσετε το IBT.
• Τα χαρακτηριστικά διόγκωσης του IBT τροποποιούνται από τη διόγκωση εντός του οστού.
• Εκ νέου επεξεργασία, ανακαίνιση, επισκευή, τροποποίηση ή επαναποστείρωση της συσκευής, έτσι ώστε να καταστεί δυνατή η περαιτέρω χρήση της, απαγορεύεται ρητά.
• Κάθε χειρουργική επέμβαση ενέχει κινδύνους. Ωστόσο, η χρήση του μπαλονιού στη θεραπεία αυτών των καταγμάτων δεν αυξάνει αυτούς τους κινδύνους από κλινική σκοπιά, σε
σύγκριση με τις παραδοσιακές μεθόδους ανύψωσης των συμπιεσμένων οστικών τεμαχίων. Αυτοί οι κίνδυνοι περιλαμβάνουν τους εξής:
o Αδυναμία σωστής ανάταξης των τεμαχίων του κατάγματος.
o Καθυστέρηση ή απουσία πώρωσης.
o Λοίμωξη.
o Νευραγγειακό τραυματισμό ή σύνδρομο διαμερίσματος που οδηγεί σε απώλεια λειτουργικότητας ή ακρωτηριασμό.
ΣΗΜΕΙΣΗ: Η σύριγγα πλήρωσης μάρκας Kyphon® παρέχει ανώτερο έλεγχο όγκου συγκριτικά με άλλα συστήματα διόγκωσης, όπως μια τυπική σύριγγα, και απαιτείται για τη διόγκωση
του IBT. Ακολουθήστε τις οδηγίες του κατασκευαστή για τη χρήση μιας σύριγγας πλήρωσης μάρκας Kyphon®. Η σύριγγα ασφάλισης Kyphon® συσκευάζεται μαζί με τη σύριγγα πλήρωσης
μάρκας Kyphon®.
ΑΝΕΠΙΘΥΜΗΤΕΣ ΕΝΕΡΓΕΙΕΣ
Στα ανεπιθύμητα συμβάντα που δυνητικά σχετίζονται με τη χρήση του IBT περιλαμβάνονται σοβαρά συμβάντα τα οποία, παρόλο που είναι σπάνια, μπορεί να είναι θανατηφόρα. Στα
ανεπιθύμητα συμβάντα περιλαμβάνονται τα εξής:
• Εμβολή λίπους, θρόμβου ή άλλων υλικών με αποτέλεσμα συμπτωματική πνευμονική εμβολή ή άλλα κλινικά συμβάματα.
• Ρήξη με κατατεμαχισμό του πληρούμενου τμήματος του IBT με αποτέλεσμα την κατακράτηση ενός τεμαχίου εντός της προσβεβλημένης περιοχής.
• Ρήξη του IBT που προκαλεί έκθεση στο σκιαγραφικό μέσο, με πιθανό αποτέλεσμα αλλεργική αντίδραση ή αναφυλαξία.
• Εν τω βάθει ή επιπολής λοίμωξη του τραύματος.
• Αιμορραγία ή αιμάτωμα.
ΟΗΓΙΕΣ ΧΡΗΣΗΣ
ΠΡΟΣΟΧΗ: Ακολουθήστε τις οδηγίες του κατασκευαστή για τη χρήση μιας σύριγγας πλήρωσης μάρκας Kyphon®.
ΠΡΟΣΟΧΗ: Τα σκιαγραφικά μέσα ενδέχεται να έχουν διαφορετικά επίπεδα ιξώδους και καθίζησης που μπορεί να προκαλέσουν μεγαλύτερους χρόνους διόγκωσης και ξεφουσκώματος.
Για το λόγο αυτό, συνιστάται η χρήση σκιαγραφικού μέσου 60%.
1. Στρέψτε το πώμα στη θύρα στειλεού για να σφίξετε το στειλεό στο IBT. Πιέστε πλήρως το έμβολο μέσα στη σύριγγα ασφάλισης Kyphon® . Προσαρτήστε τη σύριγγα ασφάλισης Kyphon®
στη θύρα διόγκωσης στο IBT.
2. Τραβήξτε προς τα πίσω το έμβολο της σύριγγας ασφάλισης Kyphon®. Στρέψτε το έμβολο για να ασφαλίσει στη θέση του, στην τελευταία εντομή της σύριγγας.
3. Αποσπάστε τη σύριγγα ασφάλισης Kyphon® από το IBT.
4. Προσαρτήστε τη θύρα σύνδεσης στη σωλήνωση της σύριγγας πλήρωσης μάρκας Kyphon® στη θύρα διόγκωσης του IBT. Το σύστημα έχει τώρα προετοιμαστεί και είναι έτοιμο για χρήση.
ΧΡΗΣΗ ΤΟΥ IBT
1. Επιλέξτε το μέγεθος του IBT με βάση τη θέση και το θεραπευτικό στόχο. Η εικόνα 1 και ο πίνακας 1 ορίζουν τη διάμετρο (D) και το μήκος (L) των IBT μετά τη διόγκωση σε νερό
θερμοκρασίας 37 °C, σε διαστήματα αύξησης του όγκου διόγκωσης έως τον μέγιστο όγκο διόγκωσης.
2. Οι διαστάσεις αυτές ενδέχεται να ποικίλουν κατά τη χρήση του προϊόντος λόγω τοπικών διακυμάνσεων στην οστική δομή.
Πίνακα 1 – ιαστάσει IBT ετά τη διόγκωση (σε νερό θεροκρασία 37 °C)
Αριθό οντέλου E103A ιαστάσει σε διόγκωση
Μέγεθος 10/3 Όγκος Μέση διάμετρος
(D1, D2) Μήκος (L)
Μέγ. όγκος διόγκωσης 4 ml 2 ml 12,9 mm 14,7 mm
Μέγ. πίεση διόγκωσης 27 atm 4 ml 17,2 mm 19,1 mm
Αριθό οντέλου E153A ιαστάσει σε διόγκωση
Μέγεθος 15/3 Όγκος Μέση διάμετρος
(D1, D2) Μήκος (L)
Μέγ. όγκος διόγκωσης 4 ml 2 ml 12,1 mm 17,4 mm
Μέγ. πίεση διόγκωσης 27 atm 4 ml 16 mm 22,1 mm
ΕΙΣΑΓΓΗ ΤΟΥ IBT
1. Για την τοποθέτηση του IBT απαιτείται ένα κανάλι προσπέλασης.
2. Ακολουθήστε τις οδηγίες χρήσης για τα επιλεγμένα εργαλεία οστικής προσπέλασης για να δημιουργήσετε ένα κανάλι προσπέλασης στο οστό.
3. Αφαιρέστε το περίβλημα εισαγωγής πριν από τη χρήση.
ΣΗΜΕΙΣΗ: Το περιφερικό άκρο του ξεφουσκωμένου IBT έχει φθάσει στο περιφερικό άκρο του σωληνίσκου όταν ο δείκτης εξόδου στον εξωτερικό αυλό του IBT εισέρχεται στο εγγύς
άκρο του σωληνίσκου.
4. Περάστε το ξεφουσκωμένο IBT μέσα στο κανάλι προσπέλασης και τοποθετήστε το υπό απεικονιστική καθοδήγηση χρησιμοποιώντας τους ακτινοσκιερούς δείκτες. Μια απαλή
περιστροφική κίνηση μαζί με την ώθηση προς τα εμπρός μπορεί να υποβοηθήσει την εισαγωγή.
5. Ενώ συγκρατείτε το IBT στη θέση του, πληρώστε στις 0,3 MPa (3 atm) για να ασφαλίσετε το IBT στη θέση του. Αφαιρέστε το στειλεό, εάν επιθυμείτε.
ΠΛΗΡΣΤΕ ΤΟΥ IBT
1. Πληρώστε το IBT υπό συνεχή απεικονιστική καθοδήγηση. Χρησιμοποιήστε την πλάγια προβολή για να παρακολουθήσετε την απόσταση από τον πρόσθιο και τον πλευρικό φλοιό.
Χρησιμοποιήστε την προσθοπίσθια προβολή για να παρακολουθήσετε τους πλευρικούς φλοιούς.
2. Εάν δε χρησιμοποιείτε συνεχή απεικόνιση, αυξάνετε τον όγκο σε μικρές δόσεις (0,25-0,5 ml). Αξιολογήστε τη θέση του βύσματος με πλάγιες και προσθιοπίσθιες προβολές πριν
προχωρήσετε σε περαιτέρω αύξηση του όγκου.
3. Σταματήστε όταν επιτευχθεί ο θεραπευτικός στόχος ή όταν οποιοδήποτε τμήμα του πληρούμενου IBT έλθει σε επαφή με το φλοιώδες οστό ή όταν επιτευχθεί μέγιστος όγκος διόγκωσης
ή/και μέγιστη πίεση διόγκωσης (Δείτε τον πίνακα 1).
ΑΦΑΙΡΕΣΗ ΤΟΥ IBT
ΠΡΟΣΟΧΗ: Μην αποσύρετε το IBT εάν δεν έχει συμπτυχθεί πλήρως το πληρούμενο εξάρτημα. Μην αποσύρετε ποτέ το IBT όταν συναντάτε αντίσταση. Προσδιορίστε ακτινοσκοπικά την
αιτία της αντίστασης και προβείτε στις απαραίτητες διορθωτικές ενέργειες.
Χρησιμοποιήστε μια σύριγγα πλήρωσης μάρκας Kyphon® για να εκκενώστε το σκιαγραφικό μέσο από το IBT μέχρι να ξεφουσκώσει πλήρως το μπαλόνι. Αφαιρέστε το IBT από το οστό
μέσω του σωληνίσκου με απαλή περιστροφική κίνηση.
• Εάν παρουσιαστεί αντίσταση, συνδέστε μια σύριγγα των 30 ml στη θύρα διόγκωσης. Τραβήξτε το έμβολο της σύριγγας προς τα πίσω μέχρι το δείκτη «30ml» για να δημιουργήσετε
κενό. Συνεχίστε την αφαίρεση του IBT.
• Επιβεβαιώστε την είσοδο του πληρούμενου τμήματος του IBT στο σωληνίσκο. Εάν το πληρούμενο εξάρτημα δε μετακινείται μέσα στο σωληνίσκο, προωθήστε το σωληνίσκο πάνω
από το IBT προς τον εγγύς ακτινοσκιερό δείκτη. Μετά την προώθηση του σωληνίσκου, αποσύρετε το IBT μέσω του σωληνίσκου. Εάν παρατηρήσετε αντίσταση, αφαιρέστε το IBT και
το σωληνίσκο ταυτόχρονα.
ΑΠΟΣΤΕΙΡΣΗ
Αποστειρωμένο με ακτινοβολία.
ΤΡΟΠΟΣ ΙΑΘΕΣΗΣ
Τα IBT παρέχονται στείρα σε αποκολλώμενη συσκευασία. Σε περίπτωση ζημιάς στην αποστειρωμένη συσκευασία, μη χρησιμοποιείτε το προϊόν και ενημερώστε τον κατασκευαστή.
ΜΗ ΠΑΡΕΧΟΜΕΝΑ ΥΛΙΚΑ
• Σύριγγα πλήρωσης μάρκας Kyphon® με σύριγγα ασφάλισης Kyphon®
• Σκιαγραφικό μέσο (60%)
• Μικρή λεκάνη
ΣΗΜΕΙΣΗ: Η σύριγγα πλήρωσης μάρκας Kyphon® με σύριγγα ασφάλισης Kyphon® διατίθεται από τη Medtronic.
ΦΥΛΑΞΗ
Τα IBT θα πρέπει να φυλάσσονται στα αρχικά υλικά αποστολής τους. Θα πρέπει να δοθεί η δέουσα προσοχή, έτσι ώστε να διασφαλιστεί ότι δεν θα προκληθεί ζημιά στα IBT. Φυλάσσετε
σε δροσερό και ξηρό χώρο.
ΠΕΡΙΟΡΙΣΜΟΙ ΕΥΘΥΝΗΣ
Η MEDTRONIC ΔΕΝ ΘΑ ΦΕΡΕΙ ΕΥΘΥΝΗ ΓΙΑ ΟΠΟΙΑΔΗΠΟΤΕ ΑΜΕΣΗ, ΕΜΜΕΣΗ, ΤΥΧΑΙΑ, ΠΑΡΕΠΟΜΕΝΗ ‘Η ΑΠΟΘΕΤΙΚΗ ΖΗΜΙΑ ΠΟΥ ΟΦΕΙΛΕΤΑΙ ΣΤΗΝ ΕΠΑΝΑΧΡΗΣΙΜΟΠΟΙΗΣΗ ΤΩΝ ΠΛΗΡΟΥΜΕΝΩΝ
ΒΥΣΜΑΤΩΝ ΟΣΤΩΝ ΓΙΑ ΤΗΝ ΑΝΤΙΜΕΤΩΠΙΣΗ ΚΑΤΑΓΜΑΤΩΝ InflateFX™.
ΣΕ ΚΑΜΙΑ ΠΕΡΙΠΤΩΣΗ Η MEDTRONIC ΔΕΝ ΦΕΡΕΙ ΕΥΘΥΝΗ ΓΙΑ ΟΠΟΙΑΔΗΠΟΤΕ ΑΜΕΣΗ, ΕΜΜΕΣΗ, ΤΥΧΑΙΑ, ΠΑΡΕΠΟΜΕΝΗ Ή ΠΑΡΑΔΕΙΓΜΑΤΙΚΗ ΖΗΜΙΑ ΠΡΟΚΑΛΟΥΜΕΝΗ Ή ΣΧΕΤΙΖΟΜΕΝΗ
ΜΕ ΤΑ ΠΛΗΡΟΥΜΕΝΑ ΒΥΣΜΑΤΩΝ ΟΣΤΩΝ ΓΙΑ ΤΗΝ ΑΝΤΙΜΕΤΩΠΙΣΗ ΚΑΤΑΓΜΑΤΩΝ InflateFX™, ΜΕ ΒΑΣΗ ΑΘΕΤΗΣΗ ΣΥΜΒΑΣΗΣ (ΣΥΜΠΕΡΙΛΑΜΒΑΝΟΜΕΝΗΣ ΤΗΣ ΑΘΕΤΗΣΗΣ ΕΓΓΥΗΣΗΣ).
ΑΙΤΗΣΕΙΣ ΓΙΑ ΠΛΗΡΟΦΟΡΙΕΣ
Για περισσότερες πληροφορίες, καλέστε το τμήμα εξυπηρέτησης πελατών.
©2013 Medtronic Sofamor Danek USA, Inc. Με επιφύλαξη παντός δικαιώματος.
porTUGUêS
INDICAÇÕES DE UTILIZAÇÃO
O calcador de osso insuflável (COI) InflateFX™ para tratamento de fracturas destina-se a ser utilizado como um calcador de osso convencional para redução de fracturas e/ou criação de
uma cavidade em osso esponjoso na mão, tíbia, rádio e calcâneo.
DESCRIÇÃO DO DISPOSITIVO
Ver a figura 1.
1. Tampa
2. Estilete
3. Abertura do estilete
4. Abertura de enchimento
5. Faixa codificada por cores
6. Faixa do marcador de saída
7. Manga de inserção
8. Marcadores radiopacos
9. Componente insuflável
• O componente insuflável do COI foi concebido para comprimir osso esponjoso e/ou mover osso cortical à medida que é enchido. O componente insuflável do COI situa-se próximo
da ponta distal do dispositivo, tal como mostrado na figura 1.
• A haste contém dois lúmenes não comunicantes. O lúmen exterior é utilizado para enchimento do COI e o lúmen central contém um estilete de reforço amovível para introdução do COI.
• A extremidade proximal da haste possui um adaptador para braço lateral. A abertura de enchimento do adaptador é contígua com o lúmen exterior. A abertura do estilete é contígua
com o lúmen interior e contém o estilete de reforço. O estilete possui uma tampa na extremidade proximal para remoção opcional.
• A faixa codificada por cores, localizada numa posição imediatamente distal em relação ao adaptador para braço lateral, indica o tamanho do balão (ou seja, uma faixa amarela para
o tamanho 10/3 e uma faixa preta para o tamanho 15/3).
• A faixa do marcador de saída, localizada no lúmen exterior, é utilizada durante a inserção do COI.
• Os marcadores radiopacos, localizados na extremidade distal e proximal da superfície funcional esvaziada, permitem uma visualização fluoroscópica do COI esvaziado durante o
posicionamento.
CONTRAINDICAÇÕES
• Distúrbio hemorrágico ou tratamento que aumente a probabilidade de hemorragia excessiva.
• Presença de infecção activa ou não completamente tratada no local onde se pretende aplicar o produto de enchimento de cavidades ósseas.
• Qualquer alergia grave conhecida a material de contraste e ao produto de enchimento de cavidades ósseas.
• Gravidez confirmada da doente.
ATENÇÃO: A lei federal (EUA) restringe a venda deste dispositivo a um médico ou sob prescrição de um médico.
ADVERTÊNCIAS
• Caso o dispositivo se parta pode ser necessário realizar uma intervenção cirúrgica ou a recuperação do mesmo.
• Não utilize este produto após o fim do prazo de validade impresso na embalagem. Numa data posterior à indicada (prazo de validade) o dispositivo poderá não ser seguro ou eficaz.
• O componente insuflável pode falhar devido a espículas ósseas afiadas ou instrumentos cirúrgicos.
• A insuflação do COI além do volume máximo de enchimento pode originar a rotura do balão antes de atingir a pressão máxima de enchimento.
• O enchimento do COI além da pressão máxima de enchimento pode originar a rotura do balão antes de atingir o volume máximo de enchimento.
• Nunca utilize ar ou outro meio gasoso para encher o balão.
PRECAUÇÕES
• O calcador de osso insuflável é um dispositivo de utilização única concebido para contacto com tecidos corporais. Não reutilizar, reprocessar ou reesterilizar. A reutilização destes
dispositivos comporta o risco de contaminação e pode causar infecções ou infecções cruzadas no doente, independentemente dos métodos de limpeza e de reesterilização. Existe
também um risco aumentado de deterioração do desempenho do dispositivo devido aos passos do reprocessamento, que poderão resultar em lesões ou mesmo na morte do doente.
• É importante que leia atentamente as instruções de utilização e estas precauções antes de utilizar o dispositivo.
• Utilize o COI antes do fim do prazo de validade indicado na embalagem.
• Não utilize se a embalagem estiver aberta ou danificada, pois a integridade do produto, incluindo a sua esterilidade, poderá estar comprometida.
• Não utilize produtos danificados. Antes de utilizar, inspeccione o COI e a embalagem para verificar se ocorreram danos.
• Antes de utilizar o COI, deve examiná-lo para verificar a sua funcionalidade e garantir que o tamanho é adequado para o procedimento específico no qual será utilizado.
• Não use este produto caso não possua a formação adequada. O COI só deve ser utilizado por médicos devidamente formados nas técnicas de utilização de calcadores de osso. Os
médicos que utilizarem os dispositivos devem estar familiarizados com a fisiologia e patologia da anatomia seleccionada.
• O COI só deve ser manuseado sob observação fluoroscópica através de equipamento radiográfico que proporcione imagens de alta qualidade.
• O COI só deve ser enchido por uma seringa de enchimento com uma capacidade de volume mínima de 14 ml.
• Encha o COI apenas com meio de contraste líquido: recomenda-se uma solução a 60%. Siga as instruções do fabricante relativamente às indicações, utilização e precauções do meio
de contraste.
• Nunca utilize ar ou outro meio gasoso para encher o COI.
• As características de enchimento do COI alteram-se com o enchimento dentro do osso.
• O reacondicionamento, a renovação, a reparação, a modificação ou a reesterilização do dispositivo para permitir utilizações adicionais são expressamente proibidos.
• Qualquer cirurgia tem riscos; contudo, a utilização do balão no tratamento destas fracturas não aumenta estes riscos do ponto de vista cirúrgico, comparado com métodos tradicionais
de elevação de fragmentos ósseos deprimidos. Estes riscos incluem:
o Falha em reduzir adequadamente os fragmentos da fractura.
o Atraso na união e não-união.
o Infecção.
o Lesão neurovascular ou síndrome compartimental conducente a perda de função ou amputação.
ΣΗΜΑΝΤΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ πληρούενο βύσα οστών για την
αντιετώπιση καταγάτων InflateFX™ (Μεγέθη 10/3 και 15/3)
InformaçÕes Importantes Sobre o calcador de osso insuflável InflateFX™
para tratamento de fracturas (tamanhos 10/3 e 15/3)
Page 2
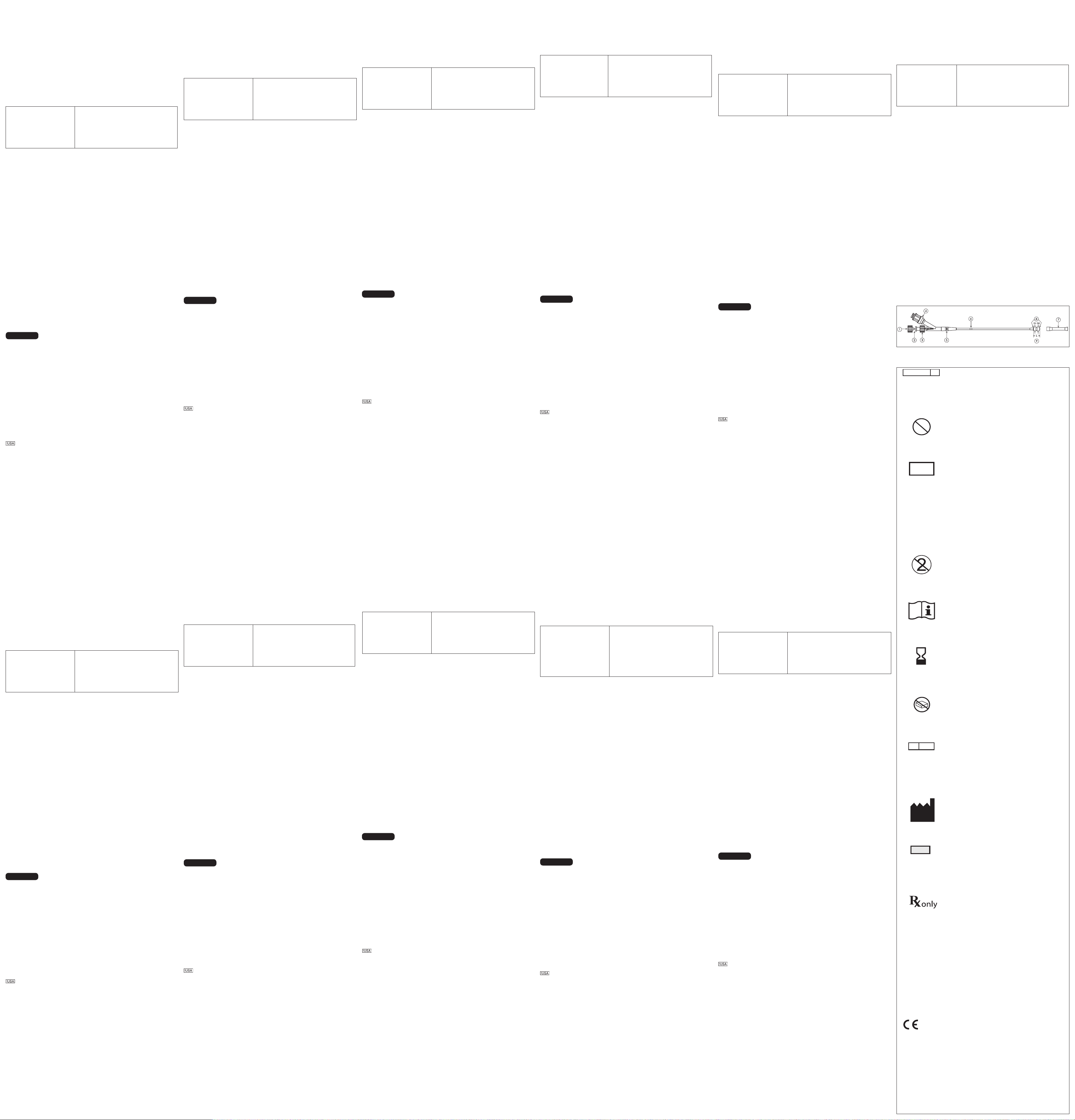
NOTA: A seringa de enchimento da marca Kyphon® proporciona um controlo superior do volume em comparação com outros sistemas de enchimento, tais como uma seringa normal,
Consult instructions for use
Consulter les instructions d’utilisation
Consulte las instrucciones de uso
Gebrauchsanweisung lesen
Consultare le istruzioni per l’uso
Raadpleeg de gebruiksaanwijzing
Se brugsanvisningen
Läs instruktioner för användning
Les bruksanvisningen
Katso käyttöohjeita
Ανατρέξτε στις οδηγίες χρήσης
Consultar instruções de utilização
Viz návod k použití
Vt kasutusjuhendit
Lásd a használati útmutatót
Iepazīstieties ar lietošanas norādījumiem
Skaitykite naudojimo instrukciją
Przeczytać instrukcję użytkowania
Oboznámte sa s pokynmi na používanie
Kullanma talimatına başvurun
Consultaţi instrucţiunile de utilizare
Glejte navodila za uporabo
Do not re-use
Ne pas réutiliser
No reutilizar
Nicht wiederverwenden
Non riutilizzare
Niet hergebruiken.
Må ikke genbruges
Får ej återanvändas
Må ikke brukes om igjen
Ei saa käyttää uudelleen
Μην επαναχρησιμοποιείτε
Não reutilizar
Nepoužívejte opakovaně
Mitte kasutada korduvalt
Újrafelhasználni tilos
Neizmantot atkārtoti
Nenaudoti pakartotinai
Nie używać powtórnie
Nepoužívajte opakovane
Tekrar kullanmayın
A nu se refolosi
Ne uporabljajte ponovno
Manufacturer
Fabricant
Fabricante
Hersteller
Produttore
Fabrikant
Fabrikant
Tillverkare
Produsent
Valmistaja
Κατασκευαστής
Fabricante
Výrobce
Tootja
Gyártó
Ražotājs
Gamintojas
Wytwórca
Výrobca
Üretici
Producător
Proizvajalec
Use-by date
Utiliser avant le
Fecha de caducidad
Verwendbar bis
Usare entro
Gebruiken vóór
Skal anvendes inden
Använd före
Brukes før
Käytä viimeistään
Ημερομηνία λήξης
Data de Validade
Datum použitelnosti
Kõlblik kuni
Szavatossági idő
Izlietot līdz
Tinka iki
Nie używać po
Použiť do
Son kullanma tarihi
A se utiliza până la data de expirare
Rok uporabnosti
For US audiences only
Ne s’applique qu’aux États-Unis
Solo aplicable en EE. UU.
Gilt nur für Leser in den USA
Valido solo per il mercato USA
Alleen van toepassing in de VS
Gælder kun i USA
Gäller endast i USA
GJELDER KUN USA
Koskee vain Yhdysvaltoja
Μόνο για πελάτες εντός των Η.Π.Α.
Apenas aplicável aos EUA
Pouze pro uživatele z USA
Üksnes USA tarbijaile
Csak egyesült államokbeli felhasználóknak
Tikai ASV auditorijai
Taikoma tik JAV
Dotyczy tylko użytkowników z USA
Len pre používateľov v USA
Sadece ABD’de yaşayanlar için
Numai pentru publicul din S.U.A.
Samo za uporabnike v ZDA
!USA
Authorized representative in the European Community
Représentant autorisé dans l’Union européenne
Representante autorizado en la Unión Europea
Autorisierte Vertretung in der Europäischen Union
Rappresentante autorizzato nell’Unione europea
Erkend vertegenwoordiger in de Europese
Gemeenschap
Autoriseret repræsentant i Den Europæiske Union
Auktoriserad representant i Europeiska unionen
Autorisert representant i EU
Valtuutettu edustaja Euroopan yhteisössä
Εξουσιοδοτημένος αντιπρόσωπος στην Ευρωπαϊκή
Κοινότητα
Representante autorizado na União Europeia
Autorizovaní zástupci v zemích Evropské unie
Volitatud esindaja Euroopa Liidus
Hivatalos képviselő az Európai Unióban
Pilnvarotais pārstāvis Eiropas Savienībā
Įgaliotas atstovas Europos Sąjungoje
Autoryzowany przedstawiciel na terenie Unii
Europejskiej
Splnomocnený zástupca v Európskej únii
Avrupa Topluluğundaki Yetkili Temsilci
Reprezentant autorizat în Comunitatea Europeană
Pooblaščeni zastopnik v Evropski skupnosti
EC REP
CAUTION: Federal law (USA) restricts this device to sale
by or on the order of a physician.
ATTENTION : La loi fédérale des États-Unis restreint la
vente de ce dispositif par un médecin ou sur prescription d’un médecin.
PRECAUCIÓN: La ley federal restringe la venta de este
dispositivo a médicos o por prescripción facultativa.
VORSICHT: Die US-amerikanische Bundesgesetzgebung
beschränkt den Verkauf dieser Vorrichtungen auf
einen Arzt bzw. auf ärztliche Anordnung
ATTENZIONE: la normativa federale statunitense limita
la vendita dei presenti dispositivi ai soli medici o
dietro presentazione di prescrizione medica.
LET OP: De federale wetgeving (VS) beperkt de verkoop
van deze apparaten tot door, of op voorschrift
van, een arts.
FORSIGTIG: Ifølge amerikansk lovgivning må disse
anordninger kun sælges af eller på foranledning
af en læge.
VARNING: Federal lagstiftning (i USA) begränsar
försäljning av dessa anordningar till läkare eller
enligt läkares förskrivning.
ADVARSEL: Føderal lovgivning (USA) tillater bare salg
av disse anordningene av lege eller etter rekvisisjon
fra en lege.
HUOMIO: LIITTOVALTION laki (USA) rajoittaa näiden
tuotteiden myynnin lääkäreiden toimesta tai
määräyksestä suoritettavaksi.
ΠΡΟΣΟΧΗ: Το ομοσπονδιακό δίκαιο (Η.Π.Α.) περιορίζει την
πώληση αυτής της συσκευής κατόπιν εντολής ιατρού.
PRECAUÇÃO: A lei federal (EUA) restringe a venda destes
aparelhos por ou sob a ordem de um médico.
UPOZORNĚNÍ: Federální zákony USA omezují prodej
těchto zařízení pouze na lékaře nebo na objednávku
lékaře
ETTEVAATUST: (USA) föderaalseadustega on lubatud
seda seadet müüa ainult arstil või arsti korraldusel.
VIGYÁZAT: A Szövetségi törvények (USA) értelmében ez
az eszköz csak orvos által vagy orvosi rendelvényre
értékesíthető.
UZMANĪBU: ASV federālais likums nosaka, ka šo ierīci
drīkst pārdot tikai ārstiem vai pēc ārsta pasūtījuma.
ATSARGIAI: pagal federalinius įstatymus (JAV) šie
įtaisai gali būti parduodami tik gydytojams arba
jų nurodymu.
OSTRZEŻENIE: Na mocy przepisów prawa federalnego (USA)
sprzedaż opisywanych produktów może być prowad-
zona wyłącznie przez lub na zlecenie lekarza.
POZOR: Federálne zákony USA obmedzujú predaj tohto
zariadenia iba na pokyn alebo objednávku lekára.
Dikkat: ABD federal kanunlarına göre bu cihaz sadece
bir doktor tarafından veya emriyle satılabilir.
Atenţionare: Legea federală (SUA) restricţionează
vânzarea acestui dispozitiv numai de către sau la
comanda unui medic.
Previdno: Po zveznem zakonu (ZDA) je možno ta
pripomoček kupiti le od zdravnika ali po naročilu
zdravnika
Do not use if package is damaged
Ne pas utiliser si l’emballage est endommagé
No utilizar si el embalaje está dañado
Bei beschädigter Verpackung nicht verwenden
Non utilizzare se la confezione appare danneggiata
Niet gebruiken als de verpakking beschadigd is
Må ikke bruges, hvis emballagen er beskadiget
Använd inte om förpackningen är skadad.
Må ikke brukes hvis emballasjen er skadet
Ei saa käyttää, jos pakkaus on vahingoittunut
Μην το χρησιμοποιείτε εάν η συσκευασία έχει υποστεί ζημιά
Não utilizar se a embalagem estiver danificada
Nepoužívejte, pokud je obal poškozen
Mitte kasutada, kui pakend on kahjustatud
Ne használja, ha a csomagolás sérült
Nelietot, ja iepakojums ir bojāts
Nenaudoti, jei pakuotė yra pažeista
Nie używać w razie uszkodzenia opakowania
Nepoužívajte, ak je poškodené balenie
Ambalaj hasarlıysa kullanmayın
A nu se folosi dacă ambalajul este deteriorat
Ne uporabljajte, če je ovojnina poškodovana
2
STERILIZE
Do not resterilize
Ne pas restériliser
No reesterilizar
Nicht resterilisieren
Non risterilizzare
Niet opnieuw steriliseren
Må ikke gensteriliseres
Omsterilisera inte
Må ikke resteriliseres
Älä steriloi uudelleen
Μην επαναποστειρώνετε
Não reesterilize
Opakovaně nesterilizujte
Mitte resteriliseerida
Ne sterilizálja újra
Atkārtoti nesterilizēt
Nesterilizuoti pakartotinai
Nie sterylizować ponownie
Nesterilizujte opakovane
Tekrar sterilize etmeyin
A nu se resteriliza
Ne sterilizirajte ponovno
STERILE R
Sterilized using irradiation
Stérilisé par irradiation
Esterilizado por radiación
Mit Strahlen sterilisiert
Sterilizzato tramite irradiazione
Gesteriliseerd met gammastraling
Steriliseret ved hjælp af bestråling
Steriliserad med strålning
Sterilisert ved bruk av stråling
Steriloitu säteilyttämällä
Αποστειρωμένο με ακτινοβολία
Esterilizado com radiação
Sterilizováno ozářením
Steriliseeritud kiirgusega
Besugárzással sterilizálva
Sterilizēts ar starojumu
Sterilizuoti naudojant švitinimą
Wyjałowione przez napromieniowanie
Sterilizované žiarením
Radyasyonla sterilize edilmiştir
Sterilizat prin iradiere
Sterilizirano z obsevanjem
Batch code
Code de lot
Número de lote
Chargencode
Codice di lotto
Groepscode
Batchkode
Satskod
Batchkode
Eräkoodi
Κωδικός παρτίδας
Código do lote
Číslo šarže
Partii kood
Tételkód
Sērijas kods
Serijos kodas
Kod partii
Číslo šarže
Parti kodu
Număr lot
Koda serije
Catalogue number
Référence catalogue
Número de catálogo
Katalog-Nr.
Numero di catalogo
Catalogusnummer
Katalognummer
Katalognummer
Katalognummer
Luettelonumero
Αριθμός καταλόγου
Número de catálogo
Katalogové číslo:
Kataloogi number
Katalógusszám
REF kataloga numurs
Katalogo numeris
Numer katalogowy
Katalógové číslo
Katalog numarası
Număr catalog
Kataloška številka
REF
LOT
0123
The device complies with European Directive MDD
93/42/EEC
Le dispositif est conforme à la directive européenne
MDD 93/42/EEC
El dispositivo cumple con la normativa europea MDD
93/42/EEC
Die Vorrichtung erfüllt die Anforderungen der
europäischen Richtlinie 93/42/EWG über
Medizinprodukte
Questo Dispositivo è conforme alla Direttiva Europea
MDD 93/42/CEE
Dit hulpmiddel voldoet aan de Europese richtlijn MDD
93/42/EEG
Anordningen overholder det europæiske direktiv
MDD 93/42/EØF
Denna anordning uppfyller Europarådets direktiv
MDD 93/42/EEG
Anordningen er i samsvar med EU-direktiv MDD
93/42/EØF
Tämä laite noudattaa eurooppalaista direktiiviä MDD
93/42/ETY
Αυτή η συσκευή συμμορφώνεται με την Ευρωπαϊκή
Οδηγία MDD 93/42/EEC
O dispositivo está em conformidade com a Directiva
Europeia 93/42/CEE relativa a dispositivos médicos
Toto zařízení splňuje požadavky evropské směrnice
93/42/EHS o zdravotnických prostředcích
Seade vastab Euroopa meditsiiniseadmete direktiivile
93/42/EMÜ
Az eszköz megfelel az orvostechnikai eszközökről szóló
93/42/EGK európai irányelvnek
Ierīce atbilst Eiropas direktīvas MDD 93/42/EEK
prasībām
Šis prietaisas atitinka Tarybos direktyvos 93/42/EEB dėl
medicinos prietaisų reikalavimus
Urządzenie jest zgodne z europejską dyrektywą w
sprawie wyrobów medycznych-MDD 93/42/EWG
Zariadenie spĺňa ustanovenia smernice EÚ MDD
93/42/EHS
Bu aygıt MDD 93/42/EEC no’lu Avrupa Direktine
uygundur
Dispozitivul respectă directiva europeană MDD
93/42/CEE
Cihaz, MDD 93/42/EEC sayılı Avrupa Direkti ile uyumludur
Dispozitivul este conform cu Directiva Europeană MDD
93/42/CEE
Ta pripomoček je v skladu z evropsko direktivo MDD
93/42/EGS
sendo necessária para encher o COI. Siga as instruções do fabricante relativas à utilização da seringa de enchimento da marca Kyphon®. A seringa de bloqueio Kyphon® é embalada
com uma seringa de enchimento da marca Kyphon®.
EVENTOS ADVERSOS
Os eventos adversos potencialmente associados à utilização do COI incluem eventos graves, embora raros, que podem ser fatais.
Os eventos adversos incluem:
• Embolia de gordura, trombo ou outros materiais que possam provocar embolia pulmonar sintomática ou outras sequelas clínicas.
• Rotura com fragmentação da parte insuflável do COI resultando na retenção de um fragmento dentro da região afectada.
• Rotura do COI que origine a exposição ao meio de contraste, com a possibilidade de ocorrência de reacção alérgica ou anafiláctica.
• Infecção superficial ou profunda da ferida.
• Hemorragia ou hematoma.
INSTRUÇÕES DE UTILIZAÇÃO
ATENÇÃO: Siga as instruções do fabricante relativas à utilização da seringa de enchimento da marca Kyphon®.
ATENÇÃO: Os meios de contraste poderão ter diferentes níveis de viscosidade e precipitação que poderão originar tempos de enchimento e esvaziamento mais lentos. Por esta razão,
recomenda-se a utilização de meio de contraste a 60%.
1. Rode a tampa da abertura do estilete para apertar o estilete no COI. Empurre o êmbolo até onde for possível para dentro da seringa de bloqueio Kyphon®. Fixe a seringa de bloqueio
Kyphon® à abertura de enchimento do COI.
2. Puxe o êmbolo da seringa de bloqueio Kyphon® para trás. Rode o êmbolo para o fixar em posição na última ranhura da seringa.
3. Separe a seringa de bloqueio Kyphon® do COI.
4. Ligue a abertura de ligação, existente na tubagem da seringa de enchimento da marca Kyphon®, à abertura de enchimento do COI. O sistema está agora preparado e pronto a ser utilizado.
UTILIZAÇÃO DO COI
1. Seleccione o tamanho do COI com base no local de aplicação e no objectivo do tratamento. A figura 1 e a tabela 1 definem o diâmetro de enchimento (D) e o comprimento de
enchimento (C) dos COI em água a 37 °C, em incrementos de volume de enchimento até ao volume máximo de enchimento.
2. Estas dimensões podem variar durante a utilização do produto devido à variação local na estrutura óssea.
Tabela 1 – Dimensões do COI cheio (em água a 37 °C)
Número do modelo E103A Dimensões do dispositivo cheio
Tamanho 10/3 Volume Diâmetro médio (D1, D2) Comprimento (L)
Volume de enchimento máx. 4 ml 2 ml 12,9 mm 14,7 mm
Pressão de enchimento máx. 27 atm 4 ml 17,2 mm 19,1 mm
Número do modelo E153A Dimensões do dispositivo cheio
Tamanho 15/3 Volume Diâmetro médio (D1, D2) Comprimento (L)
Volume de enchimento máx. 4 ml 2 ml 12,1 mm 17,4 mm
Pressão de enchimento máx. 27 atm 4 ml 16 mm 22,1 mm
INSERÇÃO DO COI
1. É necessário um canal de acesso para a colocação do COI.
2. Siga as instruções de utilização das ferramentas de acesso ao osso escolhidas para criar um canal de acesso no osso.
3. Antes da utilização, retire a manga de inserção.
NOTA: A ponta distal do COI esvaziado alcança a extremidade distal da cânula quando o marcador de saída existente no lúmen exterior do COI entra na extremidade proximal da cânula.
4. Coloque o COI esvaziado no canal de acesso e posicione-o, sob orientação imagiológica, utilizando os marcadores radiopacos. Um movimento de rotação suave acompanhando o
empurrão para a frente pode facilitar a inserção.
5. Mantendo o COI imóvel, encha até 0,3 MPa (3 atm) para fixar o COI na devida posição. Se pretender, pode retirar o estilete.
ENCHIMENTO DO COI
1. Encha o COI sob controlo imagiológico contínuo. Utilize a perspectiva lateral para controlar a distância entre o córtex anterior e lateral. Utilize a perspectiva ântero-posterior para
controlar os córtices laterais.
2. Se não utilizar um controlo imagiológico contínuo, aumente o volume em pequenos incrementos (0,25 ml–0,5 ml). Avalie a posição do calcador nas perspectivas lateral e ânteroposterior antes de aumentar ainda mais o volume.
3. Pare quando o objectivo de tratamento for alcançado, ou seja, quando qualquer uma das partes do comprimento do COI cheio entrar em contacto com o osso cortical ou for atingido
o volume de enchimento máximo e/ou a pressão de enchimento máxima (ver tabela 1).
REMOÇÃO DO COI
ATENÇÃO: Não retire o COI sem que o componente insuflável esteja totalmente esvaziado. Nunca retire o COI se sentir resistência. Determine a causa da resistência por fluoroscopia
e tome as medidas necessárias.
Com uma seringa de enchimento da marca Kyphon® evacue o meio de contraste do COI até que o balão fique completamente esvaziado. Retire o COI do osso através da cânula com
um movimento de rotação suave.
• Se sentir resistência, ligue uma seringa de 30 ml à abertura de enchimento. Puxe o êmbolo da seringa até à marca dos “30 ml” para criar vácuo. Retome a remoção do COI.
• Confirme a entrada da parte insuflável do COI na cânula. Se o componente insuflável não se deslocar para dentro da cânula, faça avançar a cânula sobre o COI até ao marcador
radiopaco proximal. Após o avanço da cânula, retire o COI através da mesma. Se sentir resistência, retire o COI e a cânula ao mesmo tempo.
ESTERILIZAÇÃO
Esterilizado por radiação.
APRESENTAÇÃO
Os COI são fornecidos estéreis numa embalagem destacável. No caso de detectar danos na embalagem esterilizada, não a utilize e informe o fabricante.
MATERIAIS NÃO FORNECIDOS
• Seringa de enchimento da marca Kyphon® com seringa de bloqueio Kyphon®
• Meio de contraste (60%)
• Pequena tigela
NOTA: A seringa de enchimento da marca Kyphon® com seringa de bloqueio Kyphon® está disponível junto da Medtronic.
ARMAZENAMENTO
Os COI devem ser armazenados nos respectivos materiais de envio. Deve ter o devido cuidado para assegurar que os COI não são danificados. Conservar em local fresco e seco.
LIMITAÇÃO DE RESPONSABILIDADE
A MEDTRONIC NÃO SE RESPONSABILIZA POR QUAISQUER DANOS DIRECTOS, INDIRECTOS, ACIDENTAIS, CONSEQUENTES ou EXEMPLARES RESULTANTES DA REUTILIZAÇÃO DOS CALCADORES
DE OSSO INSUFLÁVEIS InflateFX™ PARA TRATAMENTO DE FRACTURAS.
EM CIRCUNSTÂNCIA ALGUMA SERÁ A MEDTRONIC RESPONSÁVEL POR QUAISQUER DANOS DIRECTOS, INDIRECTOS, ACIDENTAIS, CONSEQUENTES OU EXEMPLARES RESULTANTES OU
RELACIONADOS COM OS CALCADORES DE OSSO INSUFLÁVEIS InflateFX™ PARA TRATAMENTO DE FRACTURAS, COM BASE EM QUEBRA DE CONTRATO (INCLUINDO QUEBRA DE GARANTIA).
PEDIDOS DE INFORMAÇÃO
Para mais informações, contacte o Serviço de Apoio ao Cliente.
©2013 Medtronic Sofamor Danek USA, Inc. Reservados todos os direitos.
čESKY
INDIKACE
Nafukovací kostní ucpávka InflateFX™ (Inflatable Bone Tamp, IBT) pro ošetření fraktur je určena k použití jako konvenční kostní ucpávka k redukci fraktur a/nebo k vytvoření dutiny v
porézní kosti ruky, kosti holenní, kosti vřetenní a kosti patní.
POPIS ZAŘÍZENÍ
Viz obr. 1.
1. Uzávěr
2. Stylet
3. Port styletu
4. Plnicí port
5. Barevně kódovaná páska
6. Páska výstupní značky
7. Zaváděcí objímka
8. Rentgenkontrastní značky
9. Naplnitelná součást
• Naplnitelná součást IBT je konstruována tak, aby při expanzi stlačila porézní kost nebo posunula kortikální kost. Naplnitelná součást IBT je umístěna v blízkosti distálního konce
nástroje, viz obrázek 1.
• Tubus sestává ze dvou vzájemně nepropojených lumen. Vnější lumen se používá k plnění IBT a střední lumen obsahuje vyjímatelný výztužný stylet k zavádění IBT.
• Proximální konec tubusu má boční adaptér. Plnicí port adaptéru navazuje na vnější lumen. Port styletu navazuje na vnitřní lumen a obsahuje výztužný stylet. Stylet má na proximálním
konci uzávěr, který slouží k jeho případnému vyjmutí.
• Barevně kódovaná páska umístěná těsně distálně vůči adaptéru postranní větve, označuje velikost balónku (tj. žlutá páska pro velikost 10/3 a černá páska pro velikost 15/3).
• Páska výstupní značky, umístěná na vnějším lumen, se používá při zavádění IBT.
• Rentgenkontrastní značky, umístěné na distálním a proximálním konci pracovního povrchu nenaplněného IBT, umožňují skiaskopickou vizualizaci nenaplněného IBT během jeho umísťování.
KONTRAINDIKACE
• Krvácivá porucha nebo léčba, která zvyšuje pravděpodobnost nadměrného krvácení.
• Přítomnost aktivní nebo nedoléčené infekce v místě, kam se má aplikovat kostní výplň.
• Jakákoliv známá závažná alergie na kontrastní látku a výplň kostních dutin.
• Pacientka s potvrzeným těhotenstvím.
POZOR: Podle federálních zákonů (USA) je prodej tohoto zařízení povolen pouze lékařům nebo na lékařský předpis.
VÝSTRAHY
• Dojde-li ke zlomení zařízení, může být nutné jeho vytažení nebo chirurgická intervence.
• Nepoužívejte tento výrobek po datu exspirace (Použít do) vytištěném na obalu. Prostředek nemusí být po uplynutí data exspirace (Použít do) bezpečný a účinný.
• Naplnitelná komponenta může selhat v přítomnosti ostrých kostních štěpin nebo chirurgických nástrojů.
• Expanze IBT na větší než maximální plnicí objem může způsobit prasknutí balónku ještě před dosažením maximálního plnicího tlaku.
• Expanze IBT na vyšší než maximální plnicí tlak může způsobit prasknutí balónku ještě před dosažením maximálního plnicího objemu.
• K plnění balónku nikdy nepoužívejte vzduch nebo plynné médium.
UPOZORNĚNÍ
• Nafukovací kostní ucpávka je prostředek na jednorázové použití určený ke kontaktu s tkáněmi těla. Nepoužívejte, nezpracovávejte ani nesterilizujte opakovaně. Opakované použití
těchto nástrojů s sebou nese riziko kontaminace a může u pacienta způsobit infekci nebo křížovou infekci bez ohledu na čistící a sterilizační metody. Další zpracování také zvyšuje
riziko zhoršení výkonu zařízení, což může vést ke zranění nebo smrti pacienta.
• Před použitím nástroje je důležité si pozorně přečíst návod k použití a tato upozornění.
• IBT použijte před datem konce použitelnosti uvedeným na obalu.
• Nepoužívejte, je-li obal otevřený nebo poškozený, neboť může být narušena celistvost nebo sterilita výrobku.
• Nepoužívejte poškozené výrobky. Před použitím prohlédněte IBT a jeho obal a zkontrolujte, zda nedošlo k žádnému poškození.
• Před použitím zkontrolujte správnou funkci IBT a ověřte, zda je velikost IBT vhodná pro konkrétní zákrok, pro který se má použít.
• Tento výrobek nepoužívejte, pokud jste neabsolvovali příslušné školení. IBT může používat pouze lékař, který byl vyškolen v metodice použití kostních ucpávek. Lékaři používající
tato zařízení musí být obeznámeni s fyziologií a patologií zvolené části těla.
• S IBT je dovoleno manipulovat pouze při skiaskopickém pozorování pomocí rentgenového zařízení s vysokou kvalitou obrazu.
• IBT je možno plnit výhradně pomocí plnicí stříkačky o minimálním objemu 14 ml.
• IBT naplňujte výhradně kapalnou kontrastní látkou: doporučujeme její 60 % roztok. Dodržte pokyny výrobce týkající se indikací a použití kontrastní látky a upozornění ohledně
použití kontrastní látky.
• K plnění IBT nepoužívejte vzduch ani žádný jiný plyn.
• Charakteristiky inflace IBT se mění při jeho plnění uvnitř kosti.
• Generální opravy, repasování, opravy, úpravy nebo opakované sterilizace tohoto zařízení za účelem jeho dalšího použití se výslovně zakazují.
• Všechny chirurgické zákroky představují určité riziko, ale použití balónku při léčbě těchto zlomenin tato rizika z klinického hlediska nezvyšuje ve srovnání s tradičními metodami
repozice stlačených fragmentů kosti. Tato rizika zahrnují:
o Nemožnost správně reponovat roztříštěnou kost.
o Opožděné spojení nebo selhání spojení.
o Infekce.
o Poškození neurovaskulárních struktur nebo syndrom kompartmentu vedoucí ke ztrátě funkce nebo k amputaci.
POZNÁMKA: Plnicí stříkačka značky Kyphon® poskytuje vynikající kontrolu objemu v porovnání s jinými plnicími systémy (jako je například standardní stříkačka) a je nutná k plnění IBT.
Při použití plnicí stříkačky značky Kyphon® dodržujte pokyny k použití dodané výrobcem. Blokovací stříkačka Kyphon® je přibalena k plnicí stříkačce značky Kyphon®.
NEŽÁDOUCÍ PŘÍHODY
Nežádoucí příhody, které mohou být spojené s použitím IBT zahrnují závažné příhody, které mohou být smrtelné, i když jsou vzácné.
K nežádoucím příhodám patří:
• Embolizaci tukovými částicemi, krevními sraženinami nebo jinými částicemi, vedoucí k symptomatické embolii plic nebo jiným klinickým následkům.
• Ruptura s fragmentací naplnitelné části IBT, která vede k retenci fragmentu v postižené oblasti.
• Protržení IBT vedoucí k expozici kontrastní látce, a potenciálně k alergické reakci nebo anafylaxi.
• Hloubkovou nebo povrchovou infekci rány.
• Krvácení nebo hematom.
NÁVOD NA POUŽITÍ
POZOR: Při použití plnicí stříkačky značky Kyphon® dodržujte pokyny k použití dodané výrobcem.
POZOR: Kontrastní látky mohou mít různou viskozitu a míru srážení, což může způsobit delší doby naplňování a vyprazdňování. Z tohoto důvodu doporučujeme použití 60 % roztoku
kontrastní látky.
1. Otočte uzávěr na portu styletu tak, aby se stylet upevnil na IBT. Zatáhněte píst zcela do blokovací stříkačky Kyphon®. Připevněte blokovací stříkačku Kyphon® k plnicímu portu na IBT.
2. Zatáhněte zpět píst blokovací stříkačky Kyphon®. Otočte pístem tak, aby se aretoval v místě posledního zářezu stříkačky.
3. Odpojte blokovací stříkačku Kyphon® od IBT.
4. Spojovací port na hadičce plnicí stříkačky značky Kyphon® připojte k plnicímu portu na IBT. Systém je nyní připraven k použití.
POUŽITÍ IBT
1. Zvolte velikost IBT podle místa použití a cíle léčby. Vyobrazení 1 a tabulka 1 uvádějí průměr IBT po naplnění (D) a délku IBT po naplnění (L) ve vodě o teplotě 37 °C po přírůstcích
objemu plnění až do maximálního objemu plnění.
2. Tyto rozměry se mohou lišit během používání výrobku podle lokálních rozdílů ve struktuře kosti.
Tabulka 1 – Rozměry IBT po naplnění (ve vodě o 37 °C)
Číslo modelu E103A Rozměry po naplnění
Velikost 10/3 Objem Průměrný průměr (D1, D2) Délka (L)
Max. objem plnění 4 ml 2 ml 12,9 mm 14,7 mm
Max. tlak plnění 27 atm 4 ml 17,2 mm 19,1 mm
Číslo modelu E153A Rozměry po naplnění
Velikost 15/3 Objem Průměrný průměr (D1, D2) Délka (L)
Max. objem plnění 4 ml 2 ml 12,1 mm 17,4 mm
Max. tlak plnění 27 atm 4 ml 16 mm 22,1 mm
ZAVÁDĚNÍ IBT
1. Pro zavedení IBT je nutný přístupový kanál.
2. Podle návodu k použití zvolených nástrojů pro přístup ke kosti vytvořte přístupový kanál ke kosti.
3. Před použitím odstraňte zaváděcí objímku.
POZNÁMKA: Distální konec nenaplněného IBT dosáhne distálního konce kanyly tehdy, když výstupní značka na vnějším lumen IBT vstoupí do proximálního konce kanyly.
4. Vložte nenaplněný IBT do přístupového kanálu a pod rentgenovým naváděním jej umístěte pomocí rentgenkontrastních značek. Při jejím vkládání si můžete pomoci jemnými
kroutivými pohyby doprovázejícími posun dopředu.
5. Přidržujte IBT na místě a současně ji naplňte pod tlakem 0,3 Mpa (3 atm), aby se zafixovala pozice IBT. Podle potřeby vyjměte stylet.
PLNĚNÍ IBT
1. Naplňte IBT při trvalém rentgenovém navádění. Použijte laterální projekci ke sledování vzdálenosti od předního a laterálního kortexu. Použijte předozadní (AP) projekci ke sledování
laterálních kortexů.
2. Pokud nepoužíváte nepřetržité zobrazování, zvyšujte objem plnění po malých přírůstcích (0,25-0,5 ml). Sledujte umístění ucpávky pomocí boční a AP projekce, než budete dále
zvyšovat objem.
3. Zastavte plnění, jakmile dosáhnete cíle nebo až se kterákoli část délky naplněné IBT se dostane do kontaktu s kortikální kostí nebo je dosaženo maximálního objemu a/nebo
maximálního tlaku plnění (viz tabulka 1).
VYNĚTÍ IBT
POZOR: Nafukovací kostní ucpávku (IBT) nevytahujte, dokud není naplnitelná komponenta zcela vyprázdněna. Nikdy nevytahujte IBT, pokud narazíte na odpor. Stanovte příčinu odporu
skiaskopickým zobrazením a podnikněte veškeré potřebné nápravné kroky.
Pomocí plnicí stříkačky značky Kyphon® vypusťte kontrastní látku z IBT, až se balónek zcela vyprázdní. Vytáhněte IBT z kosti skrze kanylu jemným kroutivým pohybem.
• Cítíte-li odpor, připojte k plnicímu portu 30 ml stříkačku. Stáhněte zpět píst stříkačky ke značce 30 ml, aby se vytvořil podtlak. Pokračujte ve vytahování IBT.
• Ověřte si, že naplnitelná část IBT vstoupila do kanyly. Pokud se naplnitelná součást neposunuje do kanyly, přesuňte kanylu přes IBT až k proximální rentgenkontrastní značce. Po
přesunutí kanyly vytáhněte IBT skrze kanylu. Pokud cítíte odpor, vytáhněte IBT společně s kanylou.
STERILIZACE
Sterilizováno zářením.
STAV PŘI DODÁNÍ
IBT se dodává sterilní v obalu s odtrhovacím uzávěrem. V případě, že došlo k poškození sterilního obalu, výrobek nepoužívejte a uvědomte výrobce.
MATERIÁL, KTERÝ NENÍ SOUČÁSTÍ DODÁVKY
• Plnicí stříkačka značky Kyphon® s blokovací stříkačkou Kyphon®
• Kontrastní látka (60 %)
• Malá miska
POZNÁMKA: Plnicí stříkačka značky Kyphon® s blokovací stříkačkou Kyphon® je k dispozici u společnosti Medtronic.
UCHOVÁVÁNÍ
IBT se musí skladovat v původním obalu, v němž byl dodán. Je třeba postupovat opatrně, aby nedošlo k poškození IBT. Skladujte na chladném a suchém místě.
OMEZENÍ ODPOVĚDNOSTI
SPOLEČNOST MEDTRONIC NEZODPOVÍDÁ ZA ŽÁDNÉ PŘÍMÉ, NEPŘÍMÉ, NÁHODNÉ, NÁSLEDNÉ ANI EXEMPLÁRNÍ ŠKODY VZNIKLÉ NA ZÁKLADĚ OPAKOVANÉHO POUŽITÍ NAFUKOVACÍCH
KOSTNÍCH UCPÁVEK InflateFX™ PRO OŠETŘENÍ FRAKTUR.
SPOLEČNOST MEDTRONIC V ŽÁDNÉM PŘÍPADĚ NEZODPOVÍDÁ ZA ŽÁDNÉ PŘÍMÉ, NEPŘÍMÉ, NÁHODNÉ, NÁSLEDNÉ ANI EXEMPLÁRNÍ ŠKODY VZNIKLÉ NA ZÁKLADĚ POUŽITÍ NAFUKOVACÍCH
KOSTNÍCH UCPÁVEK InflateFX™ PRO OŠETŘENÍ FRAKTUR NEBO ZPŮSOBENÉ V SOUVISLOSTI S JEJICH POUŽITÍM, NÁROKOVANÉ NA PODKLADĚ PORUŠENÍ SMLOUVY (VČETNĚ PORUŠENÍ ZÁRUKY).
ŽÁDOSTI O INFORMACE
Pro další informace se prosím obraťte na zákaznický servis.
©2013 Medtronic Sofamor Danek USA, Inc. Všechna práva vyhrazena.
EESTI
NÄIDUSTUSED
Luumurru ravi täidetav luutampoon (Inflatable Bone Tamp, IBT) InflateFX™ on ette nähtud kasutamiseks tavaliste luutampoonidena murdude vähendamiseks ja/või tühimiku tekitamiseks
poorsesse käeluusse, sääreluusse, kodarluusse ja kandluusse.
SEADME KIRJELDUS
Vt joonist 1.
1. Kork
2. Stilett
3. Stiletiava
4. Täiteava
5. Värviline märgiriba
6. Väljumismärgi riba
7. Sisestushülss
8. Röntgenkontrastsed markerid
9. Täidetav osa
• IBT täidetav osa surub täitudes poorse luu kokku ja/või liigutab kortikaalset luud. IBT täidetav osa on seadme distaalse otsa lähedal, nagu on näidatud joonisel 1.
• Varre sees on kaks omavahel mitteühendatud valendikku. Välimine on IBT täitmiseks ja sisemises on eemaldatav jäigastav stilett IBT sisseviimiseks.
• Varre proksimaalsel otsal on külgmuhv. Muhvi täiteava on ühendatud välimise valendikuga. Stiletiava on ühendatud sisemise valendikuga ja selles on jäigastav stilett. Stiletil on
võimaliku eemaldamise hõlbustamiseks kork proksimaalses otsas.
• Värviline märgiriba, mis asub kohe külgmuhvi suhtes distaalselt, näitab ballooni suurust (st kollane riba 10/3 ja must 15/3 suuruse jaoks).
• IBT paigaldamisel kasutatakse välimisel valendikul asuvat väljundimarkeri riba.
• Tühja tööpinna distaalse ja proksimaalse otsa juures olevad röntgenkontrastsed markerid võimaldavad tühja IBT-d paigalduse ajal fluoroskoopiliselt visualiseerida.
VASTUNÄIDUSTUSED
• Veritsushäire või ravi, mis suurendab ülemäärase verejooksu võimalust.
• Aktiivne või lõpuni ravimata infektsioon luutühimiku täidise manustamiskohas.
• Mis tahes teadaolev raske allergia kontrastaine ja luutühimiku täidise suhtes.
• Kinnitatud rasedusega patsient.
ETTEVAATUST! Föderaalseaduste (USA) alusel võib antud toote müük toimuda ainult arsti poolt või korraldusel.
HOIATUSED
• Seadme murdumisel võib olla vajalik kirurgiline sekkumine või seadme eemaldamine.
• Ärge kasutage antud toodet pärast pakendile trükitud kõlblikkusaja möödumist. Pärast kõlblikkusaja möödumist ei ole seadme ohutus ega efektiivsus tagatud.
• Luuogad või kirurgilised instrumendid võivad põhjustada täidetava osa tõrke.
• IBT täitmine üle maksimaalse täitemahu võib põhjustada ballooni rebenemist enne maksimaalse täiterõhu saavutamist.
• IBT täitmine üle maksimaalse täiterõhu võib põhjustada ballooni rebenemist enne maksimaalse täitemahu saavutamist.
• Ärge kunagi kasutage ballooni täitmiseks õhku ega gaasilisi aineid.
ETTEVAATUSABINÕUD
• Täidetav luutampoon on ühekordselt kasutatav seade, mis on ette nähtud kokku puutuma kehakudedega. Mitte kasutada korduvalt, mitte ümber töödelda ega uuesti steriliseerida.
Nende seadmete korduva kasutamisega kaasneb saastumisoht ning olenemata kasutatavatest puhastus- või resteriliseerimismeetoditest võib see patsiendil põhjustada infektsiooni
või ristinfektsiooni. Ümbertöötlemised võivad suurendada ka seadme tööomaduste halvenemise riski, mis võib põhjustada patsiendi vigastusi või surma.
• Enne seadme kasutamist on tähtis lugeda hoolikalt käesolevat kasutusjuhendit ja järgmisi ettevaatusabinõusid.
• Kasutage IBT-d enne pakendil oleva kõlblikkusaja lõppemist.
• Mitte kasutada avatud või kahjustatud pakendi korral, kuna toote terviklikkus, sh steriilsus, võib olla rikutud.
• Mitte kasutada kahjustatud tooteid. Enne kasutamist veenduge, et IBT ja pakend on terved.
• Enne kasutamist veenduge, et IBT on töökindel ja konkreetse protseduuri jaoks sobiva suurusega.
• Mitte kasutada antud toodet piisava kvalifikatsiooni puudumisel. IBT-d võivad kasutada ainult arstid, kes on saanud ettevalmistuse luutampoonide kasutamise alal. Toodet kasutavad
arstid peavad hästi tundma valitud kehapiirkonna füsioloogilist ja patoloogilist anatoomiat.
• IBT-d võib kasutada ainult fluoroskoopilise jälgimise all koos kvaliteetseid kujutisi andva röntgenivarustusega.
• IBT-d tohib täita ainult 14 ml minimaalse mahuga täitesüstlaga.
• Täitmiseks sobib ainult vedel kontrastaine: soovitatav on 60% lahus. Järgige tootjapoolseid juhiseid kontrastaine näidustuste, kasutuse ja ettevaatusabinõude suhtes.
• Ärge kasutage IBT täitmiseks õhku ega muud gaasilist ainet.
• Täitmine luu sisemuses muudab IBT täitmisomadusi.
• Rangelt on keelatud seadme taastamine, uuendamine, parandamine, modifitseerimine või uuesti steriliseerimine selle edasiseks kasutamiseks.
• Kõik operatsioonid on seotud riskiga; kliinilisest seisukohast ei suurenda ballooni kasutamine nende luumurdude ravis siiski neid riske võrreldes traditsiooniliste, allasurutud
luufragmentide tõstmise meetoditega. Nende riskide hulka kuuluvad:
o luumurru fragmentide nõuetekohase vähendamise ebaõnnestumine;
o hiline ühinemine ja mitteühinemine;
o infektsioon;
o funktsiooni kaotuse või amputatsiooniga lõppev neurovaskulaarne kahjustus või kompressioonisündroom.
MÄRKUS. Võrreldes teiste täitesüsteemide, nt tavalise süstlaga, võimaldab Kyphon®-i kaubamärgiga täitesüstal mahtu paremini reguleerida ning on seetõttu IBT täitmisel nõutav. Järgige
Kyphon®-i kaubamärgiga täitesüstla tootja kasutusjuhiseid. Kyphon®-i sulgursüstal on pakendatud koos Kyphon®-i kaubamärgiga täitesüstlaga.
KÕRVALNÄHUD
IBT kasutamisega on seotud ehkki harvaesinevad, kuid surmaga lõppeda võivad tõsised kõrvalnähud.
Kõrvalnähtude hulka kuuluvad:
DŮLEŽITÉ INFORMACE O nafukovací kostní ucpávce InflateFX™
pro ošetření fraktur (velikosti 10/3 a 15/3)
Oluline Teave luumurru ravi täidetava luutampooni
InflateFX™ (suurused 10/3 ja 15/3) kohta
• Rasvast, trombist või mõnest muust materjalist tingitud emboolia, mis viib sümptomaatilise kopsuemboolia või mõne muu kliinilise järelhaiguse tekkeni.
• IBT täidetava osa fragmenteerumisega rebend, mille tagajärjel fragment jääb kahjustatud piirkonda.
• IBT rebendist tulenev kontrastainega kokkupuude, mis võib põhjustada allergilist reaktsiooni või anafülaksiat.
• Sügav või pindmine haavainfektsioon.
• Verejooks või hematoom.
KASUTUSJUHISED
ETTEVAATUST! Järgige Kyphon®-i kaubamärgiga täitesüstla tootja kasutusjuhiseid.
ETTEVAATUST! Kontrastaine võib olla erineva viskoossus- ja sadenemistasemega, mis võib põhjustada täitmise ja tühjendamise aeglustumist. Seetõttu soovitatakse kasutada 60%
kontrastaine lahust.
1. Stileti kinnitamiseks IBT-le keerake stiletiaval korki. Suruge kolb lõpuni Kyphon®-i sulgursüstlasse. Kinnitage Kyphon®-i sulgursüstal IBT täiteavale.
2. Tõmmake Kyphon®-i sulgursüstla kolb tagasi. Keerake kolbi selle lukustamiseks süstla viimase pilu kohal.
3. Eemaldage Kyphon®-i sulgursüstal IBT-lt.
4. Kinnitage Kyphon®-i kaubamärgiga täitesüstla voolikul asuv ühendusava IBT täiteavale. Süsteem on nüüd ette valmistatud ja töökorras.
IBT KASUTAMINE
1. Valige IBT suurus vastavalt kohale ja ravi eesmärgile. Joonis 1 ja tabel 1 näitavad IBT täidetud diameetrit (D) ja täidetud pikkust (L) 37 °C vees, kus saavutatakse maksimaalne
täitemaht.
2. Need mõõtmed võivad toote kasutamisel varieeruda olenevalt luuehituse lokaalsest eripärast.
Tabel 1 - IBT mõõtmed täidetult (37 °C vees)
Mudeli number E103A Mõõtmed täidetult
Suurus 10/3 Maht Keskmine diameeter (D1, D2) Pikkus (L)
Max täitemaht 4 ml 2 ml 12,9 mm 14,7 mm
Max täiterõhk 27 atm 4 ml 17,2 mm 19,1 mm
Mudeli number E153A Mõõtmed täidetult
Suurus 15/3 Maht Keskmine diameeter (D1, D2) Pikkus (L)
Max täitemaht 4 ml 2 ml 12,1 mm 17,4 mm
Max täiterõhk 27 atm 4 ml 16 mm 22,1 mm
IBT PAIGALDAMINE
1. IBT paigaldamisel on oluline ligipääsukanali olemasolu.
2. Järgige luu ligipääsukanali loomiseks valitud luu ligipääsuvahendite¨ kasutusjuhiseid.
3. Eemaldage enne kasutamist sisestushülss.
MÄRKUS. Tühja IBT distaalne ots on jõudnud kanüüli distaalsesse otsa, kui IBT välise valendiku väljundi märk jõuab kanüüli proksimaalsesse otsa.
4. Asetage tühi IBT ligipääsukanalisse ja seadke see kujutist jälgides paika, kasutage seejuures röntgenkontrastseid markereid. Kerge pöörav liigutus koos edasisurumisega aitab
paigaldamisele kaasa.
5. Hoidke IBT-d paigal ja täitke see asendi fikseerimiseks rõhuni 0,3 MPa (3 atm). Soovi korral eemaldage stilett.
IBT TÄITMINE
1. Täitke IBT seda pidevalt ekraanil jälgides. Kasutage külgvaadet, et hinnata kaugust eesmisest ja külgmisest korteksist. Kasutage külgmiste korteksite hindamisel otsevaadet.
2. Ilma pideva jälgimiseta suurendage täitemahtu väikeste koguste (0,25–0,5 ml) kaupa. Hinnake enne täitmise jätkamist tampooni asendit külg- ja otsevaates.
3. Peatage täitmine, kui ravi eesmärk on saavutatud või kui mingi osa IBT kogu täidetud pikkusest puudutab kortikaalset luud või maksimaalne täitemaht ja/või täiterõhk on saavutatud
(vt tabelit 1).
IBT EEMALDAMINE
ETTEVAATUST! Ärge eemaldage IBT-d enne täidetava osa täielikku tühjenemist. Ärge tõmmake IBT-d tagasi, kui tunnete takistust. Selgitage takistuse põhjus fluoroskoobi all ja
rakendage vastavaid abimeetmeid.
Eemaldage Kyphon®-i kaubamärgiga täitesüstla abil kontrastaine IBT-st, kuni balloon on täiesti tühi. Eemaldage IBT luust läbi kanüüli ettevaatliku pöörava liigutusega.
• Takistuse korral ühendage täiteavale 30 ml süstal. Tõmmake süstla kolb vaakumi tekitamiseks tagasi kuni märgini 30 ml. Jätkake IBT eemaldamist.
• Veenduge, et IBT täidetav osa on sisenenud kanüüli. Kui täidetav osa ei liigu kanüüli, liigutage kanüüli edasi üle IBT kuni proksimaalse röntgenkontrastse markerini. Pärast kanüüli
edasist liigutamist tõmmake IBT läbi kanüüli. Kui tunnete takistust, eemaldage kanüül ja IBT koos.
STERILISEERIMINE
Steriliseeritud kiiritusega.
TARNEVIIS
IBT-d on pakitud steriilsesse lahtirebitavasse pakendisse. Steriilse pakendi kahjustuse korral mitte kasutada ja teatada tootjale.
MATERJALID, MIS PAKENDIS EI SISALDU
• Kyphon®-i kaubamärgiga täitesüstal koos Kyphon®-i sulgursüstlaga
• Kontrastaine (60%)
• Väike kauss
MÄRKUS. Kyphon®-i kaubamärgiga täitesüstal koos Kyphon®-i sulgursüstlaga on saadaval Medtronic’ust.
SÄILITAMINE
IBT-sid tuleb säilitada originaalses tarnepakendis. Tuleb hoolikalt jälgida, et IBT-d ei saaks kahjustada. Hoida jahedas ja kuivas kohas.
VASTUTUSE PIIRANGUD
MEDTRONIC EI VASTUTA MISTAHES OTSESE, KAUDSE, JUHUSLIKU EGA TEGEVUSE TULEMUSEST JOHTUVA KAHJU ega TRAHVIKULUDE EEST, MIS ON TEKKINUD SEOSES LUUMURRU RAVI
TÄIDETAVATE LUUTAMPOONIDE InflateFX™ KORDUVA KASUTAMISEGA.
KYPHON EI VASTUTA MITTE MINGIL JUHUL MISTAHES OTSESE, KAUDSE, JUHUSLIKU VÕI TEGEVUSE TULEMUSEST JOHTUVA KAHJU EGA TRAHVIKULUDE EEST, MIS ON TEKKINUD SEOSES
LUUMURRU RAVI TÄIDETAVATE LUUTAMPOONIDEGA InflateFX™ LEPINGUST MITTEKINNIPIDAMISE TÕTTU (SEALHULGAS GARANTIITINGIMUSTE RIKKUMINE).
TEABENÕUDED
Lisateabe saamiseks pöörduge klienditeeninduse poole
©2013 Medtronic Sofamor Danek USA, Inc. Kõik õigused kaitstud.
MaGYar
HASZNÁLATI JAVALLATOK
Az InflateFX™ töréskezelő felfújható csonttömörítő eszköz (IBT) hagyományos csonttömörítőként történő használat céljára szolgál a törések csökkentéséhez és/vagy a szivacsos csontbeli
üreg kialakításához a kézben, a sípcsontban, az orsócsontban és a sarokcsontban.
AZ ESZKÖZ LEÍRÁSA
Lásd az 1. ábrát.
1. Kupak
2. Mandrin
3. Mandrin nyílás
4. Feltöltő nyílás
5. Színkódolt sáv
6. Kilépési marker sáv
7. Bevezetőhüvely
8. Sugárfogó markerek
9. Feltölthető komponens
• Az IBT felfújható komponense arra szolgál, hogy feltöltődésekor összenyomja a szivacsos csontot és/vagy elmozdítsa a kortikális csontot. Az IBT felfújható komponense az 1. ábrán
látható módon az eszköz disztális csúcsához közel helyezkedik el.
• A nyél két egymástól elkülönített lument tartalmaz. A külső lumen az IBT feltöltésére szolgál, a középső lumen pedig egy kivehető merevítő mandrint tartalmaz az IBT bevezetéséhez.
• A nyél proximalis végén egy oldalkar adapter található. Az adapter feltöltő nyílása a külső lumennel áll kapcsolatban. A mandrin nyílása a belső lumennel áll kapcsolatban és ebben
helyezkedik el a merevítő mandrin. A mandrin az opcionális eltávolítás megkönnyítése érdekében proximális végén egy kupakkal van ellátva.
• Az oldalkar adapterhez képest éppen disztális helyzetben lévő színkódolt sáv a ballon méretét jelzi (azaz a sárga sáv a 10/3 méretet, a fekete sáv a 15/3 méretet).
• A külső lumenen elhelyezkedő kilépési marker sáv az IBT bevezetése során kerül alkalmazásra.
• A leeresztett munkafelület disztális és proximális végén levő sugárfogó markerek lehetővé teszik a leeresztett IBT fluoroszkópos vizualizálását pozícionálás közben.
ELLENJAVALLATOK
• Vérzési rendellenesség vagy a túlzott mértékű vérzés kockázatát növelő kezelés.
• Aktív vagy nem teljesen kezelt fertőzés jelenléte azon a helyen, ahol a csontüregkitöltő anyag alkalmazásra kerülne.
• Bármilyen ismert súlyos allergia a kontrasztanyagokra vagy a csontüregkitöltő anyagra.
• A beteg megállapított terhessége.
VIGYÁZAT: A szövetségi (USA) törvények értelmében ez az eszköz csak orvos által, vagy orvosi rendelvényre árusítható.
FIGYELMEZTETÉSEK
• Az eszköz törése beavatkozást, vagy az eszköz visszahúzását teheti szükségessé.
• Ne használja a jelen terméket a csomagolásra nyomtatott lejárati idő („Felhasználható”) után. Lejárati ideje („Felhasználható”) után az eszköz nem feltétlenül biztonságos vagy hatékony.
• A felfújható komponens az éles csontszilánkokkal vagy a sebészeti eszközökkel történő érintkezés következtében tönkremehet.
• Az IBT maximális feltöltési térfogatot meghaladó feltöltése hatására a ballon megrepedhet, mielőtt elérné a maximális feltöltési nyomást.
• Az IBT maximális feltöltési nyomást meghaladó feltöltése hatására a ballon megrepedhet, mielőtt elérné a maximális feltöltési térfogatot.
• Soha ne használjon levegőt vagy bármilyen gáznemű anyagot a ballon feltöltéséhez.
ÓVINTÉZKEDÉSEK
• A felfújható csonttömörítő eszköz a testszövetekkel rendeltetésszerűen érintkezésbe kerülő, egyszer használatos eszköz. Tilos újra felhasználni, újra feldolgozni vagy újrasterilizálni.
Az eszköz újra felhasználása a szennyeződés kockázatát hordozza, és a beteg fertőzését vagy keresztfertőzését okozhatja, a tisztítási vagy újrasterilizálási módoktól függetlenül.
Fennáll az eszköz újrafeldolgozás miatti elhasználódásának a fokozott veszélye is, amely a beteg sérüléséhez, vagy halálához vezethet.
• Fontos a használati utasítás és az itt leírt óvintézkedések gondos elolvasása az eszköz működtetése előtt.
• Az IBT-t a csomagoláson feltüntetett „Felhasználható” időpont előtt fel kell használni.
• Ne használja, ha a csomagolás fel lett nyitva vagy megsérült, ellenkező esetben veszélybe kerülhet a termék épsége, egyebek között sterilitása.
• Ne használja a terméket, ha az sérült. Használat előtt vizsgálja meg az IBT-t és annak csomagolását, hogy azok nem sérültek-e meg.
• Használat előtt az IBT-t meg kell vizsgálni működőképességét illetően és meg kell győződni róla, hogy mérete megfelel-e annak az adott eljárásnak, amelyre használni akarja.
• Ne használja ezt a terméket, ha arra nincs megfelelően kiképezve. Az IBT-t csak a csonttömörítő eljárásokra kiképzett orvosok használhatják. Az eszközt használó orvosoknak
ismerniük kell a kiválasztott anatómia fiziológiáját és pathológiáját.
• Az IBT-t kizárólag kiváló minőségű képeket nyújtó radiográfiás berendezéssel végzett fluoroszkópos megfigyelés alatt szabad manipulálni.
• Az IBT-t kizárólag minimum 14 ml térfogat kapacitású feltöltő fecskendővel szabad feltölteni.
• Az IBT-t kizárólag folyékony kontrasztanyaggal szabad felfújni: ajánlatos 60%-os oldat alkalmazása. Kövesse a gyártó útmutatásait a kontrasztanyagra vonatkozó javallatok, a
használat és a „Figyelem” szintű figyelmeztetések tekintetében.
• Soha ne használjon levegőt vagy más gázt az IBT feltöltésére.
• A csonton belüli feltöltés megváltoztatja az IBT feltöltési jellemzőit.
• Kifejezetten tilos az ismételt felhasználhatóság érdekében az eszköz helyreállítása, felújítása, javítása, módosítása, vagy újra sterilizálása.
• Minden műtétnek vannak kockázatai; azonban a ballon használata ezen törések kezeléséhez klinikai szempontból nem növeli ezeket a kockázatokat a benyomódott csontfragmentumok
kiemelésére szolgáló hagyományos módszerekhez viszonyítva. A kockázatok egyebek között az alábbiak:
o A törött fragmentumok megfelelő csökkentésének elmaradása.
o Késleltetett összeforrás vagy az összeforrás elmaradása.
o Fertőzés.
o Neurovascularis sérülés vagy rekeszszindróma, mely a funkció megszűnéséhez vagy amputációhoz vezet.
MEGJEGYZÉS: A Kyphon® márkázott feltöltőfecskendő a többi feltöltő rendszerhez, pl. egy hagyományos fecskendőhöz képest kiemelkedő térfogatszabályzást biztosít, és annak
használata kötelező az IBT feltöltéséhez.
A Kyphon® márkázott feltöltőfecskendő használatához kövesse a gyártó utasításait. A Kyphon® reteszelőfecskendő a Kyphon® márkázott feltöltőfecskendővel együtt van csomagolva.
NEMKÍVÁNATOS ESEMÉNYEK
Az IBT használatával kapcsolatba hozható nemkívánatos események között szerepelnek olyan súlyos események, amelyek ritkák ugyan, de halálosak lehetnek. A nemkívánatos
események közé tartoznak egyebek között az alábbiak:
• Zsír, thrombus vagy más anyagok okozta embólia, amely szimptomatikus tüdőembóliához vagy más klinikai következményekhez vezethet.
• Az IBT felfújható részének fragmentálódással járó megrepedése, amelynek eredményeképp egy fragmentum az érintett rész belsejében maradhat.
• Az IBT megrepedése, amelynek következtében a páciens érintkezésbe kerülhet a kontrasztanyaggal, ez pedig allergiás reakcióhoz vagy anafilaxishoz vezethet.
• Mély vagy felszínes sebfertőzés.
• Vérzés vagy vérömleny.
HASZNÁLATI UTASÍTÁS
VIGYÁZAT: A Kyphon® márkázott feltöltőfecskendő használatához kövesse a gyártó utasításait.
VIGYÁZAT: A kontrasztanyag különböző viszkozitású és kicsapási szintű lehet, amely lassabb feltöltési és leeresztési időket okozhat. Emiatt ajánlatos a 60%-os kontrasztanyag használata.
1. Csavarja el a pálcika nyílásán levő kupakot, hogy a mandrint az IBT-hez erősítse. Tolja be teljesen a dugattyút a Kyphon® reteszelőfecskendőbe. A Kyphon® reteszelőfecskendőt
csatlakoztassa az IBT-n levő feltöltő nyíláshoz.
2. Húzza vissza a Kyphon® reteszelőfecskendő dugattyúját. A dugattyút fordítsa el a fecskendőn levő utolsó bevágásban való reteszeléshez.
3. Válassza le a Kyphon® reteszelőfecskendőt az IBT-ről.
4. A Kyphon® márkázott feltöltőfecskendő csövén levő csatlakozónyílást csatlakoztassa az IBT-n levő feltöltő nyíláshoz. Ezzel a rendszer előkészítése megtörtént és az használatra
készen áll.
AZ IBT HASZNÁLATA
1. A helyszín és a kezelés célja alapján válassza ki az IBT méretét. Az 1. ábra és 1. táblázat az IBT felfújt átmérőjét (D) és felfújt hosszát (L) mutatja 37 °C-os vízben, felfújási térfogat
egységekként, egészen a maximális felfújási térfogatig.
2. Ezek a méretek a termék használata közben a csont szerkezetének helyi változásai következtében változhatnak.
1. táblázat – Az IBT méretei feltöltött állapotban (37 °C-os vízben)
Típusszám E103A Méretek feltöltött állapotban
Méret 10/3 Térfogat Átlagos átmérő (D1, D2) Hossz (L)
Max. feltöltési térfogat 4 ml 2 ml 12,9 mm 14,7 mm
Max. feltöltési nyomás 27 atm 4 ml 17,2 mm 19,1 mm
Típusszám E153A Méretek feltöltött állapotban
Méret 15/3 Térfogat Átlagos átmérő (D1, D2) Hossz (L)
Max. feltöltési térfogat 4 ml 2 ml 12,1 mm 17,4 mm
Max. feltöltési nyomás 27 atm 4 ml 16 mm 22,1 mm
AZ IBT BEVEZETÉSE
1. Az IBT elhelyezéséhez egy hozzáférési csatornára van szükség.
2. A hozzáférési csatorna csontban történő kialakításához kövesse a kiválasztott csonthozzáférési eszközök használati utasításait.
3. Használat előtt távolítsa el a bevezetőhüvelyt.
MEGJEGYZÉS: A leeresztett IBT disztális csúcsa akkor érte el a kanül disztális végét, amikor az IBT külső lumenén levő kilépési marker belép a kanül proximális végébe.
4. Helyezze a leeresztett IBT-t a hozzáférési csatornába, és képalkotásos irányítás alatt a sugárfogó markerek segítségével pozicionálja. Az előretolás közben alkalmazott óvatos csavaró
mozgás segíthet a bevezetésben.
5. Az IBT-t helyben tartva 0,3 MPa (3 atm) értékre történő feltöltéssel rögzítse a helyén az IBT-t. A mandrin szükség esetén eltávolítható.
AZ IBT FELTÖLTÉSE
1. Az IBT felfújását folyamatos képalkotásos irányítás alatt végezze. Az anterior és lateralis cortextől való távolságot a lateralis nézetben kísérje figyelemmel. A lateralis cortexeket az
AP (anterio-posterior) nézetben kísérje figyelemmel.
2. Amennyiben nem alkalmaznak folyamatos képalkotást, akkor a térfogatot kis egységekben növelje (0,25 ml – 0,5 ml). A térfogat további növelése előtt a lateralis és AP nézetekben
ellenőrizze a tömörítő eszköz helyzetét.
3. Álljon meg, ha a kezelés elérte a célját, vagy ha az IBT feltöltött hosszának bármelyik része hozzáér a kortikális csonthoz, vagy elérte a maximális feltöltési térfogatot és/vagy a
maximális feltöltési nyomást (lásd az 1. táblázatot).
AZ IBT ELTÁVOLÍTÁSA
VIGYÁZAT: Nem húzza vissza az IBT-t, ha a felfújható komponens nincs teljesen leeresztve. Soha ne húzza vissza az IBT-t, ha ellenállást észlel. Fluoroszkóposan határozza meg az ellenállás
okát és tegye meg a szükséges intézkedéseket annak elhárítására.
Használja a Kyphon® márkázott feltöltőfecskendőt, hogy kiszívassa a kontrasztanyagot az IBT-ből, amíg a ballon teljesen le nem eresztett. Óvatos csavaró mozgással vegye ki az IBT-t
a csontból a kanülön keresztül.
• Ellenállás esetén csatlakoztasson egy 30 ml-es fecskendőt a feltöltő nyíláshoz. Húzza vissza a fecskendő dugattyúját a 30ml-es jelhez a vákuum létrehozására. Folytassa az IBT
eltávolítását.
• Győződjön meg az IBT felfújható részének a kanülbe történő belépéséről. Ha a feltölthető komponens nem lép be a kanülbe, tolja a kanült az IBT-n át a proximális sugárfogó
markerig. A kanül előretolása után a kanülön keresztül húzza ki az IBT-t. Ha ellenállást észlel, az IBT-t és a kanült egyszerre vegye ki.
STERILIZÁLÁS
Sugárzással sterilizált.
KISZERELÉS
Az IBT-k steril, széthúzható csomagolásban kerülnek kiszerelésre. A steril csomagolás sérülése esetén ne használja az eszközt, és értesítse a gyártót.
NEM MELLÉKELT ANYAGOK
• Kyphon® márkázott feltöltőfecskendő Kyphon® reteszelő fecskendővel
• Kontrasztanyag (60%)
• Kisméretű tál
MEGJEGYZÉS: A Kyphon® márkázott feltöltőfecskendő a Kyphon® reteszelőfecskendővel a Medtronic-tól szerezhető be.
TÁROLÁS
Az IBT-ket eredeti csomagolóanyagaikban kell tárolni. Megfelelő módon gondoskodni kell róla, hogy az IBT-k ne sérülhessenek meg. Hűvös, száraz helyen tárolandó.
A FELELOSSÉG KORLÁTOZÁSA
A MEDTRONIC SEMMILYEN KÖRÜLMÉNYEK KÖZÖTT NEM FELEL AZ InflateFX™ TÖRÉSKEZELŐ FELFÚJHATÓ CSONTTÖMÖRÍTŐ ESZKÖZÖK ISMÉTELT HASZNÁLATÁBÓL SZÁRMAZÓ KÖZVETLEN,
KÖZVETETT, JÁRULÉKOS, KÖVETKEZMÉNYES, VAGY KÜLÖNLEGES KÁROKÉRT.
A SZERZŐDÉS MEGSZEGÉSE ESETÉN (IDEÉRTVE A GARANCIA MEGSÉRTÉSÉT IS) A MEDTRONIC SEMMILYEN KÖRÜLMÉNYEK KÖZÖTT SEM FELEL AZOKÉRT A KÖZVETLEN, KÖZVETETT,
JÁRULÉKOS, KÖVETKEZMÉNYES, VAGY KÜLÖNLEGES KÁROKÉRT, AMELYEK AZ InflateFX™ TÖRÉSKEZELŐ FELFÚJHATÓ CSONTTÖMÖRÍTŐ ESZKÖZÖK HASZNÁLATA MIATT VAGY AZOK
KÖVETKEZTÉBEN KELETKEZTEK.
INFORMÁCIÓKÉRÉS
További információkért lépjen kapcsolatba a Vevőszolgálattal.
© 2013 Medtronic Sofamor Danek USA, Inc. Minden jog fenntartva.
LaTVISKI
LIETOŠANAS INDIKĀCIJAS
InflateFX™ piepildāmā kaulu spiede (IBT - Inflatable Bone Tamp) lūzumu ārstēšanai ir paredzēta lietošanai kā tradicionālā kaulu spiede, lai reponētu lūzumus un/vai izveidotu dobumu
trabekulārajā kaulā rokā, lielajā liela kaulā, spieķa kaulā un papēdī.
IERĪCES APRAKSTS
Skatīt 1. attēlu.
1. Vāciņš
2. Stilete
3. Stiletes pieslēgvieta
4. Piepildīšanas pieslēgvieta
5. Krāsas kodēta josla
6. Izejas marķiera josla
7. Ievietošanas uzmava
8. Starojumu necaurlaidīgie marķieri
9. Piepildāmā daļa
• IBT piepildāmā sastāvdaļa ir izstrādāta, lai saspiestu trabekulāro kaulu un/vai pārvietotu kortikālo kaulu piepildīšanas laikā. IBT piepildāmā daļa atrodas ierīces distālā gala tuvumā,
kā tas parādīts 1. attēlā.
• Spalu veido divi nesavienoti lūmeni. Ārējais lūmens tiek izmantots IBT piepildīšanai, bet centrālais lūmens ietver izņemamu atbalsta stileti IBT ievietošanai.
• Spala proksimālajam galam ir sānu atzara adapters. Adaptera piepildīšanas pieslēgvieta ir saistīta ar ārējo lūmenu. Stiletes pieslēgvieta ir saistīta ar iekšējo lūmenu un ietver atbalsta
stileti. Stiletes proksimālajā galā ir vāciņš noņemšanai nepieciešamības gadījumā.
• Krāsas kodētā josla, kas atrodas nedaudz distāli attiecībā pret sānu atzara adaptera, norāda balona izmēru (t.i., dzeltena josla ir izmēram 10/3, melna josla ir izmēram 15/3).
• Izejas marķējuma josla, kas atrodas uz ārējā lūmena, tiek izmantota IBT ievietošanas laikā.
• Starojumu necaurlaidīgie marķējumi, kas atrodas uz iztukšotās darba virsmas distālā un proksimālā gala, nodrošina fluoroskopisku iztukšotā IBT vizualizāciju pozicionēšanas laikā.
KONTRINDIKĀCIJAS
• Asiņošana vai ārstēšana, kas palielina masīvas asiņošanas iespēju.
• Aktīva vai nepilnīgi izārstēta infekcija vietā, kurā tiks pielietota kaula dobuma pildviela.
• Jebkāda zināma smaga alerģija pret kontrastvielu un kaula dobuma pildvielu.
• Ja pacientei ir apstiprināta grūtniecība.
UZMANĪBU! Federālā (ASV) likumdošana ļauj šo ierīci pārdot tikai ārstiem vai pēc to rīkojuma.
BRĪDINĀJUMI
• Ja ierīce salūzt, var būt nepieciešama ķirurģiska iejaukšanās vai izņemšana.
• Nelietojiet šo izstrādājumu pēc derīguma termiņa („Izlietot līdz”) datuma, kas uzdrukāts uz iepakojuma. Pēc derīguma termiņa beigām („Izlietot līdz”) ierīce var būt nedroša vai neefektīva.
• Asas kaulu šķembas vai ķirurģiskie instrumenti var bojāt piepildāmo sastāvdaļu.
• IBT piepildīšana virs maksimālā piepildīšanas apjoma var izraisīt balona plīsumu, pirms tas sasniedz maksimālo piepildīšanas spiedienu.
• IBT piepildīšana virs maksimālā piepildīšanas spiediena var izraisīt balona plīsumu, pirms tas sasniedz maksimālo piepildīšanas apjomu.
• Nekad nelietojiet gaisu vai gāzveida vielas, lai piepildītu balonu.
PIESARDZĪBAS NORĀDES
• Piepildāmā kaulu spiede ir vienreizējās lietošanas ierīce, kas paredzēta nonākšanai saskarē ar organisma audiem. Nelietojiet, neapstrādājiet un nesterilizējiet atkārtoti. Šo ierīču
atkārtota lietošana rada kontaminācijas risku un var izraisīt pacienta inficēšanos vai savstarpēju infekcijas pārnešanu, neskatoties uz izmantotajām tīrīšanas un atkārtotas sterilizācijas
metodēm. Veikto atkārtotās apstrādes soļu dēļ pastāv arī paaugstināts ierīces funkcionēšanas pasliktināšanās risks, kas var radīt pacienta traumu vai nāvi.
• Pirms ierīces lietošanas ir svarīgi rūpīgi izlasīt lietošanas instrukciju un šīs piesardzības norādes.
• Izlietojiet IBT līdz „Izlietot līdz” datumam, kas norādīts uz iepakojuma.
• Nelietojiet, ja iepakojums ir atvērts vai bojāts, jo var būt traucēta izstrādājuma integritāte, tai skaitā sterilitāte.
• Nelietojiet bojātus izstrādājumus. Pirms lietošanas pārbaudiet IBT un iepakojumu, vai nav bojājumu.
• Pirms lietošanas pārbaudiet IBT, lai pārliecinātos par tā darbību un to, vai izmērs atbilst noteiktai procedūrai, kam tas paredzēts.
• Nelietojiet šo izstrādājumu, ja neesat atbilstoši apmācīti. IBT var izmantot tikai ārsti, kas guvuši apmācību kaulu spiedes pielietošanā. Ārstiem, kas izmanto šo ierīci, ir labi jāpārzina
izvēlētās anatomijas fizioloģija un patoloģija.
• IBT drīkst izmantot, vienīgi fluoroskopiski novērojot ar rentgenogrāfiskām iekārtām, kas nodrošina augstas kvalitātes attēlveidošanu.
• IBT ir piepildāms, tikai izmantojot piepildīšanas šļirci ar minimālo tilpumu 14 ml.
• Piepildiet IBT tikai ar šķidru kontrastvielu: ieteicams izmantot 60% šķīdumu. Ievērojiet ražotāja norādījumus par kontrastvielas indikācijām, lietošanu un brīdinājumiem.
• Nelietojiet gaisu vai citu gāzi, lai piepildītu IBT.
• IBT piepildīšanas raksturojumu maina piepildīšana kaulā iekšēji.
• Ierīces labošana, atjaunošana, remontēšana, pārveidošana vai atkārtota sterilizēšana, lai to izmantotu atkārtoti, ir stingri aizliegta.
• Jebkādai ķirurģiskajai manipulācijai ir riski, taču, balona izmantošana šo lūzumu ārstēšanā no klīniskā viedokļa nepaaugstina šos riskus salīdzinājumā ar tradicionālām saspiestu
kaulu fragmentu pacelšanas metodēm. Šie riski ietver:
o nespēju pienācīgi reponēt lūzuma fragmentus;
o novēlotu savienošanu un nesavienošanu;
o infekciju;
o nervu un asinsvadu bojājumu vai fasciālās telpas sindromu, kas izraisa funkcijas zaudējumu vai amputāciju.
PIEZĪME: Kyphon® piepildīšanas šļirce nodrošina labāku tilpuma kontroli salīdzinājumā ar citām piepildīšanas sistēmām, piemēram, standarta šļirci, un to nepieciešams lietot, lai piepildītu
IBT. Ievērojiet Kyphon® piepildīšanas šļirces ražotāja lietošanas instrukciju. Kyphon® noslēgšanas šļirce ir iepakota kopā ar Kyphon® piepildīšanas šļirci.
NEVĒLAMĀS BLAKUSPARĀDĪBAS
Ar IBT lietošanu potenciāli saistītās nevēlamās blakusparādības ietver nopietnas blakusparādības, kas, lai arī ir retas, var būt letālas.
Nevēlamās blakusparādības ietver:
• tauku, trombu vai citu daļiņu emboliju, kas izraisa simptomātisku plaušu emboliju vai citas klīniskas sekas;
• IBT piepildāmās daļas plīsumu ar fragmentāciju, kā rezultātā fragments paliek skartajā apvidū.
• IBT plīsums, kas izraisa kontrastvielas iedarbību, kura, iespējams, var radīt alerģisku reakciju vai anafilaksi.
• dziļu vai virspusēju brūces infekciju;
Fontos Információ Az InflateFX™ töréskezelő felfújható
csonttömörítő eszközről (10/3 és 15/3 méretek)
Svarīga Informācija Par InflateFX™ piepildāmo kaulu
spiedi lūzumu ārstēšanai (izmēri 10/3 un 15/3)
• asiņošanu vai hematomu.
LIETOŠANAS NORĀDĪJUMI
UZMANĪBU! Ievērojiet Kyphon® piepildīšanas šļirces ražotāja lietošanas instrukciju.
UZMANĪBU! Kontrastvielām var būt atšķirīgi viskozitātes un nogulsnēšanās līmeņi, kas var palēnināt piepildīšanas un iztukšošanas laikus. Šī iemesla dēļ ieteicams lietot 60% kontrastvielu.
1. Pagrieziet vāciņu uz stiletes pieslēgvietas, lai nostiprinātu stileti uz IBT. Iespiediet virzuli līdz galam Kyphon® noslēgšanas šļircē. Pievienojiet Kyphon® noslēgšanas šļirci IBT
piepildīšanas pieslēgvietai.
2. Pavelciet Kyphon® noslēgšanas šļirces virzuli atpakaļ. Pabīdiet virzuli, lai nostiprinātu to pozīcijā, kas atbilst pēdējai atzīmei uz šļirces.
3. Atvienojiet Kyphon® noslēgšanas šļirci no IBT.
4. Pievienojiet Kyphon® piepildīšanas šļirces caurulīšu savienojuma pieslēgvietu piepildīšanas pieslēgvietai uz IBT. Tagad sistēma ir sagatavota lietošanai.
IBT LIETOŠANA
1. Izvēlieties IBT izmēru, ņemot vērā apstrādājamo vietu un ārstēšanas mērķi. 1. attēlā un 1. tabulā ir norādīts IBT piepildītais diametrs (D) un piepildītais garums (L) ūdenī ar
temperatūru 37 °C pie piepildīšanas tilpuma palielinājumiem līdz maksimālajam piepildīšanas tilpumam.
2. Izstrādājuma lietošanas laikā šie izmēri var mainīties konkrēto atšķirību kaula struktūrā dēļ.
1. tabula – piepildīta IBT izmēri (ūdenī ar 37 °C temperatūru)
Modeļa numurs E103A Izmēri piepildītā stāvoklī
Izmērs 10/3 Tilpums Vid. diametrs (D1, D2) Garums (L)
Maks. piepildīšanas tilpums 4 ml 2 ml 12,9 mm 14,7 mm
Maks. piepildīšanas spiediens 27 atm 4 ml 17,2 mm 19,1 mm
Modeļa numurs E153A Izmēri piepildītā stāvoklī
Izmērs 15/3 Tilpums Vid. diametrs (D1, D2) Garums (L)
Maks. piepildīšanas tilpums 4 ml 2 ml 12,1 mm 17,4 mm
Maks. piepildīšanas spiediens 27 atm 4 ml 16 mm 22,1 mm
IBT IEVIETOŠANA
1. IBT ievietošanai ir nepieciešams piekļuves kanāls.
2. Lai veidotu piekļuves kanālu kaulā, ievērojiet lietošanas instrukcijas norādījumus par izraudzītajiem kaula piekļuves instrumentiem.
3. Pirms lietošanas izņemiet ievietošanas uzmavu.
PIEZĪME: Iztukšotās IBT distālais gals ir sasniedzis kaniles distālo galu, kad izejas marķieris uz IBT ārējā lūmena ir iegājis kaniles proksimālajā galā.
4. Ievietojiet iztukšoto IBT piekļuves kanālā un pozicionējiet to attēldiagnostikas kontrolē, izmantojot starojumu necaurlaidīgie marķieri. Viegla pagrieziena kustība, spiežot uz priekšu,
var palīdzēt ievadīšanā.
5. Turot IBT uz vietas, veiciet piepildīšanu līdz 3 atm, lai nostiprinātu IBT pozīcijā. Ja nepieciešams, izņemiet stileti.
IBT PIEPILDĪŠANA
1. Veiciet IBT piepildīšanu nepārtrauktā attēldiagnostikas kontrolē. Lai vērotu attālumu no priekšējās un sānu smadzeņu garozas, izmantojiet sānu projekciju. Lai novērotu sānu
smadzeņu garozas, izmantojiet AP (anterior-posterior, priekšējo-aizmugurējo) projekciju.
2. Ja nepārtraukta attēlveidošana netiek izmantota, palieliniet apjomu ar nelielu pieauguma soli (0,25 - 0,5 ml). Izvērtējiet spiedes izvietojumu sānu un AP projekcijā pirms tālāka
apjoma palielinājuma.
3. Pārtrauciet darbošanos, kad ir sasniegts procedūras mērķis vai jebkura IBT piepildītā daļa visā tā garumā sasniegusi kortikālo kaulvielu, vai ir sasniegts maksimālais piepildīšanas
apjoms un/vai maksimālais piepildīšanas spiediens (skatīt 1. tabulu).
IBT IZŅEMŠANA
UZMANĪBU! Neizņemiet IBT, ja piepildāmā sastāvdaļa nav pilnībā iztukšota. Nekad neizņemiet IBT, ja jūtat pretestību. Pretestības cēloni nosakiet, izmantojot fluoroskopiju, un, ja
nepieciešams, veiciet koriģējošu darbību.
Lietojiet Kyphon®piepildīšanas šļirci, lai atvilktu kontrastvielu no IBT, līdz balons ir pilnībā iztukšots. Izņemiet IBT no kaula caur kanili, viegli pagriežot.
• Ja jūtama pretestība, pievienojiet piepildīšanas pieslēgvietai 30 ml šļirci. Atvelciet šļirces virzuli atpakaļ līdz 30 ml atzīmei, lai radītu vakuumu. Atsāciet IBT izņemšanu.
• Pārbaudiet IBT piepildāmās daļas ieeju kanilē. Ja piepildāmā daļa nevirzās kanilē, virziet kanili pa IBT līdz proksimālajam starojumu necaurlaidīgam marķējumam. Pēc kaniles
pavirzīšanas izvelciet IBT cauri kanilei. Ja jūtama pretestība, izņemiet IBT un kanili vienlaikus.
STERILIZĀCIJA
Sterilizēts apstarojot.
PIEGĀDE
IBT tiek piegādātas sterilas atplēšamā iepakojumā. Ja sterilais iepakojums ir bojāts, nelietojiet izstrādājumu un paziņojiet ražotājam.
MATERIĀLI, KAS NETIEK PIEGĀDĀTI
• Kyphon® piepildīšanas šļirce ar Kyphon® noslēgšanas šļirci
• Kontrastviela (60%)
• Neliels trauks
PIEZĪME: Kyphon® piepildīšanas šļirci ar Kyphon® noslēgšanas šļirci var iegādāties Medtronic.
UZGLABĀŠANA
IBT jāuzglabā oriģinālajā iepakojuma materiālā. Rūpīgi sekojiet, lai nodrošinātu, ka IBT netiks bojātas. Uzglabāt vēsā, sausā vietā.
ATBILDĪBAS IEROBEŽOJUMS
MEDTRONIC NEATBILD PAR JEBKĀDIEM TIEŠIEM, NETIEŠIEM, NEJAUŠIEM VAI IZRIETOŠIEM VAI BRĪDINĀJUMA RAKSTURA BOJĀJUMIEM, KAS RADUŠIES InflateFX™ PIEPILDĀMĀS KAULU
SPIEDES LŪZUMU ĀRSTĒŠANAI ATKĀRTOTAS LIETOŠANAS REZULTĀTĀ.
MEDTRONIC NEKĀDĀ GADĪJUMA NEATBILD PAR JEBKĀDIEM TIEŠIEM, NETIEŠIEM, NEJAUŠIEM, IZRIETOŠIEM VAI BRĪDINĀJUMA RAKSTURA BOJĀJUMIEM, KAS RADUŠIES InflateFX™
PIEPILDĀMĀS KAULU SPIEDES LŪZUMU ĀRSTĒŠANAI LIETOŠANAS REZULTĀTĀ VAI SAISTĪBĀ AR TO, JA BOJĀJUMA CĒLONIS IR LĪGUMA (TAJĀ SKAITĀ GARANTIJAS) NOTEIKUMU NEIEVĒROŠANA.
INFORMĀCIJAS PIEPRASĪJUMI
Lai saņemtu plašāku informāciju, lūdzu, sazinieties ar klientu apkalpošanas nodaļu.
©2013 Medtronic Sofamor Danek USA, Inc. Visas tiesības aizsargātas.
liETUviŠKai
NAUDOJIMO INDIKACIJOS
Lūžiams gydyti skirtas slėginis kaulo užpildymo įtaisas (IBT) „InflateFX™“ gali būti naudojamas kaip įprastas kaulo užpildymo įtaisas lūžiams atstatyti ir (arba) ertmei sudaryti akytojoje
rankos kaulo, blauzdikaulio, stipinkaulio ir kulnakaulio medžiagoje.
ĮTAISO APRAŠYMAS
Žr. 1 pav.
1. Dangtelis
2. Zondas
3. Zondo jungtis
4. Pūtimo jungtis
5. Sutartinės spalvos žymeklis
6. Žiedinis išėjimo žymeklis
7. Įvedimo mova
8. Rentgenokontrastiniai žymekliai
9. Išpučiamasis komponentas
• Išpučiamasis IBT komponentas skirtas akytajai kaulinei medžiagai suspausti ir (arba) kortikaliniam kaului pajudinti išpučiant komponentą. Išpučiamasis IBT komponentas yra arti
įtaiso distalinio galo, kaip parodyta 1 pav.
• Velenėlyje yra du tarpusavyje nesusiję spindžiai. Išorinis spindis yra naudojamas IBT išpūsti, o centriniame spindyje yra išimamas standėjantis zondas, skirtas IBT įvesti.
• Proksimaliniame velenėlio gale yra adapteris laikiklis. Adapterio pūtimo jungtis liečiasi su išoriniu spindžiu. Zondo jungtis, kurioje yra kietasis zondas, liečiasi su vidiniu spindžiu.
Zondo proksimaliniame gale yra dangtelis, kurį prireikus galima nuimti.
• Sutartinės spalvos žymekliu, esančiu šiek tiek distaliau nuo adapterio laikiklio, nurodomas balionėlio dydis (pvz., geltonas žymeklis reiškia 10/3 dydį, o juodas – 15/3 dydį).
• Žiedinis išėjimo žymeklis, esantis ant išorinio spindžio, yra naudojamas IBT įvedimo metu.
• Rentgenokontrastiniai žymekliai, esantys ties distaliniu ir proksimaliniu neišpūsto darbinio paviršiaus galais, leidžia kontroliuoti neišpūsto IBT padėtį rentgenu.
KONTRAINDIKACIJOS
• Kraujavimo sutrikimas arba gydymas, dėl kurio padidėja smarkaus kraujavimo tikimybė.
• Aktyvi arba nevisiškai išgydyta infekcija numatomoje kaulo ertmių užpildo įliejimo vietoje.
• Bet kokia žinoma sunki alergija į kontrastinę medžiagą ir kaulo ertmių užpildą.
• Jei pacientei nustatytas nėštumas.
DĖMESIO: Federaliniai (JAV) įstatymai riboja šio įtaiso pardavimą – jį leidžiama parduoti tik gydytojams arba gydytojo nurodymu.
DĖMESIO
• Sulūžus įtaisui, gali reikėti įtaisą ištraukti arba atlikti chirurginę intervenciją.
• Nenaudokite įtaiso, jei ant pakuotės nurodytas galiojimo laikas pasibaigęs. Pasibaigus galiojimo laikui (tinka iki), naudoti įtaisą gali nebebūti saugu ar veiksminga.
• Aštrūs kaulo lūžgaliai arba chirurginiai instrumentai gali sukelti funkcinį išpučiamojo komponento sutrikimą.
• IBT išpūtus daugiau už maksimalų išpūtimo tūrį, balionėlis gali plyšti prieš pasiekiant maksimalų pūtimo slėgį.
• IBT pučiant didesniu už maksimalų pūtimo slėgiu, balionėlis gali plyšti prieš pasiekiant maksimalų išpūtimo tūrį.
• Niekada balionėlio neplėskite oru ar dujinėmis medžiagomis.
ATSARGUMO PRIEMONĖS
• Slėginis kaulo užpildymo įtaisas yra vienkartinio naudojimo įtaisas, skirtas liestis su kūno audiniais. Nenaudokite, neapdorokite ir nesterilizuokite pakartotinai. Pakartotinis šių
įtaisų naudojimas susijęs su užteršimo rizika ir gali sukelti pacientui infekciją ar kryžminę infekciją, nepriklausomai nuo taikomų valymo ir pakartotinio sterilizavimo metodų. Taip
pat dėl pakartotinio apdorojimo procedūros yra padidėjusi įtaiso savybių pablogėjimo rizika; dėl to galimas paciento sužalojimas arba mirtis.
• Prieš naudojant įtaisą svarbu perskaityti šias naudojimo instrukcijas ir atsargumo priemones.
• Nenaudokite IBT pasibaigus ant jo pakuotės nurodytam galiojimo laikui.
• Nenaudokite, jei pakuotė atidaryta ar pažeista, nes gali būti pažeistas gaminio vientisumas, įskaitant sterilumą.
• Nenaudokite pažeistų įtaisų. Prieš pradėdami naudoti patikrinkite, ar IBT ir pakuotė nėra pažeisti.
• Prieš pradedant naudoti reikėtų įsitikinti, kad IBT veikia tinkamai ir kad jo dydis yra tinkamas tai procedūrai, kuriai ketinama jį naudoti.
• Nenaudokite įtaiso, jeigu nebuvote tinkamai apmokyti. IBT turėtų naudoti tik tie gydytojai, kurie buvo apmokyti taikyti kaulų užpildymo metodus. Šiuos įtaisus naudojantys gydytojai
turi būti susipažinę su pasirinktos anatomijos fiziologija ir patologija.
• IBT turėtų būti naudojamas tik kontroliuojant rentgenu su kokybišką vaizdą užtikrinančia radiografine įranga.
• Išpučiant IBT, turi būti naudojamas mažiausiai 14 ml tūrio pripūtimo švirkštas.
• Pūskite į IBT tik skystą kontrastinę medžiagą; rekomenduojama naudoti 60 % tirpalą. Laikykitės gamintojo instrukcijų, kuriose aprašyti kontrastinės medžiagos indikacijos, naudojimas
ir atsargumo priemonės.
• Nenaudokite oro arba kitų dujų IBT išpūsti.
• Pučiant kaulo viduje IBT plečiamosios savybės keičiasi.
• Įtaisą remontuoti, atnaujinti, taisyti, modifikuoti ir pakartotinai sterilizuoti, siekiant pratęsti jo naudojimo laiką, yra griežtai draudžiama.
• Bet kokia operacija yra susijusi su rizika, tačiau lyginant su tradiciniais suspausto kaulo fragmentų pakėlimo metodais, klinikiniu požiūriu ši rizika nepadidėja, kai tokie lūžiai gydomi
naudojant balionėlį. Galima tokia rizika:
o Tinkamo lūžio fragmentų sumažinimo nesėkmė.
o Vėlyvas suaugimas ir nesuaugimas.
o Infekcija.
o Neurovaskulinis pažeidimas arba raumenų guolių sindromas, sukeliantis funkcijų praradimo ar amputacijos pasekmes.
PASTABOS: Firminis pripūtimo švirkštas „Kyphon®“ pasižymi geresne tūrio kontrole lyginant su kitomis pripūtimo sistemomis (pvz., standartiniu švirkštu); jis yra būtina IBT pripūtimo
priemonė. Naudodami firminį pripūtimo švirkštą „Kyphon®“, laikykitės gamintojo pateiktų naudojimo instrukcijų. Fiksuojamasis švirkštas „Kyphon®“ tiekiamas vienoje pakuotėje su
firminiu pripūtimo švirkštu „Kyphon®“.
NEPAGEIDAUJAMI REIŠKINIAI
Su IBT naudojimu susiję nepageidaujami reiškiniai apima ir sunkias komplikacijas, kurios, nors ir retos, gali būti mirtinos. Galimi nepageidaujami reiškiniai:
• Riebalų, kraujo ar kitų medžiagų embolai, sukeliantys simptominę plaučių emboliją ar kitokias klinikines pasekmes.
• Išpučiamosios IBT dalies plyšimas su fragmentacija, kuriai įvykus fragmentas gali pasilikti pakenktoje srityje.
• IBT trūkimas, sukeliantis kontrastinės medžiagos ištekėjimą, o tai gali sukelti alerginę reakciją ar anafilaksinį šoką.
• Gilios ar paviršinės žaizdos infekcija.
• Kraujavimas arba hematoma.
NAUDOJIMO TAISYKLĖS
DĖMESIO: Naudodami firminį pripūtimo švirkštą „Kyphon®“, laikykitės gamintojo pateiktų naudojimo instrukcijų.
DĖMESIO: Kontrastinė medžiaga gali būti skirtingų klampumo ir nusėdimo lygių, kurie gali sulėtinti išpūtimo ir subliūškinimo laiką. Dėl šios priežasties rekomenduojama naudoti
60 % kontrastinę medžiagą.
1. Užsukite dangtelį ant zondo jungties, kad pritvirtintumėte zondą prie IBT. Stumkite stūmoklį iki fiksuojamojo švirkšto „Kyphon®“ galo. Prijunkite fiksuojamąjį švirkštą „Kyphon®“
prie IBT pūtimo jungties.
2. Traukite fiksuojamojo švirkšto „Kyphon®“ stūmoklį atgal. Pasukite stūmoklį, kad užsifiksuotų ties paskutine švirkšto anga.
3. Ištraukite fiksuojamąjį švirkštą „Kyphon®“ iš IBT.
4. Prijunkite firminio pripūtimo švirkšto „Kyphon®“ vamzdelio jungtį prie IBT pūtimo jungties. Dabar sistema paruošta naudoti.
IBT NAUDOJIMAS
1. Parinkite IBT dydį, atsižvelgdami į vietą ir gydymo tikslą. 1 pav. ir 1 lentelė rodo išpūstų IBT diametrą (D) ir ilgį (L) 37 °C vandenyje, didinant išpūtimo tūrį iki maksimalaus išpūsto
IBT tūrio.
2. Įtaiso naudojimo metu dėl vietinių kaulų struktūros skirtumų šie matmenys gali skirtis.
1 lentelė. IBT matmenys išpūtus (37 °C vandenyje)
Modelio numeris E103A Matmenys išpūtus
Dydis 10/3 Tūris Vidutinis skersmuo (D1, D2) Ilgis (L)
Maks. išpūtimo tūris 4 ml 2 ml 12,9 mm 14,7 mm
Maks. pūtimo slėgis 27 atm 4 ml 17,2 mm 19,1 mm
Modelio numeris E153A Matmenys išpūtus
Dydis 15/3 Tūris Vidutinis skersmuo (D1, D2) Ilgis (L)
Maks. išpūtimo tūris 4 ml 2 ml 12,1 mm 17,4 mm
Maks. pūtimo slėgis 27 atm 4 ml 16 mm 22,1 mm
IBT ĮVEDIMAS
1. IBT įvesti reikalingas įvedimo kanalas.
2. Ruošdami įvedimo į kaulą kanalą, laikykitės pasirinktų įvedimo į kaulą įrankių naudojimo instrukcijų.
3. Prieš naudodami nuimkite įvedimo movą.
PASTABOS: Distalinis neišpūsto IBT galas pasiekia distalinį kaniulės galą, kai išėjimo žymeklis ant išorinio IBT spindžio pasiekia proksimalinį kaniulės galą.
4. Neišpūstą IBT įveskite į įvedimo kanalą ir naudodami rentgenokontrastinius žymeklius bei stebėdami rentgenu nustatykite reikiamą jo padėtį. Įvedimui palengvinti galite švelniai
pasukdami stumtelėti į priekį.
5. Nejudindami įvesto IBT, pūskite iki pasieksite 0,3 MPa (3 atm) slėgį, kad užfiksuotumėte IBT reikiamoje padėtyje. Jei reikia, zondą išimkite.
IBT IŠPŪTIMAS
1. Išpūskite IBT, tuo pat metu stebėdami rentgenu. Naudokite šoninę projekciją atstumui nuo priekinio ir šoninio kortikalinio kaulo paviršiaus stebėti. Naudokite priekinę ir užpakalinę
(AP) projekciją šoniniam kortikalinio kaulo paviršiui stebėti.
2. Jei negalite nuolat stebėti rentgenu, didinkite tūrį mažomis dozėmis (0,25–0,5 ml). Prieš toliau didindami tūrį įvertinkite užpildymo įtaiso padėtį šoniniame ir AP vaizde.
3. Sustokite, kai bus pasiektas gydymo tikslas arba bet kuri išpūsto IBT sienelės dalis priglus prie kortikalinio kaulo, arba bus pasiektas maksimalus išpūtimo tūris ir (arba) maksimalus
pūtimo slėgis (žr. 1 lent.).
IBT IŠTRAUKIMAS
DĖMESIO: IBT galima ištraukti tik visiškai subliūškinus išpučiamąjį komponentą. Niekada netraukite IBT esant pasipriešinimui. Stebėdami rentgenu nustatykite pasipriešinimo priežastį
ir imkitės priemonių pasipriešinimui pašalinti.
Firminiu pripūtimo švirkštu „Kyphon®“ traukite kontrastinę medžiagą iš IBT, kol iš balionėlis visiškai subliūkš. Švelniai sukdami per kaniulę ištraukite IBT iš kaulo.
• Jei jaučiamas pasipriešinimas, prie pūtimo jungties prijunkite 30 ml švirkštą. Traukite švirkšto stūmoklį atgal iki žymos „30ml“, kad susidarytų vakuumas. Toliau traukite IBT.
• Patikrinkite, ar išpučiamoji IBT dalis įvesta į kaniulę. Jei išpučiamasis komponentas neįeina į kaniulę, stumkite kaniulę per IBT iki proksimalinio rentgenokontrastinio žymeklio.
Įvedę kaniulę, per ją ištraukite IBT. Jei juntamas pasipriešinimas, ištraukite IBT ir kaniulę tuo pačiu metu.
STERILIZAVIMAS
Sterilizuota švitinant.
KAIP TIEKIAMAS
IBT tiekiami atplėšiamoje pakuotėje ir yra sterilūs. Tuo atveju, jei sterili pakuotė pažeista, instrumento nenaudokite ir praneškite apie tai gamintojui.
NEPATEIKIAMOS MEDŽIAGOS
• Firminis pripūtimo švirkštas „Kyphon®“ su fiksuojamuoju švirkštu „Kyphon®“
• Kontrastinė medžiaga (60 %)
• Dubenėlis
PASTABOS: Firminius pripūtimo švirkštus „Kyphon®“ ir fiksuojamuosius švirkštus „Kyphon®“ tiekia „Medtronic“.
LAIKYMAS
IBT turi būti laikomi pradinėse pakuotėse, kuriose buvo pristatyti. Būtina imtis tinkamų priežiūros priemonių, užtikrinančių, jog IBT nebus pažeisti. Laikyti vėsioje sausoje vietoje.
ATSAKOMYBĖS APRIBOJIMAS
MEDTRONIC NEATSAKO UŽ JOKIUS TIESIOGINIUS, NETIESIOGINIUS, ŠALUTINIUS, PASEKMINIUS AR BAUDINIUS NUOSTOLIUS, ATSIRADUSIUS DĖL PAKARTOTINIO SLĖGINIŲ KAULO UŽPILDYMO
ĮTAISŲ „InflateFX™“, SKIRTŲ LŪŽIAMS GYDYTI, NAUDOJIMO.
ESANT SUTARTIES PAŽEIDIMAMS (ĮSKAITANT GARANTINIŲ ĮSIPAREIGOJIMŲ PAŽEIDIMUS), „MEDTRONIC“ JOKIU ATVEJU NEATSAKO UŽ JOKIUS TIESIOGINIUS, NETIESIOGINIUS, ŠALUTINIUS,
PASEKMINIUS ARBA BAUDINIUS NUOSTOLIUS, ATSIRADUSIUS DĖL SLĖGINIŲ KAULO UŽPILDYMO ĮTAISŲ „InflateFX™“, SKIRTŲ LŪŽIAMS GYDYTI, ARBA SUSIJUSIUS SU JAIS.
PRAŠYMAI SUTEIKTI INFORMACIJOS
Norėdami gauti daugiau informacijos, kreipkitės į klientų aptarnavimo skyrių.
© „Medtronic Sofamor Danek USA, Inc.“, 2013 m. Visos teisės ginamos.
poLSKI
WSKAZANIA DO UŻYCIA
Napełniany balon ortopedyczny (ang. IBT) do leczenia złamań InflateFX™ jest przeznaczony do stosowania jako konwencjonalny balon ortopedyczny, w celu redukcji złamań i/lub
tworzenia pustej przestrzeni w kości gąbczastej ręki, piszczelowej, promieniowej i piętowej.
OPIS PRZYRZĄDU
Patrz Rys. 1.
1. Nakrętka
2. Mandryn
3. Port mandrynu
4. Port do napełniania
5. Pasek oznaczenia kolorem
6. Pasek znacznika wyjścia
7. Mankiet do wprowadzania
8. Cieniodajne znaczniki
9. Napełniany element
• Napełniany balon IBT jest przeznaczony do uciskania kości gąbczastej i/lub przemieszczania kości korowej w miarę napełniania go płynem. Napełniany element IBT znajduje się w
pobliżu dystalnej końcówki przyrządu, jak pokazano na Rys. 1.
• Trzonek zawiera dwa niezbieżne kanały. Kanał zewnętrzny służy do napełniania IBT, a kanał środkowy zawiera usuwalny usztywniający mandryn do wprowadzania IBT.
• Na proksymalnym końcu trzonka znajduje się łącznik ramienia bocznego. Port do napełniania na łączniku łączy się z kanałem zewnętrznym. Port mandrynu łączy się z kanałem
wewnętrznym i zawiera usztywniający mandryn. Na końcu proksymalnym mandryn ma nakrętkę w celu opcjonalnego wyjmowania mandrynu.
• Pasek oznaczenia kolorem, umieszczony dystalnie tuż obok złącza z ramieniem bocznym, wskazuje rozmiar balonu (np. żółty pasek oznacza rozmiar 10/3, a czarny pasek oznacza
rozmiar 15/3).
• Pasek znacznika wyjścia, umieszczony na kanale zewnętrznym, używany jest w czasie wprowadzania balonu IBT.
• Znaczniki cieniodajne, umieszczone na proksymalnym i dystalnym końcu opróżnionego balonu pozwalają na wizualizację fluoroskopową opróżnionego balonu IBT w czasie jego
umieszczania.
PRZECIWWSKAZANIA
• Skaza krwotoczna lub leczenie zwiększające możliwość nadmiernego krwawienia.
• Obecność czynnego lub niedoleczonego zakażenia w miejscu, w którym ma być zastosowana substancja uzupełniająca ubytki kości.
• Wszelkie znane ostre uczulenia na składniki środka kontrastowego i substancję uzupełniającą ubytki kości.
• Potwierdzona ciąża pacjentki.
PRZESTROGA: Zgodnie z prawem federalnym (USA) ten przyrząd może być sprzedawany wyłącznie przez lekarza lub z jego przepisu.
OSTRZEŻENIA
• Złamanie przyrządu może wymagać interwencji lub odzyskania narzędzia.
• Nie stosować tego produktu po upływie terminu ważności wydrukowanego na opakowaniu. Przyrząd może nie być bezpieczny lub skuteczny po upływie terminu ważności.
• Może nastąpić usterka napełnianego balonu w wyniku kontaktu z ostrymi wyrostkami kostnymi lub narzędziami chirurgicznymi.
• Napełnienie balonu IBT płynem powyżej maksymalnej objętości napełnienia może spowodować pęknięcie balonu przed osiągnięciem maksymalnego ciśnienia napełnienia.
• Napełnienie balonu IBT płynem powyżej maksymalnego ciśnienia napełnienia może spowodować pęknięcie balonu przed osiągnięciem maksymalnej objętości napełnienia.
• Nigdy nie wolno napełniać balonu powietrzem ani innym gazem.
ŚRODKI OSTROŻNOŚCI
• Napełniany balon ortopedyczny (IBT) jest przyrządem jednorazowego użytku, przeznaczonym do kontaktu z tkankami ciała. Nie używać ponownie, nie przerabiać ani nie sterylizować
ponownie. Ponowne stosowanie tych przyrządów stwarza ryzyko zanieczyszczenia i grozi zakażeniem pacjenta lub zakażeniem krzyżowym, bez względu na stosowane metody
czyszczenia i powtórnej sterylizacji. Istnieje także zwiększone ryzyko pogorszenia funkcjonowania przyrządu z powodu czynności wykonanych podczas ponownego przetwarzania,
co może prowadzić do urazu lub śmierci pacjenta.
• Ważne jest, aby przed zastosowaniem przyrządu przeczytać dokładnie Instrukcję użycia i niniejsze środki ostrożności.
• Wykorzystać balon IBT przed upływem daty ważności wydrukowanej na opakowaniu.
• Nie wolno używać, jeżeli opakowanie zostało otwarte lub uszkodzone, ponieważ może to naruszyć konstrukcję przyrządu, włącznie z jego sterylnością.
• Nie wolno używać uszkodzonych produktów. Przed użyciem sprawdzić, czy balon IBT lub jego opakowanie nie zostały uszkodzone.
• Przed użyciem należy dokonać przeglądu balonu IBT i sprawdzić, czy przyrząd funkcjonuje prawidłowo i czy jego rozmiar jest właściwy dla zabiegu, w którym ma być wykorzystany.
• Osobom bez odpowiedniego przeszkolenia nie wolno używać tego przyrządu. Balon IBT powinien być używany wyłącznie przez lekarzy przeszkolonych w zakresie stosowania
balonów ortopedycznych. Lekarze posługujący się balonem IBT powinni posiadać wiedzę z zakresu fizjologii i patologii danego elementu anatomicznego.
• Balon IBT powinien być zawsze używany pod kontrolą fluoroskopową z zastosowaniem fluoroskopu o wysokiej jakości obrazu.
• Napełniania balonu IBT można dokonywać wyłącznie pompką strzykawkową o minimalnej pojemności 14 ml.
• Balon IBT należy napełniać wyłącznie płynnym środkiem kontrastowym: Zalecany jest roztwór 60%. W kwestiach przeznaczenia środka kontrastowego, sposobu użycia i przestróg,
należy stosować się do instrukcji producenta.
• Do napełniania balonu IBT nie wolno używać powietrza ani innych gazów.
• Charakterystyka napełniania balonu IBT może być zmieniona przez warunki napotkane w kości.
• Odnawianie, odświeżanie, naprawy, modyfikacje lub ponowna sterylizacja przyrządu w celu przedłużenia jego przydatności do użycia są kategorycznie wzbronione.
• Każda operacja chirurgiczna niesie z sobą ryzyko: jednak stosowanie balonu do leczenia tego rodzaju złamań nie zwiększa wspomnianego ryzyka z klinicznego punktu widzenia,
w porównaniu z tradycyjnymi metodami unoszenia przyciśniętych fragmentów kostnych. Wspomniane ryzyko obejmuje następujące zagrożenia:
o Niepowodzenie właściwej redukcji połamanych fragmentów.
o Opóźnienie złączenia i niezłączenia.
o Zakażenie.
o Uraz nerwowo-naczyniowy lub zespół uciskowy prowadzący do utraty funkcji lub amputacji.
UWAGA: Pompka strzykawkowa Kyphon® zapewnia lepszą kontrolę objętości w porównaniu z innymi systemami napełniania, takimi jak standardowa strzykawka, i jest wymagana
do napełniania balonu IBT. W zakresie obsługi pompki strzykawkowej Kyphon® należy postępować zgodnie z Instrukcjami użycia. Strzykawka zatrzaskowa Kyphon® znajduje się w
opakowaniu wraz z pompką strzykawkową Kyphon®.
ZDARZENIA NIEPOŻĄDANE
Potencjalne zdarzenia niepożądane związane z użyciem balonu IBT obejmują poważne zdarzenia, które są rzadkie, lecz mogą być śmiertelne. Do zdarzeń niepożądanych należą:
• Zatorowość spowodowana tłuszczem, zakrzepem lub innym materiałem, powodująca objawową zatorowość płucną lub inne następstwa kliniczne.
• Pęknięcie z rozczłonkowaniem napełnianej części balonu IBT, prowadzące do uwięźnięcia fragmentu w rejonie ciała objętym zabiegiem.
• Rozerwanie balonu IBT powodujące kontakt ze środkiem kontrastowym, mogącym powodować reakcję uczuleniową lub anafilaktyczną.
• Głębokie lub powierzchniowe zakażenie rany.
• Krwawienie lub krwiak.
WSKAZANIA DO UŻYCIA
PRZESTROGA: W zakresie obsługi pompki strzykawkowej Kyphon® należy postępować zgodnie z Instrukcjami użycia.
Svarbi Informacija Apie slėginį kaulo užpildymo įtaisą „InflateFX™“,
skirtą lūžiams gydyti (10/3 ir 15/3 dydžių)
WAŻNA INFORMACJA O napełnianym balonie ortopedycznym
do leczenia złamań InflateFX™ (rozmiary 10/3 i 15/3)
PRZESTROGA: Środki kontrastowe mogą różnić się lepkością i tempem osadzania, co może przedłużyć czas napełniania i opróżniania balonu. Z tego powodu zaleca się używanie
60-procentowego roztworu środka kontrastowego.
1. Zakręcić nakrętkę na porcie mandrynu, aby go docisnąć do balonu IBT. Wepchnąć tłok całkowicie w strzykawkę zatrzaskową Kyphon® . Przymocować strzykawkę zatrzaskową
Kyphon® do portu do napełniania na balonie IBT.
2. Odciągnąć tłok strzykawki zatrzaskowej Kyphon® do tyłu. Okręcić tłok, aby go unieruchomić w pozycji na ostatniej szczelinie strzykawki.
3. Odłączyć strzykawkę zatrzaskową Kyphon® od balonu IBT.
4. Przymocować port łączący przewodu pompki strzykawkowej Kyphon® doportu do napełniania balonu IBT. Zestaw jest teraz gotowy do użycia.
STOSOWANIE BALONU IBT
1. Dokonać wyboru rozmiaru balonu IBT zależnie od umiejscowieniu i celu operacji. Rys. 1 i Tabela 1 pokazują średnicę (D) i długość (L) balonu po napełnieniu w wodzie o temp. 37
°C, w przyrostach objętości do maksymalnej objętości po napełnieniu.
2. Wymiary te mogą ulegać zmianom w trakcie używania produktu z powodu miejscowych różnic w budowie kości.
Tabela 1 – rozmiary balonu IBT napełnionego płynem (w wodzie o temperaturze 37 °C)
Numer modelu E103A Wymiary po napełnieniu
Rozmiar 10/3 Objętość Przeciętna średnica (D1, D2) Długość (L)
Maksymalna objętość napełnienia 4 ml 2 ml 12,9 mm 14,7 mm
Maksymalne ciśnienie napełnienia 27 atm 4 ml 17,2 mm 19,1 mm
Numer modelu E153A Wymiary po napełnieniu
Rozmiar 15/3 Objętość Przeciętna średnica (D1, D2) Długość (L)
Maksymalna objętość napełnienia 4 ml 2 ml 12,1 mm 17,4 mm
Maksymalne ciśnienie napełnienia 27 atm 4 ml 16 mm 22,1 mm
WPROWADZENIE BALONU IBT
1. Do wprowadzenia balonu IBT do kości potrzebny jest kanał dostępu.
2. Przy tworzeniu kanału dostępu w kości należy przestrzegać do Instrukcji użycia wybranych narzędzi do penetracji kości.
3. Przed użyciem zdjąć mankiet do wprowadzania.
UWAGA: Końcówka dystalna opróżnionego balonu IBT osiągnie dystalny koniec kaniuli, gdy pasek znacznika wyjścia na zewnętrznym kanale balonu IBT wejdzie w proksymalny
koniec kaniuli.
4. Wprowadzić pusty balon do kanału dostępu i umiejscowić go kierując się obrazem rentgenowskim i cieniującymi znacznikami. Delikatne obracanie podczas popychania ułatwia
wprowadzenie balonu.
5. Trzymając balon IBT w wybranej pozycji, unieruchomić go w danym położeniu poprzez napełnienie balonu do ciśnienia 0,3 MPa (3 atm). Jeśli trzeba, wyjąć mandryn.
NAPEŁNIANIE BALONU IBT
1. Napełniać balon IBT pod ciągłą kontrolą rentgenowską. Dla oceny odległości od przedniej i bocznej warstwy korowej kości stosować projekcję boczną. Do monitorowania bocznych
warstw korowych stosować projekcję AP (ang. anteroposterior - projekcja od przodu do tyłu).
2. Jeśli nie jest stosowane obrazowanie ciągłe, zwiększać objętość płynu w małych odstępach (0,25-0,5 ml). Sprawdzić pozycję balonu w projekcji bocznej i AP przed dodaniem
następnej porcji płynu.
3. Zakończyć proces, gdy cel zabiegu zostanie osiągnięty: gdy jakakolwiek część napełnionego balonu IBT dotknie warstwy korowej, lub gdy zostanie osiągnięta maksymalna dozwolona
objętość lub ciśnienie (patrz tabela 1).
WYJMOWANIE BALONU IBT
PRZESTROGA: Nie wolno wycofywać balonu IBT jeśli element napełniany nie jest całkowicie opróżniony. Nie wolno wyjmować balonu IBT pokonując opór. Znaleźć przyczynę oporu za
pomocą fluoroskopu i podjąć odpowiednie kroki dla jego usunięcia.
Odblokować pompkę strzykawkową Kyphon® i usunąć cały środek kontrastowy z balonu IBT, aż do kompletnego opróżnienia balonu. Delikatnym ruchem obrotowym wyjąć balon
IBT z kości poprzez kaniulę.
• W przypadku napotkania oporu, podłączyć strzykawkę 30 ml do portu do napełniania. Wycofać tłok strzykawki do znacznika 30 ml w celu wytworzenia podciśnienia. Wznowić
wyjmowanie balonu IBT.
• Potwierdzić wprowadzenie napełnianej części balonu IBT do kaniuli. Jeśli napełniany element nie wchodzi do kaniuli, należy wsunąć kaniulę po balonie IBT do proksymalnego
cieniodajnego znacznika. Po wsunięciu kaniuli wycofać balon IBT przez kaniulę. Jeśli wyczuwa się opór, wycofać jednocześnie balon IBT i kaniulę.
STERYLIZACJA
Sterylizowane przez napromienianie.
SZCZEGÓŁY DOSTAWY INSTRUMENTU
Balony IGT są dostarczane sterylne w opakowaniu otwieranym przez odklejenie. Jeśli sterylne opakowanie jest uszkodzone, nie używać przyrządu i powiadomić producenta.
MATERIAŁY NIE DOSTARCZANE
• Pompką strzykawkowa Kyphon® ze strzykawką zatrzaskową Kyphon®
• Środek kontrastowy (60%)
• Małe naczynie
UWAGA: Pompkę strzykawkowa Kyphon® ze strzykawką zatrzaskową Kyphon® można uzyskać z firmy Medtronic.
PRZECHOWYWANIE
Balony IBT należy przechowywać w ich oryginalnych opakowaniach fabrycznych. Należy podjąć wszelkie środki ostrożności, aby nie dopuścić do uszkodzenia balonu IBT. Przechowywać
w chłodnym i suchym miejscu.
OGRANICZENIE ODPOWIEDZIALNOŚCI
FIRMA MEDTRONIC NIE PONOSI ODPOWIEDZIALNOŚCI ZA ŻADNE SZKODY, BEZPOŚREDNIE, POŚREDNIE, PRZYPADKOWE, WTÓRNE, ANI ZA ODSZKODOWANIE Z NAWIĄZKĄ NA SKUTEK
POWTÓRNEGO UŻYCIA NAPEŁNIALNYCH BALONÓW ORTOPEDYCZNYCH DO LECZENIA ZŁAMAŃ InflateFX™.
FIRMA MEDTRONIC W ŻADNYM WYPADKU NIE PONOSI ODPOWIEDZIALNOŚCI ZA JAKIEKOLWIEK STRATY BEZPOŚREDNIE, POŚREDNIE, PRZYPADKOWE, WTÓRNE CZY ODSZKODOWANIE
Z NAWIĄZKĄ WYNIKAJĄCE LUB ZWIĄZANE Z UŻYCIEM NAPEŁNIANYCH BALONÓW ORTOPEDYCZNYCH DO LECZENIA ZŁAMAŃ InflateFX™ WYNIKAJĄCE Z NARUSZENIA WARUNKÓW
KONTRAKTU (W TYM GWARANCJI)
UZYSKIWANIE INFORMACJI
W celu uzyskania dodatkowych informacji prosimy kontaktować się z Działem Obsługi Klienta
©2013 Medtronic Sofamor Danek USA, Inc. Wszelkie prawa zastrzeżone.
SlovEnŠčina
INDIKÁCIE POUŽITIA
Nafukovacia kostná ubíjačka (IBT) InflateFX™ na liečbu zlomenín je určená na použitie ako konvenčná kostná ubíjačka na repozíciu zlomenín alebo na vytvorenie medzery v poréznej
kosti ruky, holennej kosti, vretennej kosti a pätovej kosti.
OPIS POMÔCKY
Pozri obr. 1.
1. Viečko
2. Sonda
3. Port sondy
4. Nafukovací port
5. Farebne okódovaný pásik
6. Pásik s výstupnými značkami
7. Zavádzacia manžeta
8. Röntgenkontrastné značky
9. Nafukovací komponent
• Nafukovací komponent ubíjačky IBT je určený na stlačenie poréznej kosti alebo posun kortikálnej kosti pri nafúknutí. Nafukovací komponent IBT sa nachádza v blízkosti distálneho
hrotu nástroja, ako je zobrazené na obrázku 1.
• Nadstavec obsahuje dva neprepojené lúmeny. Vonkajší lúmen sa používa na nafúknutie IBT a centrálny lúmen obsahuje snímateľnú spevňujúcu sondu na zavedenie IBT.
• Proximálny koniec nadstavca má na bočnom ramene adaptér. Nafukovací port adaptéra je spojený s vonkajším lúmenom. Port sondy je spojený s vnútorným lúmenom a obsahuje
spevňujúcu sondu. Sonda má na proximálnom konci viečko na prípadné odstránenie sondy.
• Farebne kódovaný pásik nachádzajúci sa tesne distálne od adaptéra na bočnom ramene označuje veľkosť balónika (t. j. žltý pásik pre veľkosť 10/3, čierny pásik pre veľkosť 15/3).
• Počas zavádzania IBT sa používa pásik s výstupnými značkami umiestnený na vonkajšom lúmene.
• Röntgenkontrastné značky umiestnené na distálnom a proximálnom konci sfúknutého pracovného povrchu umožňujú fluoroskopické zobrazenie sfúknutého IBT počas jeho
umiestňovania.
KONTRAINDIKÁCIE
• Poruchy krvácavosti alebo liečba, ktorá zvyšuje možnosť nadmerného krvácania
• Prítomnosť aktívnej alebo nedoliečenej infekcie v mieste, kde sa má aplikovať výplň kostných medzier
• Akákoľvek známa silná alergia na kontrastný materiál a výplň kostných medzier
• Potvrdené tehotenstvo pacientky
POZOR: Federálne zákony (USA) obmedzujú predaj tohto nástroja len na predaj lekárom alebo na lekársky predpis.
UPOZORNENIA
• Zlomenie nástroja môže vyžadovať zákrok alebo vytiahnutie.
• Tento produkt nepoužívajte po uplynutí dátumu exspirácie (dátume použiteľnosti) vytlačenom na obale. Po uplynutí dátumu exspirácie (dátumu použiteľnosti) nástroj už nemusí
byť bezpečný alebo účinný.
• Nafukovací komponent môže zlyhať v dôsledku ostrých kostných výbežkov alebo chirurgických nástrojov.
• Nafúknutie ubíjačky IBT nad maximálny objem nafúknutia môže spôsobiť prasknutie balónika skôr, než dosiahne maximálny tlak nafúknutia.
• Nafúknutie ubíjačky IBT nad maximálny tlak nafúknutia môže spôsobiť prasknutie balónika skôr, než dosiahne maximálny objem nafúknutia.
• Na nafúknutie balónika nikdy nepoužívajte vzduch ani plynné látky.
VAROVANIA
• Nafukovacia kostná ubíjačka je pomôcka na jedno použitie určená na kontakt s telesnými tkanivami. Nepoužívajte, nespracovávajte ani nesterilizujte opakovane. Opakované použitie
týchto pomôcok nesie so sebou riziko kontaminácie a môže spôsobiť infekciu pacienta alebo krížovú infekciu bez ohľadu na spôsoby čistenia a opakovanej sterilizácie. Taktiež vzniká
zvýšené riziko zhoršenia účinnosti pomôcky z dôvodu krokov opakovaného spracovania, čo môže viesť k poraneniu alebo smrti pacienta.
• Pred použitím nástroja je dôležité prečítať si pozorne návod na použitie a tieto bezpečnostné opatrenia.
• Ubíjačku IBT použite pred uplynutím dátumu použiteľnosti uvedenom na obale.
• Nepoužívajte, ak je balenie otvorené alebo poškodené, pretože mohlo dôjsť k porušeniu celistvosti produktu vrátane jeho sterility.
• Nepoužívajte poškodené výrobky. Pred použitím skontrolujte IBT a balenie, aby ste si overili, že nedošlo k žiadnemu poškodeniu.
• Pred použitím je potrebné skontrolovať funkčnosť IBT a zabezpečiť, aby jeho veľkosť bola vhodná pre konkrétnu procedúru, na ktorú má byť použitý.
• Výrobok nepoužívajte, ak nie ste adekvátne zaškolení. IBT môžu aplikovať jedine lekári zaškolení v oblasti techník utesňovania kosti. Lekári používajúci tieto nástroje musia poznať
fyziológiu a patológiu vybranej časti tela.
• S IBT možno manipulovať jedine pri fluoroskopickej vizualizácii pomocou röntgenového zariadenia, ktoré poskytuje snímky vysokej kvality.
• Ubíjačka IBT sa môže nafukovať iba pomocou nafukovacej striekačky s objemom minimálne 14 ml.
• Ubíjačku IBT nafukujte len tekutou kontrastnou látkou: odporúča sa 60 % roztok. Dodržujte pokyny výrobcu týkajúce sa indikácií a použitia kontrastnej látky a súvisiacich upozornení.
• Na nafúknutie IBT nepoužívajte vzduch alebo iný plyn.
• Vlastnosti nafúknutia IBT sa menia pri nafúknutí v kosti.
• Úprava, renovácia, oprava, pozmenenie alebo opätovná sterilizácia nástroja s cieľom umožniť ďalšie použitie sa výslovne zakazujú.
• Každý chirurgický zákrok zahŕňa riziká, však použitie balónika pri liečbe týchto zlomenín z klinického hľadiska nezvyšuje tieto riziká v porovnaní s tradičnými metódami nadvihnutia
poklesnutých úlomkov kostí. K týmto rizikám patrí:
o nemožnosť správnej repozície úlomkov zo zlomeniny,
o oneskorené zhojenie alebo nezhojenie,
o infekcia,
o neurovaskulárne poranenie alebo kompartment syndróm vedúce k strate funkcie alebo amputácii.
POZNÁMKA: Nafukovacia striekačka značky Kyphon® zabezpečuje vynikajúcu kontrolu objemu v porovnaní s inými nafukovacími systémami, ako napríklad štandardnou striekačkou, a
vyžaduje sa na nafúknutie systému IBT. Dodržiavajte návod na použitie od výrobcu nafukovacej striekačky značky Kyphon®. Poistná striekačka Kyphon® sa dodáva spolu s nafukovacou
striekačkou značky Kyphon®.
NEŽIADUCE REAKCIE
Medzi nežiaduce reakcie potenciálne súvisiace s použitím ubíjačky IBT patria vážne udalosti, ktoré napriek svojej zriedkavosti môžu byť fatálne.
Medzi nežiaduce reakcie patrí:
• embolus z tuku, trombu alebo iných materiálov, vedúci k symptomatickej pľúcnej embólii alebo iným klinickým následkom,
• prasknutie s roztrieštením nafukovanej časti ubíjačky IBT vedúce k zadržaniu úlomku v postihnutej oblasti,
• prasknutie IBT spôsobujúce expozíciu kontrastnej látke, čo môže viesť k alergickej reakcii alebo anafylaxii,
• hĺbková alebo povrchová infekcia rany,
• krvácanie alebo hematóm.
NÁVOD NA POUŽITIE
POZOR: Dodržiavajte návod na použitie od výrobcu nafukovacej striekačky značky Kyphon®.
POZOR: Kontrastné látky môžu mať rôznu viskozitu a zrážanlivosť, čo môže predĺžiť čas potrebný na nafúknutie a vypustenie IBT. Z tohto dôvodu sa odporúča použitie 60 % roztoku
kontrastnej látky.
1. Otočením viečka na porte sondy sa sonda upevní na ubíjačku IBT. Piest úplne zatlačte do poistnej striekačky Kyphon®. Poistnú striekačku Kyphon® pripojte k nafukovaciemu portu
na ubíjačke IBT.
2. Piest poistnej striekačky Kyphon® potiahnite dozadu. Otočte piestom, aby sa zaistil v poslednej štrbine v striekačke.
3. Poistnú striekačku Kyphon® odpojte od ubíjačky IBT.
4. Napájací port na hadičke nafukovacej striekačky značky Kyphon® pripojte k nafukovaciemu portu na ubíjačke IBT. Systém je teraz úplne pripravený na použitie.
POUŽITIE SYSTÉMU IBT
1. Veľkosť IBT zvoľte na základe miesta a cieľa terapie. Na obr. 1 a v tabuľke 1 sa uvádza nafúknutý priemer IBT (D) a nafúknutá dĺžka (L) IBT vo vode s teplotou 37 °C pri stupňovaní
nafukovacieho objemu až po maximálny objem nafúknutia.
2. Tieto rozmery sa môžu meniť počas aplikácie produktu v dôsledku lokálnych variácií štruktúry kosti.
Tabuľka 1 – Rozmery nafúknutej ubíjačky IBT (vo vode teploty 37 °C)
Číslo modelu E103A Rozmery po nafúknutí
Veľkosť 10/3 Objem Priemerný priemer
(D1, D2) Dĺžka (L)
Max. objem nafúknutia 4 ml 2 ml 12,9mm 14,7 mm
Max. tlak nafúknutia 27 atm 4 ml 17,2mm 19,1 mm
Číslo modelu E153A Rozmery po nafúknutí
Veľkosť 15/3 Objem Priemerný priemer
(D1, D2) Dĺžka (L)
Max. objem nafúknutia 4 ml 2 ml 12,1 mm 17,4 mm
Max. tlak nafúknutia 27 atm 4 ml 16 mm 22,1 mm
ZAVEDENIE IBT
1. Na umiestnenie IBT je potrebný prístupový kanál.
2. Pri vytváraní prístupového kanálu do kosti dodržujte návod na použitie pre zvolené nástroje na prístup ku kosti.
3. Pred použitím odstráňte zavádzaciu manžetu.
POZNÁMKA: Distálny hrot sfúknutého IBT dosiahne distálny koniec kanyly, keď výstupná značka na vonkajšom lúmene IBT vojde do proximálneho konca kanyly.
4. Vyfúknutú ubíjačku IBT vložte do prístupového kanálu a pomocou röntgenkontrastných značiek ju umiestnite pomocou zobrazovacieho navádzania. Zavádzanie je možné uľahčiť
pomocou jemného točivého pohybu s tlakom vpred.
5. Ubíjačku IBT držte na mieste a nafúknite na 0,3 MPa (3 atm), čím sa IBT zaistí v polohe. Vytiahnite sondu, ak je to žiaduce.
NAFÚKNUTIE IBT
1. IBT nafúknite pod kontrolou pomocou nepretržitého zobrazovacieho navádzania. Vzdialenosť od prednej a laterálnej kôry monitorujte pomocou laterálnej projekcie. Laterálne kôry
monitorujte pomocou AP projekcie.
2. Ak sa nepoužíva nepretržité zobrazovanie, v malých prírastkoch zvyšujte objem (0,25 – 0,5 ml). Pred ďalším zvýšením objemu zhodnoťte polohu ubíjačky v laterálnej a AP projekcii.
3. Po dosiahnutí cieľa liečby alebo keď sa ktorákoľvek časť dĺžky nafúknutej ubíjačky IBT dotýka kortikálnej kosti, resp. po dosiahnutí maximálneho objemu alebo maximálneho tlaku
nafúknutia (pozri tabuľku č. 1) prestaňte zvyšovať objem.
VYTIAHNUTIE IBT
POZOR: Ubíjačku IBT nevyťahujte, ak nafukovací komponent nie je úplne vyfúknutý. IBT nikdy nevyťahujte, ak narazíte na odpor. Príčinu odporu zistite röntgenologicky a vykonajte
všetky požadované nápravné zásahy.
Nafukovacou striekačkou značky Kyphon® vyprázdňujte kontrastnú látku zo systému IBT, až kým sa balónik úplne nevyfúkne. IBT vytiahnite z kosti cez kanylu jemným točivým pohybom.
• Ak pocítite odpor, k nafukovaciemu portu pripojte striekačku objemu 30 ml. Piest striekačky potiahnite naspäť na značku 30 ml, aby sa vytvoril podtlak. Pokračujte vo vyťahovaní IBT.
• Overte, či nafukovacia časť IBT vstúpila do kanyly. Ak nafukovací komponent neprejde do kanyly, posúvajte kanylu ponad IBT k proximálnej röntgenkontrastnej značke. Po zasunutí
kanyly cez ňu vytiahnite IBT. Ak zaznamenáte odpor, súbežne vytiahnite IBT a kanylu.
STERILIZÁCIA
Sterilizované žiarením.
SPÔSOB DODÁVKY
Ubíjačky IBT sa dodávajú sterilné v odlepovacom balení. V prípade poškodenia sterilného balenia produkt nepoužite a chybu oznámte výrobcovi.
NEDODÁVANÉ MATERIÁLY
• Nafukovacia striekačka značky Kyphon® s poistnou striekačkou Kyphon®
• Kontrastná látka (60 %)
• Miska
POZNÁMKA: Nafukovacia striekačka značky Kyphon® s poistnou striekačkou Kyphon® je k dispozícii od spoločnosti Medtronic.
USKLADNENIE
Ubíjačky IBT sa musia prechovávať v pôvodných materiáloch, v akých boli dodané. Je potrebné venovať náležitú pozornosť tomu, aby nedošlo k poškodeniu ubíjačky IBT. Skladujte na
chladnom suchom mieste.
OBMEDZENIE ZODPOVEDNOSTI
SPOLOČNOSŤ MEDTRONIC NEBUDE ZODPOVEDNÁ ZA ŽIADNE PRIAME, NEPRIAME, VEDĽAJŠIE, NÁSLEDNÉ ANI PRÍKLADNÉ ODŠKODNENIE VYPLÝVAJÚCE Z OPAKOVANÉHO POUŽITIA
NAFUKOVACÍCH KOSTNÝCH UBÍJAČIEK InflateFX™ NA LIEČBU ZLOMENÍN.
SPOLOČNOSŤ MEDTRONIC NIE JE V ŽIADNOM PRÍPADE ZODPOVEDNÁ ZA ŽIADNE PRIAME, NEPRIAME, VEDĽAJŠIE, NÁSLEDNÉ ANI PRÍKLADNÉ ODŠKODNENIE VYPLÝVAJÚCE Z POUŽITIA
NAFUKOVACÍCH KOSTNÝCH UBÍJAČIEK InflateFX™ NA LIEČBU ZLOMENÍN ALEBO V SPOJITOSTI S NIMI NA ZÁKLADE PORUŠENIA ZMLUVY (VRÁTANE PORUŠENIA ZÁRUKY).
ŽIADOSTI O INFORMÁCIE
Ak potrebujete ďalšie informácie, obráťte sa na zákaznícky servis.
©2013 Medtronic Sofamor Danek USA, Inc. Všetky práva sú vyhradené.
TüRKçE
KULLANMA ENDİKASYONLARI
InflateFX™ Kırık Yönetimi Şişirilebilir Kemik Tamponunun (IBT) el, tibia, radyus ve kalkaneusta kanselöz kemikte bir boşluk oluşturulması ve/veya kırıkların redüksiyonu için geleneksel
kemik tamponların yerine kullanılması amaçlanmıştır.
CİHAZIN TARİFİ
Bakınız Şekil 1.
1. Kapak
2. Stile
3. Stile Portu
4. Şişirme Portu
5. Renk Kodlu Bant
6. Çıkış İşareti Bandı
7. İnsersiyon Manşonu
8. Radyoopak İşaretler
9. Şişirilebilir Bileşen
• IBT Şişirilebilir Bileşeni şişerken kanselöz kemiği sıkıştırmak ve/veya kortikal kemiği hareket ettirmek üzere tasarlanmıştır. IBT’nin Şişirilebilir Bileşeni Şekil 1’de gösterildiği gibi
cihazın distal ucuna yakındır.
• Gövde, birbiriyle iletişimi olmayan iki adet lümen içerir. Dış lümen, IBT şişirme için kullanılırken merkez lümen, IBT insersiyonu için çıkarılabilir bir sertleştirici Stile içerir.
• Gövdenin proksimal ucunda bir yan kol adaptörü vardır. Adaptörün Şişirme Portu dış lümenle bitişiktir. Stile Portu iç lümenle bitişiktir ve sertleştirici Stileyi içerir. Stilenin proksimal
ucunda isteğe bağlı çıkarma için bir Kapak vardır.
• Yan kol adaptörünün hemen distalinde bulunan Renk Kodlu Bant, balon büyüklüğüne işaret eder (yani 10/3 büyüklüğü için sarı bir bant ve 15/3 büyüklüğü için siyah bir bant).
• Dış lümende bulunan Çıkış İşareti Bandı, IBT insersiyonu sırasında kullanılır.
• Söndürülmüş çalışma yüzeyinin distal ve proksimal ucunda bulunan Radyoopak İşaretler, konumlandırma sırasında söndürülmüş IBT’nin floroskopik olarak görüntülenmesini
mümkün kılar.
KONTRENDİKASYONLAR
• Aşırı kanama olasılığını arttıran kanama bozukluğu veya tedavisi.
• Kemik boşluğu dolgusunun uygulanacağı yerde aktif veya tam tedavi edilmemiş enfeksiyon varlığı.
• Kontrast madde ve kemik boşluğu dolgusuna karşı bilinen herhangi bir şiddetli alerji.
• Hastada doğrulanmış gebelik bulunması.
DİKKAT: ABD federal kanunlarına göre bu cihaz sadece bir doktor tarafından veya emriyle satılabilir.
UYARILAR
• Cihazın kırılması, girişim veya geri almayı gerektirebilir.
• Bu ürünü ambalajda basılı son kullanma tarihinden sonra kullanmayın. Cihaz son kullanma tarihinden sonra güvenli veya etkili olmayabilir.
• Şişirilebilir Bileşen sivri kemik çıkıntıları veya cerrahi aletler nedeniyle başarısız olabilir.
• IBT’yi maksimum şişirme hacminin ötesine şişirmek balonun maksimum şişirme basıncına ulaşmadan patlamasına neden olabilir.
• IBT’yi maksimum şişirme basıncının ötesine şişirmek balonun maksimum şişirme basıncına ulaşmadan patlamasına neden olabilir.
• Balonu şişirmek için asla hava veya gaz halinde materyaller kullanmayın.
ÖNLEMLER
• Şişirilebilir Kemik Tamponu vücut dokularına temas etmesi amaçlanmış tek kullanımlık bir cihazdır. Tekrar kullanmayın, tekrar işleme koymayın ve tekrar sterilize etmeyin. Bu
cihazların tekrar kullanılması kontaminasyon riski taşır ve temizlik ve tekrar sterilizasyon yöntemleri ne olursa olsun hastada enfeksiyon veya çapraz enfeksiyona neden olabilir.
Ayrıca tekrar işleme koyma basamakları, cihaz performansının bozulma riskini artırır ve bu da hastanın yaralanmasına veya ölümüne yol açabilir.
• Cihazı çalıştırmadan önce Kullanma Talimatını ve bu önlemleri dikkatle okumak önemlidir.
• IBT’yi ambalaj üzerinde belirtilen son kullanma tarihinden önce kullanın.
• Ambalaj açılmış veya hasarlıysa kullanmayın çünkü sterilite dahil ürün bütünlüğü olumsuz etkilenebilir.
• Hasarlı ürünleri kullanmayın. Kullanımdan önce IBT ve ambalajını herhangi bir hasar oluşmadığını doğrulamak için inceleyin.
• Kullanımdan önce IBT, işlevselliğini doğrulamak ve büyüklüğünün kullanılacağı spesifik işlem için uygun olduğundan emin olmak için incelenmelidir.
• Bu ürünü, uygun şekilde eğitim almamışsanız kullanmayın. IBT sadece kemik tamponu kullanımı teknikleri konusunda eğitim almış doktorlar tarafından kullanılmalıdır. Cihazları
kullanan doktorlar seçilen anatominin fizyoloji ve patolojisine aşina olmalıdır.
• IBT, sadece yüksek kalitede görüntüler sağlayan radyografik ekipmanla floroskopik gözlem altında hareket ettirilmelidir.
• IBT sadece minimum 14 ml hacim kapasitesi bulunan bir Şişirme Şırıngası kullanılarak şişirilmelidir.
• IBT’yi sadece sıvı kontrast madde ile şişirin: %60 solüsyon önerilir. Kontrast madde endikasyonları, kullanımı ve dikkat edilecek noktalar için üreticinin talimatını izleyin.
• IBT’yi şişirmek için hava veya başka bir gaz kullanmayın.
• IBT’nin şişme özellikleri kemik içinde şişirmeyle değişir.
• Daha fazla kullanılmasını sağlamak için cihazın onarılması, yenilenmesi, tamir edilmesi, değiştirilmesi veya tekrar sterilize edilmesi kesinlikle yasaklanmıştır.
• Her cerrahinin riskleri vardır; ancak, balonu bu kırıkların tedavisinde kullanmak deprese kemik parçalarını kaldırmanın geleneksel yöntemleriyle karşılaştırıldığında bu riskleri klinik
açıdan arttırmaz. Bu riskler arasında şunlar vardır:
o Kırık parçalarını uygun şekilde redükte edememe.
o Gecikmiş birleşme ve birleşmeme.
o Enfeksiyon.
o Nörovasküler hasar veya kompartman sendromu ve bunun sonucunda işlev kaybı veya ampütasyon.
NOT: Kyphon® markalı şişirme şırıngası standart bir şırınga gibi diğer şişirme sistemlerine göre üstün hacim kontrolü sağlar ve IBT’nin şişirilmesi için gereklidir. Kyphon® markalı şişirme
şırıngasının kullanımı için üreticinin Kullanma Talimatını izleyin. Kyphon® Kilitlenen Şırıngası, Kyphon® markalı şişirme şırıngasıyla paketlenmiştir.
ADVERS OLAYLAR
IBT kullanımıyla ilişkili olabilecek advers olaylar arasında nadir olsalar da ölümcül olabilen ciddi olaylar da vardır.
Advers olaylar arasında şunlar vardır:
• Semptomatik pulmoner emboli veya başka klinik sonuçlara neden olabilecek şekilde yağ, trombus veya başka materyallerin embolisi.
• IBT şişirilebilir kısmının parçalanmasıyla rüptür oluşması ve sonuçta bir parçanın etkilenen bölge içinde kalması.
• IBT’nin rüptürü ve bunun sonucunda kontrast maddeye maruz kalmayla alerjik reaksiyon veya anafilaksiyle sonuçlanma olasılığı.
DÔLEŽITÉ INFORMÁCIE o nafukovacej kostnej ubíjačke
InflateFX™ na liečbu zlomenín (veľkosti 10/3 a 15/3)
InflateFX™ Kırık Yönetimi Şişirilebilir Kemik Tamponu
Hakkinda Önemli Bilgi (Boyut 10/3 ve 15/3)
• Derin veya yüzeysel yara enfeksiyonu.
• Kanama veya hematom.
KULLANMA TALİMATLARI
DİKKAT: Kyphon® markalı şişirme şırıngasının kullanımı için üreticinin Kullanma Talimatını izleyin.
DİKKAT: Kontrast maddelerin daha uzun ve kısa şişirme ve söndürme sürelerine neden olabilen farklı viskozite ve presipitasyon düzeyleri olabilir. Bu nedenle %60 kontrast madde
kullanımı önerilir.
1. Stileyi IBT üzerinde sıkılaştırmak için Stile Portu üzerindeki kapağı çevirin. Pistonu Kyphon® Kilitlenen Şırıngası içine tümüyle itin. Kyphon® Kilitlenen Şırıngasını IBT üzerindeki
Şişirme Portuna takın.
2. Kyphon® Kilitlenen Şırıngası pistonunu geri çekin. Pistonu şırınga üzerindeki son yuva üzerinde yerine kilitlemek için çevirin.
3. Kyphon® Kilitlenen Şırıngasını IBT’den ayırın.
4. Kyphon® Şişirme Şırıngası tüpü üzerindeki bağlantı portunu IBT üzerindeki Şişirme Portuna takın. Sistem artık hazırlanmıştır ve kullanıma hazırdır.
IBT KULLANIMI
1. IBT büyüklüğünü bölge ve tedavi hedefine göre seçin. Şekil 1 ve Tablo 1 IBT’lerin maksimum şişirme hacmine şişirme hacmi kademeleriyle 37°C su içinde şişirilmiş çapını (D) ve
şişirilmiş uzunluğunu (L) vermektedir.
2. Bu boyutlar ürün kullanımı sırasında kemik yapısındaki yerel değişiklikler nedeniyle değişebilir.
Tablo 1 - IBT Şişirilmiş Boyutları (37°C suda)
Model Numarası E103A Şişirilmiş Boyutlar
Büyüklük 10/3 Hacim Ort. Çap (D1, D2) Uzunluk (L)
Maks. Şişirme Hacmi 4 ml 2 ml 12,9 mm 14,7 mm
Maks. Şişirme Basıncı 27 atm 4 ml 17,2 mm 19,1 mm
Model Numarası E153A Şişirilmiş Boyutlar
Büyüklük 15/3 Hacim Ort. Çap (D1, D2) Uzunluk (L)
Maks. Şişirme Hacmi 4 ml 2 ml 12,1 mm 17,4 mm
Maks. Şişirme Basıncı 27 atm 4 ml 16 mm 22,1 mm
IBT İNSERSİYONU
1. IBT yerleştirme için bir erişim kanalı gereklidir.
2. Kemiğe bir erişim kanalı oluşturmak için seçilen kemik erişimi aletleri için Kullanma Talimatını izleyin.
3. İnsersiyon Manşonunu kullanımdan önce çıkarın.
NOT: IBT dış lümenindeki Çıkış İşareti, kanülün proksimal ucuna girdiğinde, söndürülmüş IBT’nin distal ucu kanülün distal ucuna ulaşmıştır.
4. Söndürülmüş IBT’yi erişim kanalına yerleştirin ve Radyoopak İşaretleri kullanarak görüntü kılavuzluğu altında konumlandırın. İleri itmeyle birlikte hafif bir çevirme hareketi insersiyona
yardımcı olabilir.
5. IBT’yi yerinde tutarken IBT’yi konumunda sabitlemek üzere 3 atm değerine şişirin. İsterseniz Stileyi çıkarın.
IBT’Yİ ŞİŞİRME
1. IBT’yi sürekli görüntü kılavuzluğu altında şişirin. Anterior ve lateral korteksten mesafeyi izlemek üzere lateral görüntü kullanın. Lateral korteksleri izlemek üzere ön – arka (AP)
görüntü kullanın.
2. Sürekli görüntüleme kullanılmıyorsa hacmi küçük miktarlarla (0,25 - 0,5 ml) arttırın. Daha fazla hacim arttırmayla devam etmeden önce lateral ve AP görüntülerde tampon
pozisyonunu değerlendirin.
3. Tedavi hedefine ulaşıldığında veya IBT şişmiş uzunluğunun herhangi bir kısmı kortikal kemiğe temas ettiğinde veya maksimum şişirme hacmi ve/veya maksimum şişirme basıncına
ulaşıldığında durun (Bakınız Tablo 1).
IBT’Yİ ÇIKARMA
DİKKAT: IBT’yi Şişirilebilir Bileşen tamamen sönmeden geri çekmeyin. IBT’yi asla dirence karşı geri çekmeyin. Floroskopi altında direnç nedenini belirleyin ve gerekli çözümleyici
eylemleri yapın.
Kyphon® markalı şişirme şırıngasını kullanarak balon tamamen sönünceye kadar kontrast maddeyi IBT’den boşaltın. IBT’yi kemikten, kanül içinden hafif çevirmeli bir hareketle çıkarın.
• Direnç varsa Şişirme Portuna bir 30 ml şırınga takın. Şırınga pistonunu “30 ml” işaretine geri çekerek vakum oluşturun. IBT’yi çıkarmaya devam edin.
• IBT’nin şişirilebilir kısmının kanüle girdiğini doğrulayın. Şişirilebilir Bileşen kanül içine hareket etmezse kanülü IBT üzerinden proksimal Radyoopak İşarete kadar ilerletin. Kanülü
ilerlettikten sonra IBT’yi kanül içinden geri çekin. Dirençle karşılaşılırsa IBT ve kanülü aynı anda çıkarın.
STERİLİZASYON
Radyasyonla sterilize edilmiştir.
SAĞLANMA ŞEKLİ
IBT’ler, soyularak açılan bir ambalajda steril olarak sağlanır. Steril ambalajda hasar olması durumunda, kullanmayın ve üreticiye haber verin.
SAĞLANMAYAN MATERYALLER
• Kyphon® Kilitlenen Şırıngalı Kyphon® markalı şişirme şırıngası
• Kontrast Madde (%60)
• Küçük Çanak
NOT: Kyphon® Kilitlenen Şırıngalı Kyphon® markalı şişirme şırıngası Medtronic’ten sağlanabilir.
SAKLAMA
IBT’ler orijinal sevkıyat materyalinde saklanmalıdır. IBT’lerin zarar görmemesini sağlamak için gerekli özen gösterilmelidir. Serin, kuru bir yerde saklayın.
SORUMLULUK SINIRLANDIRMASI
MEDTRONIC, InflateFX™ KIRIK YÖNETİMİ ŞİŞİRİLEBİLİR KEMİK TAMPONLARININTEKRAR KULLANIMINDAN KAYNAKLANAN DOĞRUDAN, DOLAYLI, ARIZİ, SONUÇSAL VEYA ÖRNEK NİTELİĞİNDEKİ
HASARLARDAN SORUMLU TUTULAMAZ.
MEDTRONIC HİÇBİR ŞEKİLDE InflateFX™ KIRIK YÖNETİMİ ŞİŞİRİLEBİLİR KEMİK TAMPONLARI YÜZÜNDEN VEYA İLİŞKİLİ OLARAK SÖZLEŞME İHLALİ (GARANTİ İHLALİ DAHİL) NEDENİYLE DOĞAN
HERHANGİ BİR DOĞRUDAN, DOLAYLI, ARIZİ, SONUÇSAL VEYA ÖRNEK NİTELİĞİNDEKİ HASARDAN SORUMLU OLMAYACAKTIR.
BİLGİ TALEPLERİ
Daha fazla bilgi için lütfen Müşteri Hizmetleriyle bağlantı kurun.
©2013 Medtronic Sofamor Danek USA, Inc. Tüm hakları saklıdır.
RoMÂnĂ
INDICAŢII DE UTILIZARE
Dispozitivul gonflabil de plombare osoasă pentru gestionarea fracturilor InflateFX™ (IBT – Inflatable Bone Tamp) este destinat pentru utilizare ca dispozitiv de plombare osoasă convenţional
pentru reducerea fracturilor şi/sau crearea unei cavităţi în osul spongios la nivelul mâinii, tibiei, radiusului şi calcaneului.
DESCRIEREA DISPOZITIVULUI
Vezi Figura 1.
1. Capac
2. Stilet
3. Portul stiletului
4. Portul de gonflare
5. Bandă cu cod color
6. Banda pentru marcaj ieşire
7. Manşonul de inserţie
8. Markeri radioopaci
9. Componenta gonflabilă
• Componenta gonflabilă a dispozitivului IBT este concepută pentru a comprima osul spongios şi/sau a deplasa osul cortical pe măsura gonflării dispozitivului. Componenta gonflabilă
a IBT se află lângă vârful distal al dispozitivului, aşa cum se indică în Figura 1.
• Tija conţine două lumene care nu comunică. Lumenul exterior este folosit pentru gonflarea IBT şi lumenul central conţine un stilet detaşabil de rigidizare pentru inserarea IBT.
• Capătul proximal al tijei are un adaptor cu braţ lateral. Portul de gonflare al adaptorului este contiguu cu lumenul exterior. Portul stiletului este contiguu cu lumenul interior şi
conţine stiletul de rigidizare. Stiletul are un capac la capătul proximal pentru scoatere opţională.
• Banda cu cod de culori, care se află imediat distal faţă de adaptorul cu braţ lateral, indică dimensiunea balonului (adică, o bandă galbenă pentru dimensiunea 10/3 şi o bandă
neagră pentru dimensiunea 15/3).
• Banda cu marcaj pentru ieşire aflată pe lumenul exterior este folosită în timpul inserţiei IBT.
• Markerii radioopaci aflaţi la capătul distal şi proximal al suprafeţei de lucru degonflate permit vizualizarea fluoroscopică a IBT degonflat în timpul plasării acestuia.
CONTRAINDICAŢII
• Tulburare hemoragică sau tratament care sporeşte probabilitatea de sângerare excesivă.
• Prezenţa unei infecţii active sau incomplet tratate în locul unde trebuie aplicată umplutura pentru cavităţi osoase.
• Orice alergie severă cunoscută la materialul de contrast şi umplutura pentru cavităţi osoase.
• Sarcină confirmată a pacientei.
ATENŢIONARE: Legea federală (SUA) restricţionează vânzarea acestui dispozitiv numai de către sau la comanda unui medic.
AVERTISMENTE
• Dacă dispozitivul se rupe, ar putea fi nevoie de o intervenţie sau de recuperarea acestuia.
• Nu utilizaţi acest produs după data de expirare (a se utiliza până la) tipărită pe ambalaj. Dispozitivul îşi poate pierde siguranţa şi eficacitatea după data sa de expirare (a se utiliza până la).
• Componenta gonflabilă poate ceda din cauza spiculilor osoşi ascuţiţi sau instrumentelor chirurgicale.
• Gonflarea IBT peste volumul maxim de gonflare poate cauza spargerea balonului înainte de atingerea presiunii maxime de gonflare.
• Gonflarea IBT peste presiunea maximă de gonflare poate cauza spargerea balonului înainte de atingerea volumului maxim de gonflare.
• Nu utilizaţi niciodată aer sau materii gazoase pentru gonflarea balonului.
PRECAUŢII
• Dispozitivul gonflabil de plombare osoasă este un dispozitiv de unică folosinţă proiectat să aibă contact cu ţesuturile corpului. Nu reutilizaţi, reprocesaţi sau resterilizaţi. Refolosirea
acestor dispozitive poartă riscul contaminării şi poate cauza infectarea sau infectarea încrucişată a pacientului, indiferent de metodele de curăţare şi resterilizare. Există, de asemenea,
un risc crescut de deteriorare a performanței dispozitivului datorită etapelor de reprocesare, care ar putea duce la rănirea sau decesul pacientului.
• Este important să se citească cu grijă instrucţiunile de folosire şi aceste precauţii înainte de operarea dispozitivului.
• Folosiţi IBT înainte de data de expirare menţionată pe ambalaj.
• Nu folosiţi dacă ambalajul este deschis sau deteriorat, deoarece integritatea produsului, inclusiv sterilitatea, pot fi compromise.
• A nu se utiliza produsele deteriorate. Înainte de folosire, inspectaţi IBT şi ambalajul pentru a verifica dacă nu s-au produs daune.
• Înainte de a fi folosit, trebuie verificat că IBT funcţionează şi că mărimea acestuia este adecvată pentru procedura specifică pentru care urmează a fi folosit.
• Nu utilizaţi acest produs dacă nu aţi fost instruit în mod adecvat. IBT trebuie utilizat numai de medici instruiţi în tehnica folosirii tamponului osos. Medicii care utilizează dispozitivele
trebuie să fie familiarizaţi cu fiziologia şi patologia părţii anatomice selectate.
• IBT trebuie manipulat numai sub monitorizare fluoroscopică, cu echipament radiografic care furnizează imagini de calitate superioară.
• IBT trebuie gonflat numai folosind o seringă de gonflare cu volum de minim 14 ml.
• Gonflaţi IBT numai cu mediu de contrast lichid: Se recomandă o soluţie de 60%. Urmaţi instrucţiunile producătorului pentru indicaţii, mod de folosire şi atenţionări referitoare la
mediul de contrast.
• Nu folosiţi aer sau alt gaz pentru a gonfla IBT.
• Caracteristicile de gonflare ale IBT sunt modificate prin gonflarea în interiorul osului.
• Recondiţionarea, remodelarea, repararea, modificarea sau resterilizarea dispozitivului în vederea utilizării ulterioare sunt interzise în mod expres.
• Orice intervenţie chirurgicală prezintă riscuri; cu toate acestea, utilizarea balonului în tratamentul acestor fracturi nu duce la creşterea acestor riscuri din punct de vedere clinic,
comparativ cu metodele tradiţionale de ridicare a fragmentelor de os înfundate. Aceste riscuri includ:
o Nereducerea corespunzătoare a fragmentelor fracturii.
o Întârzierea uniunii şi non-uniunii.
o Infecţie.
o Vătămare neurovasculară sau sindrom compartimental care duce la pierderea funcţiei sau amputare.
NOTĂ: Seringa de gonflare marca Kyphon® oferă un control superior al volumului comparativ cu alte sisteme de gonflare, cum ar fi seringa obişnuită, şi este necesară pentru gonflarea IBT.
Respectaţi instrucţiunile de utilizare ale producătorului seringii de gonflare marca Kyphon®. Seringa de blocare Kyphon® este ambalată împreună cu seringa de gonflare marca Kyphon®.
EVENIMENTE ADVERSE
Evenimentele adverse care pot fi asociate cu folosirea dispozitivului IBT includ evenimente grave, care, deşi rare, pot fi fatale.
Aceste evenimente includ:
• Embolism produs de grăsime, trombusuri sau alte materiale, cu cauzarea de embolism pulmonar simptomatic sau alte sechele clinice.
• Ruptură cu fragmentarea părţii gonflabile a dispozitivului IBT, cu producerea retenţiei unui fragment în interiorul regiunii afectate.
• Ruperea IBT rezultând în expunerea la mediul de contrast, putând provoca o reacţie alergică sau anafilaxie.
• Infecţie profundă sau superficială a rănii.
• Sângerare sau hematom.
ÎNDRUMĂRI DE UTILIZARE
ATENŢIONARE: Respectaţi instrucţiunile de utilizare ale producătorului seringii de gonflare marca Kyphon®.
ATENŢIONARE: Mediile de contrast pot avea nivele diferite de vâscozitate şi precipitare care pot cauza prelungirea timpului de gonflare şi de degonflare. Din acest motiv, se recomandă
folosirea unui mediu de contrast de 60%.
1. Răsuciţi capacul pe portul stiletului pentru a strânge stiletul pe IBT. Împingeţi pistonul complet în seringa de blocare Kyphon®. Ataşaţi seringa de blocare Kyphon® la portul de
gonflare de pe IBT.
2. Trageţi înapoi pistonul seringii de blocare Kyphon®. Rotiţi pistonul pentru a-l bloca pe ultimul lăcaş din seringă.
3. Detaşaţi seringa de blocare Kyphon® de la IBT.
4. Ataşaţi portul de conectare de pe tubul seringii de gonflare marca Kyphon® la portul de gonflare de pe IBT. Sistemul este acum pregătit şi gata de folosire.
UTILIZAREA IBT
1. Selectaţi mărimea IBT pe baza locului şi obiectivului tratamentului. Figura 1 şi Tabelul 1 indică diametrul (D) şi lungimea (L) dispozitivelor IBT în stare gonflată, în apă la temperatura
de 37 °C, pentru diferite volume de gonflare, până la volumul de gonflare maxim.
2. Aceste dimensiuni pot varia în timpul folosirii produsului datorită variaţiei locale în structura osoasă.
Tabelul 1 - Dimensiunile dispozitivului IBT gonflat (în apă la 37 °C)
Numărul modelului E103A Dimensiunile gonflate
Mărime 10/3 Volum Diametru mediu (D1, D2) Lungime (L)
Volumul maxim de gonflare 4 ml 2 ml 12,9 mm 14,7 mm
Presiunea maximă de gonflare 27 atm 4 ml 17,2 mm 19,1 mm
Numărul modelului E153A Dimensiunile gonflate
Mărime 15/3 Volum Diametru mediu (D1, D2) Lungime (L)
Volumul maxim de gonflare 4 ml 2 ml 12,1 mm 17,4 mm
Presiunea maximă de gonflare 27 atm 4 ml 16 mm 22,1 mm
INSERAREA IBT
1. Pentru plasarea IBT este necesar un canal de acces.
2. Respectaţi instrucţiunile de utilizare pentru sculele de acces ale osului selectat pentru a crea un canal de acces în os.
3. Scoateţi manşonul de inserţie înainte de folosire.
NOTĂ: Vârful distal al IBT degonflat a atins capătul distal al canulei atunci când marcajul pentru ieşire de pe lumenul exterior al IBT intră în capătul proximal al canulei.
4. Aşezaţi IBT negonflat în canalul de acces şi plasaţi-l sub ghidare imagistică folosind markerii radioopaci. O uşoară mişcare de răsucire o dată cu împingerea înainte poate ajuta inserţia.
5. În timp ce ţineţi IBT fixat, gonflaţi la 0,3 MPa (3 atm) pentru a asigura fixarea poziţiei IBT. Scoateţi stiletul, dacă doriţi.
GONFLAREA IBT
1. Gonflaţi IBT sub ghidare imagistică continuă. Folosiţi vederea laterală pentru a monitoriza distanţa de la cortexul anterior şi lateral. Folosiţi vederea anteroposterioară pentru a
monitoriza corticalele laterale.
2. Dacă nu se utilizează o metodă de imagistică continuă, măriţi volumul în incremente mici (0,25 - 0,5 ml). Determinaţi poziţia tamponului în vedere laterală şi anteroposterioară
înainte de a continua cu creşterea volumului.
3. Încetaţi atunci când obiectivul tratamentului sau orice parte a lungimii gonflate a IBT face contact cu osul cortical sau se ajunge la volumul şi/sau presiunea maximă de gonflaţie
(Vezi Tabelul 1).
SCOATEREA IBT
ATENŢIONARE: A nu se retrage dispozitivul IBT decât atunci când componenta gonflabilă este complet degonflată. Nu retrageţi niciodată IBT prin învingerea rezistenţei. Determinaţi
cauza rezistenţei sub fluoroscopie şi luaţi măsurile necesare de remediere.
Utilizaţi o seringă de gonflare marca Kyphon® pentru a evacua mediul de contrast din IBT până ce balonul este complet degonflat. Scoateţi IBT din os prin canulă cu o uşoară mişcare de răsucire.
• Dacă există rezistenţă, conectaţi o seringă de 30 ml la portul de gonflare. Trageţi pistonul seringii înapoi până la semnul 30 ml pentru a crea un vid. Continuaţi scoaterea IBT.
• Confirmaţi intrarea porţiunii gonflabile a IBT în canulă. Dacă componenta gonflabilă nu se mişcă în canulă, avansaţi canula peste IBT până la cel mai apropiat marker radioopac.
După avansarea canulei, retrageţi IBT prin canulă. Dacă observaţi o rezistenţă, scoateţi IBT şi canula simultan.
STERILIZAREA
Sterilizat prin iradiere.
MOD DE PREZENTARE
IBT este furnizat steril într-un ambalaj care se deschide prin dezlipire. În eventualitatea în care ambalajul steril este deteriorat, nu se va folosi şi se va anunţa fabricantul.
MATERIALE NEFURNIZATE
• Seringă de gonflare marca Kyphon® cu seringă de blocare Kyphon®
• Mediu de Contrast (60%)
• Recipient mic
NOTĂ: Seringa de gonflare marca Kyphon® împreună cu seringa de blocare Kyphon® este disponibilă de la Medtronic.
MOD DE DEPOZITARE
IBT trebuie păstrat în ambalajul original. Trebuie avut grijă ca IBT să nu se deterioreze. A se depozita într-un loc răcoros şi uscat.
LIMITAREA RĂSPUNDERII
MEDTRONIC NU VA RĂSPUNDE PENTRU ORICE DAUNE DIRECTE, INDIRECTE, ACCIDENTALE, PE CALE DE CONSECINŢĂ SAU EXEMPLARE REZULTATE DIN REUTILIZAREA DISPOZITIVELOR
GONFLABILE DE PLOMBARE OSOASĂ PENTRU GESTIONAREA FRACTURILOR InflateFX™.
ÎN NICIUN CAZ MEDTRONIC NU VA RĂSPUNDE PENTRU ORICE DAUNE DIRECTE, INDIRECTE, ACCIDENTALE, PE CALE DE CONSECINŢĂ SAU EXEMPLARE CARE REZULTĂ DIN SAU ÎN LEGĂTURĂ
CU DISPOZITIVUL GONFLABIL DE PLOMBARE OSOASĂ PENTRU GESTIONAREA FRACTURILOR InflateFX™, DATORATE ÎNCĂLCĂRII CONTRACTULUI (INCLUSIV ÎNCĂLCAREA GARANŢIEI).
SOLICITARE DE INFORMAŢII
Pentru informații suplimentare vă rugăm să contactați Serviciul Clienți.
©2013 Medtronic Sofamor Danek USA Inc. Toate drepturile rezervate.
SlovEnčina
INDIKACIJE ZA UPORABO
Polnljivi kostni tampon za oskrbo zlomov InflateFX™ (IBT – Inflatable Bone Tamp) se uporablja kot klasični kostni tampon za zmanjšanje zlomov in/ali praznega prostora v spongiozni
kostnini v dlaneh, golenici, koželjnici in petnici.
OPIS PRIPOMOČKA
Glejte sliko 1.
1. pokrovček
2. stilet
3. odprtina za stilet
4. odprtina za polnjenje
5. barvni obroček
6. izhodni označevalec
7. uvajalni tulec
8. radioopačni označevalci
9. polnljiva komponenta
• Polnljiva komponenta IBT je zasnovana tako, da pri polnjenju omogoča kompresijo spongiozne kostnine in/ali premik kortikalne kosti. Polnilna komponenta tampona IBT je
nameščena blizu distalne konice pripomočka, kot je prikazano na sliki 1.
• Cevka vsebuje dva nepovezana lumna. Zunanji lumen je namenjen polnjenju tampona IBT, osrednji lumen pa vsebuje odstranljiv utrjevalni stilet za vstavljanje tampona IBT.
• Proksimalni konec cevkeima stranski adapter. Odprtina za polnjenje adapterja je povezana z zunanjim lumnom. Odprtina za stilet je povezana z notranjim lumnom in vsebuje
utrjevalni stilet. Na proksimalnem koncu stileta je pokrovček, ki se lahko po potrebi odstrani.
• Barvni obroček, nameščen distalno od stranskega adapterja, prikazuje velikost balona (tj. rumen obroček za velikost 10/3 in črn obroček za velikost 15/3).
• Izhodni označevalec na zunanjem lumnu se uporablja med vstavljanjem tampona IBT.
• Radioopačnioznačevalci na distalnem in proksimalnem koncu izpraznjene delovne površine omogočajo fluoroskopsko vizualizacijo izpraznjenega tampona IBT med nameščanjem.
KONTRAINDIKACIJE
• Motnje v strjevanju krvi ali zdravljenje, ki poveča tveganje za prekomerno krvavitev.
• Ob prisotnosti aktivnih ali nepozdravljenih okužb na mestu, kamor se vnaša polnilo kostnega prostora.
• Vse poznane hude alergije na kontrastno sredstvo in polnilo kostnega prostora.
• Bolnice s potrjeno nosečnostjo.
PREVIDNOSTNO OPOZORILO: Po zveznem zakonu (ZDA) je možno ta pripomoček kupiti le od zdravnika ali po naročilu zdravnika.
OPOZORILA
• Če se pripomoček zlomi, bo morda potreben poseg ali odstranitev.
• Izdelka ne uporabljajte po izteku roka uporabnosti (uporabno do), natisnjenega na ovojnini. Po izteku roka uporabnosti (uporabno do) pripomoček morda ni več varen ali učinkovit.
• Polnljiva komponenta lahko odpove zaradi ostrih kostnih bodic ali kirurških inštrumentov.
• Polnjenje tampona IBT, ki presega največji volumen polnjenja, lahko povzroči, da balon poči, preden doseže največji tlak polnjenja.
• Polnjenje tampona IBT, ki presega največji tlak polnjenja, lahko povzroči, da balon poči, preden doseže največji volumen polnjenja.
• Balona nikoli ne polnite z zrakom ali plinastimi snovmi.
PREVIDNOSTNI UKREPI
• Polnljivi kostni tampon je pripomoček za enkratno uporabo, ki pride v stik s telesnimi tkivi. Pripomoček ni namenjen ponovni uporabi, predelavi za uporabo ali ponovni sterilizaciji.
Ponovna uporaba teh pripomočkov predstavlja tveganje za kontaminacijo in lahko povzroči okužbo bolnika ali navzkrižno okužbo, ne glede na metode čiščenja in ponovne sterilizacije.
Obstaja tudi povečano tveganje za poslabšanje delovanja pripomočka zaradi korakov predelave kar lahko privede do poškodbe ali smrti bolnika.
• Pomembno je, da pred uporabo pripomočka pazljivo preberete navodila za uporabo in te previdnostne ukrepe.
• Tampon IBT uporabite pred iztekom roka uporabnosti, ki je naveden na ovojnini.
• Ne uporabite, če je ovojnina odprta ali poškodovana, saj je lahko ogrožena neoporečnost izdelka, vključno s sterilnostjo.
• Ne uporabljajte poškodovanih izdelkov. Pred uporabo preglejte IBT in ovojnino, da nista poškodovana.
• Pred uporabo preverite delovanje tampona IBT in primernost velikosti tampona IBT za nameravani poseg.
• Tega izdelka ne smete uporabljati, če niste primerno usposobljeni. Tampon IBT lahko uporabljajo le zdravniki, ki so usposobljeni v tehnikah uporabe kostnih tamponov. Zdravniki,
ki uporabljajo pripomočke, morajo poznati fiziologijo in patologijo anatomskega mesta, kjer se bo poseg izvajal.
• Delo s tamponom IBT se lahko izvaja le s pomočjo fluoroskopskega opazovanja z radiografsko opremo, ki zagotavlja visokokakovostne slike.
• Tampon IBT lahko polnite le s polnilno brizgo z najmanjšim volumnom 14 ml.
• Tampon IBT polnite samo s tekočim kontrastnim sredstvom: priporočamo 60-odstotno raztopino. Pri indikacijah, uporabi in previdnostnih ukrepih kontrastnega sredstva upoštevajte
navodila proizvajalca.
• Za polnjenje tampona IBT ne uporabljajte zraka ali drugega plina.
• Polnilne lastnosti tampona IBT so drugačne pri polnjenju znotraj kosti.
• Izrecno je prepovedano obnavljanje, predelava, popravljanje, spreminjanje ali ponovna sterilizacija pripomočka za namen ponovne uporabe.
• Vsaka operacija ima tveganja, a uporaba balon pri zdravljenju tovrstnih zlomov s kliničnega vidika ne povečuje teh tveganj v primerjavi s tradicionalnimi metodami dvigovanja
vdrtih kostnih fragmentov. Ta tveganja vključujejo:
o nepravilno zmanjšanje fragmentov zloma;
o zapoznelo zaraščanje ali nezaraščanje;
o okužbo;
o nevrovaskularne poškodbe ali utesnitveni sindrom, ki povzroči izgubo funkcije ali amputacijo.
OPOMBA: Polnilna brizga Kyphon® omogoča boljši nadzor nad volumnom v primerjavi z drugimi polnilnimi sistemi, kot je standardna brizga, zato je njena uporaba pri polnjenju tampona
IBT obvezna. Za uporabo polnilne brizge Kyphon® sledite navodilom proizvajalca. Zaklepna brizga Kyphon® je priložena polnilni brizgi Kyphon®.
NEŽELENI DOGODKI
Neželeni dogodki ki so lahko povezani z uporabo IBT, vključujejo resne dogodke, ki so lahko, čeprav redko, smrtni.
Neželeni dogodki vključujejo:
• maščobno embolijo, trombusno embolijo ali embolijo druge vrste, ki povzroči simptomatsko pljučno embolijo ali druga klinična stanja;
• rupturo s fragmentacijo polnljivega dela IBT, ki povzroči zastoj fragmenta na prizadetem območju;
• rupturo tampona IBT, ki povzroči izpostavljenost kontrastnemu sredstvu, kar lahko privede do alergične reakcije ali anafilakse;
• globoke ali površinske okužbe rane;
• krvavitev ali hematom.
INFORMAŢII IMPORTANTE PRIVIND dispozitivul de plombare osoasă
pentru gestionarea fracturilor InflateFX™ (Mărimi 10/3 şi 15/3)
Pomembne informacije o polnljivem kostnem tamponu
za oskrbo zlomov InflateFX™ (velikosti 10/3 in 15/3)
NAVODILA ZA UPORABO
PREVIDNOSTNO OPOZORILO: Za uporabo polnilne brizge Kyphon® sledite navodilom proizvajalca.
PREVIDNOSTNO OPOZORILO: Kontrastna sredstva imajo lahko različne viskoznosti in stopnje obarjanja, kar lahko povzroči počasnejše polnjenje in praznjenje. Zaradi tega priporočamo
uporabo 60-odstotne raztopine kontrastnega sredstva.
1. Zasučite pokrovček na odprtini za stilet ter tako pričvrstite stilet na tampon IBT. Potisnite bat do konca v zaklepno brizgo Kyphon® Namestite zaklepno brizgo Kyphon® na odprtinoza
polnjenje na tamponu IBT.
2. Povlecite bat zaklepne brizge Kyphon® nazaj. Zavrtite bat, da ga zaklenete na položaju zadnje zareze na brizgi.
3. Odstranite zaklepno brizgo Kyphon® s tampona IBT.
4. Namestite priključek na cevi polnilne brizge Kyphon® na odprtinoza polnjenje na tamponu IBT. Sistem je sedaj pripravljen za uporabo.
UPORABA IBT
1. Izberite velikost IBT, ki ustreza anatomskemu mestu in namenu postopka. Na sliki 1 in v tabeli 1 so prikazani premeri (D) in dolžine (L) IBT v napolnjenem stanju (v vodi pri 37 °C)
pri naraščajočem volumnu polnitve do največjega volumna polnitve.
2. Te dimenzije lahko med uporabo izdelka variirajo zaradi lokalnih variacij v strukturi kosti.
Tabela 1 – dimenzije tampona IBT v napolnjenem stanju (v vodi pri 37 °C)
številka modela E103A dimenzije v napolnjenem stanju
velikost 10/3 volumen povp. premer (D1, D2) dolžina (L)
največji volumen polnitve 4 ml 2 ml 12,9 mm 14,7 mm
največji tlak polnitve 27 atm 4 ml 17,2 mm 19,1 mm
številka modela E153A dimenzije v napolnjenem stanju
velikost 15/3 volumen povp. premer (D1, D2) dolžina (L)
največji volumen polnitve 4 ml 2 ml 12,1 mm 17,4 mm
največji tlak polnitve 27 atm 4 ml 16 mm 22,1 mm
VSTAVITEV IBT
1. Za namestitev tampona IBT potrebujete pristopni kanal.
2. Sledite navodilom za uporabo izbranih pripomočkov za dostop do kosti in v kosti ustvarite pristopni kanal.
3. Pred uporabo odstranite uvajalni tulec.
OPOMBA: Distalna konica izpraznjenega tampona IBT doseže distalni konec kanile, ko izhodni označevalec na zunanjem lumnu tampona IBT vstopi v proksimalni konec kanile.
4. Vstavite izpraznjen tampon IBT v pristopni kanal in ga namestite s pomočjo slikovnih navodil in z uporabo radioopačnih označevalcev. Za lažje vstavljanje nežno sučite in sočasno
potiskajte pripomoček.
5. Tampon IBT držite na mestu in ga napolnite do 0,3 MPa (3 atm), da ga namestite v želeni položaj. Če želite, odstranite stilet.
POLNJENJE IBT
1. IBT polnite ob stalnem spremljanju slikovnih navodil. S pomočjo lateralnega pogleda preverite razdaljo od anteriornega in lateralnega korteksa. Lateralne kortekse preverite z
anteroposteriornim (AP) pogledom.
2. Če ne izvajate stalnega slikanja, povečujte volumen v majhnih korakih (0,25 – 0,5 ml). Preverite položaj tampona v lateralnem in AP pogledu, preden povečate volumen.
3. Postopek zaključite, ko je dosežen cilj postopka, in sicer, ko se katerikoli del napolnjenega tampona IBT dotakne kortikalne kosti, oziroma ko dosežete največji volumen polnitve in/
ali največji tlak polnitve (glejte tabelo 1).
ODSTRANITEV IBT
PREVIDNOSTNO OPOZORILO: Tampona IBT ne izvlecite, dokler ni polnilna komponenta povsem prazna. Nikoli ne odstranite tampona IBT, če naletite na odpor. S fluoroskopijo določite
vzrok odpora in izvedite potrebne ukrepe za odpravo stanja.
Uporabite polnilno brizgo Kyphon® in odstranite kontrastno sredstvo iz tampona IBT, dokler ni balon popolnoma prazen. Odstranite tampon IBT iz kosti skozi kanilo z nežnim sukanjem.
• Če pride do odpora, na odprtino za polnjenje namestite 30 ml brizgo. Bat brizge povlecite do oznake “30 ml”, da ustvarite vakuum. Nadaljujte z odstranjevanjem tampona IBT.
• Potrdite vstop polnilnega dela IBT v kanilo. Če se polnilna komponenta ne pomakne v kanilo, pomaknite kanilo preko tampona IBT proti proksimalnemu radioopačnemu označevalcu.
Po pomiku kanile odstranite tampon IBT skozi kanilo. Če naletite na odpor, odstranite tampon IBT in kanilo sočasno.
STERILIZACIJA
Sterilizirano z obsevanjem.
PAKIRANJE
Tamponi IBT so dobavljeni v sterilni obliki v stični ovojnini. Če je sterilna ovojnina poškodovana, izdelka ne uporabite in o tem obvestite proizvajalca.
NEPRILOŽENE POTREBŠČINE
• polnilna brizga Kyphon® z zaklepno brizgo Kyphon®.
• kontrastno sredstvo (60%)
• majhna posoda
OPOMBA: Polnilna brizga Kyphon® z zaklepno brizgo Kyphon® je na voljo pri podjetju Medtronic.
SHRANJEVANJE
Tampone IBT je potrebno shranjevati v originalnem pakiranju. Tampone IBT je potrebno primerno zavarovati pred poškodovanjem. Hranite na suhem in hladnem mestu.
OMEJITEV ODGOVORNOSTI
PODJETJE MEDTRONIC NE ODGOVARJA ZA NIKAKRŠNO NEPOSREDNO, POSREDNO, NAKLJUČNO, POSLEDIČNO ALI EKSEMPLARIČNO ŠKODO, NASTALO ZARADI PONOVNE UPORABE POLNLJIVIH
KOSTNIH TAMPONOV ZA OSKRBO ZLOMOV InflateFX™.
PODJETJE MEDTRONIC V NOBENEM PRIMERU NE ODGOVARJA ZA NIKAKRŠNO NEPOSREDNO, POSREDNO, SLUČAJNO, POSLEDIČNO ALI EKSEMPLARIČNO ŠKODO, NASTALO PRI ALI V POVEZAVI
Z UPORABO POLNLJIVIH KOSTNIH TAMPONOV ZA OSKRBO ZLOMOV InflateFX™ , ZARADI KRŠENJA POGODBE (VKLJUČNO S KRŠENJEM GARANCIJE).
POVPRAŠEVANJE PO INFORMACIJAH
Za dodatne informacije se obrnite na službo za stranke.
©2013 Medtronic Sofamor Danek USA, Inc. Vse pravice pridržane.
Figure 1: inflatable Bone Tamp (IBT)
Symbol Definitions
 Loading...
Loading...