
FLEXCATH™ SELECT 990065
0088
Steerable Sheath
Řiditelné pouzdro
Styrbar sheath
Steuerbare Schleuse
Κατευθυνόμενο θηκάρι
Introductor dirigible
Ohjattava holkki
Gaine orientable
Irányítható hüvely
Introduttore orientabile
Stuurbare sheath
Styrbar hylse
Osłona sterowalna
Bainha direcionável
Bainha direcionável
Управляемый интродьюсер
Ovládateľné puzdro
Styrbar skida
Yönlendirilebilir Kılıf
Technical Manual • Technická příručka • Teknisk håndbog • Gebrauchsanweisung •
Τεχνικό εγχειρίδιο • Manual técnico • Tekninen opas • Manuel technique • Műszaki leírás •
Manuale tecnico • Technische handleiding • Teknisk håndbok • Instrukcja techniczna •
Manual técnico • Manual técnico • Техническое руководство • Technická príručka •
Teknisk manual • Teknik El Kitabı
Federal law (USA) restricts this device to sale by or on
Caution:
the order of a physician.

The following list includes trademarks or registered trademarks of Medtronic in the United States and possibly in other
countries. All other trademarks are the property of their respective owners.
Následující seznam uvádí ochranné známky nebo registrované ochranné známky společnosti Medtronic v USA a
případně v jiných zemích. Všechny ostatní ochranné známky jsou majetkem příslušných vlastníků.
Følgende liste indeholder varemærker eller registrerede varemærker tilhørende Medtronic i USA og muligvis i andre
lande. Alle andre varemærker tilhører de respektive ejere.
Die folgende Liste beinhaltet Marken oder eingetragene Marken von Medtronic in den USA und möglicherweise in
anderen Ländern. Alle anderen Marken sind Eigentum ihrer jeweiligen Inhaber.
Ο ακόλουθος κατάλογος περιλαμβάνει εμπορικά σήματα ή σήματα κατατεθέντα της Medtronic στις Ηνωμένες
Πολιτείες και πιθανόν σε άλλες χώρες. Όλα τα άλλα εμπορικά σήματα είναι ιδιοκτησία των αντίστοιχων κατόχων
τους.
La siguiente lista incluye marcas comerciales o marcas registradas de Medtronic en los Estados Unidos y
posiblemente en otros países. Todas las marcas comerciales son propiedad de sus propietarios respectivos.
Seuraava luettelo sisältää Medtronic-yhtiön tavaramerkit ja rekisteröidyt tavaramerkit Yhdysvalloissa ja
mahdollisestimuissa maissa. Kaikki muut tavaramerkit ovat niiden omistajien omaisuutta.
La liste suivante inclut des marques commerciales ou des marques déposées de Medtronic aux États-Unis et
eventuellement dans d'autres pays. Toutes les autres marques commerciales sont la propriété de leurs détenteurs
respectifs.
Az alábbi lista a Medtronic Egyesült Államokban és valószínűleg más országokban érvényes védjegyeit vagy
bejegyzett védjegyeit tartalmazza. Minden egyéb védjegy a megfelelő tulajdonosok tulajdonát képezi.
L'elenco seguente include marchi di fabbrica o marchi registrati della Medtronic negli Stati Uniti ed eventualmente in
altri Paesi. Tutti gli altri marchi di fabbrica sono di proprietà dei rispettivi proprietari.
In de onderstaande lijst staan de gedeponeerde of geregistreerde handelsmerken van Medtronic in de Verenigde
Staten en mogelijk in andere landen. Alle andere handelsmerken zijn het eigendom van de desbetreffende eigenaar.
Den følgende listen inneholder varemerker eller registrerte varemerker for Medtronic i USA og eventuelt i andre land.
Alle andre varemerker tilhører de respektive eierne.
Poniższa lista zawiera znaki towarowe lub zastrzeżone znaki towarowe firmy Medtronic w Stanach Zjednoczonych i
prawdopodobnie w innych krajach. Wszystkie pozostałe znaki towarowe są własnością ich prawowitych właścicieli.
A lista a seguir inclui marcas comerciais ou marcas comerciais registradas da Medtronic nos Estados Unidos e
possivelmente em outros países.Todas as outras marcas comerciais são propriedade dos seus respectivos
proprietários.
A lista que se segue inclui marcas comerciais ou marcas comerciais registadas da Medtronic nos EUA e
possivelmente noutros países. Todas as outras marcas comerciais são propriedade dos respetivos detentores.
Следующий список включает товарные знаки или зарегистрированные товарные знаки корпорации
Medtronic в США и, возможно, в других странах. Все другие товарные знаки являются собственностью их
владельцев.
Nasledujúci zoznam obsahuje ochranné známky alebo registrované ochranné známky spoločnosti Medtronic v USA
a prípadne v ďalších krajinách. Všetky ostatné ochranné známky sú majetkom príslušných vlastníkov.
Följande lista innehåller varumärken eller registrerade varumärken som tillhör Medtronic i USA och möjligen i andra
länder. Alla övriga varumärken tillhör respektive innehavare.
Aşağıdaki liste Medtronic şirketinin Amerika Birleşik Devletleri'nde ve muhtemelen diğer ülkelerdeki ticari markalarını
veya tescilli ticari markalarını içerir. Diğer ticari markaların tümü ilgili sahiplerinin mülkiyetindedir.
FlexCath, Medtronic

Explanation of symbols • Vysvětlení symbolů • Symbolforklaring • Erläuterung der
Symbole • Επεξήγηση των συμβόλων • Explicación de los símbolos • Symboleiden
selitykset • Explication des symboles • A szimbólumok magyarázata • Spiegazione dei
simboli • Verklaring van de symbolen • Symbolforklaring • Objaśnienie symboli •
Explicação dos símbolos • Explicação dos símbolos • Объяснение символов •
Vysvetlivky k symbolom • Förklaring av symboler • Sembollerin açıklaması
The following list of symbols and abbreviations applies to various products. Refer to the package
labels to see which symbols apply to this product. • Následující seznam symbolů a zkratek platí
pro různé produkty. Symboly týkající se tohoto produktu naleznete na štítcích obalu. • Følgende
liste over symboler og forkortelser gælder for en række forskellige produkter. Se mærkaterne på
emballagen for at se, hvilke symboler der gælder for dette produkt. • Die folgende Symbol- und
Abkürzungsliste gilt für verschiedene Produkte. Die für dieses Produkt zutreffenden Symbole
finden Sie auf dem jeweiligen Verpackungsetikett. • Ο ακόλουθος κατάλογος συμβόλων και
συντμήσεων ισχύει για διάφορα προϊόντα. Ανατρέξτε στις ετικέτες της συσκευασίας για να
δείτε ποια σύμβολα ισχύουν για το παρόν προϊόν. • La siguiente lista de símbolos y abreviaturas
es aplicable a varios productos. Consulte las etiquetas del envase para comprobar qué símbolos
se utilizan con este producto. • Seuraavassa luetellut symbolit ja lyhenteet koskevat monia
tuotteita. Katso pakkausetiketeistä, mitkä symbolit koskevat tätä tuotetta. • La liste de symboles
et abréviations suivante s’applique à divers produits. Se reporter aux étiquettes sur l’emballage
pour savoir quels symboles s’appliquent à ce produit. • Az alábbi listában szereplő szimbólumok
és rövidítések több termékre vonatkoznak. A termékre vonatkozó szimbólumok a csomagolás
címkéin találhatók. • L’elenco di simboli e abbreviazioni che segue è valido per vari prodotti. Per
sapere quali simboli si applicano a questo prodotto, si prega di fare riferimento alle etichette sulla
confezione. • De volgende lijst met symbolen en afkortingen heeft betrekking op verschillende
producten. Controleer het verpakkingslabel om te zien welke symbolen op dit product van
toepassing zijn. • Denne listen med symboler og forkortelser gjelder for forskjellige produkter. Se
på pakningen for å fastslå hvilke symboler som gjelder for dette produktet. • Poniższa lista symboli
i skrótów ma zastosowanie do różnych produktów. Należy zapoznać się z etykietą na
opakowaniu, aby określić, które symbole dotyczą niniejszego produktu. • A seguinte lista de
símbolos e abreviaturas aplica-se a vários produtos. Consulte as etiquetas da embalagem para
ver quais símbolos se aplicam a este produto. • A seguinte lista de símbolos e abreviaturas
aplica-se a vários produtos. Consulte as etiquetas da embalagem para ver que símbolos se
aplicam a este produto. • Следующий перечень символов и сокращений применим к
различным продуктам. См. на этикетках упаковки, какие символы применимы к данному
продукту. • Nasledujúci zoznam symbolov a skratiek sa vzťahuje na rôzne produkty. Prezrite si
označenie na obale a zistite, ktoré symboly sa vzťahujú na tento produkt. • Följande lista med
symboler och förkortningar gäller för olika produkter. Se förpackningsetiketterna för de symboler
som gäller denna produkt. • Aşağıdaki semboller ve kısaltmalar listesi çeşitli ürünler için geçerlidir.
Bu ürün için hangi sembollerin geçerli olduğunu görmek için ambalaj etiketlerine başvurun.
Lot number • Číslo šarže • Partinummer • Losnummer • Αριθμός παρτίδας • Número
de lote • Eränumero • Numéro de lot • Tételszám • Numero di lotto • Partijnummer •
Lotnummer • Numer partii produkcyjnej • Número de lote • Número de lote • Номер
партии • Číslo šarže • Lotnummer • Lot numarası
Reorder number • Číslo pro novou objednávku • Genbestillingsnummer •
Bestellnummer • Αριθμός νέας παραγγελίας • Número de referencia •
Uusintatilausnumero • Numéro de commande • Utánrendelési szám • Numero di
catalogo • Bestelnummer • Bestillingsnummer • Numer do ponownego zamawiania •
Número para novo pedido • Número para nova encomenda • Номер для заказа •
Číslo pre ďalšie objednávky • Återbeställningsnummer • Yeniden sipariş numarası
Use-by • Datum použitelnosti • Anvendes inden • Ver wendbar bis einschließlich •
Χρήση έως • Fecha de caducidad • Käytettävä viimeistään • Date de péremption •
Lejárat • Data di scadenza • Uiterste gebruiksdatum • Siste forbruksdag • Termin
ważności • Prazo de validade • Utilizar até • Срок годности • Dátum najneskoršej
spotreby • Sista förbrukningsdag • Son kullanma tarihi
Sterilized using ethylene oxide • Sterilizováno ethylenoxidem • Steriliseret med
etylenoxid • Mit Ethylenoxid sterilisiert • Αποστειρωμένο με αιθυλενοξείδιο •
Esterilizado mediante óxido de etileno • Steriloitu etyleenioksidilla • Stérilisé à l’oxyde
d’éthylène • Etilén-oxiddal sterilizálva • Sterilizzato a ossido di etilene • Gesteriliseerd
met ethyleenoxide • Sterilisert med etylenoksid • Sterylizowany tlenkiem etylenu •
Esterilizado com óxido de etileno • Esterilizado utilizando óxido de etileno •
Стерилизовано этиленоксидом • Sterilizované pomocou etylénoxidu • Steriliserad
med etylenoxid • Etilen oksit ile sterilize edilmiştir
Do not re-use • Nepoužívejte opakovaně • Må ikke genanvendes • Nicht
wiederverwenden • Μην το επαναχρησιμοποιείτε • No reutilizar • Älä käytä uudelleen
• Ne pas réutiliser • Újrafelhasználni tilos • Non riutilizzare • Niet opnieuw gebruiken •
Skal ikke brukes flere ganger • Nie używać powtórnie • Não reutilizar • Não reutilizar •
Не использовать повторно • Nepoužívajte opakovane • Får inte återanvändas •
Yeniden kullanmayın
Do not resterilize • Neprovádějte resterilizaci • Må ikke resteriliseres • Nicht
resterilisieren • Μην επαναποστειρώνετε • No reesterilizar • Älä steriloi uudelleen •
Ne pas restériliser • Nem újrasterilizálható • Non risterilizzare • Niet opnieuw
steriliseren • Skal ikke resteriliseres • Nie sterylizować ponownie • Não reesterilizar •
Não reesterilizar • Не стерилизовать повторно • Opakovane nesterilizujte • Får inte
omsteriliseras • Yeniden sterilize etmeyin
Do not use if package is damaged • Nepoužívejte, je-li obal poškozený • Må ikke
anvendes, hvis emballagen er beskadiget • Nicht verwenden, wenn die Verpackung
beschädigt ist • Μη χρησιμοποιείτε εάν η συσκευασία υποστεί ζημιά • No utilizar si el
envase está dañado • Älä käytä, jos pakkaus on vaurioitunut • Ne pas utiliser si
l’emballage est endommagé • Ne használja fel, ha a csomagolás sérült • Non
utilizzare se l’imballaggio non è integro • Niet gebruiken als de verpakking beschadigd
is • Skal ikke brukes hvis pakningen er skadet • Nie stosować, jeśli opakowanie jest
uszkodzone • Não utilizar se a embalagem estiver danificada • Não utilizar se a
embalagem estiver danificada • Не использовать, если упаковка повреждена •
Nepoužívajte, ak je obal poškodený • Får ej användas om förpackningen är skadad •
Ambalaj hasarlıysa kullanmayın
Consult instructions for use • Viz návod k použití • Se brugsanvisningen •
Gebrauchsanweisung lesen • Συμβουλευτείτε τις οδηγίες χρήσης • Consultar
instrucciones de uso • Katso käyttöohjeet • Consulter le mode d’emploi • Lásd a
használati útmutatót • Consultare le istruzioni per l’uso • Zie gebruiksaanwijzing • Se
i bruksanvisningen • Należy zapoznać się z instrukcją użytkowania • Consultar as
instruções de utilização • Consultar as instruções de utilização • См. инструкцию по
эксплуатации • Pozrite si pokyny na používanie • Läs bruksanvisningen • Kullanım
talimatlarına bakın
Keep dry • Udržujte v suchu • Skal opbevares tørt • Trocken aufbewahren •
Διατηρήστε στεγνό • Mantener seco • Säilytä kuivassa • À conserver dans un endroit
sec • Szárazon tartandó • Mantenere asciutto • Droog bewaren • Skal holdes tørr •
Chronić przed wilgocią • Manter em local seco • Manter seco • Хранить в сухом
месте • Uschovajte v suchu • Förvaras torrt • Kuru yerde saklayın
Storage temperature limit • Mezní hodnoty skladovací teploty • Temperaturgrænse
ved opbevaring • Grenzwerte Lagerungstemperatur • Όριο θερμοκρασίας
αποθήκευσης • Límite de temperatura de almacenamiento • Säilytyslämpötilaraja •
Limite de température de stockage • Tárolási hőmérséklet határértéke • Limite della
temperatura di conservazione • Bereik opslagtemperatuur • Temperaturgrense,
oppbevaring • Dopuszczalna temperatura przechowywania • Limite de temperatura
de armazenamento • Limite da temperatura de armazenamento • Диапазон
температуры хранения • Hraničné hodnoty skladovacej teploty • Temperaturgräns
vid förvaring • Saklama sıcaklığı sınırı
Transit temperature limit • Mezní hodnoty teploty při přepravě • Temperaturgrænse
under transport • Grenzwerte Transporttemperatur • Όριο θερμοκρασίας μεταφοράς
• Límite de temperatura de transporte • Kuljetuslämpötilaraja • Limite de température
de transport • Szállítási hőmérséklet határértéke • Limite della temperatura di
trasporto • Bereikt transporttemperatuur • Temperaturgrense, forsendelse •
Dopuszczalna temperatura transportu • Limite de temperatura de transporte • Limite
da temperatura de transporte • Диапазон температуры транспортировки •
3

Hraničné hodnoty teploty pri preprave • Temperaturgräns vid transport • Nakliyat
sıcaklığı sınırı
Humidity limitation • Mezní hodnoty vlhkosti • Grænse for luftfugtighed •
Luftfeuchtigkeitsbereich • Όριο υγρασίας • Limitación de humedad • Kosteusrajoitus •
Limite d’humidité • Páratartalom-határok • Limiti di umidità • Vochtigheidsbereik • Krav
til fuktighet • Ograniczenia wilgotności • Limites de umidade • Limites de humidade •
Пределы влажности • Hraničné hodnoty vlhkosti • Begränsning för luftfuktighet •
Nemlilik sınırlaması
Product documentation • Průvodní dokumentace • Produktdokumentation •
Produktdokumentation • Τεκμηρίωση προϊόντος • Documentación del producto •
Tuotedokumentaatio • Documentation du produit • Termékdokumentáció •
Documentazione sul prodotto • Productdocumentatie • Produktdokumentasjon •
Dokumentacja produktu • Documentação do produto • Documentação do produto •
Документация по продукту • Dokumentácia k produktu • Produktdokumentation •
Ürünle ilgili belgeler
Package contents • Obsah balení • Pakkens indhold • Packungsinhalt • Περιεχόμενα
συσκευασίας • Contenido del envase • Pakkauksen sisältö • Contenu de l’emballage •
A csomag tartalma • Contenuto della confezione • Inhoud van de verpakking •
Pakningens innhold • Zawartość opakowania • Conteúdo da embalagem • Conteúdo
da embalagem • Содержимое упаковки • Obsah balenia • Förpackningens innehåll
• Ambalaj içeriği
Fragile, handle with care • Křehké, manipulujte opatrně • Skrøbelig, skal håndteres
med forsigtighed • Vorsicht: zerbrechlich • Εύθραυστο, χειριστείτε με προσοχή •
Frágil, manipular con cuidado • Helposti särkyvä, käsittele varovasti • Fragile, à
manipuler avec précaution • Törékeny, óvatosan kezelendő • Fragile, maneggiare con
cura • Breekbaar, voorzichtig hanteren • Må håndteres med forsiktighet • Delikatne,
zachować ostrożność • Frágil, manusear com cuidado • Frágil, manusear com
cuidado • Хрупкое, обращайтесь с осторожностью • Krehké, manipulujte opatrne •
Ömtålig, hanteras varsamt • Kırılabilir, dikkatle taşıyın
Inner diameter • Vnitřní průměr • Indvendig diameter • Innendurchmesser •
Εσωτερική διάμετρος • Diámetro interno • Sisäläpimitta • Diamètre interne • Belső
átmérő • Diametro interno • Binnendiameter • Indre diameter • Średnica wewnętrzna •
Diâmetro interno • Diâmetro interno • Внутренний диаметр • Vnútorný priemer • Inre
diameter • İç çapı
Manufacturer • Výrobce • Fabrikant • Hersteller • Κατασκευαστής • Fabricante •
Valmistaja • Fabricant • Gyár tó • Fabbricante • Fabrikant • Produsent • Producent •
Fabricante • Fabricante • Производитель • Výrobca • Tillverkare • Üretici
Authorized representative in the European Community • Autorizovaný zástupce pro
Evropské společenství • Autoriseret repræsentant i EU • Autorisierter Repräsentant in
der Europäischen Gemeinschaft • Εξουσιοδοτημένος αντιπρόσωπος στην
Ευρωπαϊκή Κοινότητα • Representante autorizado en la Comunidad Europea •
Valtuutettu edustaja Euroopan yhteisön alueella • Représentant autorisé dans la
Communauté européenne • Hivatalos képviselet az Európai Közösségben •
Rappresentante autorizzato nella Comunità europea • Geautoriseerd
vertegenwoordiger in de Europese Gemeenschap • Autorisert representant i Det
europeiske fellesskap • Autoryzowany przedstawiciel w Unii Europejskiej •
Representante autorizado na Comunidade Europeia • Representante autorizado na
Comunidade Europeia • Уполномоченный представитель в Европейском
сообществе • Autorizovaný zástupca pre Európske spoločenstvo • Auktoriserad
representant inom EG • Avrupa Topluluğu’ndaki yetkili temsilci
For US audiences only • Pouze pro uživatele v USA • Gælder kun i USA • Gilt nur für
Leser in den USA • Μόνο για πελάτες εντός των ΗΠΑ • Solo aplicable en EE. UU. •
Koskee vain Yhdysvaltoja • Ne s’applique qu’aux États-Unis • Csak egyesült
államokbeli felhasználóknak • Esclusivamente per il mercato statunitense • Alleen
van toepassing voor de VS • Gjelder kun USA • Dotyczy tylko odbiorców w USA •
Aplicável apenas aos EUA • Aplicável apenas aos EUA • Только для США • Len pre
používateľov v USA • Gäller endast i USA • Yalnızca ABD’deki kullanıcılar için
Conformité Européenne (European Conformity). This symbol means that the device
fully complies with European Council Directive 93/42/EEC. • Conformité Européenne
(Evropská shoda). Tento symbol znamená, že zařízení zcela splňuje požadavky
směrnice Evropské rady 93/42/EHS. • Conformité Européenne (Europæisk
standard). Dette symbol betyder, at enheden fuldt ud overholder Det Europæiske
Råds Direktiv 93/42/EØF. • Conformité Européenne (Europäische Konformität).
Dieses Symbol besagt, dass das Gerät allen Vorschriften der Direktive 93/42/EWG
des Europäischen Rates entspricht. • Conformité Européenne (Ευρωπαϊκή
Συμμόρφωση). Το σύμβολο αυτό σημαίνει ότι το προϊόν συμμορφώνεται πλήρως με
την Οδηγία 93/42/ΕΟΚ του Ευρωπαϊκού Συμβουλίου. • Conformité Européenne
(Conformidad Europea). Este símbolo indica que el dispositivo cumple totalmente la
Directiva 93/42/CEE del Consejo Europeo. • Conformité Européenne
(eurooppalainen vaatimustenmukaisuus). Tämä symboli tarkoittaa, että laite on
kaikilta osin Euroopan unionin neuvoston direktiivin 93/42/ETY mukainen. •
Conformité Européenne. Ce symbole signifie que l’appareil est entièrement conforme
à la Directive 93/42/CEE du Conseil de l’Union européenne. • Conformité Européenne
(Európai Megfelelőség). Ez a szimbólum azt jelenti, hogy az eszköz teljes mértékben
megfelel az Európai Tanács 93/42/EGK irányelvében foglalt követelményeknek. •
Conformité Européenne (Conformità europea). Questo simbolo indica che il
dispositivo è conforme alla Direttiva del Consiglio europeo 93/42/CEE. • Conformité
Européenne (Europese Conformiteit). Dit symbool betekent dat het product volledig
voldoet aan de Europese Richtlijn 93/42/EEG. • Conformité Européenne (samsvar
med europeisk standard). Dette symbolet betyr at enheten er fullstendig i samsvar
med EU-direktiv 93/42/EØF. • Conformité Européenne (Zgodność z normami Unii
Europejskiej). Symbol ten oznacza, że urządzenie spełnia wszystkie wymagania
europejskiej dyrektywy Rady 93/42/EWG. • Conformité Européenne (Conformidade
Europeia). Este símbolo significa que o dispositivo está em total conformidade com a
Diretiva do Conselho Europeu 93/42/CEE. • Conformité Européenne (Conformidade
Europeia). Este símbolo significa que o dispositivo está em total conformidade com a
Diretiva do Conselho Europeu 93/42/CEE. • Conformité Européenne (Европейское
соответствие). Этот символ обозначает, что устройство полностью
соответствует требованиям директивы Европейского Совета 93/42/EEC. •
Conformité Européenne (Zhoda s požiadavkami EÚ). Tento symbol znamená, že
zariadenie spĺňa všetky požiadavky smernice Európskej rady 93/42/EHS. •
Conformité Européenne (Europeisk standard). Denna symbol betyder att enheten
uppfyller alla krav i rådets direktiv 93/42/EEG. • Conformité Européenne (Avrupa
Normlarına Uygunluk). Bu sembol, cihazın 93/42/EEC sayılı Avrupa Konseyi Direktifi
ile tamamen uyumlu olduğu anlamına gelir.
4

1 Description
65 cm
(25.6 in)
16 cm
(6.3 in)
86 cm
(33.9 in)
The Medtronic FlexCath™ Select Steerable Sheath is a percutaneous catheter introducer fitted
with a valve to allow for introduction, withdrawal, and exchange of catheters and wires while
minimizing blood loss. A side port with stopcock is integrated to allow continuous drip infusion,
injection through the center lumen, flushing, aspiration, blood sampling, and pressure monitoring.
Figure 1. FlexCath Select Steerable Sheath
A dilator is packaged with the FlexCath Select Steerable Sheath. The sheath is described in the
following table:
Model
990065 3.3 mm (10 Fr)
The sheath can be deflected to provide additional maneuverability to catheters that are advanced
through the sheath and into the right or left chamber of the heart.
The 10 Fr FlexCath Select Steerable Sheath can be used with Medtronic diagnostic and ablation
catheter sizes up to 9 Fr.
The 10 Fr FlexCath Select Steerable Sheath dilator is compatible with 89 cm and longer Merit
Medical HeartSpan Transseptal Needles.
Inner diameter Outer diameter Usable length
(0.13 in)
4.3 mm (13 Fr) (0.17 in) 65 cm (25.6 in)
1.1 Contents of package
The FlexCath Select Steerable Sheath is supplied sterile. The package contains the following
items:
• 1 steerable sheath
• 1 dilator
• Product documentation
2 Indications for use
The FlexCath Select Steerable Sheath is intended for percutaneous catheter introduction into the
vasculature and into the chambers of the heart, including the left side of the heart through the
interatrial septum. The sheath deflection facilitates catheter positioning.
3 Contraindications
The FlexCath Select Steerable Sheath is contraindicated for placement in the left atrium or
ventricle if any of the following conditions apply to the patient:
• The patient has an intra-atrial septal patch or occluder, or has had other surgical intervention
in or adjacent to the intra-atrial septum.
• The patient has a left atrial thrombus.
• The patient has known or suspected atrial myxoma.
4 Warnings and precautions
Ablation energy – When using the sheath in the presence of ablation energy, care must be taken
to ensure that all ablating elements are outside the sheath.
Air aspiration – Remove the guide wire from the sheath prior to aspirating and flushing the
sheath. This action minimizes the aspiration of air through the valve of the sheath.
Anticoagulation therapy – Administer appropriate levels of periprocedural anticoagulation
therapy for patients undergoing left-sided and transseptal cardiac procedures and for selected
patients undergoing right-sided procedures. To minimize bleeding and thrombotic complications,
administer periprocedural anticoagulation therapy according to the institution’s standards.
Back-Bleeding – Make sure the stopcock is in a closed position after flushing or aspiration to
prevent unintended back-bleeding through the side port.
Biohazard disposal – Discard all used devices and sterile components in accordance with
hospital procedures.
Contrast injection – Do not use a power injection system for injection of contrast solution into the
sheath.
Dilator twisting – Do not twist the dilator during or after snapping into the valve hub. Doing so may
cause misalignment of the dilator tip at the distal end with respect to the side port at the proximal
end.
Do not resterilize – Do not resterilize this device for purpose of reuse. Resterilization may
compromise the structural integrity of the device or create a risk of contamination from the device
that could result in patient injury, illness, or death.
Embolism risk – Introducing any catheter or sheath into the circulatory system entails the risk of
air embolism, which can occlude vessels and lead to tissue infarction with serious consequences.
Use of catheters smaller than 9 Fr with this device may have an increased risk of air embolism.
Always advance and withdraw components slowly and use flushing to minimize the vacuum
created and therefore minimize the risk of air embolism.
Expiration date – Check to verify that the sheath is within its expiration date. Do not use if the
product date has expired.
Femoral vein damage – Care should be taken to minimize damage to the femoral vein and
access site upon sheath insertion, manipulation, or withdrawal. Complications associated with
femoral vein catheterization include hematoma and thrombosis.
Fluoroscopy required for sheath placement – Use of fluoroscopy during sheath manipulation
and placement is strongly advised. Manipulating the sheath without fluoroscopy may result in
damage to cardiac and vascular structures.
For single use only – This device is intended only to be used once for a single patient. Do not
reuse, reprocess, or resterilize this device for purpose of reuse. Reuse, reprocessing, or
resterilization may compromise the structural integrity of the device or create a risk of
contamination of the device that could result in patient injury, illness, or death.
Frequent flushing – Regular flushing of the sheath is recommended:
• To prevent blood stagnation, clots, emboli, and serious patient injury.
• To prevent contrast solution from sticking inside the lumen after each contrast injection.
Handling and care – When handling the device:
• Use extreme care when manipulating the device. Lack of careful attention can result in injury
such as perforation, tamponade, induction of arrhythmia, or heart block.
• Do not use excessive force to advance or withdraw the device, especially if resistance is
encountered.
• Avoid positioning the device around the chordae tendineae, which increases the likelihood of
entrapment within the heart, and may necessitate surgical intervention or repair of injured
tissues.
• Do not use the sheath if it is kinked or damaged.
Left atrial access – Do not advance the dilator or sheath through the interatrial septum without
first confirming left atrial access to prevent advancing these components into an undesired
location.
5
English

Necessary hospital equipment – Keep external defibrillation equipment nearby for immediate
use during use of steerable sheath assembly.
Other catheters, devices or wires – Avoid sheath entanglement with other catheters, devices
or wires. Such entanglement may necessitate surgical intervention.
Prosthetic heart valves – Do not pass the device through a prosthetic heart valve (mechanical
or tissue). The device may become trapped in the valve, damaging the valve and causing valvular
insufficiency or premature failure of the prosthetic valve.
Qualified users – This equipment should be used only by or under the supervision of physicians
trained in cardiac catheterization procedures.
Required use environment – Cardiac catheterization procedures should be performed only in
a fully equipped facility.
Side port aspiration – Aspirate the side port when withdrawing the dilator, catheter, needle,
wires or other devices.
Side port obstruction – Care should be taken to prevent any obstruction of the side port to
ensure that a saline flush is effective.
Significant blood leakage – Care should be taken to observe that there is not significant blood
leakage through the hemostatic valve during the procedure.
Sterile package inspection – Inspect the sterile packaging and device prior to use. If the sterile
packaging or the device exhibits damage, do not use the device. Contact your local Medtronic
representative.
X-ray and fluoroscopic exposure – The use of fluoroscopy during catheter ablation procedures
presents the potential for significant x-ray exposure to both patients and laboratory staff.
Extensive exposure can result in acute radiation injury and increased risk for somatic and genetic
effects. Only perform catheter ablation after giving adequate attention to the potential radiation
exposure associated with the procedure, and taking steps to minimize this exposure. Give careful
consideration and avoid x-ray exposure before using the device in pregnant women.
5 Adverse events
Potential adverse events associated with cannulation of the peripheral vasculature and
intracardiac placement of the sheath and dilator may include, but are not limited to, the following
conditions:
• Access site complications (hematoma,
infection, thrombosis, ecchymosis, AV fistula, bleeding from puncture site, hemorrhage)
• Air embolism
• Arrhythmia (atrial fibrillation, atrial flutter,
ventricular tachycardia)
• Cardiac arrest
• Chest discomfort, pain or pressure
• Coronary artery spasm, dissection, thrombosis
• Death
• Endocarditis
• Heart block, requiring permanent pacemaker
• Hemothorax
• Myocardial infarction
• Perforation of cardiac or surrounding tissue
• Pericardial effusion, tamponade
• Pericarditis
• Pleural effusion
• Pneumothorax
• Pseudoaneurysm
• Pulmonary edema
• Pulmonary embolism
• Stroke
• Thrombus
• Transient ischemic attack (TIA)
• Vasovagal reaction
6 Instructions for use
Note: Before introducing the sheath into the patient, test the deflection mechanism to ensure that
it is operational.
1. Using an aseptic technique, create a vascular access with an appropriate introducer.
2. Insert a compatible guide wire (see Specifications) through the vasculature and into the
desired position using standard vascular access techniques.
3. Flush the sheath side port and dilator lumen with sterile saline solution.
4. Ensure that the sheath is in a neutral (non-deflected) position and wet the dilator shaft with
sterile saline solution before inserting it through the hemostasis valve.
5. Begin assembling the dilator and sheath together by introducing the distal tip of the dilator
into the hemostasis valve so that the curved edge of the dilator is perpendicular to the
hemostasis valve (see Figure 2).
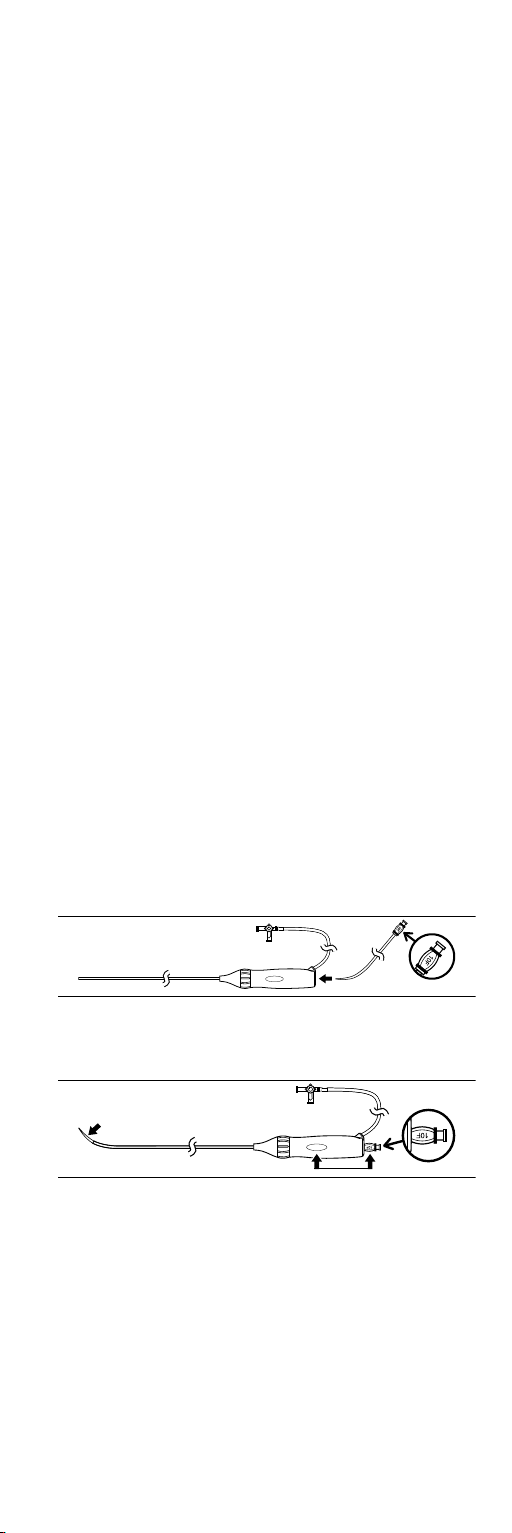
Figure 2. FlexCath Select Steerable Sheath
6. Continue advancing the dilator into the sheath until the dilator hub positively snaps into the
sheath hub.
Note: The label on the dilator hub should be in line with the label on the sheath handle so that
the curve of the dilator is aligned in the same orientation of the sheath deflection direction,
and side port (see Figure 3).
Figure 3. FlexCath Select Steerable Sheath
7. Thread the sheath dilator assembly over the guide wire and into the vasculature using a slight
twisting motion into the SVC.
8. Remove the guide wire.
9. Insert the properly prepared transseptal needle into the sheath dilator assembly so that the
curvature indicator on the transseptal needle is aligned with the side port.
Note: The transseptal needle should be used together with a stylet to prevent skiving of the
inner lumen of the dilator.
10. Pull the assembly down to the right atrium to prepare for the transseptal puncture.
11. Under fluoroscopic guidance, perform the transseptal puncture using pressure
measurements, contrast injection, or both. Confirm correct placement in the left atrium.
12. Pull the transseptal needle into the dilator and slowly remove the dilator and needle
assembly from the sheath.
Note: Remove the dilator slowly to reduce the possibility of creating a vacuum in the sheath.
Blood should aspirate freely through the side port. If not, withdraw the sheath because the
sheath tip may be resting against the wall of the atrium or a pulmonary vein.
13. Aspirate blood through the side port and be sure that the sheath is clear of air. Perform
aspiration or spontaneous bleed back before inserting a catheter into the sheath.
Note: Perform this step after all catheter exchanges.
14. After access with the sheath is achieved, maintain anticoagulation therapy.
15. Prepare the catheter according to the instructions for use from the manufacturer.
16. Insert the catheter and position the sheath.
English
6

Notes:
• Wetting the catheter shaft may help with ease of insertion.
• The hemostasis valve has a positive stop to prevent any capture devices from opening
the seal.
• To minimize the vacuum created, always insert and withdraw components slowly.
• The sheath should also be flushed while a catheter is inserted.
17. Before the sheath is withdrawn, ensure that it is in neutral (non-deflected) position.
7 Specifications
Overall length
Usable length 65 cm (25.6 in)
Inner diameter 3.3 mm (10 Fr) (0.13 in)
Outer diameter 4.3 mm (13 Fr) (0.17 in)
Dilator length 86 cm (33.9 in)
Radiopaque marker 5 mm (0.2 in) proximal to sheath tip
Guide wire compatibility 0.81 mm (0.032 in) to 0.89 mm (0.035 in)
Transseptal needle compatibil-
ity
Environmental parameters
Recommended transit temperature
Recommended storage temperature
Operation 15°C to 30°C (59°F to 86°F) at altitudes less than 2400 m
81 cm (31.9 in)
89 cm (35.0 in) or longer
−35°C to 58°C (−31°F to 136°F); 85% relative humidity
(non-condensing)
Average of 22°C (72°F) with a standard deviation of 2.7°C
(4.86°F) and actionable control limits of 15°C to 30°C (59°F to
86°F)
(8000 feet) above sea level
8 Medtronic disclaimer of warranty
For complete warranty information, see the accompanying disclaimer of warranty document.
9 Service
Medtronic employs highly trained representatives and engineers located throughout the world to
serve you and, upon request, to provide training to qualified hospital personnel in the use of
Medtronic products. Medtronic also maintains a professional staff to provide technical
consultation to product users. For more information, contact your local Medtronic representative,
or call or write Medtronic at the appropriate telephone number or address listed on the back cover.
7
English

1 Popis
65 cm
(25,6 in)
16 cm
(6,3 in)
86 cm
(33,9 in)
Řiditelné pouzdro Medtronic FlexCath™ Select je perkutánní zavaděč katétrů opatřený ventilem,
který umožňuje zavádění, vytahování a výměnu katétrů a drátů při minimalizaci krevních ztrát.
Zabudovaný boční port s uzavíracím kohoutem umožňuje podání kontinuální kapénkové infuze,
vstřikování přes středové lumen, proplachování, aspiraci, odebírání vzorků krve a monitorování
tlaku.
Obrázek 1. Řiditelné pouzdro FlexCath Select
K řiditelnému pouzdru FlexCath Select je přibalen dilatátor. Popis pouzdra uvádí následující
tabulka:
Model
990065 3,3 mm (10 Fr)
Pouzdro lze ohnout tak, aby poskytovalo další možnosti manévrování s katétry zasunovanými
skrz toto pouzdro a do pravé nebo levé srdeční dutiny.
Řiditelné pouzdro FlexCath Select o velikosti 10 Fr lze použít s diagnostickými a ablačními katétry
společnosti Medtronic o velikostech do 9 Fr.
Dilatátor řiditelného pouzdra FlexCath Select o velikosti 10 Fr je kompatibilní s transseptálními
jehlami Merit Medical HeartSpan o délce 89 cm a delšími.
Vnitřní průměr Vnější průměr Využitelná délka
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Obsah balení
Řiditelné pouzdro FlexCath Select je dodáváno sterilní. Balení obsahuje následující položky:
• 1 řiditelné pouzdro,
• 1 dilatátor,
• průvodní dokumentaci.
2 Indikace k použití
Řiditelné pouzdro FlexCath Select je určeno k perkutánnímu zavedení katétru do cévního
systému a do srdečních dutin (včetně zavedení do levé strany srdce přes mezisíňové septum).
Ohnutí pouzdra usnadňuje umístění katétru.
3 Kontraindikace
Umístění řiditelného pouzdra FlexCath Select do levé síně či komory je kontraindikováno za
jakéhokoli z následujících stavů pacienta:
• Pacient má záplatu nebo okludor mezisíňového septa nebo podstoupil jiný chirurgický zákrok
v oblasti mezisíňového septa nebo v jeho sousedství.
• Pacient má trombus v levé síni.
• Pacient má diagnostikován myxom síně nebo podezření na něj.
4 Varování a bezpečnostní opatření
Ablační energie – Při používání pouzdra v místech, kam se aplikuje ablační energie, je nutno
zajistit, aby se všechny ablační elementy nalézaly mimo pouzdro.
Aspirace vzduchu – Před aspirací a propláchnutím pouzdra vyjměte z pouzdra vodicí drát. Tímto
opatřením se minimalizuje aspirace vzduchu skrz ventil pouzdra.
Antikoagulační léčba – U pacientů, kteří podstoupí levostranné a transseptální kardiologické
zákroky a u vybraných pacientů, kteří podstoupí pravostranné zákroky, je třeba v období kolem
zákroku dosáhnout vhodné hladiny antikoagulační léčby. Antikoagulační léčbu v období kolem
zákroku podávejte podle standardů platných ve vaší nemocnici tak, aby se minimalizovalo
krvácení a trombotické komplikace.
Zpětné krvácení – Po proplachování nebo aspiraci zařízení se ujistěte, že je uzavírací kohout
v uzavřené poloze, abyste zabránili nechtěnému zpětnému krvácení přes boční port.
Likvidace biologicky nebezpečných materiálů – Všechna použitá zařízení a sterilní
komponenty zlikvidujte v souladu s platnými nemocničními postupy.
Injekce kontrastní látky – Ke vstřikování kontrastního roztoku do pouzdra nepoužívejte tlakový
injekční systém.
Kroucení dilatátorem – Nekruťte s dilatátorem během zasouvání nebo po zaklapnutí do ústí
ventilu. Mohlo by dojít k chybnému vyrovnání špičky dilatátoru na distálním konci vzhledem
k bočnímu portu na proximálním konci.
Neprovádějte resterilizaci – Tento nástroj nesmí být resterilizován za účelem opakovaného
použití. Resterilizace může ohrozit strukturální integritu nástroje nebo způsobit riziko
kontaminace způsobené nástrojem, což by mohlo mít za následek poranění, onemocnění nebo
smrt pacienta.
Riziko embolie – Zavedení jakéhokoli katétru či pouzdra do oběhové soustavy představuje riziko
vzduchové embolie, která může způsobit uzávěr cév a vést ke tkáňovému infarktu se závažnými
následky. Použití katétrů menších než 9 Fr s tímto zařízením může vést ke zvýšenému riziku
vzduchové embolie. Součásti vždy zasunujte a vytahujte pomalu a provádějte proplachování, aby
se minimalizoval vytvořený podtlak a tím také riziko vzduchové embolie.
Datum exspirace – Zkontrolujte, zda neuplynulo datum exspirace pouzdra. Nepoužívejte
produkt po uplynutí data jeho exspirace.
Poškození femorální žíly – Postupujte opatrně, abyste minimalizovali poškození femorální žíly
a místa vstupu při zavádění pouzdra, manipulaci s ním nebo jeho vytahování. Mezi komplikace
související s katetrizací femorální žíly patří hematom a trombóza.
Nutnost fluoroskopické kontroly umístění pouzdra – Důrazně doporučujeme sledovat
manipulaci s pouzdrem a jeho umístění pomocí fluoroskopie. Manipulace s pouzdrem bez
fluoroskopické kontroly může mít za následek poškození srdečních a cévních struktur.
Pouze k jednorázovému použití – Tento nástroj je určen výhradně k použití u jediného pacienta.
Nepoužívejte nástroj opakovaně, nerenovujte ani neresterilizujte za účelem opakovaného použití.
Opakované použití, renovace nebo resterilizace mohou ohrozit strukturální integritu nástroje nebo
vytvořit riziko kontaminace nástroje, což by mohlo mít za následek poranění, onemocnění nebo
smrt pacienta.
Časté proplachování – Doporučuje se pravidelně proplachovat pouzdro:
• aby nedocházelo ke stagnaci krve, vzniku sraženin, embolizaci a závažným poraněním
pacienta;
• po každém vstříknutí kontrastní látky, abyste zabránili ulpění kontrastního roztoku uvnitř
lumen.
Pokyny k manipulaci a péče – Při manipulaci se zařízením:
• Při manipulaci s tímto nástrojem postupujte velmi opatrně. Při nedostatku pozornosti a
pečlivosti může dojít k poranění, například k perforaci, tamponádě, indukci arytmie nebo
srdeční blokádě.
• Při zasunování nebo vytahování nástroje nepoužívejte nadměrnou sílu, zejména pocítíte-li
odpor.
Česky
8

• Zabraňte obtočení nástroje kolem chordae tendineae, které zvyšuje pravděpodobnost
zachycení nástroje v srdci s následnou nutností chirurgického zákroku nebo chirurgické
reparace poraněných tkání.
• Nepoužívejte pouzdro, pokud je zkroucené nebo poškozené.
Přístup do levé síně – Nezavádějte dilatátor ani pouzdro přes mezisíňovou přepážku, dokud
nepotvrdíte přístup do levé síně, aby nedošlo k zavedení těchto komponent na nežádoucí místo.
Potřebné nemocniční vybavení – Mějte k dispozici na dosah zařízení pro externí defibrilaci,
které by bylo možné při práci s řiditelným pouzdrem okamžitě použít.
Jiné katétry, zařízení nebo drátěné nástroje – Zabraňte zapletení pouzdra s jinými katétry,
zařízeními nebo drátěnými nástroji. Důsledkem může být nutnost provedení chirurgického
zákroku.
Náhrady srdečních chlopní – Neprotahujte nástroj náhradou srdeční chlopně (mechanickou
ani tkáňovou). Mohlo by dojít k zachycení nástroje v chlopni, poškození chlopně a následně
k insuficienci nebo předčasnému selhání náhrady chlopně.
Kvalifikovaní uživatelé – Tento nástroj smí být používán pouze lékařem vyškoleným k provádění
srdeční katetrizace nebo pod dohledem takového lékaře.
Prostředí vyžadované pro použití – Srdeční katetrizaci lze provádět pouze v plně vybaveném
zdravotnickém zařízení.
Aspirace přes boční port – Při vytahování dilatátoru, katétru, jehly, drátů nebo jiných zařízení
aspirujte přes boční port.
Ucpání bočního portu – Dávejte pozor, aby nedošlo k obstrukci bočního portu a tak bylo
zajištěno účinné proplachování fyziologickým roztokem.
Významný únik krve – Pečlivě sledujte, zda během zákroku nedochází k významnému úniku
krve hemostatickým ventilem.
Kontrola sterilního balení – Před použitím prohlédněte sterilní balení a nástroj. Pokud je sterilní
obal nebo nástroj poškozen, nástroj nepoužívejte. Kontaktujte místního zástupce společnosti
Medtronic.
Expozice při rentgenování a fluoroskopii – Při použití fluoroskopie během postupů
katetrizační ablace může dojít k významné expozici rentgenovému záření u pacientů i
u laboratorních zaměstnanců. Důsledkem rozsáhlé expozice může být akutní poškození zdraví
radiací a rovněž zvýšené nebezpečí somatických a genetických účinků. Katetrizační ablaci lze
provádět pouze po náležitém zvážení možnosti expozice účinkům radiace v souvislosti
s postupem a podniknutí kroků pro minimalizaci této expozice. Použití tohoto zařízení u těhotných
žen pečlivě zvažte; těhotné ženy nevystavujte působení rentgenového záření.
5 Nežádoucí účinky
Mezi možné nežádoucí účinky související s kanylací periferních cév a intrakardiálním zaváděním
pouzdra a dilatátoru patří mimo jiné následující stavy:
• komplikace v místě přístupu (hematom,
infekce, trombóza, ekchymóza, AV píštěl,
krvácení z místa punkce, rozsáhlé krvácení),
• vzduchová embolie,
• arytmie (fibrilace síní, síňový flutter,
komorová tachykardie),
• srdeční zástava,
• tíseň, bolest nebo tlak na hrudníku,
• spasmus, disekce, trombóza koronárních
tepen,
• smrt,
• endokarditida,
• srdeční blok, vyžadující trvalou kardiostimulaci,
• hemotorax,
• infarkt myokardu,
• perforace srdeční nebo okolní tkáně,
• perikardiální efúze, tamponáda,
• perikarditida,
• pleurální efúze,
• pneumotorax,
• pseudoaneuryzma,
• plicní edém,
• plicní embolie,
• cévní mozková příhoda,
• trombus,
• tranzientní ischemická ataka (TIA),
• vazovagální reakce.
6 Návod k použití
Poznámka: Před zavedením pouzdra do těla pacienta vyzkoušejte ohýbací mechanismus,
abyste se ujistili, že funguje.
1. S použitím aseptické techniky vytvořte cévní přístup pomocí vhodného zavaděče.
2. Zaveďte kompatibilní vodicí drát (viz Specifikace) do cévního systému a do požadovaného
místa pomocí standardní techniky pro zavádění z cévního přístupu.
3. Propláchněte boční port pouzdra a lumen dilatátoru sterilním fyziologickým roztokem.
4. Ujistěte se, že je pouzdro v neutrální pozici (není vychýlené), a před zasunutím skrz
hemostatický ventil navlhčete tělo dilatátoru sterilním fyziologickým roztokem.
5. Začněte sestavovat dilatátor a pouzdro. Nejprve zasuňte distální hrot dilatátoru do
hemostatického ventilu tak, aby byl zakřivený okraj dilatátoru kolmý k hemostatickému
ventilu (viz Obrázek 2).
Obrázek 2. Řiditelné pouzdro FlexCath Select
6. Dilatátor posunujte dále do pouzdra, až ústí dilatátoru spolehlivě zapadne do ústí pouzdra.
Poznámka: Štítek na ústí dilatátoru by měl být v yrovnán se štítkem na rukojeti pouzdra tak,
aby byla orientace zakřivené části dilatátoru stejná jako směr ohýbání pouzdra, a s bočním
portem (viz Obrázek 3).
Obrázek 3. Řiditelné pouzdro FlexCath Select
7. Zasunujte sestavu dilatátoru a pouzdra po vodicím drátu do cévního systému a do horní duté
žíly mírně kroutivým pohybem.
8. Vyjměte vodicí drát.
9. Zaveďte správným způsobem připravenou transseptální jehlu do sestav y dilatátoru a
pouzdra tak, aby byl ukazatel zakřivení na transseptální jehle vyrovnán s bočním portem.
Poznámka: Transseptální jehla se musí používat společně se styletem, aby se zabránilo
seříznutí vnitřního lumen dilatátoru.
10. Pro přípravu k transseptální punkci stáhněte sestavu dolů do pravé síně.
11. Proveďte transseptální punkci pod fluoroskopickým naváděním; přitom použijte měření
tlaku, nástřik kontrastní látky nebo obojí. Potvrďte správné umístění systému v levé síni.
12. Vtáhněte transseptální jehlu do dilatátoru a pomalu vytahujte sestavu dilatátoru a jehly
z pouzdra.
Poznámka: Vytahujte dilatátor pomalu, abyste snížili riziko vytvoření vakua v pouzdře. Krev
by měla volně aspirovat přes boční port. Pokud tomu tak není, povytáhněte pouzdro, protože
se hrot pouzdra může opírat o stěnu síně nebo plicní žílu.
9
Česky

13. Aspirujte krev z bočního portu a ujistěte se, že v pouzdře není žádný vzduch. Před zasunutím
katétru do pouzdra proveďte aspiraci nebo umožněte spontánní zpětné vytékání krve.
Poznámka: Tento krok proveďte po každé výměně katétru.
14. Po zajištění přístupu pomocí pouzdra pokračujte v antikoagulační terapii.
15. Připravte katétr podle návodu k použití od výrobce.
16. Zasuňte katétr a umístěte pouzdro.
Poznámky:
• Navlhčení těla katétru může usnadnit zavádění.
• Hemostatický ventil má pozitivní zarážku, která zabrání, aby zachycená zařízení porušila
těsnění.
• Součásti vždy zasunujte a vytahujte pomalu, abyste minimalizovali vytvořený podtlak.
• Pouzdro by se mělo rovněž proplachovat se zasunutým katétrem.
17. Před vytažením pouzdra se ujistěte, že je v neutrální poloze (není ohnuté).
7 Specifikace
Celková délka
Využitelná délka 65 cm (25,6 in)
Vnitřní průměr 3,3 mm (10 Fr) (0,13 in)
Vnější průměr 4,3 mm (13 Fr) (0,17 in)
Délka dilatátoru 86 cm (33,9 in)
Rentgenkontrastní značka 5 mm (0,2 in) proximálně od hrotu pouzdra
Kompatibilita vodicího drátu 0,81 mm (0,032 in) až 0,89 mm (0,035 in)
Kompatibilita transseptální jehly 89 cm (35,0 in) nebo delší
Parametry prostředí
Doporučená teplota při přepravě
Doporučená teplota skladování
Použití 15°C až 30°C (59°F až 86°F) v nadmořských výškách nižších
81 cm (31,9 in)
−35°C až 58°C (−31°F až 136°F); 85% relativní vlhkost
(nekondenzující)
Průměrná teplota 22°C (72°F) se standardní odchylkou 2,7°C
(4,86°F), u teplot nižších než 15°C (59°F) a vyšších než 30°C
(86°F) je zapotřebí provést protiopatření
než 2400 m (8000 stop) nad mořem
8 Odmítnutí záruky společnosti Medtronic
Úplné informace o záruce naleznete v přiloženém prohlášení o odmítnutí záruky.
9 Servis
Společnost Medtronic zaměstnává vysoce vyškolené zástupce a techniky z celého světa, kteří
jsou připraveni vám pomoci a na základě žádosti poskytnout kvalifikovanému nemocničnímu
personálu školení týkající se používání produktů společnosti Medtronic. Společnost Medtronic
má také k dispozici profesionální pracovníky, kteří uživatelům produktů poskytují odborné
konzultace. Další informace získáte od místního zástupce společnosti Medtronic, nebo můžete
telefonicky či písemně kontaktovat společnost Medtronic na adrese nebo telefonním čísle, které
jsou uvedeny na zadní straně obalu.
Česky
10

1 Beskrivelse
65 cm
(25,6 in)
16 cm
(6,3 in)
86 cm
(33,9 in)
FlexCath™ Select styrbar sheath fra Medtronic er en perkutan kateterindfører med en ventil, der
giver mulighed for indføring, tilbagetrækning og ombytning af katetre og wirer med minimalt
blodtab. En integreret sideport med stophane giver mulighed for kontinuerligt drop, injektion
gennem det centrale lumen, skylning, aspiration, blodprøvetagning og trykmonitorering.
Figur 1. FlexCath Select styrbar sheath
En dilatator leveres sammen med FlexCath Select styrbar sheath. Sheathen er beskrevet i
følgende tabel:
Model
990065 3,3 mm (10 Fr)
Sheathen kan bøjes, så det giver ekstra mulighed for at manøvrere katetrene, som skal føres frem
gennem sheathen og ind i det højre eller venstre hjertekammer.
10 Fr FlexCath Select styrbar sheath kan bruges sammen med Medtronic diagnostiske katetre og
ablationskatetre i størrelser op til 9 Fr.
Dilatatoren til 10 Fr FlexCath Select styrbar sheath er kompatibel med Merit Medical HeartSpan
transseptale kanyler på 89 cm og længere.
Indvendig diameter Udvendig diameter Arbejdslængde
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Pakkens indhold
FlexCath Select styrbar sheath leveres steril. Pakken indeholder følgende:
• 1 styrbar sheath
• 1 dilatator
• Produktdokumentation
2 Indikationer for anvendelse
FlexCath Select styrbar sheath er beregnet til perkutan kateterindføring i venesystemet og
hjertekamrene, herunder venstre side af hjertet via septum interatriale. Bøjeligheden af vores
sheath gør det nemmere at placere kateteret.
3 Kontraindikationer
FlexCath Select styrbar sheath er kontraindiceret til anbringelse i venstre atrium eller
ventrikel, hvis en af følgende tilstande gælder for patienten:
• Patienten har en patch eller okkluder i septum interatriale eller har fået foretaget et andet
kirurgisk indgreb i eller grænsende op til septum interatriale.
• Patienten har en trombe i venstre atrium.
• Patienten har kendt eller mistænkt atrialt myksom.
4 Advarsler og forholdsregler
Ablationsenergi – Når sheathen anvendes ved tilstedeværelse af ablationsenergi, skal der
udvises omhu for at sikre, at alle ablationselementer er uden for sheathen.
Luftaspiration – Fjern guidewiren fra sheathen, inden sheathen aspireres og skylles. Dette
minimerer aspiration af luft gennem sheathens ventil.
Antikoagulationsbehandling – Anvend passende perioperativ antikoagulationsbehandling til
patienter, der får foretaget venstresidige og transseptale procedurer og til udvalgte patienter, der
får foretaget højresidige procedurer. Administrer antikoagulationsbehandling under proceduren i
henhold til institutionens standarder for at minimere komplikationer som blødning og trombose.
Tilbageløb af blod – Sørg for, at stophanen er lukket efter gennemskylning eller aspiration, så
der ikke utilsigtet løber blod tilbage gennem sideporten.
Klinisk risikoaffald – Alle brugte enheder og sterile komponenter skal kasseres i
overensstemmelse med hospitalets procedurer.
Injektion af kontrast – Der må ikke anvendes en kraftig injektionssprøjte til injektion af
kontrastvæske i sheathen.
Vridning af dilatatoren – Dilatatoren må ikke vrides under eller efter, at den klikkes ind i
ventilmuffen. Hvis dette gøres, kan dilatatorspidsen komme til at sidde skævt i den distale ende
i forhold til sideporten i den proksimale ende.
Må ikke resteriliseres – Denne enhed må ikke resteriliseres med henblik på genbrug.
Resterilisering kan ødelægge kateterets struktur og funktion eller skabe risiko for kontaminering
af kateteret, hvilket kan føre til personskade, sygdom eller død for patienten.
Risiko for emboli – Indføring af enhver type kateter eller sheath i kredsløbssystemet medfører
risiko for luftemboli, der kan tilstoppe blodkar og føre til vævsinfarkt med alvorlige konsekvenser
til følge. Hvis der bruges katetre, der er mindre end 9 Fr, sammen med denne enhed, kan det øge
risikoen for luftemboli. Før altid komponenter langsomt frem og tilbage, og brug skylning for at
minimere det vakuum, der dannes. Dermed reduceres risikoen for luftemboli.
Udløbsdato – Kontrollér, at sheathen ikke har overskredet udløbsdatoen. Må ikke anvendes, hvis
udløbsdatoen er overskredet.
Beskadigelse af vena femoralis – Der bør udvises forsigtighed for at reducere beskadigelse af
vena femoralis og indføringsstedet ved indføring, manipulering og tilbagetrækning af sheathen.
Komplikationer forbundet med indføringen af kateter i vena femoralis omfatter hæmatom og
trombose.
Fluoroskopi påkrævet til anbringelse af sheath – Det anbefales på det kraftigste at anvende
fluoroskopi ved håndtering og anbringelse af en sheath. Håndtering af en sheath uden fluoroskopi
kan føre til skader på hjerte- og karstrukturer.
Kun til engangsbrug – Denne enhed er kun beregnet til engangsbrug på en enkelt patient.
Denne enhed må ikke genbruges, genbehandles eller resteriliseres med henblik på genbrug.
Genanvendelse, genbehandling eller resterilisering kan ødelægge kateterets struktur og funktion
eller skabe risiko for kontaminering af kateteret, hvilket kan føre til personskade, sygdom eller død
for patienten.
Regelmæssig skylning – Regelmæssig skylning af sheathen anbefales:
• For at undgå blodstagnation, koagel, emboli og alvorlig patientskade.
• For at undgå at kontrastvæske klæber fast til indersiden af lumen efter hver injektion af
kontrastvæske.
Håndtering og pleje – Ved håndtering af enheden:
• Udvis stor forsigtighed, når kateteret manøvreres. Manglende omhu og koncentration kan
resultere i kliniske komplikationer såsom perforering, tamponade, inducering af arytmi eller
hjerteblok.
• Brug ikke for mange kræfter ved indføring og tilbagetrækning af kateteret – især hvis der
mødes modstand.
• Undgå at placere kateteret omkring chordae tendineae, hvilket øger risikoen for, at kateteret
kan sætte sig fast i hjertet, og kan nødvendiggøre kirurgisk indgreb eller reparation af
beskadiget væv.
• Kateteret må ikke anvendes, hvis det er kinket eller beskadiget.
Venstre atriel adgang – For at forhindre at dilatatoren eller sheathen føres ind et uønsket sted,
må de ikke føres frem gennem septum interatriale uden først at bekræfte adgang til venstre atrium.
11
Dansk
Nødvendigt hospitalsudstyr – Eksternt defibrilleringsudstyr skal være klar til øjeblikkelig brug,
når den styrbare sheathenhed anvendes.
Andre katetre, enheder eller wirer – Sørg for, at sheathen ikke vikles ind i andre katetre,
enheder eller wirer. En sådan sammenvikling kan gøre kirurgisk indgreb nødvendigt.
Hjerteklapproteser – Før ikke kateteret gennem en hjerteklapprotese (mekanisk eller væv).
Kateteret kan sætte sig fast i klappen, beskadige klappen og forårsage klapinsufficiens eller fejl
i klapprotesen.
Kvalificerede brugere – Dette udstyr bør kun anvendes af eller under overvågning af læger, som
er uddannet i procedurerer for indføring af katetre i hjertet.
Påkrævet klinisk miljø – Der må kun udføres kardiale kateteriseringsprocedurer på en fuldt
udstyret klinik.
Aspiration af sideport – Aspirer sideporten, når dilatator, kateter, kanyle, wirer eller andre
enheder trækkes tilbage.
Tilstoppet sideport – Man skal være omhyggelig med at undgå enhver tilstopning af sideporten
for at sikre, at en gennemskylning med saltvand er effektiv.
Betydelig blødning – Det bør omhyggeligt sikres, at der ikke kan konstateres betydelig blødning
gennem hæmostaseventilen under proceduren.
Kontrol af steril emballage – Kontroller den sterile emballage og udstyret inden brug. Hvis den
sterile emballage eller udstyret er beskadiget, må udstyret ikke tages i brug. Kontakt den lokale
Medtronic-repræsentant.
Udsættelse for røntgen og fluoroskopi – Anvendelse af fluoroskopi under
kateterablationsprocedurer udgør en signifikant risiko for røntgenstrålebelastning af både
patienter og laboratoriepersonale. Omfattende belastning kan medføre akut strålingsskade og
forøget risiko for somatiske og genetiske følgevirkninger. Kateterablation må først foretages, når
den potentielle strålebelastning, der er forbundet med proceduren, er taget i betragtning, og når
der er truffet foranstaltninger for at reducere denne belastning. Foretag grundig overvejelse, og
undgå anvendelse af røntgen før brug af udstyret til gravide kvinder.
5 Komplikationer
Mulige komplikationer relateret til kanylering i den perifere vaskulatur og intrakardial placering af
sheathen og dilatatoren indbefatter, men er ikke begrænset til, følgende hændelser:
• Komplikationer ved adgangsstedet
(hæmatom, infektion, trombose, ekkymose, AV-fistel, blødning ved punkturstedet, hæmorragi)
• Luftemboli
• Arytmi (atrieflimren, atrieflagren, ventrikulær takykardi)
• Hjertestop
• Ubehag, smerter eller trykken i brystet
• Sammentrækning af koronararterie, dissektion, trombose
• Død
• Endocarditis
• Hjerteblok, der kræver permanent pacemaker
• Hæmothorax
• Myokardieinfarkt
• Perforering af hjerte- eller omgivende væv
• Perikardialt ekssudat, tamponade
• Pericarditis
• Pleural effusion
• Pneumothorax
• Pseudoaneurysme
• Lungeødem
• Lungeemboli
• Apopleksi
• Trombe
• Transitorisk iskæmisk attak (TIA)
• Vasovagalt anfald
6 Brugsanvisning
Bemærk: Afprøv bøjningsmekanismen, inden sheathen føres ind i patienten, for at sikre at den
fungerer.
1. Brug aseptisk udstyr til at skabe adgang til karbanen med et passende indføringsudstyr.
2. Indfør en kompatibel guidewire (se Specifikationer) gennem venesystemet og ind i den
ønskede position ved brug af standardmæssige, vaskulære adgangsteknikker.
3. Skyl sheathens sidepor t og dilatatorens lumen med sterilt saltvand.
4. Sørg for, at sheathen er i neutral (ikke bøjet) position, og fugt dilatatorens skaft med sterilt
saltvand, inden den føres ind i hæmostaseventilen.
5. Begynd med at samle dilatatoren og sheathen ved at føre dilatatorens distale spids ind i
hæmostaseventilen, så dilatatorens buede kant er vinkelret i forhold til hæmostaseventilen
(se Figur 2).
Figur 2. FlexCath Select styrbar sheath
6. Fortsæt med at føre dilatatoren ind i sheathen, indtil muffen på dilatatoren klikker på plads i
sheathens muffe.
Bemærk: Mærkaten på dilatatorens muffe skal flugte med mærkaten på sheathens
håndtag, så dilatatorens krumning følger samme retning som sheathens bøjning og sideport
(se Figur 3).
Figur 3. FlexCath Select styrbar sheath
7. Sæt sheath/dilatator-enheden ind over guidewiren og ind i venesystemet ved at dreje den let
ind i SVC.
8. Fjern guidewiren.
9. Indfør den korrekt klargjorte transseptale kanyle i sheath/dilatator-enheden, så
krumningsindikatoren på den transseptale kanyle flugter med sideporten.
Bemærk: Den transseptale nål skal anvendes sammen med en stilet for at forhindre
skærfning af dilatatorens indvendige lumen.
10. Træk enheden ned til højre atrium som forberedelse til den transseptale punktur.
11. Udfør den transseptale punktur under fluoroskopi ved hjælp af trykmålinger, injektion af
kontrastvæske, eller begge dele. Bekræft korrekt placering i venstre atrium.
12. Træk den transseptale kanyle ind i dilatatoren, og træk langsomt dilatator/kanyle-enheden
ud af sheathen.
Bemærk: Tag dilatatoren langsomt ud for at nedsætte risikoen for dannelse af et undertr yk
i sheathen. Blodet skal aspirere frit gennem sideporten. Hvis dette ikke er tilfældet, skal
sheathen trækkes tilbage, da spidsen måske hviler mod atrievæggen eller en lungevene.
13. Aspirér blod gennem sideporten, og sørg for, at der ikke er luft i sheathen. Udfør aspiration
eller spontant tilbageløb, før kateteret indføres i sheathen.
Bemærk: Udfør dette trin efter alle kateterudskiftninger.
14. Når der er opnået adgang med sheathen, skal der fortsat ydes antikoagulationsbehandling.
15. Klargør kateteret i henhold til brugsanvisningen fra producenten.
16. Indfør kateteret, og anbring sheathen.
Dansk
12

Bemærkninger:
• Det kan være nemmere at indføre kateteret, hvis det fugtes.
• Hæmostaseventilen har et positivt stop for at forhindre, at indfangningsanordninger
åbner forseglingen.
• Komponenterne skal altid indføres og udtrækkes langsomt for at minimere det vakuum,
der skabes.
• Sheathen bør også skylles, mens et kateter indføres.
17. Inden sheathen trækkes ud, skal det sikres, at den er i neutral (ikke bøjet) position.
7 Specifikationer
Samlet længde
Arbejdslængde 65 cm (25,6 in)
Indvendig diameter 3,3 mm (10 Fr) (0,13 in)
Udvendig diameter 4,3 mm (13 Fr) (0,17 in)
Dilatatorens længde 86 cm (33,9 in)
Røntgenmarkør 5 mm (0,2 in) proksimalt i forhold til sheathens spids
Guidewire-kompatibilitet 0,81 mm (0,032 in) til 0,89 mm (0,035 in)
Kompatibilitet for transseptal
nål
Miljømæssige parametre
Anbefalet temperatur under
transport
Anbefalet opbevaringstemperatur
Drift 15°C til 30°C (59°F til 86°F) ved højder under 2400 m (8000
81 cm (31,9 in)
89 cm (35,0 in) eller længere
−35°C til 58°C (−31°F til 136°F); 85% relativ luftfugtighed
(ikke-kondenserende)
Gennemsnit på 22°C (72°F) med en standardafvigelse på
2,7°C (4,86°F) og handlingsrettede kontrolgrænser på 15°C til
30°C (59°F til 86°F)
fod) over havets overflade
8 Medtronic ansvarsfraskrivelse
Der henvises til det medfølgende ansvarsfraskrivelsesdokument for detaljerede
garantioplysninger.
9 Service
Verden over beskæftiger Medtronic højtuddannede repræsentanter og teknikere, der står til
Deres rådighed, og som på anmodning oplærer uddannet hospitalspersonale i anvendelsen af
produkter fra Medtronic. Medtronic har en stab af professionelle medarbejdere, som tilbyder
teknisk rådgivning til brugere af produkterne. For yderligere oplysninger bedes De kontakte den
lokale Medtronic-repræsentant eller henvende Dem telefonisk eller skriftligt til Medtronic på det
relevante telefonnummer eller den relevante adresse, der står anført på omslagets bagside.
13
Dansk

1 Beschreibung
65 cm
(25,6 Zoll)
16 cm
(6,3 Zoll)
86 cm
(33,9 Zoll)
Die steuerbare Medtronic FlexCath™ Select Schleuse ist eine perkutane Kathetereinführhilfe,
die über ein Ventil verfügt. Dieses ermöglicht das Einführen, Zurückziehen und Wechseln von
Kathetern und Führungsdrähten und hält den Blutverlust minimal. Es ist ein Seitenanschluss mit
Absperrhahn integriert, der eine Dauertropfinfusion oder Injektion in das zentrale Lumen der
Schleuse sowie deren Spülung, die Aspiration von Flüssigkeit und die Entnahme von Blutproben
sowie eine Drucküberwachung ermöglicht.
Abbildung 1. Steuerbare FlexCath Select Schleuse
Zum Lieferumfang der steuerbaren FlexCath Select Schleuse gehört ein Dilatator. Die Schleuse
ist in der nachstehenden Tabelle beschrieben:
Modell
990065 3,3 mm (10 Fr)
Die Schleuse kann gebogen werden, um die Manövrierfähigkeit beim Vorschieben von Kathetern
zu verbessern, die über die Schleuse in die rechte oder linke Herzkammer eingeführt werden.
Die steuerbare 10 Fr FlexCath Select Schleuse kann zusammen mit Diagnose- und
Ablationskathetern von Medtronic in Größen bis zu 9 Fr verwendet werden.
Der Dilatator der steuerbaren FlexCath Select Schleuse von 10 Fr ist mit transseptalen Nadeln
von Merit Medical HeartSpan von mindestens 89 cm Länge kompatibel.
Innendurchmesser Außendurchmesser Nutzbare Länge
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Verpackungsinhalt
Die steuerbare FlexCath Select Schleuse wird steril geliefert. Die Verpackung enthält folgende
Komponenten:
• 1 steuerbare Schleuse
• 1 Dilatator
• Produktdokumentation
2 Indikationen
Die steuerbare FlexCath Select Schleuse ist zur perkutanen Einführung von Kathetern in das
Gefäßsystem und in die Herzkammern vorgesehen, u. a. auch über das Vorhofseptum in die linke
Herzhälfte. Die Biegbarkeit der Schleuse erleichtert die Positionierung des Katheters.
3 Kontraindikationen
Die steuerbare FlexCath Select Schleuse ist für die Positionierung im linken Atrium oder Ventrikel
kontraindiziert, wenn eine der folgenden Bedingungen auf den Patienten zutrifft:
• Wenn sich der Patient einem Patch- oder Okkluder-Verschluss des Vorhofseptums oder
einem sonstigen chirurgischen Eingriff im Bereich des Vorhofseptums unterzogen hat.
• Wenn der Patient einen linksatrialen Thrombus hat.
• Bei Patienten mit nachgewiesenem oder vermutetem Vorhofmyxom.
4 Warnungen und Vorsichtsmaßnahmen
Ablationsenergie – Wenn die Schleuse während der Anwendung von Ablationsenergie
verwendet wird, ist darauf zu achten, dass sich alle Ablationselemente außerhalb der Schleuse
befinden.
Luftaspiration – Vor dem Aspirieren und Spülen den Führungsdraht aus der Schleuse entfernen.
Dadurch wird die Luftaspiration durch das Schleusenventil minimiert.
Therapie mit Antikoagulanzien – Während linksseitiger oder transseptaler Prozeduren am
Herzen immer eine Antikoagulationstherapie in geeigneter Dosis durchführen; während
rechtsseitiger Prozeduren eine Antikoagulationstherapie vom jeweiligen Patienten abhängig
machen. Zur Vermeidung von Blutungen und thrombotischen Komplikationen während des
Verfahrens die Antikoagulationstherapie gemäß den Richtlinien der medizinischen Einrichtung
durchführen.
Rückentlüftung – Achten Sie darauf, dass der Absperrhahn nach dem Spülen oder Aspirieren
geschlossen wird, um eine unerwünschte Rückentlüftung durch den Seitenanschluss zu
vermeiden.
Entsorgung von biologischem Gefahrgut – Alle gebrauchten Produkte und sterilen
Komponenten den Vorschriften des Krankenhauses entsprechend entsorgen.
Kontrastmittelinjektion – Kein automatisches Injektionssystem für die Injektion von
Kontrastmittellösung in die Schleuse verwenden.
Verdrehen des Dilatators – Drehen Sie den Dilatator nicht während oder nach dem Einrasten in
den Ventilanschluss. Dies kann zu einer Fehlausrichtung der Dilatatorspitze am distalen Ende
gegenüber dem Seitenanschluss am proximalen Ende führen.
Nicht resterilisieren – Dieses Produkt darf nicht zum Zwecke der Wiederverwendung
resterilisiert werden. Durch eine Resterilisierung kann die strukturelle Integrität des Produkts
beeinträchtigt werden und eine Kontamination des Produkts entstehen, die zu Verletzungen, zur
Erkrankung oder zum Tod des Patienten führen kann.
Emboliegefahr – Das Einführen eines Katheters oder einer Schleuse in das Kreislaufsystem
birgt das Risiko einer Luftembolie, die zu Gefäßverschlüssen und zu Gewebeinfarkten mit
schwerwiegenden Folgen führen kann. Die Ver wendung dieses Geräts mit Kathetern mit weniger
als 9 Fr kann ein erhöhtes Risiko für Luftembolien zur Folge haben. Die Komponenten langsam
vorschieben und zurückziehen und ausreichend spülen, um den entstandenen Unterdruck
möglichst gering zu halten und dadurch die Gefahr einer Luftembolie zu minimieren.
Verwendbarkeitsdatum – Sicherstellen, dass das Verfallsdatum der Schleuse noch nicht
abgelaufen ist. Das Produkt nach Ablauf des Verfallsdatums nicht mehr ver wenden.
Verletzung der Femoralvene – Sorgfältig darauf achten, dass es beim Einführen, Bewegen
oder Zurückziehen der Schleuse zu keinen größeren Verletzungen der Femoralvene oder der
Zugangsstelle kommt. Zu den möglichen Komplikationen bei einer Katheterisierung der
Femoralvene gehören Hämatome und Thrombosen.
Schleusenplatzierung nur unter Durchleuchtung – Es wird nachdrücklich empfohlen, die
Schleuse nur unter Durchleuchtung zu platzieren und zu bewegen. Jede Bewegung der Schleuse
ohne Durchleuchtungskontrolle kann zur Beschädigung von Herz- und Gefäßstrukturen führen.
Nur zum einmaligen Gebrauch bestimmt – Dieses Produkt darf nur ein einziges Mal und nur
bei einem einzelnen Patienten verwendet werden. Das Produkt nicht wiederverwenden,
aufbereiten oder zum Zwecke der Wiederverwendung resterilisieren. Durch Wieder verwendung,
Aufbereitung oder Resterilisierung kann die strukturelle Integrität des Produkts beeinträchtigt
werden und eine Kontamination des Produkts entstehen, die zu Verletzungen, zur Erkrankung
oder zum Tod des Patienten führen kann.
Häufiges Spülen – Es wird empfohlen, die Schleuse regelmäßig zu spülen:
• zur Vermeidung eines Blutstaus, eines Blutpfropfs, einer Embolie und anderer schwerer
Verletzungen des Patienten
• zur Vermeidung eines Anhaftens von Kontrastmittel im Lumen der Schleuse nach jeder
Kontrastmittelinjektion
Sorgfaltspflichten und Pflege – Beim Umgang mit dem Produkt Folgendes beachten:
Deutsch
14

• Beim Hantieren mit dem Produkt äußerst vorsichtig sein. Durch mangelnde Sorgfalt kann es
zu Verletzungen wie z. B. Perforationen, Tamponaden, der Induzierung von Arrhythmien oder
einem Herzblock kommen.
• Beim Vorschieben oder Zurückziehen des Produkts – besonders bei spürbarem
Widerstand – keine übermäßige Kraft aufwenden.
• Eine Positionierung des Produkts im Bereich der Chordae tendineae ist zu vermeiden, weil es
hierbei leichter zum Hängenbleiben des Produkts innerhalb des Herzens kommen kann.
Dadurch kann eine chirurgische Intervention oder Wiederherstellung des verletzten
Gewebes notwendig werden.
• Die Schleuse nicht verwenden, wenn sie geknickt oder beschädigt ist.
Linksatrialer Zugang – Den Dilatator oder die Schleuse nicht ohne vorherige Kontrolle des
linksatrialen Zugangs über das Vorhofseptum vorschieben. So wird ein Vorschieben dieser
Komponenten an einen unerwünschten Ort verhindert.
Erforderliche Klinikausstattung – Ein externes Defibrillationsgerät zum unmittelbaren Einsatz
während der Verwendung des steuerbaren Schleusensystems bereithalten.
Andere Katheter, Geräte oder Drähte – Eine mögliche Verwicklung der Schleuse mit anderen
Kathetern, Geräten oder Drähten vermeiden. Durch eine solche Verwicklung kann eine
chirurgische Intervention notwendig werden.
Herzklappenprothesen – Das Produkt nicht durch eine Herzklappenprothese (mechanisch
oder biologisch) führen. Das Produkt könnte innerhalb der Herzklappenprothese hängenbleiben,
diese beschädigen und dadurch eine Klappeninsuffizienz oder ein vorzeitiges Versagen der
Herzklappenprothese verursachen.
Qualifikation des Anwenders – Dieses Produkt darf nur von in der Herzkatheterisierung
hinreichend geschulten Ärzten oder unter deren Aufsicht verwendet werden.
Anforderungen an die Einsatzumgebung – Herzkatheterisierungen dürfen nur in voll
ausgerüsteten Einrichtungen durchgeführt werden.
Aspiration durch den Seitenanschluss – Beim Zurückziehen von Dilatator, Katheter, Nadel,
Drähten oder anderen Geräten durch den Seitenanschluss aspirieren.
Blockade des Seitenanschlusses – Sorgfältig darauf achten, dass der Seitenanschluss nicht
blockiert wird, um eine effektive Spülung mit Kochsalzlösung zu gewährleisten.
Signifikanter Blutaustritt – Sorgfältig darauf achten, dass es während der Prozedur zu keinem
starken Blutaustritt durch das Hämostaseventil kommt.
Überprüfung der Sterilverpackung – Die Sterilverpackung und das Produkt vor der
Verwendung überprüfen. Bei Anzeichen einer Beschädigung der Sterilverpackung oder des
Produkts darf das Produkt nicht verwendet werden. Wenden Sie sich bitte an Ihren örtlichen
Medtronic Repräsentanten.
Strahlenbelastung durch Röntgen und Fluoroskopie – Bei der Durchführung von
Ablationsprozeduren unter Durchleuchtung können sowohl Patienten als auch Labormitarbeiter
einer erheblichen Strahlenbelastung ausgesetzt werden. Eine längere Exposition kann akute
Strahlenschäden zur Folge haben und ist mit einem erhöhten Risiko somatischer und genetischer
Auswirkungen verbunden. Eine Katheterablation darf nur nach angemessener Beachtung der mit
der Prozedur verbundenen möglichen Strahlenbelastung durchgeführt werden, wobei
Maßnahmen zur Minimierung der Strahlenbelastung zu treffen sind. Bei Schwangeren sind
Röntgenaufnahmen zu vermeiden und ein etwaiger Einsatz des Katheters sorgfältig abzuwägen.
5 Unerwünschte Nebenwirkungen
Bei der Kanülierung peripherer Gefäße und bei der intrakardialen Positionierung von Schleuse
und Dilatator kann es unter anderem zu den folgenden Komplikationen kommen:
• Komplikationen an der Zugangsstelle
(Hämatom, Infektion, Thrombose, Ekchymose, AV-Fistel, Blutung aus der Einstichstelle, Hämorrhagie)
• Luftembolie
• Arrhythmie (Vorhofflimmern, Vorhofflattern, ventrikuläre Tachykardie)
• Herzstillstand
• Unbehagen, Schmerzen oder Druckgefühl
in der Brust
• Koronararterienspasmus, Dissektion,
Thrombose
• Tod
• Endokarditis
• A-V Block, der die dauerhafte Implantation
eines Herzschrittmachers notwendig
macht
• Hämothorax
• Myokardinfarkt
• Perforation von kardialem oder umgebendem Gewebe
• Perikarderguss oder -tamponade
• Perikarditis
• Pleuraerguss
• Pneumothorax
• Pseudoaneurysma
• Lungenödem
• Lungenembolie
• Schlaganfall
• Thrombus
• transitorisch-ischämische Attacke (TIA)
• vasovagale Reaktion
6 Gebrauchsanweisung
Hinweis: Vor dem Einführen der Schleuse in den Patienten den Biegemechanismus auf
Funktionstüchtigkeit prüfen.
1. Unter aseptischen Bedingungen mithilfe eines geeigneten Einführbestecks einen
Gefäßzugang schaffen.
2. Unter Anwendung der üblichen Methoden zur Herstellung eines Gefäßzugangs einen
kompatiblen Führungsdraht (siehe Spezifikationen) durch das Gefäßsystem einführen und
bis zur gewünschten Position vorschieben.
3. Den Seitenanschluss der Schleuse und das Dilatatorlumen mit steriler Kochsalzlösung
spülen.
4. Eine neutrale Stellung der Schleuse (nicht gebogen) sicherstellen und den Dilatatorschaft
vor der Einführung durch das Hämostaseventil mit steriler Kochsalzlösung anfeuchten.
5. Mit dem Zusammenbau von Dilatator und Schleuse beginnen, indem die distale
Dilatatorspitze in das Hämostaseventil eingeführt wird, sodass sich die gebogene Kante des
Dilatators senkrecht zum Hämostaseventil befindet (siehe Abbildung 2).
Abbildung 2. Steuerbare FlexCath Select Schleuse
6. Den Dilatator weiter in die Schleuse vorschieben, bis der Dilatatoranschluss im
Schleusenanschluss einrastet.
Hinweis: Die Ausrichtung der Beschriftung auf dem Dilatatoranschluss sollte mit der
Ausrichtung der Beschriftung auf dem Schleusengriff übereinstimmen, damit die Biegung
des Dilatators mit der Ablenkrichtung der Schleuse und dem Seitenanschluss
übereinstimmt (siehe Abbildung 3).
Abbildung 3. Steuerbare FlexCath Select Schleuse
15
Deutsch

7. Das Schleusen-Dilatator-System mit einer leichten Drehbewegung in die Vena cava superior
auf den Führungsdraht fädeln und in das Gefäßsystem einführen.
8. Den Führungsdraht entfernen.
9. Die ordnungsgemäß vorbereitete transseptale Nadel in das Schleusen-Dilatator-System
einführen, sodass der Biegungsindikator auf der transseptalen Nadel auf den
Seitenanschluss ausgerichtet ist.
Hinweis: Die transseptale Nadel sollte zusammen mit einem Mandrin verwendet werden,
um ein Ausschälen des Innenlumens des Dilatators zu vermeiden.
10. Das System nach unten zum rechten Vorhof bewegen, um die transseptale Punktion
vorzubereiten.
11. Unter fluoroskopischer Kontrolle die transseptale Punktion mithilfe von Druckmessungen,
Kontrastmittelinjektion oder beidem durchführen. Die korrekte Positionierung im linken
Atrium sicherstellen.
12. Die transseptale Nadel in den Dilatator ziehen und den Dilatator sowie die Nadel langsam
von der Schleuse entfernen.
Hinweis: Den Dilatator langsam entfernen, um die Wahrscheinlichkeit der Entstehung eines
Vakuums in der Schleuse zu reduzieren. Blut sollte frei durch den seitlichen Por t aspiriert
werden. Ist dies nicht der Fall, die Schleuse zurückziehen, da die Schleusenspitze eventuell
an der Wand des Vorhofs oder einer Pulmonalvene anliegt.
13. Blut durch den seitlichen Port aspirieren und sicherstellen, dass die Schleuse entlüftet ist.
Vor dem Einführen eines Katheters in die Schleuse eine Aspiration durchführen oder die
Spontanblutung zurücklaufen lassen.
Hinweis: Diesen Schritt nach allen Katheterwechseln durchführen.
14. Nach Herstellung des Zugangs mit der Schleuse die Antikoagulationstherapie
aufrechterhalten.
15. Den Katheter gemäß der Gebrauchsanweisung des Herstellers vorbereiten.
16. Den Katheter einführen und die Schleuse positionieren.
Hinweise:
• Das Befeuchten des Katheterschafts kann das Einführen erleichtern.
• Das Hämostaseventil verfügt über eine Sperre, um ein Öffnen der Dichtung durch
jegliche Einführhilfen zu vermeiden.
• Um den dabei entstehenden Unterdruck möglichst niedrig zu halten, die Komponenten
immer langsam einführen und zurückziehen.
• Die Schleuse sollte auch bei eingeführtem Katheter gespült werden.
17. Vor dem Herausziehen der Schleuse sicherstellen, dass sie sich in der Neutralstellung (nicht
gebogen) befindet.
7 Spezifikationen
Gesamtlänge
Nutzbare Länge 65 cm (25,6 in)
Innendurchmesser 3,3 mm (10 Fr) (0,13 in)
Außendurchmesser 4,3 mm (13 Fr) (0,17 in)
Länge des Dilatators 86 cm (33,9 in)
Röntgenmarkierung 5 mm (0,2 in) proximal der Schleusenspitze
Kompatibilität des Führungs-
drahts
Kompatibilität der transseptalen
Nadel
Umgebungsparameter
Empfohlene Transpor ttemperatur
Empfohlene Lagerungstemperatur
Betrieb 15°C bis 30°C (59°F bis 86°F) bei einer Höhe von weniger als
81 cm (31,9 in)
0,81 mm (0,032 in) bis 0,89 mm (0,035 in)
89 cm (35,0 in) oder länger
−35°C bis 58°C (−31°F bis 136°F); 85 % relative Luftfeuchtigkeit (nicht kondensierend)
Durchschnittlich 22°C (72°F) mit einer Standardabweichung
von 2,7°C (4,86°F). Bei Temperaturen unter 15°C (59°F) und
über 30°C (86°F) müssen Gegenmaßnahmen ergriffen werden.
2400 m (8000 Fuß) über dem Meeresspiegel
8 Medtronic Haftungsausschluss
Vollständige Informationen zum Haftungsausschluss finden Sie im beiliegenden
Garantiedokument.
9 Wartung
Medtronic beschäftigt überall auf der Welt hervorragend ausgebildete Repräsentanten und
Ingenieure, die Ihnen bei Fragen oder Problemen zur Seite stehen. Auf Anfrage führen unsere
Mitarbeiter auch Schulungen durch, um medizinisches Fachpersonal in der Verwendung von
Medtronic Produkten zu unterweisen. Medtronic beschäftigt außerdem fachlich versierte
Mitarbeiter, die Anwender unserer Produkte in technischen Fragen beraten. Für weitere
Informationen steht Ihnen Ihr Medtronic Repräsentant zur Verfügung. Sie können auch mit einer
der für Sie zuständigen und auf der Rückseite aufgeführten Medtronic Vertretungen telefonisch
oder schriftlich Kontakt aufnehmen.
Deutsch
16

1 Περιγραφή
65 cm
(25,6 in)
16 cm
(6,3 in)
86 cm
(33,9 in)
Το κατευθυνόμενο θηκάρι FlexCath™ Select της Medtronic είναι ένας διαδερμικός εισαγωγέας
καθετήρα που διαθέτει μια βαλβίδα για να επιτρέπει την εισαγωγή, την απόσυρση και την
αλλαγή καθετήρων και συρμάτων, ενώ ελαχιστοποιεί την απώλεια αίματος. Μια πλευρική θύρα
με στρόφιγγα είναι ενσωματωμένη ώστε να επιτρέπει συνεχή στάγδην έγχυση, έγχυση μέσω
του κεντρικού αυλού, έκπλυση, αναρρόφηση, δειγματοληψία αίματος και παρακολούθηση της
πίεσης.
Εικόνα 1. Κατευθυνόμενο θηκάρι FlexCath Select
Ένας διαστολέας περιέχεται στη συσκευασία μαζί με το κατευθυνόμενο θηκάρι FlexCath
Select. Το θηκάρι περιγράφεται στον ακόλουθο πίνακα:
Μοντέλο
990065 3,3 mm (10 Fr)
Το θηκάρι μπορεί να εκτρέπεται ώστε να παρέχει επιπρόσθετη ευελιξία σε καθετήρες οι οποίοι
προωθούνται μέσω του θηκαριού και εντός της δεξιάς ή αριστερής κοιλότητας της καρδιάς.
Το κατευθυνόμενο θηκάρι FlexCath Select 10 Fr μπορεί να χρησιμοποιηθεί με μεγέθη
διαγνωστικών καθετήρων και καθετήρων κατάλυσης της Medtronic έως και 9 Fr.
Ο διαστολέας του κατευθυνόμενου θηκαριού FlexCath Select 10 Fr είναι συμβατός με τις
διαδιαφραγματικές βελόνες HeartSpan της Merit Medical μήκους 89 cm και μακρύτερες.
Εσωτερική διάμετρος Εξωτερική διάμετρος Ωφέλιμο μήκος
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Περιεχόμενα συσκευασίας
Το κατευθυνόμενο θηκάρι FlexCath Select διατίθεται αποστειρωμένο. Η συσκευασία περιέχει
τα εξής τεμάχια:
• 1 κατευθυνόμενο θηκάρι
• 1 διαστολέα
• Τεκμηρίωση προϊόντος
2 Ενδείξεις χρήσης
Το κατευθυνόμενο θηκάρι FlexCath Select προορίζεται για την εισαγωγή διαδερμικού
καθετήρα μέσα στο αγγειακό σύστημα και μέσα στις κοιλότητες της καρδιάς,
περιλαμβανομένης της αριστερής πλευράς της καρδιάς μέσω του μεσοκολπικού
διαφράγματος. Η εκτροπή του θηκαριού διευκολύνει την τοποθέτηση του καθετήρα.
3 Αντενδείξεις
Το κατευθυνόμενο θηκάρι FlexCath Select αντενδείκνυται για τοποθέτηση στον αριστερό
κόλπο ή στην αριστερή κοιλία, εάν οποιεσδήποτε από τις ακόλουθες συνθήκες ισχύουν για τον
ασθενή:
• Ο ασθενής έχει εμβάλωμα μεσοκολπικού διαφράγματος ή συσκευή απόφραξης, ή είχε
υποβληθεί σε άλλη χειρουργική επέμβαση μέσα ή δίπλα στο μεσοκολπικό διάφραγμα.
• Ο ασθενής έχει θρόμβο στον αριστερό κόλπο.
• Ο ασθενής παρουσίασε ή υπήρχε υποψία κολπικού μυξώματος.
4 Προειδοποιήσεις και προφυλάξεις
Ενέργεια κατάλυσης – Όταν χρησιμοποιείτε το θηκάρι υπό την παρουσία ενέργειας
κατάλυσης, μεριμνήστε ώστε να διασφαλίσετε ότι όλα τα στοιχεία κατάλυσης βρίσκονται
εκτός του θηκαριού.
Αναρρόφηση αέρα – Αφαιρέστε το οδηγό σύρμα από το θηκάρι πριν από την αναρρόφηση και
έκπλυση του θηκαριού. Αυτή η ενέργεια ελαχιστοποιεί την αναρρόφηση αέρα μέσω της
βαλβίδας του θηκαριού.
Αντιπηκτική αγωγή – Χορηγήστε κατάλληλα επίπεδα περιδιαδικαστικής αντιπηκτικής
αγωγής σε ασθενείς οι οποίοι υποβάλλονται σε αριστερόπλευρες και διαδιαφραγματικές
καρδιακές επεμβάσεις και σε επιλεγμένους ασθενείς οι οποίοι υποβάλλονται σε δεξιόπλευρες
επεμβάσεις. Για να ελαχιστοποιήσετε την αιμορραγία και τις θρομβωτικές επιπλοκές,
χορηγήστε περιδιαδικαστική αντιπηκτική αγωγή σύμφωνα με τα πρότυπα του ιδρύματος.
Ανάδρομη αιμορραγία – Βεβαιωθείτε ότι η στρόφιγγα βρίσκεται σε κλειστή θέση μετά την
έκπλυση ή την αναρρόφηση για να αποτρέψετε ακούσια ανάδρομη αιμορραγία μέσω της
πλευρικής θύρας.
Απόρριψη βιολογικώς επικίνδυνων αποβλήτων – Απορρίψτε όλα τα χρησιμοποιημένα
προϊόντα και τα αποστειρωμένα εξαρτήματα σύμφωνα με τις νοσοκομειακές διαδικασίες.
Έγχυση σκιαγραφικού – Μη χρησιμοποιείτε σύστημα υποβοηθούμενης έγχυσης για την
έγχυση σκιαγραφικού διαλύματος εντός του θηκαριού.
Συστροφή διαστολέα – Μη συστρέφετε τον διαστολέα κατά τη διάρκεια ή μετά την ασφάλισή
του στον ομφαλό της βαλβίδας. Η ενέργεια αυτή ενδέχεται να προκαλέσει εσφαλμένη
ευθυγράμμιση του άκρου του διαστολέα στο άπω άκρο σε σχέση με την πλευρική θύρα στο
εγγύς άκρο.
Μην το επαναποστειρώνετε – Μην επαναποστειρώνετε το παρόν προϊόν με σκοπό την
επαναχρησιμοποίηση. Η επαναποστείρωση ενδέχεται να επηρεάσει αρνητικά τη δομική
ακεραιότητα του προϊόντος ή να προκαλέσει κίνδυνο μόλυνσης από το προϊόν που θα
μπορούσε να έχει ως αποτέλεσμα τον τραυματισμό, την ασθένεια ή το θάνατο του ασθενούς.
Κίνδυνος εμβολής – Η εισαγωγή οποιουδήποτε καθετήρα ή θηκαριού στο κυκλοφορικό
σύστημα συνεπιφέρει τον κίνδυνο εμβολής αέρα, που μπορεί να αποφράξει αγγεία και να
προκαλέσει έμφρακτο ιστού με σοβαρές συνέπειες. Η χρήση καθετήρων μικρότερων από 9 Fr
με το παρόν προϊόν ενδέχεται να ενέχει αυξημένο κίνδυνο εμβολής αέρα. Πάντοτε να
προωθείτε και να αποσύρετε τα εξαρτήματα αργά και να χρησιμοποιείτε έκπλυση για να
ελαχιστοποιήσετε το κενό που δημιουργείται και κατά συνέπεια να ελαχιστοποιήσετε τον
κίνδυνο εμβολής αέρα.
Ημερομηνία λήξης – Ελέγξτε για να επαληθεύσετε ότι δεν έχει παρέλθει η ημερομηνία λήξης
του θηκαριού. Μην το χρησιμοποιήσετε εάν η ημερομηνία λήξης του προϊόντος έχει παρέλθει.
Βλάβη μηριαίας φλέβας – Θα πρέπει να προσέχετε να ελαχιστοποιήσετε τη βλάβη στη
μηριαία φλέβα και στη θέση προσπέλασης κατά την εισαγωγή, το χειρισμό και την απόσυρση
του θηκαριού. Οι επιπλοκές που συσχετίζονται με τον καθετηριασμό μηριαίας φλέβας
περιλαμβάνουν αιμάτωμα και θρόμβωση.
Απαιτείται ακτινοσκόπηση για την τοποθέτηση του θηκαριού – Η χρήση
ακτινοσκόπησης κατά το χειρισμό και την τοποθέτηση του θηκαριού συνιστάται θερμά. Ο
χειρισμός του θηκαριού χωρίς ακτινοσκόπηση μπορεί να έχει ως αποτέλεσμα τη βλάβη σε
καρδιακές και αγγειακές δομές.
Για μία μόνο χρήση – Το παρόν προϊόν προορίζεται για μία μόνο χρήση σε έναν ασθενή. Μην
επαναχρησιμοποιείτε, μην επανεπεξεργάζεστε και μην επαναποστειρώνετε το παρόν προϊόν
με σκοπό την επαναχρησιμοποίηση. Η επαναχρησιμοποίηση, η επανεπεξεργασία και η
επαναποστείρωση μπορεί να επηρεάσουν αρνητικά τη δομική ακεραιότητα του προϊόντος ή να
προκαλέσουν κίνδυνο μόλυνσης του προϊόντος που θα μπορούσε να έχει ως αποτέλεσμα τον
τραυματισμό, την ασθένεια ή το θάνατο του ασθενούς.
Συχνή έκπλυση – Συνιστάται η τακτική έκπλυση του θηκαριού:
17
Ελληνικά

• Για την αποτροπή λίμνασης αίματος, θρόμβων, εμβόλων και σοβαρού τραυματισμού του
ασθενούς.
• Για την αποτροπή της προσκόλλησης του σκιαγραφικού διαλύματος στο εσωτερικό του
αυλού μετά από κάθε έγχυση σκιαγραφικού μέσου.
Χειρισμός και φροντίδα – Όταν χειρίζεστε το προϊόν:
• Να προσέχετε ιδιαιτέρως κατά το χειρισμό του προϊόντος. Η έλλειψη ιδιαίτερης προσοχής
μπορεί να έχει ως αποτέλεσμα τραυματισμό, όπως διάτρηση, επιπωματισμό, επαγωγή
αρρυθμίας ή καρδιακό αποκλεισμό.
• Μη χρησιμοποιείτε υπερβολική δύναμη για να προωθήσετε ή να αποσύρετε το προϊόν,
ιδιαιτέρως εάν συναντάται αντίσταση.
• Αποφύγετε την τοποθέτηση του προϊόντος γύρω από τις τενόντιες χορδές, γεγονός το
οποίο αυξάνει την πιθανότητα εγκλωβισμού μέσα στην καρδιά και ενδέχεται να καταστήσει
αναγκαία τη χειρουργική επέμβαση ή την αποκατάσταση των τραυματισμένων ιστών.
• Μη χρησιμοποιείτε το θηκάρι εάν έχει συστραφεί ή καταστραφεί.
Αριστερή κολπική προσπέλαση – Μην προωθείτε τον διαστολέα ή το θηκάρι μέσω του
μεσοκολπικού διαφράγματος χωρίς πρώτα να επιβεβαιώσετε την αριστερή κολπική
προσπέλαση, ώστε να αποτραπεί η προώθηση αυτών των στοιχείων σε ανεπιθύμητη θέση.
Απαραίτητος νοσοκομειακός εξοπλισμός – Διατηρείτε εξωτερικό εξοπλισμό
βηματοδότησης σε κοντινή απόσταση για άμεση χρήση κατά τη διάρκεια της χρήσης του
συναρμολογήματος του κατευθυνόμενου θηκαριού.
Άλλοι καθετήρες, συσκευές ή σύρματα – Αποφύγετε εμπλοκή του θηκαριού με άλλους
καθετήρες, συσκευές ή σύρματα. Μια τέτοια εμπλοκή ενδέχεται να καταστήσει αναγκαία τη
χειρουργική παρέμβαση.
Προσθετικές καρδιακές βαλβίδες – Να μην επιτρέπετε τη διέλευση του προϊόντος μέσα
από προσθετική καρδιακή βαλβίδα (μηχανική ή ιστού). Το προϊόν μπορεί να εγκλωβιστεί στη
βαλβίδα, καταστρέφοντας τη βαλβίδα και προκαλώντας βαλβιδική ανεπάρκεια ή πρόωρη
ανεπάρκεια της προσθετικής βαλβίδας.
Εκπαιδευμένοι χρήστες – Ο παρών εξοπλισμός θα πρέπει να χρησιμοποιείται μόνο με ή υπό
την επίβλεψη ιατρών εκπαιδευμένων σε επεμβάσεις καρδιακού καθετηριασμού.
Απαιτούμενο περιβάλλον χρήσης – Οι επεμβάσεις καρδιακού καθετηριασμού πρέπει να
πραγματοποιούνται μόνο σε πλήρως εξοπλισμένη μονάδα.
Αναρρόφηση από την πλευρική θύρα – Πραγματοποιήστε αναρρόφηση από την πλευρική
θύρα όταν αποσύρετε τον διαστολέα, τον καθετήρα, τη βελόνα, τα σύρματα ή άλλα προϊόντα.
Απόφραξη πλευρικής θύρας – Θα πρέπει να προσέχετε προκειμένου να αποτραπεί
οποιαδήποτε απόφραξη της πλευρικής θύρας για να διασφαλίσετε την αποτελεσματική
έκπλυση με φυσιολογικό ορό.
Σημαντική διαφυγή αίματος – Θα πρέπει να παρακολουθείτε προσεκτικά να μην υπάρχει
σημαντική διαφυγή αίματος μέσω της αιμοστατικής βαλβίδας κατά τη διαδικασία.
Επιθεώρηση στείρας συσκευασίας – Επιθεωρήστε την αποστειρωμένη συσκευασία και το
προϊόν πριν τη χρήση. Εάν η αποστειρωμένη συσκευασία ή το προϊόν παρουσιάζει ζημία, μη
χρησιμοποιήσετε το προϊόν. Επικοινωνήστε με τον τοπικό αντιπρόσωπο της Medtronic.
Έκθεση σε ακτίνες Χ και ακτινοσκόπηση – Η χρήση ακτινοσκόπησης κατά τις επεμβάσεις
καθετηριασμού κατάλυσης εγκυμονεί το ενδεχόμενο σημαντικής έκθεσης σε ακτίνες Χ τόσο
για τους ασθενείς όσο και για το εργαστηριακό προσωπικό. Η παρατεταμένη έκθεση μπορεί να
έχει ως αποτέλεσμα οξεία ακτινοπληξία και αυξημένο κίνδυνο σωματικών και γενετικών
επιπτώσεων. Πραγματοποιήστε καθετηριασμό κατάλυσης μόνο αφού δώσετε επαρκή
προσοχή στην ενδεχόμενη έκθεση στην ακτινοβολία που συσχετίζεται με την επέμβαση και
αφού λάβετε μέτρα για την ελαχιστοποίηση της έκθεσης αυτής. Εξετάστε προσεκτικά τους
ενδεχόμενους κινδύνους και αποφύγετε την έκθεση σε ακτίνες X πριν χρησιμοποιήσετε το
προϊόν σε εγκύους.
5 Ανεπιθύμητα συμβάντα
Τα ενδεχόμενα ανεπιθύμητα συμβάντα που συσχετίζονται με τον καθετηριασμό του
περιφερικού αγγειακού συστήματος και την ενδοκαρδιακή τοποθέτηση του θηκαριού και του
διαστολέα ενδέχεται να περιλαμβάνουν, μεταξύ άλλων, τις ακόλουθες παθήσεις:
• Επιπλοκές θέσης προσπέλασης (αιμάτωμα, μόλυνση, θρόμβωση, εκχύμωση,
αρτηριοφλεβικό συρίγγιο, αιμορραγία
από τη θέση κέντησης, αιμορραγία)
• Εμβολή αέρα
• Αρρυθμία (κολπική μαρμαρυγή, κολπικός
πτερυγισμός, κοιλιακή ταχυκαρδία)
• Καρδιακή ανακοπή
• Θωρακική δυσφορία, πόνος ή πίεση
• Σπασμός στεφανιαίας αρτηρίας, διαχωρισμός, θρόμβωση
• Θάνατος
• Ενδοκαρδίτιδα
• Καρδιακός αποκλεισμός, που απαιτεί
μόνιμο βηματοδότη
• Αιμοθώρακας
• Έμφραγμα του μυοκαρδίου
• Διάτρηση του καρδιακού ή περιβάλλοντα
ιστού
• Περικαρδιακή συλλογή, επιπωματισμός
• Περικαρδίτιδα
• Υπεζωκοτική συλλογή
• Πνευμονοθώρακας
• Ψευδοανεύρυσμα
• Πνευμονικό οίδημα
• Πνευμονική εμβολή
• Εγκεφαλικό επεισόδιο
• Θρόμβος
• Παροδικό ισχαιμικό επεισόδιο (ΠΙΕ)
• Αγγειοπαρασυμπαθητική αντίδραση
6 Οδηγίες χρήσης
Σημείωση: Πριν από την εισαγωγή του θηκαριού στον ασθενή, ελέγξτε το μηχανισμό
εκτροπής για να διασφαλίσετε ότι λειτουργεί.
1. Ενώ χρησιμοποιείτε άσηπτη τεχνική, δημιουργήστε πρόσβαση στο αγγείο με τον
κατάλληλο εισαγωγέα.
2. Εισαγάγετε ένα συμβατό οδηγό σύρμα (βλ. Προδιαγραφές) μέσω του αγγειακού
συστήματος και εντός της επιθυμητής θέσης χρησιμοποιώντας συνήθεις τεχνικές
αγγειακής προσπέλασης.
3. Εκπλύνετε την πλευρική θύρα του θηκαριού και τον αυλό του διαστολέα με στείρο
διάλυμα φυσιολογικού ορού.
4. Βεβαιωθείτε ότι το θηκάρι βρίσκεται σε ουδέτερη (χωρίς εκτροπή) θέση και υγράνετε τον
άξονα του διαστολέα με στείρο διάλυμα φυσιολογικού ορού πριν να τον εισαγάγετε μέσω
της αιμοστατικής βαλβίδας.
5. Αρχίστε να συναρμολογείτε τον διαστολέα και το θηκάρι μεταξύ τους εισαγάγοντας το
άπω άκρο του διαστολέα στην αιμοστατική βαλβίδα, έτσι ώστε το καμπύλο άκρο του
διαστολέα να είναι κατακόρυφο ως προς την αιμοστατική βαλβίδα (βλ. Εικ. 2).
Εικόνα 2. Κατευθυνόμενο θηκάρι FlexCath Select
6. Συνεχίστε να προωθείτε τον διαστολέα μέσα στο θηκάρι μέχρι ο ομφαλός του διαστολέα
να ασφαλίσει απόλυτα μέσα στον ομφαλό του θηκαριού.
Σημείωση: Η σήμανση στον ομφαλό του διαστολέα θα πρέπει να είναι ευθυγραμμισμένη
με τη σήμανση στη λαβή του θηκαριού, έτσι ώστε η καμπύλη του διαστολέα να
ευθυγραμμιστεί προς τον ίδιο προσανατολισμό με την κατεύθυνση εκτροπής του
θηκαριού και με την πλευρική θύρα (βλ. Εικ. 3).
Ελληνικά
18

Εικόνα 3. Κατευθυνόμενο θηκάρι FlexCath Select
7. Περάστε το συναρμολόγημα θηκαριού-διαστολέα πάνω από το οδηγό σύρμα και εντός
του αγγειακού συστήματος με μικρή κίνηση συστροφής μέσα στην άνω κοίλη φλέβα
(SVC).
8. Αφαιρέστε το οδηγό σύρμα.
9. Εισαγάγετε την κατάλληλα προετοιμασμένη διαδιαφραγματική βελόνα στο
συναρμολόγημα θηκαριού-διαστολέα, έτσι ώστε ο δείκτης καμπύλωσης στη
διαδιαφραγματική βελόνα να ευθυγραμμιστεί με την πλευρική θύρα.
Σημείωση: Η διαδιαφραγματική βελόνα θα πρέπει να χρησιμοποιηθεί μαζί με ένα στυλεό,
για να αποτραπεί η απόξεση του εσωτερικού τοιχώματος του αυλού του διαστολέα.
10. Έλξατε το συναρμολόγημα προς τα κάτω στο δεξιό κόλπο για να προετοιμάσετε τη
διαδιαφραγματική κέντηση.
11. Υπό ακτινοσκοπική καθοδήγηση, πραγματοποιήστε τη διαδιαφραγματική κέντηση
χρησιμοποιώντας μετρήσεις πίεσης, έγχυση σκιαγραφικού ή και τα δύο. Επιβεβαιώστε τη
σωστή τοποθέτηση στον αριστερό κόλπο.
12. Τραβήξτε τη διαδιαφραγματική βελόνα μέσα στον διαστολέα και αφαιρέστε αργά το
συναρμολόγημα διαστολέα και βελόνας από το θηκάρι.
Σημείωση: Αφαιρέστε αργά το διαστολέα για να μειώσετε την πιθανότητα δημιουργίας
κενού μέσα στο θηκάρι. Το αίμα θα πρέπει να αναρροφάται ελεύθερα μέσω της πλαϊνής
θύρας. Εάν δεν συμβαίνει αυτό, αποσύρετε το θηκάρι, διότι το άκρο του θηκαριού μπορεί
να ακουμπάει στο τοίχωμα του κόλπου ή σε μια πνευμονική φλέβα.
13. Αναρροφήστε αίμα μέσω της πλαϊνής θύρας και βεβαιωθείτε ότι δεν υπάρχει αέρας στο
θηκάρι. Πραγματοποιήστε αναρρόφηση ή αυθόρμητη εκτόνωση μικρής ποσότητας
αίματος πριν από την εισαγωγή ενός καθετήρα μέσα στο θηκάρι.
Σημείωση: Διεξάγετε αυτό το βήμα μετά από κάθε αλλαγή καθετήρα.
14. Μετά την επίτευξη προσπέλασης με το θηκάρι, διατηρήστε την αντιπηκτική αγωγή.
15. Προετοιμάστε τον καθετήρα σύμφωνα με τις οδηγίες χρήσης του κατασκευαστή.
16. Εισαγάγετε τον καθετήρα και τοποθετήστε το θηκάρι.
Σημειώσεις:
• Η ύγρανση του άξονα του καθετήρα μπορεί να διευκολύνει την εισαγωγή.
• Η αιμοστατική βαλβίδα έχει έναν θετικό αναστολέα για να αποτρέπεται το άνοιγμα
της σφράγισης από τυχόν συσκευές σύλληψης.
• Για να ελαχιστοποιείτε το κενό που δημιουργείται, πάντα να εισάγετε και να
αποσύρετε τα εξαρτήματα αργά.
• Το θηκάρι θα πρέπει επίσης να εκπλυθεί ενώ ο καθετήρας είναι εισηγμένος.
17. Πριν από την απόσυρση του θηκαριού, διασφαλίστε ότι βρίσκεται σε ουδέτερη (χωρίς
εκτροπή) θέση.
7 Προδιαγραφές
Ολικό μήκος
Ωφέλιμο μήκος 65 cm (25,6 in)
Εσωτερική διάμετρος 3,3 mm (10 Fr) (0,13 in)
Εξωτερική διάμετρος 4,3 mm (13 Fr) (0,17 in)
Μήκος διαστολέα 86 cm (33,9 in)
Ακτινοσκιερός δείκτης 5 mm (0,2 in) εγγύς του άκρου του θηκαριού
Συμβατότητα οδηγού σύρμα-
τος
Συμβατότητα διαδιαφραγματι-
κής βελόνας
Περιβαλλοντικές παράμετροι
Συνιστώμενη θερμοκρασία
μεταφοράς
Συνιστώμενη θερμοκρασία
αποθήκευσης
Λειτουργία 15°C έως 30°C (59°F έως 86°F) σε υψόμετρο μικρότερο από
81 cm (31,9 in)
0,81 mm (0,032 in) έως 0,89 mm (0,035 in)
89 cm (35,0 in) ή μακρύτερη
−35°C έως 58°C (−31°F έως 136°F), 85% σχετική υγρασία
(χωρίς συμπύκνωση)
Μέσος όρος 22°C (72°F) με τυπική απόκλιση 2,7°C (4,86°F)
και λειτουργικά όρια ελέγχου 15°C έως 30°C (59°F έως 86°F)
2400 m (8000 πόδια) πάνω από την επιφάνεια της θάλασσας
8 Δήλωση αποποίησης της εγγύησης της Medtronic
Για πλήρεις πληροφορίες σχετικά με την εγγύηση, βλ. συνοδευτικό έγγραφο της αποποιητικής
δήλωσης της εγγύησης.
9 Συντήρηση
Η Medtronic απασχολεί αντιπροσώπους και μηχανικούς με υψηλό επίπεδο εκπαίδευσης, οι
οποίοι βρίσκονται σε ολόκληρο τον κόσμο για την εξυπηρέτησή σας και, κατόπιν αιτήματος, για
την παροχή εκπαίδευσης σε καταρτισμένο νοσοκομειακό προσωπικό στη χρήση των
προϊόντων της Medtronic. H Medtronic διατηρεί επίσης προσωπικό από επαγγελματίες για την
παροχή τεχνικών συμβουλών σε χρήστες των προϊόντων. Για περισσότερες πληροφορίες,
επικοινωνήστε με τον τοπικό αντιπρόσωπο της Medtronic ή τηλεφωνήστε ή στείλτε επιστολή
στη Medtronic στον κατάλληλο αριθμό τηλεφώνου ή τη διεύθυνση που παρατίθεται στο
οπισθόφυλλο.
19
Ελληνικά

1 Descripción
65 cm
(25,6 pulg.
)
16 cm
(6,3 pulg.)
86 cm
(33,9 pulg.)
El introductor dirigible FlexCath™ Select de Medtronic es un introductor percutáneo de catéteres
provisto de una válvula que permite la introducción, la extracción y el cambio de catéteres y guías
al tiempo que minimiza la pérdida de sangre. Se incluye un puerto lateral con una llave de paso
que permite realizar infusión por goteo continuo, inyección a través de la luz central, lavado,
aspiración, toma de muestras de sangre y monitorización de la presión.
Figura 1. Introductor dirigible FlexCath Select
El envase del introductor dirigible FlexCath Select incluye un dilatador. El introductor está descrito
en la tabla siguiente:
Modelo
990065 3,3 mm (10 Fr)
La deflexión del introductor permite mejorar la maniobrabilidad de los catéteres que se
introducen a través del mismo hasta las cavidades derechas o izquierdas del corazón.
El introductor dirigible FlexCath Select de 10 Fr puede utilizarse con catéteres de ablación y
catéteres de diagnóstico de Medtronic de tamaños de hasta 9 Fr.
El dilatador del introductor dirigible FlexCath Select de 10 Fr es compatible con las agujas
transeptales HeartSpan de Merit Medical Systems de longitud igual o superior a 89 cm.
Diámetro interno Diámetro externo Longitud útil
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Contenido del envase
El introductor dirigible FlexCath Select se suministra estéril. El envase contiene los siguientes
elementos:
• 1 introductor dirigible
• 1 dilatador
• Documentación del producto
2 Indicaciones de uso
El introductor dirigible FlexCath Select está indicado para la introducción percutánea de
catéteres en la vasculatura y en las cavidades cardíacas, incluidas las cavidades izquierdas del
corazón a través del tabique interauricular. La deflexión del introductor facilita la colocación del
catéter.
3 Contraindicaciones
El introductor dirigible FlexCath Select está contraindicado para la colocación en la aurícula o el
ventrículo izquierdos si el paciente presenta alguna de las siguientes situaciones:
• El paciente tiene un oclusor o un parche septal intraauricular o se ha sometido a otra
intervención quirúrgica en el tabique intraauricular o cerca de él.
• El paciente presenta un trombo en la aurícula izquierda.
• El paciente presenta o se sospecha que presenta un mixoma auricular.
4 Advertencias y medidas preventivas
Energía de ablación – Cuando se utilice el introductor en presencia de energía de ablación,
debe tener cuidado de asegurarse de que todos los elementos de ablación se encuentren fuera
del introductor.
Aspiración de aire – Antes de aspirar y lavar el introductor, retire la guía del mismo. De este
modo se reduce al mínimo la aspiración de aire a través de la válvula del introductor.
Tratamiento anticoagulante – Administre niveles adecuados de tratamiento anticoagulante
durante el procedimiento y en los períodos inmediatamente anterior y posterior a los pacientes
sometidos a procedimientos cardíacos transeptales y del lado izquierdo, así como a ciertos
pacientes sometidos a procedimientos del lado derecho. Para reducir al mínimo las
complicaciones hemorrágicas y trombóticas, administre a los pacientes tratamiento
anticoagulante durante el procedimiento y en los períodos inmediatamente anterior y posterior
conforme a las normas del centro.
Hemorragia retrógrada – Asegúrese de que la llave de paso esté en la posición cerrada
después de lavar o aspirar el dispositivo a fin de evitar una hemorragia retrógrada accidental a
través del puerto lateral.
Eliminación de materiales de riesgo biológico – Deseche todos los dispositivos usados y los
componentes estériles con arreglo a los procedimientos del hospital.
Inyección de contraste – No use un sistema de inyección automático para la inyección de la
solución de contraste en el interior del introductor.
Giro del dilatador – No gire el dilatador al encajarlo en el conector de la válvula o después de
hacerlo. Si lo hace, podría producirse un alineamiento incorrecto de la punta del dilatador en el
extremo distal con respecto al puerto lateral en el extremo proximal.
No reesterilizar – No reesterilice este dispositivo para reutilizarlo. La reesterilización puede
poner en peligro la integridad estructural del dispositivo o generar un riesgo de contaminación del
mismo que podría provocar al paciente lesiones, enfermedades e incluso la muerte.
Riesgo de embolia – La introducción de cualquier catéter o introductor en el sistema circulatorio
conlleva un riesgo de embolia gaseosa, que puede obstruir los vasos y provocar un infarto de
tejidos con consecuencias graves. El uso de catéteres menores de 9 Fr con este dispositivo
puede aumentar el riesgo de embolia gaseosa. Haga avanzar y retire siempre los componentes
lentamente y utilice lavados para reducir al mínimo el vacío creado y, por tanto, el riesgo de
embolia gaseosa.
Fecha de caducidad – Compruebe que el introductor se encuentra dentro de su período de
validez. No lo utilice si ha expirado la fecha de caducidad.
Lesión en la vena femoral – Debe tenerse cuidado para reducir al mínimo la lesión de la vena
femoral y del punto de acceso al insertar, manipular o retirar el introductor. Algunas de las
complicaciones asociadas al cateterismo de las venas femorales son la formación de
hematomas y trombosis.
Necesidad de fluoroscopia para la colocación del introductor – Se recomienda
encarecidamente la utilización de fluoroscopia durante la manipulación y la colocación del
introductor. Si se manipula el introductor sin fluoroscopia, podrían producirse lesiones de
estructuras cardíacas y vasculares.
Válido para un solo uso – Este dispositivo está indicado únicamente para utilizarse una vez en
un solo paciente. No reutilice, reprocese ni reesterilice este dispositivo para reutilizarlo. La
reutilización, el reprocesamiento o la reesterilización del dispositivo pueden poner en peligro la
integridad estructural del dispositivo o generar un riesgo de contaminación del mismo que podría
provocar al paciente lesiones, enfermedades e incluso la muerte.
Lavado frecuente – Se recomienda lavar periódicamente el introductor:
• Para evitar el estancamiento de sangre, la formación de coágulos y émbolos, y lesiones
graves al paciente.
• Para evitar que la solución de contraste se adhiera al interior de la luz después de cada
inyección de contraste.
Manipulación y cuidado – Cuando manipule el dispositivo:
Español
20

• Extreme el cuidado al manipular el dispositivo. Si no se presta gran atención pueden
producirse lesiones tales como perforaciones, taponamiento, inducción de arritmias o
bloqueo cardíaco.
• No ejerza demasiada fuerza para hacer avanzar o retirar el dispositivo, especialmente si
encuentra resistencia.
• No coloque el dispositivo alrededor de las cuerdas tendinosas, ya que esto aumenta la
probabilidad de atrapamiento del dispositivo en el interior del corazón y podría hacer
necesaria una intervención quirúrgica o la reparación quirúrgica de los tejidos lesionados.
• No utilice el introductor si está doblado o dañado.
Acceso a la aurícula izquierda – No haga avanzar el dilatador ni el introductor a través del
tabique interauricular sin confirmar antes el acceso a la aurícula izquierda a fin de evitar el avance
de estos componentes hasta un lugar no deseado.
Equipos hospitalarios necesarios – Tenga a mano un equipo de desfibrilación externa para su
uso inmediato durante la utilización del conjunto de introductor dirigible.
Otros catéteres, dispositivos o guías – Evite que el introductor se enrede con otros catéteres,
dispositivos o guías. Si se enreda, podría ser necesaria una intervención quirúrgica.
Prótesis valvulares cardíacas – No haga pasar el dispositivo a través de una prótesis valvular
cardíaca (mecánica o tisular). El dispositivo podría quedar atrapado en la válvula y dañarla,
causando insuficiencia valvular o el fallo prematuro de la prótesis valvular.
Usuarios cualificados – Este equipo debe ser utilizado exclusivamente por médicos con
formación en procedimientos de cateterismo cardíaco o bajo su supervisión.
Entorno de uso necesario – Los procedimientos de cateterización cardíaca deben realizarse
únicamente en una sala totalmente equipada.
Aspiración por el puerto lateral – Aspire por el puerto lateral al extraer el dilatador, catéter,
aguja, guías u otros dispositivos.
Obstrucción del puerto lateral – Debe tenerse cuidado de evitar la obstrucción del puerto
lateral a fin de garantizar un lavado eficaz con solución salina.
Escape importante de sangre – Debe comprobarse que no haya un escape importante de
sangre a través de la válvula hemostática durante el procedimiento.
Inspección del envase estéril – Examine el envase estéril y el dispositivo antes de su
utilización. No utilice el dispositivo si el envase estéril o el dispositivo presentan daños. Póngase
en contacto con el representante local de Medtronic.
Exposición radiográfica y fluoroscópica – La utilización de un fluoroscopio durante los
procedimientos de ablación con catéter presenta la posibilidad de una exposición importante a
rayos x tanto para el paciente como para el personal de laboratorio. Una exposición excesiva
puede provocar una lesión por radiación aguda y el aumento del riesgo de efectos somáticos y
genéticos. Realice la ablación con catéter sólo después de haber valorado adecuadamente la
posible exposición a radiación asociada con el procedimiento y de haber adoptado las medidas
necesarias para reducir al mínimo dicha exposición. Valore detenidamente la utilización del
dispositivo en mujeres embarazadas y evite exponerlas a los rayos X.
5 Reacciones adversas
Algunas de las posibles reacciones adversas asociadas a la canulación de vasos periféricos y a
la colocación intracardíaca del introductor y del dilatador son, entre otras, las siguientes:
• complicaciones en el lugar de acceso
(hematoma, infección, trombosis, equimosis, fístula arteriovenosa, hemorragia en el
lugar de punción, hemorragia)
• embolia gaseosa
• arritmia (fibrilación auricular, aleteo auricular, taquicardia ventricular)
• parada cardíaca
• molestias, dolor u opresión torácicos
• espasmo, disección o trombosis coronarios
• muerte
• endocarditis
• bloqueo cardíaco que requiere un marcapasos permanente
• hemotórax
• infarto de miocardio
• perforación del tejido cardíaco o circundante
• derrame o taponamiento pericárdico
• pericarditis
• derrame pleural
• neumotórax
• seudoaneurisma
• edema pulmonar
• embolia pulmonar
• ictus
• trombo
• accidente isquémico transitorio (AIT)
• reacción vasovagal
6 Instrucciones de uso
Nota: Antes de introducir el introductor en el paciente, compruebe el mecanismo de deflexión
para asegurarse de que funciona correctamente.
1. Utilizando una técnica aséptica, cree un acceso vascular con un introductor apropiado.
2. Inser te una guía compatible (consulte la sección Especificaciones) a través de la
vasculatura hasta la posición que desee empleando técnicas convencionales de acceso
vascular.
3. Lave el puerto lateral del introductor y la luz del dilatador con solución salina estéril.
4. Asegúrese de que el introductor se encuentra en una posición neutra (sin deflexión) y
humedezca el cuerpo del dilatador con solución salina estéril antes de insertarlo a través de
la válvula hemostática.
5. Comience a ensamblar el dilatador y el introductor introduciendo la punta distal del dilatador
en la válvula hemostática de manera que el borde curvo del dilatador esté perpendicular a
la válvula hemostática (consulte la Figura 2).
Figura 2. Introductor dirigible FlexCath Select
6. Continúe haciendo avanzar el dilatador en el introductor hasta que el conector del dilatador
encaje firmemente en el conector del introductor.
Nota: La etiqueta del conector del dilatador debe estar en línea con la etiqueta del mango
del introductor de manera que la curva del dilatador esté alineada en la misma orientación
de la dirección de deflexión del introductor y con el puerto lateral (consulte la Figura 3).
Figura 3. Introductor dirigible FlexCath Select
7. Pase el conjunto dilatador-introductor sobre la guía hasta el interior de la vasculatura con un
ligero movimiento de giro para introducirlo en la vena cava superior.
8. Retire la guía.
9. Inser te la aguja transeptal debidamente preparada en el conjunto dilatador-introductor de
manera que el indicador de curvatura de la aguja transeptal esté alineado con el puerto
lateral.
Nota: La aguja transeptal debe usarse junto con un fiador para evitar cortar la luz interior del
dilatador.
21
Español

10. Introduzca el conjunto en la aurícula derecha como preparación para la punción transeptal.
11. Con seguimiento fluoroscópico, realice la punción transeptal utilizando mediciones de
presión, inyección de contraste o ambos. Confirme la colocación correcta en la aurícula
izquierda.
12. Tire de la aguja transeptal al interior del dilatador y extraiga lentamente el conjunto
dilatador-aguja del introductor.
Nota: Retire lentamente el dilatador para reducir la posibilidad de crear un vacío en el
introductor. La sangre debería aspirarse libremente a través del puerto lateral. Si no es así,
retire el introductor porque es posible que la punta del introductor esté en contacto con la
pared de la aurícula o de una vena pulmonar.
13. Aspire sangre a través del puerto lateral y asegúrese de que el introductor no contiene aire.
Aspire o espere a que refluya sangre de forma espontánea antes de insertar un catéter en
el introductor.
Nota: Realice este paso después de todo cambio de catéter.
14. Tras lograr el acceso con el introductor, mantenga el tratamiento anticoagulante.
15. Prepare el catéter según las instrucciones de uso del fabricante.
16. Inser te el catéter y sitúe el introductor.
Notas:
• Humedecer el cuerpo del catéter puede facilitar la inserción.
• La válvula hemostática tiene un tope positivo para evitar que algún dispositivo de
captura abra el sellado.
• Inserte y retire siempre los componentes lentamente a fin de reducir al mínimo el vacío
creado.
• El introductor también debe lavarse mientras se introduce un catéter.
17. Antes de retirar el introductor, asegúrese de que se encuentra en la posición neutra (sin
deflexión).
7 Especificaciones
Longitud total
Longitud útil 65 cm (25,6 in)
Diámetro interno 3,3 mm (10 Fr) (0,13 in)
Diámetro externo 4,3 mm (13 Fr) (0,17 in)
Longitud del dilatador 86 cm (33,9 in)
Marca radiopaca 5 mm (0,2 in) proximal a la punta del introductor
Compatibilidad de la guía 0,81 mm (0,032 in) a 0,89 mm (0,035 in)
Compatibilidad de la aguja tran-
septal
Parámetros ambientales
Temperatura de transporte
recomendada
Temperatura de almacenamiento recomendada
Funcionamiento 15°C a 30°C (59°F a 86°F) a altitudes inferiores a 2.400 m
81 cm (31,9 in)
89 cm (35,0 in) o más larga
−35°C a 58°C (−31°F a 136°F); humedad relativa del 85 % (sin
condensación)
Media de 22°C (72°F) con una desviación estándar de 2,7°C
(4,86°F) y límites de control aplicables de 15°C a 30°C (59°F
a 86°F)
(8.000 pies) sobre el nivel del mar
8 Renuncia de responsabilidad de Medtronic
Para obtener información completa acerca de la garantía, consulte el documento de renuncia de
responsabilidad adjunto.
9 Reparación
Medtronic cuenta con representantes y técnicos muy cualificados en todo el mundo para servir
al cliente y proporcionar, bajo demanda, formación sobre la utilización de los productos de
Medtronic a personal hospitalario cualificado. Además, Medtronic dispone de un equipo de
profesionales para proporcionar ayuda técnica a los usuarios de sus productos. Para obtener
más información, póngase en contacto con el representante local de Medtronic, o bien llame o
escriba a Medtronic al número de teléfono o la dirección adecuados que figuran en la
contraportada.
Español
22

1 Kuvaus
65 cm
(25,6 in)
16 cm
(6,3 in)
86 cm
(33,9 in)
Ohjattava Medtronic FlexCath™ Select -holkki on perkutaanisen katetrin sisäänviejä, jossa on
venttiili. Venttiili mahdollistaa katetrien ja vaijereiden sisäänviennin, poiston ja vaihdon ja minimoi
samalla verenhukan. Siinä on sulkuhanallinen sivuportti, jota käytetään jatkuvaan
tippainfuusioon, injektioon keskiluumenin kautta, huuhteluun, aspirointiin, verinäytteiden ottoon
ja paineenvalvontaan.
Kuva 1. Ohjattava FlexCath Select -holkki
Ohjattavan FlexCath Select -holkin pakkauksessa on mukana laajennin. Holkki kuvataan
seuraavassa taulukossa:
Malli
990065 3,3 mm (10 Fr)
Holkkia voidaan taivuttaa, jotta katetreja on helpompi ohjata, kun niitä työnnetään holkin läpi ja
sydämen oikeaan tai vasempaan lokeroon.
10 Fr:n ohjattavan FlexCath Select -holkin kanssa voidaan käyttää Medtronic-yhtiön diagnostisia
katetreja ja ablaatiokatetreja, joiden koko on enintään 9 Fr.
10 Fr:n ohjattavan FlexCath Select -holkin laajennin on yhteensopiva 89 cm:n ja sitä pitempien
transseptaalisten Merit Medical HeartSpan -neulojen kanssa.
Sisäläpimitta Ulkoläpimitta Käyttöpituus
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Pakkauksen sisältö
Ohjattava FlexCath Select -holkki toimitetaan steriilinä. Pakkauksessa on seuraavat osat:
• 1 ohjattava holkki
• 1 laajennin
• tuotedokumentaatio.
2 Käyttöaiheet
Ohjattava FlexCath Select -holkki on tarkoitettu perkutaanisen katetrin sisäänvientiin verisuoniin
ja sydämen lokeroihin, myös sydämen vasempaan puoliskoon eteisväliseinän läpi. Holkin
taivuttaminen helpottaa katetrin asettamista.
3 Vasta-aiheet
Ohjattavan FlexCath Select -holkin asettaminen vasempaan eteiseen tai kammioon on
vasta-aiheista, jos potilaalla on jokin seuraavista tiloista:
• Potilaalla on eteisväliseinän paikka tai sulkulaite, tai hänelle on tehty muu eteisväliseinän tai
sen viereisen rakenteen kirurginen toimenpide.
• Potilaalla on vasemman eteisen trombi.
• Potilaalla tiedetään tai epäillään olevan eteismyksooma.
4 Vaarat ja varotoimet
Ablaatioenergia – Kun holkkia käytetään ablaatioenergian käytön aikana, on huolehdittava, että
kaikki ablaatio-osat ovat holkin ulkopuolella.
Ilman aspirointi – Poista ohjainvaijeri holkista ennen holkin aspirointia ja huuhtelua. Tämä
toimenpide minimoi ilman aspiroinnin holkin venttiilin läpi.
Antikoagulaatiohoito – Anna sopiva annos antikoagulaatiohoitoa ennen toimenpidettä, sen
aikana ja sen jälkeen potilaille, joille tehdään sydämen vasemman puoliskon ja väliseinän
toimenpiteitä ja tietyille potilaille, joille tehdään oikean puoliskon toimenpiteitä. Minimoi
verenvuoto ja tromboottiset komplikaatiot antamalla antikoagulaatiohoitoa ennen toimenpidettä,
sen aikana ja sen jälkeen laitoksen käytännön mukaisesti.
Veren takaisinvuoto – Varmista, että sulkuhana on suljetussa asennossa huuhtelun tai
aspiroinnin jälkeen, jotta veri ei vuoda tahattomasti takaisin sivuportin läpi.
Tartuntavaarallisten jätteiden hävittäminen – Hävitä kaikki käytetyt laitteet ja steriilit osat
sairaalan käytäntöjen mukaisesti.
Varjoaineinjektio – Älä injektoi varjoainetta holkkiin injektiojärjestelmällä.
Laajentimen kiertäminen – Älä kierrä laajenninta, kun napsautat sen kiinni venttiilin kantaan tai
tämän jälkeen. Se voi johtaa laajentimen kärjen väärään kohdistukseen distaalisessa päässä
suhteessa proksimaalisen pään sivuporttiin.
Älä steriloi uudelleen – Älä steriloi laitetta uudelleen uudelleenkäyttötarkoituksessa.
Uudelleensterilointi voi heikentää laitteen rakennetta tai aiheuttaa laitteesta johtuvan
kontaminaatiovaaran, mikä voi johtaa potilaan vammautumiseen, sairastumiseen tai kuolemaan.
Emboliariski – Minkä tahansa katetrin tai holkin vieminen verenkiertoon voi aiheuttaa
ilmaemboliariskin. Ilmaembolia voi tukkia suonet ja johtaa kudosinfarktiin, jolla on vakavia
seurauksia. Ilmaemboliariski saattaa olla suurempi, jos laitteen kanssa käytetään alle 9 Fr:n
katetreja. Työnnä ja vedä osia aina hitaasti ja käytä huuhtelua, jotta syntynyt alipaine on
mahdollisimman pieni ja siitä johtuva ilmaemboliariski minimoituu.
Viimeinen käyttöpäivämäärä – Tarkista, ettei holkin viimeinen käyttöpäivämäärä ole
umpeutunut. Älä käytä tuotetta, jos sen viimeinen käyttöpäivämäärä on umpeutunut.
Reisilaskimon vaurioituminen – Minimoi reisilaskimon ja sisäänvientikohdan vauriot olemalla
huolellinen holkin sisäänviennissä, ohjauksessa ja poistossa. Reisilaskimon katetrointiin liittyviä
komplikaatioita ovat hematooma ja tromboosi.
Holkin saa asettaa vain fluoroskopiassa – Fluoroskopian käyttö on ehdottoman suositeltavaa
holkin ohjauksen ja asetuksen aikana. Holkin ohjaus ilman fluoroskopiaa voi vaurioittaa sydän- ja
verisuonirakenteita.
Tarkoitettu vain kertakäyttöön – Laite on tarkoitettu käytettäväksi vain kerran yhdelle potilaalle.
Älä käytä, käsittele tai steriloi laitetta uudelleen uudelleenkäyttötarkoituksessa.
Uudelleenkäyttö, -käsittely tai -sterilointi voi heikentää laitteen rakennetta tai aiheuttaa laitteen
kontaminaatiovaaran, mikä voi johtaa potilaan vammautumiseen, sairastumiseen tai kuolemaan.
Tiheä huuhtelu – Holkin säännöllistä huuhtelua suositellaan
• veren patoutumisen, hyytymien, embolusten ja potilaan vakavien vammojen estämiseksi
• jokaisen varjoaineinjektion jälkeen, jotta varjoaine ei tartu luumenin sisäpuolelle.
Käsittely ja hoito – Toimi näin, kun käsittelet laitetta:
• Ohjaa laitetta erittäin varovasti. Huolimattomuus voi aiheuttaa vammoja, kuten perforaation,
tamponaation, rytmihäiriöitä tai sydänkatkoksen.
• Älä käytä liikaa voimaa, kun työnnät tai vedät laitetta, etenkin jos siinä tuntuu vastusta.
• Vältä laitteen asettamista jännerihmojen alueelle, koska tällöin laite voi jäädä helpommin
kiinni sydämen sisään. Tämä voi edellyttää kirurgista toimenpidettä tai vaurioituneiden
kudosten korjaamista.
• Älä käytä holkkia, jos se on taittunut tai vaurioitunut.
Yhteys vasempaan eteiseen – Älä työnnä laajenninta tai holkkia eteisväliseinän läpi
varmistamatta ensin yhteyttä vasempaan eteiseen. Tämä estää osien työntämisen väärään
paikkaan.
Tarvittavat sairaalalaitteet – Pidä ulkoiset defibrillaatiolaitteet lähellä, jotta niitä voidaan käyttää
heti ohjattavan holkkikokoonpanon käytön aikana.
23
Suomi

Muut katetrit, laitteet tai vaijerit – Varo, ettei holkki takerru muihin katetreihin, laitteisiin tai
vaijereihin. Takertuminen voi edellyttää kirurgista toimenpidettä.
Sydänläppäproteesit – Älä vie laitetta sydänläppäproteesin (mekaanisen läpän tai kudosläpän)
läpi. Laite voi jäädä kiinni läppään ja vaurioittaa siten läppää ja aiheuttaa läppäproteesin
läppävuodon tai ennenaikaisen hajoamisen.
Pätevät käyttäjät – Laitteiden käyttö on sallittua vain sydänkatetrointitoimenpiteisiin koulutetuille
lääkäreille tai tällaisten lääkäreiden valvonnassa.
Vaadittu käyttöympäristö – Sydänkatetrointitoimenpiteitä saa tehdä vain täysin varustetussa
laitoksessa.
Sivuportin aspirointi – Aspiroi sivuporttia, kun poistat laajentimen, katetrin, neulan, vaijerit tai
muut laitteet.
Sivuportin tukkeutuminen – Huolehdi, ettei sivuportti tukkeudu, jotta keittosuolaliuoshuuhtelu
on tehokasta.
Merkittävä verenvuoto – Tarkkaile huolellisesti, ettei hemostaasiventtiilin läpi vuoda
merkittävän paljon verta toimenpiteen aikana.
Steriilin pakkauksen tarkistaminen – Tarkista steriili pakkaus ja laite ennen käyttöä. Jos
steriilissä pakkauksessa tai laitteessa on vaurioita, älä käytä laitetta. Ota yhteys paikalliseen
Medtronic-edustajaan.
Röntgenkuvaus- ja fluoroskopia-altistus – Fluoroskopian käyttö
katetriablaatiotoimenpiteiden aikana voi johtaa sekä potilaiden että laboratoriohenkilökunnan
merkittävään röntgensäteilyaltistukseen. Suuri altistus voi johtaa akuuttiin säteilyvammaan sekä
suurentaa somaattisten ja geneettisten vaikutusten riskiä. Tee katetriablaatio vasta sitten, kun
olet huomioinut asianmukaisesti toimenpiteeseen mahdollisesti liittyvän säteilyaltistuksen ja
minimoinut tämän altistuksen tarvittavin toimenpitein. Vältä raskaana olevien naisten
röntgenkuvausta ja harkitse sitä huolellisesti ennen laitteen käyttöä.
5 Haittatapahtumat
Mahdollisia haittatapahtumia, joita liittyy ääreisverisuonten kanylointiin sekä holkin ja laajentimen
asetukseen sydämen sisään, ovat muun muassa seuraavat tilat:
• sisäänvientikohdan komplikaatiot (hematooma, infektio, tromboosi, ekkymoosi,
AV-fisteli, punktiokohdan verenvuoto,
verenvuoto)
• ilmaembolia
• rytmihäiriö (eteisvärinä, eteislepatus, kammiotakykardia)
• sydämenpysähdys
• epämukava tunne, kipu tai puristus rinnassa
• sepelvaltimon kouristus, dissekoituma,
tromboosi
• kuolema
• endokardiitti
• sydänkatkos, joka edellyttää pysyvää tahdistinta
• veririnta
• sydäninfarkti
• sydänkudoksen tai ympäröivän kudoksen
puhkeaminen
• perikardiumin effuusio, tamponaatio
• perikardiitti
• pleuraeffuusio
• ilmarinta
• pseudoaneurysma
• keuhkopöhö
• keuhkoembolia
• aivohalvaus
• trombi
• ohimenevä aivoverenkiertohäiriö (TIA)
• vasovagaalinen reaktio.
6 Käyttöohjeet
Huomautus: Ennen kuin viet holkin potilaaseen, testaa taivutusmekanismia ja varmista, että se
toimii.
1. Avaa verisuoniyhteys sopivalla sisäänviejällä käyttäen aseptista tekniikkaa.
2. Vie yhteensopiva ohjainvaijeri (katso Tekniset tiedot) verisuonten läpi ja haluttuun kohtaan
tavanomaisilla sisäänvientimenetelmillä.
3. Huuhtele holkin sivupor tti ja laajenninluumen steriilillä keittosuolaliuoksella.
4. Varmista, että holkki on neutraalissa asennossa (ei taivutettuna), ja kastele laajentimen varsi
steriilillä keittosuolaliuoksella, ennen kuin viet sen hemostaasiventtiilin läpi.
5. Aloita laajentimen ja holkin kokoaminen yhteen viemällä laajentimen distaalinen kärki
hemostaasiventtiiliin niin, että laajentimen kaareva reuna on kohtisuorassa
hemostaasiventtiiliin nähden (katso Kuva 2).
Kuva 2. Ohjattava FlexCath Select -holkki
6. Jatka laajentimen työntämistä holkkiin, kunnes laajentimen kanta napsahtaa kiinni holkin
kantaan.
Huomautus: Laajentimen kannan merkinnän pitää olla kohdakkain holkin kahvan
merkinnän kanssa niin, että laajentimen kaareva osa on samansuuntainen kuin holkin
taivutussuunta ja sivuportti (katso Kuva 3).
Kuva 3. Ohjattava FlexCath Select -holkki
7. Pujota holkki-laajenninkokoonpano ohjainvaijerin päälle ja verisuoniin ja pienellä
kiertoliikkeellä yläonttolaskimoon.
8. Poista ohjainvaijeri.
9. Vie asianmukaisesti valmisteltu transseptaalinen neula holkki-laajenninkokoonpanoon niin,
että transseptaalisen neulan kaarevuusilmaisin on kohdistettu sivuporttiin.
Huomautus: Transseptaalisen neulan kanssa on käytettävä mandriinia, jotta neula ei kaavi
laajentimen sisäluumenia.
10. Vedä kokoonpano alas oikeaan eteiseen transseptaalisen punktion valmistelua varten.
11. Tee transseptaalinen punktio fluoroskopiaohjauksessa käyttämällä apuna painemittauksia,
varjoaineinjektiota tai molempia. Varmista oikea sijainti vasemmassa eteisessä.
12. Vedä transseptaalinen neula laajentimeen ja poista laajennin-neulakokoonpano hitaasti
holkista.
Huomautus: Poista laajennin hitaasti, jotta holkkiin ei muodostu alipainetta. Verta pitäisi
pystyä aspiroimaan vapaasti sivuportin kautta. Jos näin ei ole, vedä holkkia taaksepäin,
koska holkin kärki voi olla eteisen tai keuhkolaskimon seinämää vasten.
13. Aspiroi verta sivuportin kautta ja varmista, ettei holkissa ole ilmaa. Aspiroi tai anna veren
vuotaa itsestään takaisin, ennen kuin viet katetrin holkkiin.
Huomautus: Tee tämä toimenpide jokaisen katetrinvaihdon jälkeen.
14. Kun yhteys on saatu holkin avulla, ylläpidä antikoagulaatiohoitoa.
15. Valmistele katetri valmistajan toimittamien käyttöohjeiden mukaisesti.
16. Vie katetri sisään ja aseta holkki paikalleen.
Suomi
24

Huomautukset:
• Katetrin varren kasteleminen voi helpottaa sisäänvientiä.
• Hemostaasiventtiilissä on vaste, joka estää sisäänvientiapuvälineitä avaamasta
tiivistettä.
• Minimoi syntyvä alipaine työntämällä ja vetämällä osia aina hitaasti.
• Holkkia pitää myös huuhdella katetrin sisäänviennin aikana.
17. Ennen kuin vedät holkin pois, varmista, että se on neutraalissa asennossa (ei taivutettuna).
7 Tekniset tiedot
Kokonaispituus
Käyttöpituus 65 cm (25,6 in)
Sisäläpimitta 3,3 mm (10 Fr) (0,13 in)
Ulkoläpimitta 4,3 mm (13 Fr) (0,17 in)
Laajentimen pituus 86 cm (33,9 in)
Röntgenpositiivinen merkki 5 mm (0,2 in) proksimaaliseen suuntaan holkin kärjestä
Ohjainvaijerin yhteensopivuus 0,81 mm–0,89 mm (0,032 in–0,035 in)
Transseptaalisen neulan
yhteensopivuus
Ympäristöparametrit
Suositeltu kuljetuslämpötila –35°C...+58°C (–31°F...+136°F); suhteellinen ilmankosteus
Suositeltu säilytyslämpötila Keskiarvo 22°C (72°F), keskihajonta 2,7°C (4,86°F) ja toi-
Käyttäminen 15°C–30°C (59°F–86°F), kun korkeus merenpinnasta on alle
81 cm (31,9 in)
89 cm (35,0 in) tai pitempi
85 % (tiivistymätön)
menpiteitä edellyttävät valvontarajat 15°C ja 30°C (59°F ja
86°F)
2 400 m (8 000 jalkaa)
8 Medtronic-yhtiön takuuta koskeva vastuuvapauslauseke
Katso täydelliset takuutiedot mukana toimitetusta vastuuvapauslausekeasiakirjasta.
9 Huolto
Medtronic-yhtiöllä on eri puolilla maailmaa hyvin koulutettuja edustajia ja teknikoita, jotka
palvelevat käyttäjiä ja antavat pyydettäessä Medtronic-tuotteisiin liittyvää koulutusta pätevälle
sairaalahenkilökunnalle. Lisäksi Medtronic-yhtiöllä on ammattitaitoista henkilökuntaa, joka
neuvoo tuotteiden käyttäjiä teknisissä asioissa. Pyydä lisätietoja ottamalla yhteys paikalliseen
Medtronic-edustajaan tai soita tai kirjoita Medtronic-yhtiölle. Puhelinnumerot ja osoitteet ovat
takakannessa.
25
Suomi

1 Description
65 cm
(25,6 po)
16 cm
(6,3 po)
86 cm
(33,9 po)
La gaine orientable FlexCath™ Select de Medtronic est une gaine percutanée de cathéter
équipée d’une valve permettant l’introduction, le retrait et l’échange de cathéters et de fils guides
tout en minimisant les pertes sanguines. Un port latéral avec robinet est intégré pour permettre
une perfusion continue, des injections via la lumière centrale, le rinçage, l’aspiration, le
prélèvement d’échantillons sanguins et la surveillance de la tension artérielle.
Figure 1. Gaine orientable FlexCath Select
Un dilatateur est fourni avec la gaine orientable FlexCath Select. La gaine est décrite dans le
tableau suivant :
Modèle
990065 3,3 mm (10 Fr)
La gaine peut être courbée afin d’accroître la manœuvrabilité des cathéters qui sont introduits
dans la chambre droite ou gauche du cœur par la gaine.
La gaine orientable FlexCath Select de taille 10 Fr peut être utilisée avec les cathéters de
diagnostic et d’ablation de Medtronic de taille 9 Fr maximum.
Le dilatateur de la gaine orientable FlexCath Select 10 Fr est compatible avec les aiguilles
transseptales HeartSpan de 89 cm et plus de Merit Medical.
Diamètre interne Diamètre externe Longueur utile
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Contenu de l’emballage
La gaine orientable FlexCath Select est fournie stérile. L’emballage contient les éléments
suivants :
• 1 gaine orientable
• 1 dilatateur
• Documentation du produit
2 Indications d’utilisation
La gaine orientable FlexCath Select est conçue pour une introduction percutanée du cathéter
dans le système vasculaire et dans les chambres du cœur, notamment au niveau du côté gauche
du cœur à travers le septum interauriculaire. La courbure de cette gaine facilite le positionnement
du cathéter.
3 Contre-indications
La mise en place de la gaine orientable FlexCath Select dans l’oreillette ou le ventricule gauche
est contre-indiquée dans les circonstances suivantes :
• Le patient présente un patch ou un dispositif d’occlusion du septum interauriculaire, ou a subi
une autre intervention chirurgicale dans le septum interauriculaire ou dans une zone
adjacente.
• Le patient présente un thrombus atrial gauche.
• Le patient a fait l’objet d’un diagnostic ou d’une suspicion de myxome auriculaire.
4 Avertissements et précautions
Énergie d’ablation – Lorsque la gaine est utilisée avec une énergie d’ablation, il convient de
veiller à ce que tous les éléments servant à l’ablation se trouvent à l’extérieur de la gaine.
Aspiration d’air – Avant d’aspirer et de rincer la gaine, retirer le fil guide de la gaine. Cette action
minimise l’aspiration de l’air via la valve de la gaine.
Traitement anticoagulant – Administrez un traitement anticoagulant périopératoire approprié
pour les patients devant subir un cathétérisme cardiaque gauche par voie transseptale ainsi que
pour certains patients devant subir un cathétérisme cardiaque droit. Afin de minimiser les
complications hémorragiques et thrombotiques, administrez un traitement anticoagulant
périopératoire conformément aux pratiques de l’établissement.
Reflux sanguin – Vérifiez que le robinet est bien fermé après le rinçage ou l’aspiration afin de
prévenir tout reflux sanguin involontaire par le port latéral.
Élimination des risques biologiques – Jetez tous les appareils et composants stériles usagés
conformément aux procédures hospitalières.
Injection de produit de contraste - N’utilisez pas de systèmes d’injection électriques pour
l’injection de solution de contraste dans la gaine.
Torsion du dilatateur – Ne tordez pas le dilatateur lorsque vous l’enclenchez dans l’embase de
la valve ou par la suite. Cela pourrait provoquer un alignement incorrect de l’extrémité du dilatateur
à l’extrémité distale par rapport au port latéral à l’extrémité proximale.
Ne pas restériliser – Ne pas restériliser ce dispositif aux fins de le réutiliser. La restérilisation
risque de compromettre l’intégrité structurelle du dispositif ou de créer un risque de contamination
par le dispositif, ce qui pourrait entraîner des lésions, des maladies ou le décès du patient.
Risque d’embolie – L’introduction de tout cathéter ou gaine dans la circulation sanguine
comporte un risque d’aéro-embolie qui peut obstruer les vaisseaux et entraîner un infarctus
tissulaire susceptible d’avoir de graves conséquences. L’utilisation de cathéters de moins de 9 Fr
avec cet appareil peut présenter un risque accru d’aéro-embolie. Avancez et retirez
systématiquement les composants lentement, et procédez à un rinçage afin de minimiser le vide
créé, et donc le risque d’aéro-embolie.
Date de péremption – Vérifier la date de péremption de la gaine. Ne pas utiliser si la date est
passée.
Lésions de la veine fémorale – Prendre soin de minimiser les lésions occasionnées à la veine
fémorale et au site d’accès au niveau de l’insertion, de la manipulation ou du retrait de la gaine.
Les complications associées au cathétérisme de la veine fémorale sont notamment les
hématomes et les thromboses.
Radioscopie requise pour la mise en place de la gaine – Il est vivement conseillé d’utiliser le
guidage radioscopique durant la manipulation et la mise en place de la gaine. Toute manipulation
de la gaine sans guidage radioscopique peut entraîner des lésions des structures cardiaques et
vasculaires.
À usage unique exclusivement – Ce dispositif est destiné à un patient unique et doit être utilisé
une seule fois. Ne pas réutiliser, retraiter ni restériliser ce dispositif dans le but de le réutiliser. La
réutilisation, le retraitement ou la restérilisation risque de compromettre l’intégrité de la structure
du dispositif et/ou de le contaminer, ce qui pourrait entraîner des blessures, une maladie ou le
décès du patient.
Rinçage fréquent – Un rinçage régulier de la gaine est recommandé :
• pour empêcher la stagnation du sang, les caillots, les embolies et de graves blessures du
patient,
• pour éviter que la solution de contraste n’adhère dans la lumière après chaque injection de
solution de contraste.
Manipulation et entretien – Lors de la manipulation de l’appareil :
• Manipulez l’appareil avec un soin extrême afin d’éviter des lésions telles que perforation,
tamponnade, induction d’une arythmie ou bloc cardiaque.
• Ne pas forcer pour faire avancer ou retirer le dispositif, en particulier en cas de résistance.
Français
26

• Éviter de positionner le dispositif autour des cordages tendineux, car cela augmente le risque
que le dispositif reste coincé dans le cœur et peut nécessiter une intervention chirurgicale ou
la réparation des tissus lésés.
• N’utilisez pas la gaine si elle est pliée ou endommagée.
Accès atrial gauche – N’avancez pas le dilatateur ou la gaine à travers le septum interauriculaire
sans d’abord confirmer l’accès atrial gauche afin d’éviter d’avancer ces composants dans un
emplacement non souhaité.
Équipement hospitalier nécessaire – Gardez à proximité un équipement de défibrillation
externe pour usage immédiat durant l’utilisation de la gaine orientable.
Autres cathéters, appareils ou fils guides – Évitez tout enchevêtrement de la gaine avec
d’autres cathéters, appareils ou fils guides. Un tel enchevêtrement pourrait nécessiter une
intervention chirurgicale.
Prothèses valvulaires cardiaques – Ne pas faire passer le dispositif à travers une prothèse
valvulaire (mécanique ou tissulaire) afin d’éviter qu’il ne se coince dans la valve ou ne
l’endommage, ce qui pourrait entraîner une insuffisance valvulaire ou une défaillance prématurée
de la prothèse.
Utilisateurs qualifiés – Cet équipement ne doit être utilisé que par des médecins formés aux
interventions de cathétérisme cardiaque ou sous leur contrôle.
Environnement d’utilisation requis – Toutes les interventions de cathétérisme cardiaque
doivent se dérouler uniquement dans un établissement équipé de tout le matériel nécessaire.
Aspiration du port latéral – Aspirez le port latéral lors du retrait du dilatateur, du cathéter, de
l’aiguille, des fils guides ou d’autres appareils.
Obstruction du port latéral – Veiller à éviter toute obstruction du port latéral afin de garantir
l’efficacité du rinçage par la solution saline.
Fuites sanguines importantes – Vérifiez l’absence de fuites de sang importantes via la valve
hémostatique au cours de la procédure.
Inspection de l’emballage stérile – Inspecter l’emballage stérile et le dispositif avant utilisation.
Si l’emballage stérile ou l’appareil semble endommagé, n’utilisez pas l’appareil. Contactez votre
représentant local de Medtronic.
Exposition aux rayons X et à la radioscopie – L’utilisation de la fluoroscopie pendant les
interventions d’ablation par cathéter présente un risque d’exposition importante aux rayons X à la
fois pour les patients et le personnel du laboratoire. Une exposition importante peut entraîner une
lésion par irradiation aiguë et un risque accru d’effets somatiques et génétiques. N’effectuer
l’ablation par cathéter qu’après avoir examiné l’exposition possible aux radiations pendant
l’intervention et avoir pris les mesures nécessaires pour limiter cette exposition. Il convient d’en
tenir particulièrement compte et d’éviter toute exposition aux rayons X avant d’utiliser
l’équipement chez la femme enceinte.
5 Effets indésirables
Les éventuels effets secondaires associés à la canulation du système vasculaire périphérique et
la mise en place intracardiaque de la gaine et du dilatateur sont, entre autres, les suivants :
Complications au site d’accès (hématome,
•
infection, thrombose, ecchymose, fistule
artério-veineuse, saignement du site
d’injection, hémorragie)
• Aéro-embolie
• Arythmie (fibrillation atriale, flutter atrial,
tachycardie ventriculaire)
• Arrêt cardiaque
• Gêne, douleur ou pression thoracique
• Spasme, dissection ou thrombose coronaire
• Décès
• Endocardite
• Bloc cardiaque nécessitant l’implantation
d’un stimulateur cardiaque permanent
• Hémothorax
• Infarctus du myocarde
• Perforation du tissu cardiaque ou environnant
• Épanchement péricardique, tamponnade
• Péricardite
• Épanchement pleural
• Pneumothorax
• Pseudo-anévrisme
• Œdème pulmonaire
• Embolie pulmonaire
• Accident vasculaire cérébral
• Thrombus
• Attaque ischémique transitoire
• Réaction vasovagale
6 Mode d’emploi
Remarque : Avant d’introduire la gaine dans le corps du patient, testez le bon fonctionnement du
mécanisme de courbure.
1. En utilisant une technique aseptique, créer un accès vasculaire à l’aide d’un introducteur
approprié.
2. Insérer un fil guide compatible (voir les spécifications) par le système vasculaire et dans la
position souhaitée en utilisant les techniques d’accès vasculaire standard.
3. Rincez la lumière du port latéral de la gaine et du dilatateur avec une solution saline stérile.
4. Assurez-vous que la gaine est en position neutre (non courbée) et trempez la tige du
dilatateur dans une solution saline stérile avant de l’insérer par la valve hémostatique.
5. Commencez à assembler le dilatateur et la gaine en introduisant l’extrémité distale du
dilatateur dans la valve hémostatique de sorte que le bord courbe du dilatateur soit
perpendiculaire à la valve hémostatique (voir Figure 2).
Figure 2. Gaine orientable FlexCath Select
6. Continuez à faire progresser le dilatateur dans la gaine jusqu’à ce que l’embase du dilatateur
s’enclenche et se verrouille dans l’embase de la gaine.
Remarque : L’étiquette sur l’embase du dilatateur doit être alignée avec l’étiquette sur le
manche de la gaine de sorte que la courbe du dilatateur soit alignée dans la même direction
que la courbure de la gaine et le port latéral (voir Figure 3).
Figure 3. Gaine orientable FlexCath Select
7. Enfilez l’ensemble gaine/dilatateur par-dessus le fil guide et dans le système vasculaire en
appliquant un léger mouvement de torsion au niveau de la VCS.
8. Retirez le fil guide.
9. Insérez l’aiguille transseptale correctement préparée dans l’ensemble gaine/dilatateur de
sorte que l’indicateur de courbure sur l’aiguille transseptale soit aligné avec le port latéral.
Remarque : L’aiguille transseptale doit être utilisée avec un mandrin afin d’éviter de couper
la lumière interne du dilatateur.
10. Tirer l’ensemble vers le bas afin de le placer dans l’oreillette droite pour préparer la ponction
transseptale.
11. Sous guidage fluoroscopique, réaliser la ponction transseptale en utilisant des mesures de
la tension artérielle, l’injection d’un produit de contraste ou les deux. Vérifiez le placement
correct dans l’oreillette gauche.
27
Français

12. Tirez l’aiguille transseptale dans le dilatateur et retirez lentement l’ensemble
dilatateur/aiguille de la gaine.
Remarque : Retirez lentement le dilatateur pour réduire le risque de création d’un vide dans
la gaine. Le sang doit être librement aspiré par le port latéral. Si ce n’est pas le cas, retirer la
gaine, car il se peut que son extrémité appuie contre la paroi de l’oreillette ou une veine
pulmonaire.
13. Aspirer le sang par le port latéral et vérifier l’absence d’air dans la gaine. Procédez à
l’aspiration ou au reflux sanguin spontané avant d’insérer un cathéter dans la gaine.
Remarque : Effectuez cette étape après tous les échanges de cathéter.
14. Une fois l’accès ouvert via la gaine, maintenez le traitement anticoagulant.
15. Préparez le cathéter conformément au mode d’emploi du fabricant.
16. Insérez le cathéter et positionnez la gaine.
Remarques :
• L’humectation du corps du cathéter peut aider à faciliter l’insertion.
• La valve hémostatique dispose d’une butée positive pour éviter qu’un dispositif de
capture quelconque n’ouvre le joint.
• Afin de minimiser le vide créé, insérez et retirez systématiquement les composants
lentement.
• La gaine devrait également être rincée lors de l’insertion d’un cathéter.
17. Avant le retrait de la gaine, s’assurer qu’elle est en position neutre (non courbée).
7 Caractéristiques techniques
Longueur totale
Longueur utile 65 cm (25,6 in)
Diamètre interne 3,3 mm (10 Fr) (0,13 in)
Diamètre externe 4,3 mm (13 Fr) (0,17 in)
Longueur du dilatateur 86 cm (33,9 in)
Marqueur radio-opaque 5 mm (0,2 in) en proximalité de l’extrémité de la gaine
Compatibilité avec les fils gui-
des
Compatibilité avec les aiguilles
transseptales
Paramètres environnementaux
Température de transport
recommandée
Température de stockage
recommandée
Fonctionnement 15°C à 30°C (59°F à 86°F) à des altitudes inférieures à 2400 m
81 cm (31,9 in)
0,81 mm (0,032 in) à 0,89 mm (0,035 in)
89 cm (35,0 in) ou plus
–35°C à 58°C (–31°F à 136°F) ; humidité relative de 85% (sans
condensation)
Moyenne de 22°C (72°F) avec écart type de 2,7°C (4,86°F) et
limites d’intervention de 15°C à 30°C (59°F à 86°F)
(8000 pieds) au-dessus du niveau de la mer
8 Déni de garantie de Medtronic
Pour obtenir des informations complètes sur la garantie, référez-vous au document de déni de
garantie joint.
9 Entretien
Medtronic emploie des représentants et des ingénieurs hautement formés dans le monde entier
afin d’assister les utilisateurs et, sur demande, de dispenser des formations à l’intention du
personnel hospitalier qualifié sur l’utilisation des produits de Medtronic. Medtronic dispose aussi
de conseillers professionnels chargés de fournir une assistance technique aux utilisateurs de
produits. Pour plus d’informations, contactez votre représentant local de Medtronic ou contactez
Medtronic par téléphone ou par écrit. Les coordonnées figurent au dos du manuel.
Français
28

1 Leírás
65 cm
(25,6 inch)
16 cm
(6,3 inch)
86 cm
(33,9 inch)
A Medtronic FlexCath™ Select irányítható hüvely perkután katéterbevezető eszköz. Szeleppel
látták el, amely lehetővé teszi a katéterek és drótok bevezetését, visszahúzását és kicserélését,
miközben a lehető legkisebbre csökkenti a vérveszteséget. Az eszközbe zárócsapos oldalsó
csatlakozót építettek, amely lehetővé teszi a folyamatos cseppinfúzió-beadást, a középső
lumenen keresztüli befecskendezést, az öblítést, a folyadékfelszívást, vérminták levételét és a
nyomásellenőrzést.
1. ábra. FlexCath Select irányítható hüvely
A FlexCath Select irányítható hüvelyhez egy tágítót is mellékeltünk. A hüvely adatait az alábbi
táblázat tartalmazza:
Típus
990065 3,3 mm (10 Fr)
A hüvely meghajlítható, ami tovább növeli a hüvelyen át a szív jobb vagy bal üregébe felvezetett
katéterek irányíthatóságát.
A 10 Fr méretű FlexCath Select irányítható hüvelyek legfeljebb 9 Fr méretű Medtronic
diagnosztikai és ablációs katéterekkel használhatók.
A 10 Fr méretű FlexCath Select irányítható hüvelyhez tartozó tágító a legalább 89 cm-es Merit
Medical HeartSpan transzszeptális tűkkel kompatibilis.
Belső átmérő Külső átmérő Hasznos hossz
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 A csomag tartalma
A FlexCath Select irányítható hüvelyt sterilen szállítjuk. A csomag az alábbi tételeket tartalmazza:
• 1 db irányítható hüvely
• 1 db tágító
• termékdokumentáció
2 Alkalmazási terület
A FlexCath Select irányítható hüvely alkalmazási területe a katéterek perkután bevezetése az
érrendszerbe és a szív üregeibe, ideért ve a szív bal oldalába a pitvari szeptumon keresztül történő
bevezetést is. A hüvely meghajlítása megkönnyíti a katéter pozicionálását.
3 Ellenjavallatok
A FlexCath Select irányítható hüvely bal pitvarba vagy kamrába történő behelyezése ellenjavallt,
ha a betegre vonatkozóan a következők bármelyike fennáll:
• A beteg pitvari foltplasztikát vagy okkludert visel, vagy egyéb sebészi beavatkozáson esett át
a pitvari szeptumon vagy annak közvetlen közelében.
• A betegnek bal pitvari thrombusa van.
• A betegnek ismert vagy feltételezett pitvari mixómája van.
4 Figyelmeztetések és előírások
Ablációs energia – Ha a hüvelyt ablációs energia jelenlétében használja, ügyelnie kell arra, hogy
az összes ablációs elem a hüvelyen kívül legyen.
A levegő kiszívása – A hüvely visszaszívása és öblítése előtt távolítsa el a hüvelyből a
vezetődrótot. Ezzel a lehető legkisebbre csökkentheti a hüvely szelepén át bejutó levegő
mennyiségét.
Antikoaguláns kezelés – A beavatkozás körüli időszakban alkalmazzon megfelelő
antikoaguláns kezelést azokon a betegeken, akiknek a szívén bal oldali és transzszeptális
beavatkozásokat hajtanak végre, és egyes esetekben olyan betegeken is, akiken jobb oldali
beavatkozásokat végeznek. A beavatkozás alatt és után alkalmazzon az intézmény előírásainak
megfelelő antikoaguláns kezelést, ezáltal a lehető legkisebbre csökkentve a vérzést és a
trombotikus szövődményeket.
Vérvisszafolyás – Az oldalsó csatlakozón keresztüli, véletlen vérvisszafolyás megelőzése
érdekében az átöblítést vagy aspirációt követően ügyeljen arra, hogy a zárócsap zárva legyen.
A biológiai veszélyt jelentő anyagok ártalmatlanítása – Minden használt eszközt és steril
alkotóelemet a kórházi eljárásoknak megfelelően ártalmatlanítson.
A kontrasztanyag befecskendezése – A kontrasztanyagnak a hüvelybe való
befecskendezéséhez ne használjon motoros injekciós rendszert.
A tágító elfordítása – A szelepcsatlakozóba történő bepattintás alatt vagy után ne fordítsa el a
tágítót. Ezzel ugyanis a tágítónak a disztális végen lévő hegye elmozdulhat a proximális végen
lévő oldalsó csatlakozóhoz viszonyítva.
Ne sterilizálja újra – Ezt az eszközt tilos ismételt felhasználás céljából újrasterilizálni. Az
újrasterilizálás károsíthatja az eszköz szerkezeti épségét, illetve az eszköz által okozott fertőzés
veszélyét hordozhatja magában, ami a beteg sérülését, megbetegedését vagy halálát okozhatja.
Az embólia kockázata – Bármilyen katéternek vagy hüvelynek a keringési rendszerbe történő
bevezetése magában hordozza a légembólia kockázatát, ami érelzáródást okozhat, és súlyos
következményekkel járó szövetelhaláshoz vezethet. A légembólia fokozott kockázata áll fenn, ha
ezt az eszközt 9 Fr méretnél kisebb katéterekkel használja. Az alkotóelemeket mindig lassan tolja
előre és húzza vissza, és alkalmazzon átöblítést, hogy a lehető legkisebbre csökkentse a
keletkező vákuumot és ezáltal a légembólia kockázatát.
Lejárati idő – Ellenőrizze, hogy a hüvely nem lépte-e túl a lejárati idejét. Ne használja fel a
terméket a lejárati idején túl.
A combvisszér sérülése – Óvatosan kell eljárni annak érdekében, hogy a lehető legkisebbre
csökkentse a combvisszér és a behatolási hely sérülését a hüvely behelyezése, mozgatása vagy
visszahúzása közben. A combvisszér katéterezésével kapcsolatos szövődmények között
szerepel a vérömleny és a trombózis.
A hüvely elhelyezéséhez képalkotásos műveletkövetés szükséges – A hüvely mozgatása
és elhelyezése közben erősen ajánlott a röntgenátvilágítás alkalmazása. A hüvely
röntgenátvilágítás nélkül történő mozgatása károsíthatja a szív és az érrendszer anatómiai
képleteit.
Kizárólag egyszeri használatra – Ezt az eszközt kizárólag egy betegen, egy alkalommal
történő felhasználásra szánták. Ezt az eszközt tilos újrafelhasználás céljából ismételten
felhasználni, újrafeldolgozni vagy újrasterilizálni. Az ismételt felhasználás, az újrafeldolgozás
vagy az újrasterilzálás károsíthatja az eszköz szerkezeti épségét, illetve az eszköz
fertőződésének veszélyét hordozhatja magában, ami a beteg sérülését, megbetegedését vagy
halálát okozhatja.
Gyakori öblítés – A hüvely rendszeres öblítése ajánlott:
• annak érdekében, hogy megelőzzük a vérpangást, a véralvadékok képződését, az
embólusokat és a beteg súlyos sérülését;
• minden egyes kontrasztanyag-injekció után a kontrasztanyagoldat lumenbe történő
beragadásának megelőzésére.
Kezelés és gondozás – Az eszköz kezelésekor :
29
Magyar

• Különösen óvatosan járjon el az eszköz mozgatása közben. A kellő figyelem hiánya sérülést,
például perforációt, tamponádot okozhat, valamint aritmiát és szívblokkot is kiválthat.
• Ne alkalmazzon túlzott erőt az eszköz előretolása vagy visszahúzása közben, különösen
akkor, ha ellenállást érez.
• Kerülje az eszköznek az ínhúrok közelében történő elhelyezését, mivel ez megnöveli az
eszköz szívbe történő beszorulásának valószínűségét, ami sebészi beavatkozást vagy a
sérült szövetek helyreállítását teheti szükségessé.
• Ne használja a hüvelyt, ha az meghurkolódott vagy sérült.
Bal pitvari hozzáférés – Csak azt követően vezesse be a tágítót vagy a hüvelyt az interatriális
szeptumon keresztül, hogy előbb ellenőrizte a bal pitvari hozzáférést, hogy megelőzze ezen
alkotóelemeknek a bejutását nem kívánt területekre.
Szükséges kórházi felszerelés – Az irányítható hüvely eszközegyüttesének alkalmazása során
legyen készenlétben azonnal használható külső defibrillátor.
Egyéb katéterek, eszközök és huzalok – Kerülje el, hogy a hüvely összeakadjon egyéb
katéterekkel, eszközökkel vagy huzalokkal. Az ilyen összeakadás sebészi beavatkozást tehet
szükségessé.
Műbillentyűk – Ne vezesse át az eszközt sem mechanikai, sem szövetalapú műbillentyűn. Az
eszköz beszorulhat a billentyűbe, ami ezáltal megsérülhet, ami billentyűelégtelenséghez vagy a
műbillentyű idő előtti meghibásodásához vezethet.
Szakképzett felhasználók – Ezt az eszközt kizárólag szívkatéterezési beavatkozásokban jártas
orvosok, illetve a felügyeletük alatt dolgozó orvosok használhatják.
Előírt használati környezet – Szívkatéterezést csak teljesen felszerelt létesítményben szabad
végezni.
Az oldalsó csatlakozás aspirációja – A tágító, katéter, tű, huzalok vagy más eszközök
visszahúzásakor aspirálja az oldalsó csatlakozót.
Az oldalsó csatlakozó elzáródása – Ügyeljen arra, hogy megelőzze az oldalsó csatlakozó
mindennemű elzáródását, és ezáltal biztosítsa a fiziológiás sóoldattal történő folyamatos öblítést.
Jelentős vérszivárgás – Gondosan figyelje, hogy a beavatkozás közben nincs-e jelentős
vérszivárgás a vérzésgátló szelepen keresztül.
Steril csomag ellenőrzése – Használat előtt szemrevételezéssel ellenőrizze a steril
csomagolást és az eszközt. Ne használja fel az eszközt, ha sérülés látható rajta vagy a steril
csomagoláson. Forduljon a helyi Medtronic képviselethez.
A röntgensugár vagy a röntgenátvilágítás sugárterhelése – A katéteres ablációs eljárások
során alkalmazott röntgenátvilágítás miatt a betegek és a laboratóriumi személyzet is jelentős
röntgensugárzásnak lehet kitéve. A nagy terhelés akut, sugár okozta sérüléshez vezethet,
valamint a testi és genetikai hatások kockázatát is megnövelheti. Csak akkor végezze el a
katéteres ablációt, amikor már kellően figyelembe vette az eljárással együtt járó sugárterhelést,
és megtette a lépéseket a terhelés minimalizálására. Az eszköz terhes nők esetében történő
alkalmazása előtt gondosan mérlegelje a körülményeket, kerülve a röntgensugárzásnak való
kitételt.
5 Szövődmények
A perifériás érrendszer kanülálásával és a hüvely, illetve a tágító intrakardiális behelyezésével
kapcsolatos lehetséges szövődmények többek között a következők lehetnek:
a bevezetési hellyel kapcsolatos kompliká-
•
ciók (vérömleny, fertőzés, trombózis, véraláfutás, arteriovenózus fisztula, vérzés a
punkciós helyen, vérzés)
• légembólia
• aritmia (pitvarfibrilláció, pitvarlebegés,
kamrai tachycardia)
• szívmegállás
• mellkasi szorítóérzés, fájdalom vagy nyomásérzés
• koszorúérgörcs, disszekció, trombózis
• halál
• szívbelhártya-gyulladás
• állandó pacemaker beültetését szükségessé tevő szívblokk
• vérömleny a mellüregben
• szívinfarktus
• a szív vagy a környező szövetek perforációja
• perikardiális folyadékgyülem, tamponád
• szívburokgyulladás
• mellhártya-folyadékgyülem
• légmell
• álaneurizma
• tüdőödéma
• tüdőembólia
• stroke
• trombus
• átmeneti vérellátási zavar (TIA)
• vasovagalis reflex
6 Használati utasítás
Megjegyzés: A hüvely betegbe történő bevezetése előtt a hajlítómechanizmus ellenőrzésével
győződjön meg annak megfelelő működéséről.
1. Aszeptikus technika alkalmazásával és egy megfelelő bevezetőeszközzel hozzon létre
érhozzáférést.
2. A szokásos érhozzáférési technikák alkalmazásával helyezzen be egy kompatibilis
vezetődrótot (lásd a Műszaki adatok című pontot) az érrendszeren keresztül a kívánt
pozícióba.
3. Öblítse át steril fiziológiás sóoldattal a hüvely oldalsó csatlakozóját és az értágító lumenét.
4. Győződjön meg arról, hogy a hüvely semleges (meg nem hajlított) helyzetben van, és a
vérzésgátló szelepen keresztül történő behelyezés előtt nedvesítse meg az értágító szárát
steril fiziológiás sóoldattal.
5. A tágító és a hüvely összeillesztésének megkezdéséhez vezesse be a tágító disztális végét
a vérzésgátló szelepbe úgy, hogy a tágító széle merőleges legyen a vérzésgátló szelepre
(lásd: 2. ábra).
2. ábra. FlexCath Select irányítható hüvely
6. Folytassa a tágítónak a hüvelybe való előretolását addig, amíg a tágító csatlakozófeje jól
érzékelhetően a helyére nem pattan a hüvely csatlakozófejében.
Megjegyzés: A tágító csatlakozófején a címke essen egy vonalba a hüvelynyélen lévő
címkével ahhoz, hogy a tágító ívelt része azonos irányban álljon a hüvely meghajlásának az
irányával, valamint az oldalsó csatlakozóval (lásd: 3. ábra).
3. ábra. FlexCath Select irányítható hüvely
7. Enyhe csavaró mozdulattal csavarja rá a hüvely és a tágító együttesét a vezetődrótra, majd
be a vena cava superiorba.
8. Húzza ki a vezetődrótot.
9. Helyezze be a megfelelően előkészített transzszeptális tűt a hüvely és a tágító együttesébe
úgy, hogy a transzszeptális tűn lévő görbületjelző az oldalsó csatlakozóhoz igazodjon.
Megjegyzés: A transzszeptális tűt javasolt vezetőszondával együtt használni, hogy a tágító
belső lumene ne súrolódjon.
Magyar
30

10. Húzza le az eszközegyüttest a jobb pitvarba, ezzel előkészítve a transzszeptális punkciót.
11. Röntgenátvilágítás mellett végezze el a transzszeptális punkciót nyomásmérések,
kontrasztanyag-befecskendezés vagy mindkettő segítségével. Győződjön meg a megfelelő
pozicionálásról a bal pitvarban.
12. Húzza bele a transzszeptális tűt a tágítóba, majd lassan húzza ki a tágító és tű együttesét a
hüvelyből.
Megjegyzés: A tágító kihúzását lassan végezze, így kevésbé valószínű, hogy vákuum jön
létre a hüvelyben. A vérnek az oldalsó csatlakozón szabadon kell átjutnia. Ha nincs szabad
átfolyás, ki kell húzni a hüvelyt, mert annak vége valószínűleg a pitvar falának vagy egy
tüdővénának nyomódik.
13. Szívjon vissza vért az oldalsó csatlakozón át, és győződjön meg arról, hogy a hüvelyben nem
maradt levegő. Mielőtt katétert vezetne a hüvelybe, végezzen visszaszívást, vagy tegyen
lehetővé spontán vérvisszafolyást.
Megjegyzés: Minden katétercserét követően végezze el ezt a lépést.
14. A hüvely sikeres behelyezését követően gondoskodjon az antikoaguláns kezelés
fenntartásáról.
15. Készítse elő a katétert a gyártó által biztosított használati utasítást követve.
16. Helyezze be a katétert, és irányítsa a megfelelő pozícióba a hüvelyt.
Megjegyzések:
• A behelyezést megkönnyítheti a katéterszár megnedvesítése.
• A vérzésgátló szelep része egy továbbhaladást gátló ütközőelem, amely
megakadályozza, hogy a befogóeszközök megsértsék a tömítést.
• Hogy minél kisebb vákuum keletkezzen, az egyes alkotóelemek behelyezését és
visszahúzását mindig lassan végezze.
• A hüvely a katéter behelyezésének ideje alatt is öblíthető.
17. A hüvely visszahúzása előtt győződjön meg arról, hogy a hüvely semleges (meg nem
hajlított) helyzetben van.
7 Műszaki adatok
Teljes hossz
Hasznos hossz 65 cm (25,6 in)
Belső átmérő 3,3 mm (10 Fr) (0,13 in)
Külső átmérő 4,3 mm (13 Fr) (0,17 in)
Az értágító hossza 86 cm (33,9 in)
Sugárfogó jelölés 5 mm (0,2 in) proximálisan a hüvely hegyétől
A vezetődrót kompatibilitása 0,81 mm (0,032 in) és 0,89 mm (0,035 in) között
Az eszközzel használható
transzszeptális tű
Környezeti paraméterek
Ajánlott szállítási hőmérséklet
Ajánlott tárolási hőmérséklet 22°C (72°F) átlaghőmérséklet 2,7°C (4,86°F) szórással, vala-
Működtetés 15°C és 30°C (59°F és 86°F) között, 2400 m-es (8000 láb)
81 cm (31,9 in)
legalább 89 cm (35,0 in) hosszú
−35°C és 58°C (−31°F és 136°F) között; 85% (nem kondenzálódó) relatív páratartalmon
mint 15°C és 30°C (59°F és 86°F) közötti határértékekkel,
melyeken kívül be kell avatkozni
tengerszint feletti magasság alatt
8 A Medtronic szavatossági nyilatkozata
A szavatosságra vonatkozó teljes információ tekintetében lásd a mellékelt, szavatosságra
vonatkozó dokumentumot.
9 Szerviz
A Medtronic magasan képzett képviselői és mérnökei az egész világon rendelkezésre állnak, és
külön kérésre oktatást tartanak a szakképzett kórházi személyzet számára a Medtronic
termékeinek használatáról. A Medtronic ezenkívül olyan szakembereket is alkalmaz, akik
szakmai tanácsokkal segítik a termék felhasználóit. További információért forduljon a Medtronic
helyi képviselőjéhez, illetve telefonáljon vagy írjon a Medtronic részére. A telefonszámok és címek
a hátsó borítón találhatók.
31
Magyar

1 Descrizione
65 cm
(25,6 in)
16 cm
(6,3 in)
86 cm
(33,9 in)
L’introduttore orientabile FlexCath™ Select di Medtronic è un introduttore per catetere
percutaneo dotato di una valvola per consentire l’introduzione, l’estrazione e lo scambio dei
cateteri e dei fili riducendo al minimo la perdita di sangue. Una porta laterale con rubinetto è
integrata per consentire l’infusione continua goccia a goccia, l’iniezione attraverso il lume
centrale, l’irrigazione, l’aspirazione, il campionamento sanguigno e il monitoraggio della
pressione.
Figura 1. Introduttore orientabile FlexCath Select
Unitamente all’introduttore orientabile FlexCath Select viene fornito anche un dilatatore. Le
caratteristiche dell’introduttore sono illustrate nella seguente tabella:
Modello
990065 3,3 mm (10 Fr)
È possibile flettere l’introduttore per migliorare la manovrabilità dei cateteri che vengono fatti
avanzare attraverso l’introduttore e all’interno della camera cardiaca destra o sinistra.
L’introduttore orientabile FlexCath Select da 10 Fr può essere utilizzato con cateteri diagnostici e
per ablazione Medtronic di dimensioni massime pari a 9 Fr.
Il dilatatore per introduttore orientabile FlexCath Select da 10 Fr è compatibile con gli aghi
transettali Merit Medical HeartSpan da 89 cm o di lunghezza maggiore.
Diametro interno Diametro esterno Lunghezza utile
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Contenuto della confezione
L’introduttore orientabile FlexCath Select viene fornito sterile. La confezione contiene i seguenti
articoli:
• 1 introduttore orientabile
• 1 dilatatore
• Documentazione sul prodotto
2 Indicazioni d’uso
L’introduttore orientabile FlexCath Select è stato progettato per l’inserimento di un catetere
percutaneo nel sistema vascolare e nelle camere cardiache, compresa la parte sinistra del cuore,
attraverso il setto interatriale. La deflessione dell’introduttore facilita il posizionamento del
catetere.
3 Controindicazioni
L’uso dell’introduttore orientabile FlexCath Select è controindicato per il posizionamento nel
ventricolo o nell’atrio sinistro se il paziente presenta almeno una delle seguenti condizioni:
• Il paziente ha un patch o un occlusore settale interatriale o ha subito altri interventi chirurgici
nel setto interatriale o vicino ad esso.
• Il paziente ha un trombo atriale sinistro.
• Il paziente ha un mixoma atriale riconosciuto o sospetto.
4 Avvertenze e precauzioni
Energia di ablazione – Quando si utilizza l’introduttore in presenza di energia di ablazione,
procedere con cautela per assicurarsi che tutti gli elementi di ablazione siano al di fuori
dell’introduttore.
Aspirazione dell’aria – Rimuovere il filo guida dall’introduttore, quindi aspirare ed irrigare
l’introduttore. In tal modo si ridurrà al minimo l’aspirazione dell’aria attraverso la valvola
dell’introduttore.
Terapia anticoagulante – Somministrare la terapia anticoagulante periprocedurale in dosi
adeguate ai pazienti che si sottopongono a procedura cardiaca sinistra e transettale e a pazienti
selezionati che dovranno subire procedure a destra. Per ridurre al minimo il rischio di complicanze
emorragiche e trombotiche, somministrare la terapia anticoagulante periprocedurale secondo gli
standard della struttura.
Sanguinamento di ritorno – Assicurarsi che il rubinetto sia in posizione chiusa dopo
l’irrigazione o l’aspirazione per evitare un sanguinamento di ritorno accidentale attraverso la porta
laterale.
Smaltimento di rifiuti a rischio biologico – Smaltire tutti i dispositivi e i componenti sterili
utilizzati conformemente alle procedure ospedaliere.
Iniezione della soluzione di contrasto – Non utilizzare un iniettore automatico per l’iniezione
della soluzione di contrasto nell’introduttore.
Rotazione del dilatatore – Non ruotare il dilatatore al momento di bloccarlo nel raccordo della
valvola o dopo averlo bloccato. In caso contrario, la punta del dilatatore sull’estremità distale non
sarà allineata correttamente rispetto alla porta laterale sull’estremità prossimale.
Non risterilizzare – Non risterilizzare il dispositivo a scopo di riutilizzo. La risterilizzazione
potrebbe compromettere l’integrità strutturale del dispositivo o creare un rischio di
contaminazione del dispositivo che potrebbe comportare lesioni, malattia o decesso del
paziente.
Rischio di embolia – L’introduzione di un catetere o di un introduttore nel sistema circolatorio
comporta il rischio di embolia gassosa, con possibile occlusione dei vasi e conseguente infarto
dei tessuti con gravi conseguenze. L’utilizzo di cateteri di diametro inferiore a 9 Fr con questo
dispositivo comporta un rischio maggiore di embolia gassosa. Fare sempre avanzare e ritirare i
componenti lentamente e utilizzare l’irrigazione per ridurre al minimo il vuoto creato e quindi il
rischio di embolia gassosa.
Data di scadenza – Accertarsi che la data di scadenza dell’introduttore non sia stata superata.
Non utilizzare se il prodotto è scaduto.
Danni alla vena femorale – Al momento dell’inserimento, della manipolazione o dell’estrazione
dell’introduttore, occorre prestare attenzione per ridurre al minimo i danni alla vena femorale e al
sito di accesso. Complicanze associate all’impianto di un catetere nella vena femorale
comprendono ematoma e trombosi.
Fluoroscopia necessaria per il posizionamento dell’introduttore – Si raccomanda
vivamente l’uso della fluoroscopia durante la manipolazione e il posizionamento dell’introduttore.
La manipolazione dell’introduttore senza l’uso della fluoroscopia potrebbe causare danni alle
strutture cardiache e vascolari.
Esclusivamente monouso – Il dispositivo è destinato esclusivamente ad un singolo impiego su
un singolo paziente. Non riutilizzare, rigenerare o risterilizzare il dispositivo a scopo di riutilizzo. Il
riutilizzo, la rigenerazione o la risterilizzazione potrebbero compromettere l’integrità strutturale del
dispositivo o creare un rischio di contaminazione del dispositivo che potrebbe comportare lesioni,
malattia o morte del paziente.
Irrigazione frequente – Si raccomanda di irrigare regolarmente l’introduttore:
• Per evitare ristagni di sangue, coaguli, emboli e gravi lesioni al paziente.
• Per evitare che la soluzione di contrasto aderisca all’interno del lume dopo ogni iniezione.
Manipolazione e cura – Quando si utilizza il dispositivo:
Italiano
32

• Adottare estrema cautela durante la manipolazione del dispositivo. In caso contrario,
possono derivarne lesioni, quali perforazioni, tamponamento cardiaco, induzione di aritmia o
blocco cardiaco.
• Non forzare in alcun modo l’avanzamento o l’estrazione del dispositivo, specialmente se si
incontra resistenza.
• Evitare il posizionamento del dispositivo in prossimità delle corde tendinee, in quanto ciò
aumenta la probabilità di intrappolamento nel cuore. In tal caso, potrebbe rendersi necessario
un intervento chirurgico o la riparazione dei tessuti interessati.
• Non utilizzare l’introduttore se risulta piegato o danneggiato.
Accesso nell’atrio sinistro – Non far avanzare il dilatatore o l’introduttore attraverso il setto
interatriale senza prima avere confermato l’accesso nell’atrio sinistro. In caso contrario, i
componenti possono essere inseriti in una posizione non desiderata.
Attrezzatura ospedaliera necessaria – Tenere a portata di mano un defibrillatore esterno
pronto all’uso durante l’utilizzo dell’introduttore assemblato.
Altri cateteri, dispositivi o fili – Evitare che l’introduttore rimanga impigliato con altri cateteri,
dispositivi o fili. In caso contrario potrebbe rendersi necessario un intervento chirurgico.
Protesi valvolari cardiache – Evitare di far passare il dispositivo attraverso una valvola cardiaca
protesica (meccanica o biologica). Vi è la possibilità che il dispositivo si blocchi o danneggi la
valvola, provocando un’insufficienza valvolare o un cedimento prematuro della valvola protesica
stessa.
Utenti qualificati – L’apparecchiatura deve essere utilizzata solo da par te o sotto la super visione
di medici addestrati nell’esecuzione di interventi di impianto di un catetere.
Ambiente d’utilizzo necessario – Gli interventi di cateterizzazione cardiaca devono essere
eseguiti solo in una struttura completamente attrezzata.
Aspirazione della porta laterale – Aspirare la porta laterale durante l’estrazione del dilatatore,
del catetere, dell’ago, dei fili o di altri dispositivi.
Ostruzione della porta laterale – Prestare attenzione per evitare qualsiasi ostruzione della
porta laterale e garantire l’efficacia dell’irrigazione di soluzione salina.
Perdita di sangue significativa – Prestare attenzione per evitare che vi siano perdite di sangue
significative attraverso la valvola emostatica durante l’intervento.
Ispezione della confezione sterile – Ispezionare la confezione sterile e il dispositivo prima
dell’uso. Se la confezione sterile o il dispositivo mostrano danni, non utilizzare il dispositivo.
Contattare il rappresentante locale Medtronic.
Esposizione a raggi X e a fluoroscopia – L’utilizzo della fluoroscopia durante gli interventi di
ablazione eseguiti con catetere presenta potenziali rischi derivanti dall’esposizione ai raggi X sia
per il paziente che per gli operatori sanitari. Un’esposizione eccessiva può causare gravi danni da
radiazioni e aumentare il rischio di ripercussioni somatiche e genetiche. Eseguire l’ablazione con
catetere solo dopo avere prestato la dovuta attenzione ai potenziali rischi derivanti
dall’esposizione alle radiazioni associate all’intervento e aver adottato ogni misura precauzionale
per ridurre al minimo tale esposizione. Nelle pazienti in stato di gravidanza, valutare con estrema
attenzione l’uso del dispositivo ed evitare l’esposizione ai raggi X.
5 Effetti indesiderati
I possibilli effetti indesiderati associati all’inserimento di cannule nei vasi periferici e il
posizionamento intracardiaco dell’introduttore e del dilatatore possono comprendere le seguenti
condizioni, senza limitarsi ad esse:
• Complicanze alla sede di accesso (ematoma, infezione, trombosi, ecchimosi,
fistola AV, sanguinamento dalla sede di
introduzione, emorragia)
• Embolia gassosa
• Aritmia (fibrillazione atriale, flutter atriale,
tachicardia ventricolare)
• Arresto cardiaco
• Sensazione di disagio, dolore o pressione
al torace
• Spasmo, dissezione, trombosi dell’arteria
coronarica
• Decesso
• Endocardite
• Arresto cardiaco, con necessità d’impianto
di un pacemaker permanente
• Emotorace
• Infarto miocardico
• Perforazione del tessuto cardiaco o circostante
• Versamento pericardico, tamponamento
• Pericardite
• Versamento pleurico
• Pneumotorace
• Pseudoaneurisma
• Edema polmonare
• Embolia polmonare
• Ictus
• Trombo
• Attacco ischemico transitorio (TIA)
• Reazione vasovagale
6 Istruzioni per l’uso
Nota: prima di inserire l’introduttore nel paziente, testare il meccanismo di deflessione per
assicurarsi che sia funzionante.
1. Tramite tecnica asettica, creare un accesso vascolare utilizzando l’introduttore appropriato.
2. Inserire un filo guida compatibile (vedere la sezione Specifiche) attraverso il sistema
vascolare e nella posizione desiderata avvalendosi di tecniche di accesso vascolare
standard.
3. Irrigare la porta laterale dell’introduttore e il lume del dilatatore con soluzione salina sterile.
4. Assicurarsi che l’introduttore si trovi in posizione neutra (non flesso) e bagnare l’asta del
dilatatore con soluzione salina sterile prima di inserirlo attraverso la valvola emostatica.
5. Iniziare ad assemblare il dilatatore e l’introduttore introducendo la punta distale del dilatatore
nella valvola emostatica in modo che il bordo ricurvo del dilatatore sia perpendicolare alla
valvola emostatica (Figura 2).
Figura 2. Introduttore orientabile FlexCath Select
6. Continuare a far avanzare il dilatatore nell’introduttore fino a bloccare in posizione il raccordo
del dilatatore all’interno del raccordo dell’introduttore.
Nota: l’etichetta sul raccordo del dilatatore deve essere allineata con l’etichetta
dell’impugnatura dell’introduttore in modo che la curva del dilatatore sia allineata con lo
stesso orientamento della direzione di flessione dell’introduttore e con la porta laterale
(Figura 3).
Figura 3. Introduttore orientabile FlexCath Select
7. Con un leggero movimento di torsione all’interno della vena cava superiore, avvitare il
gruppo introduttore-dilatatore sul filo guida e all’interno del sistema vascolare.
8. Rimuovere il filo guida.
9. Inserire l’ago transettale adeguatamente preparato nel gruppo introduttore-dilatatore in
modo da allineare l’indicatore di curvatura sull’ago transettale con la porta laterale.
33
Italiano

Nota: l’ago transettale dovrà essere utilizzato con un mandrino, per evitare danni al lume
interno del dilatatore.
10. Portare il gruppo verso il basso, fino a farlo scendere nell’atrio destro, in modo da preparare
la puntura transettale.
11. Sotto guida fluoroscopica, praticare la puntura transettale utilizzando una misurazione della
pressione e/o un’iniezione di mezzo di contrasto. Confermare il corretto posizionamento
nell’atrio sinistro.
12. Tirare l’ago transettale nel dilatatore e rimuovere lentamente il dilatatore e l’ago
dall’introduttore.
Nota: il dilatatore va rimosso lentamente per ridurre la possibilità di creare vuoto
nell’introduttore. Il sangue dovrebbe essere aspirato senza problemi attraverso la porta
laterale. In caso contrario, ritirare l’introduttore, in quanto la punta potrebbe essere in
contatto con la parete dell’atrio o di una vena polmonare.
13. Aspirare il sangue attraverso la porta laterale e assicurarsi che l’introduttore sia privo di aria.
Eseguire l’aspirazione o il sanguinamento spontaneo prima di inserire il catetere
nell’introduttore.
Nota: eseguire questo passaggio dopo tutti i cambi di catetere.
14. Dopo aver effettuato l’accesso con l’introduttore, mantenere la terapia anticoagulante.
15. Preparare il catetere in base alle istruzioni per l’uso del produttore.
16. Inserire il catetere e posizionare l’introduttore.
Note:
• Per facilitare l’inserimento, è possibile bagnare l’asta del catetere.
• La valvola emostatica è dotata di un arresto positivo per impedire che i dispositivi di
cattura aprano il sigillo.
• Inserire ed estrarre sempre lentamente i componenti per ridurre al minimo il vuoto creato.
• L’introduttore dovrà essere irrigato anche mentre il catetere è inserito.
17. Prima dell’estrazione dell’introduttore, accer tarsi che questo si trovi in posizione neutra (non
deflessa).
7 Specifiche tecniche
Lunghezza totale
Lunghezza utile 65 cm (25,6 in)
Diametro interno 3,3 mm (10 Fr) (0,13 in)
Diametro esterno 4,3 mm (13 Fr) (0,17 in)
Lunghezza del dilatatore 86 cm (33,9 in)
Marker radiopaco 5 mm (0,2 in) prossimale alla punta dell’introduttore
Compatibilità del filo guida Da 0,81 mm (0,032 in) a 0,89 mm (0,035 in)
Compatibilità dell’ago transet-
tale
Parametri ambientali
Temperatura di trasporto raccomandata
Temperatura di conservazione raccomandata
Temperatura di funzionamento
81 cm (31,9 in)
89 cm (35,0 in) o maggiore
Da -35°C a 58°C (da -31°F a 136°F); umidità relativa 85%
(senza condensa)
Media di 22°C (72°F) con deviazione standard di 2,7°C
(4,86°F) e limiti di controllo azionabile da 15°C a 30°C (da 59°F
a 86°F)
Da 15°C a 30°C (da 59°F a 86°F) ad altitudini inferiori a 2400 m
(8000 piedi) sul livello del mare
8 Esclusione dalla garanzia Medtronic
Per informazioni esaurienti sull’esclusione dalla garanzia, leggere il documento allegato.
9 Assistenza
Medtronic si avvale su scala mondiale di rappresentanti e tecnici altamente qualificati in grado di
assistere i clienti e, all’occorrenza, di provvedere alla formazione di personale ospedaliero
qualificato sull’utilizzo dei prodotti Medtronic. Medtronic si avvale inoltre della collaborazione di
professionisti capaci di fornire consulenza tecnica agli utenti dei prodotti. Per ulteriori
informazioni, rivolgersi al rappresentante locale Medtronic oppure scrivere agli indirizzi o
telefonare ai numeri telefonici Medtronic riportati sul retro di copertina.
Italiano
34

1 Beschrijving
65 cm
(25,6 inch)
16 cm
(6,3 inch)
86 cm
(33,9 inch)
De FlexCath™ Select stuurbare sheath van Medtronic is een percutane katheterintroducer die is
voorzien van een klep waardoor katheters en draden kunnen worden ingebracht, teruggetrokken
en uitgewisseld en die bloedverlies tot een minimum beperkt. Er is een zijpoort met een plugkraan
ingebouwd waardoor een druppelinfuus kan worden toegediend. Ook kunnen door deze zijpoort
injecties worden toegediend (via het centrale lumen), kunnen spoelingen en aspiraties worden
uitgevoerd, kunnen bloedmonsters worden genomen en kan de bloeddruk worden bewaakt.
Afbeelding 1. FlexCath Select stuurbare sheath
Bij de FlexCath Select stuurbare sheath is een dilatator verpakt. De sheath is beschreven in de
onderstaande tabel:
Model
990065 3,3 mm (10 Fr)
De sheath kan worden gebogen, zodat er gemakkelijker kan worden gemanoeuvreerd met
katheters die via de sheath worden ingebracht in de rechter- of linkerhartkamer.
De FlexCath Select stuurbare sheath van 10 Fr kan worden gebruikt met diagnostische- en
ablatiekatheters van Medtronic met maten tot 9 Fr.
De dilatator voor de FlexCath Select stuurbare sheath van 10 Fr is compatibel met transseptale
naalden van Merit Medical HeartSpan van 89 cm en langer.
Binnendiameter Buitendiameter Bruikbare lengte
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Inhoud van de verpakking
De FlexCath Select stuurbare sheath wordt steriel geleverd. De verpakking bevat de volgende
onderdelen:
• 1 stuurbare sheath
• 1 dilatator
• Productdocumentatie
2 Indicaties voor gebruik
De FlexCath Select stuurbare sheath is bedoeld voor de percutane introductie van katheters in de
bloedvaten en de hartkamers, inclusief de linkerkant van het hart door het interatriale septum.
Dankzij de buigbare sheath kan de katheter gemakkelijk in de juiste positie worden geplaatst.
3 Contra-indicaties
De FlexCath Select stuurbare sheath is gecontra-indiceerd voor plaatsing in het linkeratrium
of -ventrikel als een van de volgende situaties zich voordoet bij de patiënt:
• De patiënt heeft een intra-atriale septale patch, of occluder, of heeft een andere operatieve
ingreep ondergaan aan of in de buurt van het intra-atriale septum.
• De patiënt heeft een linksatriale trombus.
• De patiënt heeft een bekend of vermoed atriaal myxoma.
4 Waarschuwingen en voorzorgsmaatregelen
Ablatie-energie – Wanneer de sheath wordt gebruikt met ablatie-energie, moet er goed op
worden gelet dat alle ablatie-elementen zich buiten de sheath bevinden.
Luchtaspiratie – Haal de voerdraad uit de sheath voordat u de sheath aspireert en spoelt.
Hierdoor blijft het aspireren van lucht door de klep van de sheath beperkt.
Antistollingstherapie – Bij patiënten die linkszijdige en transseptale cardiale procedures
ondergaan, en bij bepaalde patiënten die rechtszijdige procedures ondergaan, moet het juiste
niveau van periprocedurale antistollingstherapie worden toegediend. Om bloedingen en
trombotische complicaties te minimaliseren, dient u periproceduraal antistollingstherapie toe
volgens de regels van het ziekenhuis.
Terugstromen van bloed – Zorg dat de kraan na het spoelen of aspireren in gesloten positie
staat, om onbedoeld terugstromen van bloed via de zijpoort te voorkomen.
Afvoeren als gevaarlijk biologisch afval – Werp alle gebruikte producten en steriele
componenten weg overeenkomstig de in het ziekenhuis geldende richtlijnen.
Injectie van contrastvloeistof – Gebruik geen automatisch injectiesysteem voor het injecteren
van contrastoplossing in de sheath.
Draaien van de dilatator – De dilatator mag niet worden gedraaid tijdens of na het vastklikken
ervan in de hub van de klep. Dit kan leiden tot verkeerde uitlijning van de dilatatortip aan het distale
uiteinde ten opzichte van de zijpoort aan het proximale uiteinde.
Niet hersteriliseren – Het product mag niet worden gehersteriliseerd met het doel om het
opnieuw te gebruiken. Door het hersteriliseren kan het apparaat worden besmet of de structuur
van het product worden aangetast wat kan resulteren in letsel, ziekte of overlijden van de patiënt.
Risico van embolie – De introductie van een katheter of sheath in de bloedsomloop brengt altijd
het risico op luchtembolie met zich mee, waardoor bloedvaten kunnen worden afgesloten en
weefselinfarcten kunnen optreden. Dit kan ernstige gevolgen hebben. Bij het gebruik van
katheters kleiner dan 9 Fr in combinatie met dit product is het risico van een luchtembolie groter.
Het wordt aangeraden onderdelen altijd voorzichtig in te brengen en terug te trekken en te
spoelen, zodat er maar een beperkt vacuüm ontstaat. Het risico van luchtembolie is dan beperkt.
Vervaldatum – Controleer of de uiterste gebruiksdatum van de sheath nog niet verstreken is. Niet
gebruiken als deze datum verstreken is.
Beschadiging van de vena femoralis – Bij het inbrengen, manipuleren en terugtrekken van de
sheath moet schade aan de vena femoralis en de toegangslocatie zoveel mogelijk worden
vermeden. Complicaties die kunnen optreden bij katheterisatie van de vena femoralis zijn onder
andere hematoom en trombose.
Röntgendoorlichting vereist tijdens plaatsing van de sheath – Het wordt bij manipulatie en
plaatsing van de sheath ten strengste aangeraden om gebruik te maken van röntgendoorlichting.
Manipulatie van de sheath zonder röntgendoorlichting kan beschadiging van de cardiale en
vasculaire structuren veroorzaken.
Uitsluitend voor eenmalig gebruik – Dit product is bedoeld om eenmalig te worden gebruikt bij
één patiënt. Het product mag niet worden hergebruikt of gehersteriliseerd met het doel om het
opnieuw te gebruiken. Door het opnieuw gebruiken, verwerken ten behoeve van hergebruik of
hersteriliseren kan het product worden besmet of de structuur ervan worden aangetast wat kan
resulteren in letsel, ziekte of overlijden van de patiënt.
Regelmatig spoelen – Het wordt aangeraden de sheath regelmatig te spoelen:
• Om bloedstagnatie, stolsels, embolieën en ernstig letsel bij de patiënt te voorkomen.
• Om te voorkomen dat contrastoplossing na iedere contrastinjectie binnen het lumen
vastplakt.
Gebruik en hantering – Bij het hanteren van het product:
• Wees buitengewoon voorzichtig bij het manipuleren van het product. Bij onvoorzichtig
gebruik kunnen verwondingen zoals perforatie, tamponnade, inductie van aritmieën, of
hartblok optreden.
• Gebruik geen overmatige kracht bij het opvoeren of terugtrekken van het product. Wees
vooral voorzichtig als u weerstand voelt.
35
Nederlands

• Vermijd plaatsing van het product in de buurt van de chordae tendineae, aangezien de kans
dat het product vast komt te zitten in het hart hierdoor wordt vergroot. Als dat gebeurt, moet
mogelijk een operatieve ingreep of herstel van de beschadigde weefsels worden uitgevoerd.
• Gebruik de sheath niet als deze geknikt of beschadigd is.
Linksatriale toegang – Voer de dilatator of sheath niet op via het interatriale septum zonder eerst
te bevestigen dat de linksatriale toegang tot stand is gebracht, om opvoeren van deze onderdelen
naar een ongewenste locatie te voorkomen.
Benodigde ziekenhuisapparatuur – Houd externe defibrillatieapparatuur beschikbaar zodat
direct kan worden ingegrepen tijdens het gebruik van de stuurbare sheath.
Andere katheters, producten en draden – Let op dat de sheath niet verstrikt raakt in andere
katheters, producten of draden. Door verstrikking kan een operatieve ingreep noodzakelijk zijn.
Hartklepprotheses – Let op dat het product niet door een hartklepprothese (mechanisch of
weefsel) wordt opgevoerd. Het product kan vastraken in de klep, waardoor de klep kan worden
beschadigd en valvulaire insufficiëntie of prematuur falen van de hartklep kan optreden.
Gekwalificeerde gebruikers – Dit product mag alleen worden gebruikt door of onder supervisie
van artsen die ervaring hebben met cardiale katheterisatieprocedures.
Vereiste gebruiksomgeving – Cardiale katheterisatieprocedures mogen uitsluitend worden
uitgevoerd in een compleet uitgeruste faciliteit.
Aspiratie van de zijpoort – Aspireer de zijpoort bij het terugtrekken van de dilatator, katheter,
naald, draden of andere producten.
Obstructie van de zijpoort – Let op dat de spoeling met zoutoplossing niet wordt belemmerd
door obstructie van de zijpoort.
Significante bloedlekkage – Let op dat er tijdens de procedure geen significante bloedlekkage
door de hemostaseklep plaatsvindt.
Inspectie van de steriele verpakking – Inspecteer de steriele verpakking en het product vóór
gebruik. Gebruik het product niet als de steriele verpakking of het product beschadigd is. Neem
contact op met Medtronic.
Blootstelling aan röntgenstralen en -doorlichting – Bij het gebruik van röntgendoorlichting
tijdens katheterablatieprocedures bestaat er een kans dat patiënten en laboratoriumpersoneel
aan intensieve röntgenstraling worden blootgesteld. Overmatige blootstelling aan
röntgenstraling kan resulteren in acuut stralingsletsel en een verhoogd risico op somatische en
genetische effecten. Voer een katheterablatie uitsluitend uit nadat het risico op
stralingsblootstelling tijdens de procedure goed is overwogen en stappen zijn ondernomen om de
blootstelling tot een minimum te beperken. Overweeg de potentiële risico’s zorgvuldig en vermijd
blootstelling aan röntgenstraling voordat u het product gebruikt bij zwangere vrouwen.
5 Bijwerkingen
Potentiële bijwerkingen die worden geassocieerd met canulatie van de perifere bloedvaten en
intracardiale plaatsing van de sheath en de dilatator zijn onder andere, doch zijn niet beperkt tot:
• Complicaties bij de toegangsweg (hematoom, infectie, trombose, ecchymose,
AV-fistel, bloedingen bij de injectieplaats
en elders)
• Luchtembolie
• Aritmie (atriale fibrillatie, atriale flutter, ventriculaire tachycardie)
• Hartstilstand
• Benauwdheid, pijn of druk op de borst
• Coronair spasme, dissectie, trombose
• Overlijden
• Endocarditis
• Hartblok waarvoor een permanente pacemaker vereist is
• Hemothorax
• Myocardinfarct
• Perforatie van het cardiale of omringende
weefsel
• Pericardiale effusie, tamponnade
• Pericarditis
• Pleurale effusie
• Pneumothorax
• Pseudo-aneurysma
• Pulmonair oedeem
• Pulmonaire embolie
• Beroerte
• Trombus
• TIA
• Vasovagale reactie
6 Gebruiksinstructies
Opmerking: Voordat u de sheath inbrengt bij de patiënt, dient u het buigingsmechanisme te
testen om te zien of dit werkt.
1. Breng door middel van een aseptische techniek een vasculaire toegang tot stand met behulp
van een geschikte introducer.
2. Breng een compatibele voerdraad (zie Specificaties) door de bloedvaten in naar de
gewenste positie met gebruikmaking van de standaardtechnieken voor vasculaire toegang.
3. Spoel de zijpoor t van de sheath en het lumen van de dilatator met steriele zoutoplossing.
4. Zorg dat de sheath in een neutrale (niet-gebogen) positie staat en bevochtig de schacht van
de dilatator met steriele zoutoplossing voordat u deze inbrengt via de hemostaseklep.
5. Monteer de dilatator en de sheath op elkaar door de distale tip van de dilatator in te brengen
in de hemostaseklep zodat de gebogen rand van de dilatator zich loodrecht op de
hemostaseklep bevindt (zie Afbeelding 2).
Afbeelding 2. FlexCath Select stuurbare sheath
6. Blijf de dilatator opvoeren in de sheath totdat de dilatatorhub vastklikt in de sheathhub.
Opmerking: Het label op de dilatatorhub moet op één lijn liggen met het label op de
handgreep van de sheath zodat de curve van de dilatator in dezelfde richting ligt als de
buiging van de sheath en de zijpoort (zie Afbeelding 3).
Afbeelding 3. FlexCath Select stuurbare sheath
7. Voer de sheath-dilatatorcombinatie langzaam op over de voerdraad in de vasculatuur en
gebruik een licht draaiende beweging in de SVC.
8. Verwijder de voerdraad.
9. Breng de correct voorbereide transseptale naald zodanig in de sheath-dilatatorcombinatie
in dat de krommingsindicator op de transseptale naald op één lijn ligt met de zijpoort.
Opmerking: De transseptale naald moet worden gebruikt in combinatie met een stilet om te
voorkomen dat het binnenlumen van de dilatator beschadigd raakt.
10. Trek de combinatie naar beneden in het rechteratrium als voorbereiding op de transseptale
punctie.
11. Voer een transseptale punctie uit met gebruik van drukmetingen en/of het injecteren van
contrastvloeistof. Zorg voor een correcte plaatsing in het linkeratrium.
12. Trek de transseptale naald in de dilatator en verwijder de dilatator-naaldcombinatie
langzaam uit de sheath.
Opmerking: Verwijder de dilatator langzaam, om te voorkomen dat er een vacuüm in de
sheath ontstaat. Bloed moet vrij door de zijpoort kunnen aspireren. Als dat niet het geval is,
Nederlands
36

moet u de sheath terugtrekken, omdat de tip van de sheath dan mogelijk tegen de
atriumwand of tegen een longader aanligt.
13. Aspireer bloed door de zijpoort en zorg ervoor dat de sheath geen lucht bevat. Pas aspiratie
of spontane terugbloeding toe voordat er een katheter in de sheath wordt ingebracht.
Opmerking: Voer deze stap uit na alle katheterwissels.
14. Nadat toegang met de sheath tot stand is gebracht, moet antistollingstherapie worden
gehandhaafd.
15. Bereid de katheter voor volgens de gebruiksinstructies van de fabrikant.
16. Breng de katheter in en plaats de sheath in de gewenste positie.
Opmerkingen:
• De schacht van de dilatator kan makkelijker worden ingebracht door deze te
bevochtigen.
• De hemostaseklep heeft een positieve stop om te voorkomen dat capture-apparaten de
afdichting doorbreken.
• Om een vacuüm te minimaliseren, wordt het aangeraden onderdelen altijd voorzichtig in
te brengen en terug te trekken.
• De sheath moet ook worden gespoeld terwijl een katheter is ingebracht.
17. Zorg ervoor dat de sheath vóórdat u deze terugtrekt, in de neutrale (niet-gebogen) positie
staat.
7 Specificaties
Algehele lengte
Bruikbare lengte 65 cm (25,6 in)
Binnendiameter 3,3 mm (10 Fr) (0,13 in)
Buitendiameter 4,3 mm (13 Fr) (0,17 in)
Dilatatorlengte 86 cm (33,9 in)
Radiopake markering 5 mm (0,2 in) proximaal ten opzichte van de tip van de sheath
Compatibiliteit met voerdraden 0,81 mm (0,032 in) tot 0,89 mm (0,035 in)
Compatibiliteit met transseptale
naalden
Omgevingsparameters
Aanbevolen transporttemperatuur
Aanbevolen opslagtemperatuur
Bedrijf 15°C tot 30°C (59°F tot 86°F), bij een hoogte van minder dan
81 cm (31,9 in)
89 cm (35,0 in) of langer
-35°C tot 58°C (-31°F tot 136°F); 85% relatieve luchtvochtigheid (niet-condenserend)
Gemiddeld 22°C (72°F) met standaarddeviatie van 2,7°C
(4,86°F) en actie-vereiste grenswaarden van 15°C tot 30°C
(59°F tot 86°F)
2400 m (8000 ft) boven zeeniveau
8 Uitsluiting van garantie door Medtronic
Raadpleeg het bijgesloten garantiedocument voor volledige informatie over de garantie.
9 Service
Medtronic beschikt over hoogopgeleide vertegenwoordigers en technici op locaties in de hele
wereld die u van dienst kunnen zijn en op verzoek training voor gekwalificeerd
ziekenhuispersoneel in het gebruik van Medtronic-producten kunnen verzorgen. Medtronic
beschikt ook over een professionele staf die technische adviezen kan verstrekken aan gebruikers
van de producten. Neem voor meer informatie contact op met Medtronic. Zie het telefoonnummer
of adres van Medtronic dat op de achterzijde van deze handleiding staat vermeld.
37
Nederlands

1 Beskrivelse
65 cm
(25,6 in)
16 cm
(6,3 in)
86 cm
(33,9 in)
Medtronic FlexCath™ Select styrbar hylse er en perkutan kateterintroducer med en ventil som
gjør det mulig å føre inn, trekke tilbake og skifte katetre og guidewirer med minimalt blodtap.
Hylsen har en integrert sideport med stoppekran, som kan brukes til kontinuerlig infusjon,
injeksjon gjennom det midtre lumenet, skylling, aspirasjon, blodprøvetaking og trykkovervåking.
Figur 1. FlexCath Select styrbar hylse
FlexCath Select styrbar hylse leveres med en dilatator. Hylsen er beskrevet i følgende tabell:
Modell
990065 3,3 mm (10 Fr)
Hylsen kan krummes slik at det blir lettere å manøvrere katetre som føres gjennom hylsen og inn
i høyre eller venstre hjertekammer.
FlexCath Select styrbar hylse på 10 Fr kan brukes sammen med diagnostiske katetre og
ablasjonskatetre fra Medtronic med en størrelse på opptil 9 Fr.
Dilatatoren for FlexCath Select styrbar hylse på 10 Fr er kompatibel med Merit Medical HeartSpan
transseptale nåler med en lengde på 89 cm eller mer.
Indre diameter Ytre diameter Nyttbar lengde
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Pakningens innhold
FlexCath Select styrbar hylse leveres steril. Pakningen inneholder følgende:
• 1 styrbar hylse
• 1 dilatator
• Produktdokumentasjon
2 Indikasjoner for bruk
FlexCath Select styrbar hylse er ment for perkutan kateterinnføring i blodkarene og kamrene i
hjertet, inkludert den venstre siden av hjertet gjennom det intraatriale septum. Krumning av hylsen
kan gjøre det lettere å posisjonere kateteret.
3 Kontraindikasjoner
FlexCath Select styrbar hylse er kontraindisert for plassering i venstre atrium eller ventrikkel hvis
noen av følgende forhold gjelder pasienten:
• Pasienten har en intraatrial septumpatch eller okkluder, eller har hatt andre kirurgiske inngrep
i eller ved det intraatriale septum.
• Pasienten har en trombe i venstre atrium.
• Pasienten har kjent eller mistenkt atrialt myksom.
4 Advarsler og forholdsregler
Ablasjonsenergi – Når hylsen brukes med ablasjonsenergi, må du passe på at alle
ablasjonselementer er utenfor hylsen.
Aspirasjon av luft – Fjern guidewiren fra hylsen før aspirasjon og skylling av hylsen. Denne
handlingen minimerer aspirasjon av luft gjennom ventilen på hylsen.
Antikoagulasjonsbehandling – Administrer tilstrekkelig antikoagulasjonsbehandling i
forbindelse med prosedyren for pasienter som skal gjennomgå en venstresidig og transseptal
hjerteprosedyre, og for utvalgte pasienter som skal gjennomgå en høyresidig prosedyre. For å
minimere blødning og trombotiske komplikasjoner skal det gis antikoagulasjonsbehandling i
forbindelse med prosedyren i henhold til institusjonens standarder.
Tilbakestrømning av blod – Forsikre deg om at stoppekranen er i lukket posisjon etter skylling
eller aspirasjon for å unngå utilsiktet tilbakestrømning av blod gjennom sideporten.
Biologisk farlig avfall – Kast utstyr og sterile komponenter som er brukt, i samsvar med
sykehusets retningslinjer.
Kontrastinjeksjon – Bruk ikke et automatisk trykksystem til å injisere kontrastmiddel i hylsen.
Ditatatorvridning – Du må ikke vri dilatatoren mens eller etter at den låses på plass i
ventilkoblingen. Dette kan føre til feil plassering av dilatator tuppen ved den distale tuppen i forhold
til sideporten ved den proksimale enden.
Skal ikke resteriliseres – Dette produktet må ikke resteriliseres med tanke på gjenbruk.
Resterilisering kan skade produktets strukturelle integritet eller skape risiko for at produktet
overfører smitte, noe som kan medføre skade, sykdom eller død for pasienten.
Risiko for emboli – Når et kateter eller en hylse føres inn i sirkulasjonssystemet, medfører det
risiko for luftemboli som kan okkludere blodårer og føre til vevsnekrose med alvorlige
konsekvenser. Bruk av katetre som er mindre enn 9 Fr sammen med denne enheten, kan medføre
økt risiko for luftemboli. Sørg alltid for at komponenter føres frem og trekkes tilbake sakte, og bruk
skylling slik at det dannes minst mulig vakuum og risikoen for luftemboli reduseres til et minimum.
Utløpsdato – Forsikre deg om at hylsen ikke er gått ut på dato. Produktet skal ikke brukes hvis det
har gått ut på dato.
Skade på v. femoralis – Pass på at du gjør minst mulig skade på v. femoralis og tilgangsstedet
ved innføring, manipulering og tilbaketrekking av hylsen. Komplikasjoner forbundet med
kateterisering av v. femoralis omfatter hematom og trombose.
Gjennomlysning ved plassering av hylsen – Det anbefales på det sterkeste å bruke
gjennomlysning ved manipulering og plassering av hylsen. Manipulering av hylsen uten
gjennomlysning kan føre til skade på hjerte- og karstrukturer.
Kun for engangsbruk – Dette produktet skal kun brukes én gang på én pasient. Produktet må
ikke brukes på nytt eller reprosesseres eller resteriliseres med tanke på gjenbruk.
Reprosessering, resterilisering eller gjenbruk kan skade produktets strukturelle integritet eller
skape risiko for at produktet overfører smitte, noe som kan medføre skade, sykdom eller død for
pasienten.
Hyppig skylling – Regelmessig skylling av hylsen anbefales:
• For å unngå blodstagnasjon, levring, emboli og alvorlig pasientskade.
• For å fjerne rester av kontrastmiddel fra lumenet etter hver kontrastinjeksjon.
Vedlikehold og håndtering – Når du håndterer enheten:
• Vær svært forsiktig når du manipulerer produktet. Manglende forsiktighet kan føre til skade
som perforasjon, tamponade, induksjon av arytmi eller AV-blokk.
• Bruk ikke for stor kraft når produktet føres frem eller trekkes tilbake, spesielt hvis du merker
motstand.
• Unngå å posisjonere produktet rundt chordae tendinae fordi dette øker faren for at produktet
kan sette seg fast i hjertet, og kan gjøre det nødvendig med kirurgisk intervensjon eller
reparasjon av skadet vev.
• Bruk ikke hylsen hvis den har knekk eller er skadet.
Venstre atrial tilgang – Før ikke dilatatoren eller hylsen frem gjennom det interatriale septum
uten at du først har bekreftet venstre atriale tilgang, slik at komponentene ikke føres frem til en
uønsket plassering.
Nødvendig sykehusutstyr – Ha eksternt defibrilleringsutstyr i nærheten for øyeblikkelig bruk når
du bruker den styrbare hylseenheten.
Norsk
38

Andre katetre, enheter eller vaiere – Unngå at hylsen vikler seg inn i andre katetre, enheter eller
vaiere. Dette kan gjøre det nødvendig med kirurgisk intervensjon.
Hjerteklaffproteser – Før ikke produktet gjennom en hjerteklaffprotese (mekanisk eller vev).
Produktet kan sette seg fast i klaffen, skade klaffen og forårsake valvulær dysfunksjon eller
prematur svikt av klaffeprotesen.
Kvalifiserte brukere – Dette utstyret skal kun brukes av lege eller under tilsyn av lege som har fått
opplæring i hjertekateterisering.
Krav til omgivelsene ved bruk – Kryoablasjonsprosedyrer skal kun utføres i et fullt utstyrt lokale.
Sideportaspirasjon – Aspirer sideporten når du trekker ut dilatatoren, kateteret, nålen, vaiere
eller andre enheter.
Tiltetting av sideporten – For å sikre kontinuerlig saltvannsskylling må du passe på at
sideporten ikke tettes til.
Betydelig blodlekkasje – Pass på at det ikke lekker betydelige mengder blod gjennom
hemostaseventilen under prosedyren.
Kontroll av den sterile emballasjen – Kontroller den sterile emballasjen og produktet før bruk.
Hvis den sterile emballasjen eller produktet har tegn på skade, skal produktet ikke brukes. Ta
kontakt med den lokale Medtronic-representanten.
Eksponering for røntgen og gjennomlysning – Ved bruk av gjennomlysning under
kateterablasjonsprosedyrer kan både pasienter og laboratoriepersonell bli utsatt for betydelig
røntgeneksponering. Langvarig eksponering kan føre til akutt stråleskade og økt fare for
somatiske og genetiske effekter. Ved kateterablasjon skal den mulige strålingseksponeringen i
forbindelse med prosedyren vurderes, og det må iverksettes nødvendige tiltak for å redusere
denne eksponeringen. Overvei nøye før produktet brukes på gravide kvinner, og unngå
røntgeneksponering.
5 Bivirkninger
Potensielle bivirkninger forbundet med kanylering av perifere blodårer og plassering av hylse og
dilatator i hjertet omfatter, men er ikke begrenset til, følgende:
• Komplikasjoner på tilgangsstedet (hematom, infeksjon, trombose, ekkymose,
AV-fistel, blødning fra innstikkstedet,
hemoragi)
• Luftemboli
• Arytmi (atrieflimmer, atrieflutter, ventrikulær takykardi)
• Hjertestans
• Ubehag, smerte eller trykk i brystet
• Spasme, disseksjon eller trombose i koronararterie
• Død
• Endokarditt
• AV-blokk som krever permanent pacemaker
• Hemotoraks
• Myokardinfarkt
• Perforasjon av vev i og rundt hjertet
• Perikardial effusjon, tamponade
• Perikarditt
• Pleural efffusjon
• Pneumotoraks
• Pseudoaneurisme
• Lungeødem
• Lungeemboli
• Slag
• Trombe
• Transient iskemisk attakk (TIA)
• Vasovagal reaksjon
6 Bruksanvisning
Merk! Før hylsen føres inn i pasienten, skal du teste krumningsmekanismen for å sikre at den
fungerer som den skal.
1. Bruk aseptisk teknikk og opprett tilgang til blodåren ved hjelp av en egnet introducer.
2. Før en kompatibel guidewire (se Spesifikasjoner) gjennom blodkarene og inn i ønsket
posisjon ved hjelp av standardteknikker for vaskulær tilgang.
3. Skyll hylsens sideport- og dilatatorlumen med sterilt saltvann.
4. Sørg for at hylsen er i en nøytral (ikke-bøyd) posisjon, og fukt dilatatorskaftet med sterilt
saltvann før innføring gjennom hemostaseventilen.
5. Begynn å montere dilatatoren og hylsen sammen ved å føre den distale tuppen på
dilatatoren inn i hemostaseventilen slik at den bøyde enden på dilatatoren er vinkelrett på
hemostaseventilen (se Figur 2).
Figur 2. FlexCath Select styrbar hylse
6. Fortsett å føre dilatatoren inn i hylsen til dilatatormuffen låses på plass i hylsemuffen.
Merk! Etiketten på dilatatormuffen skal være på linje med merket på hylsehåndtaket, slik at
dilatatorens krumning er i samme retning som orienteringen til hylsekrumningen, og
sideporten (se Figur 3).
Figur 3. FlexCath Select styrbar hylse
7. Før hylse/dilatator-enheten over guidewiren og inn i blodkaret med en lett vridende
bevegelse inn i SVC.
8. Fjern guidewiren.
9. Før inn den riktig klargjorte transseptale nålen i hylse/dilatator-enheten slik at
krumningsindikatoren på den transseptale nålen er på linje med sideporten.
Merk! Den transseptale nålen skal brukes sammen med en mandreng for å unngå at
dilatatorens indre lumen skjæres opp.
10. Trekk enheten ned i høyre atrium for å klargjøre for transseptal punksjon.
11. Bruk gjennomlysning og utfør transseptal punksjon med trykkmålinger, kontrastinjeksjon
eller begge deler. Bekreft riktig plassering i venstre atrium.
12. Skyv den transseptalen nålen inn i dilatatoren og fjern dilatator/nål-enheten sakte fra hylsen.
Merk! Fjern dilatatoren langsomt for å redusere faren for at det skapes vakuum i hylsen. Blod
skal kunne aspireres fritt gjennom sideporten. Hvis ikke skal du trekke tilbake hylsen,
ettersom det kan være at hylsens tupp ligger inn mot veggen i atriet eller i en lungevene.
13. Aspirer blod gjennom sideporten, og forsikre deg om at det ikke er luft i hylsen. Utfør
aspirasjon eller spontan tilbakeflow av blod før du setter kateteret i hylsen.
Merk! Utfør dette trinnet etter alle kateterutskiftninger.
14. Når det er opprettet tilgang, skal antikoagulasjonsbehandling opprettholdes.
15. Klargjør kateteret i henhold til instruksjonene fra produsenten.
16. Før inn kateteret og posisjoner hylsen.
Merk!
• Det kan hjelpe innføringen hvis du fukter kateterskaftet.
• Hemostaseventilen har et fast anslag for å hindre at innføringshylser åpner forseglingen.
39
Norsk

• Komponentene skal alltid føres inn og trekkes ut langsomt slik at det dannes minst mulig
vakuum.
• Hylsen skal også skylles mens et kateter er på plass.
17. Før hylsen trekkes tilbake, må du forsikre deg om at den er i nøytral (ikke krummet) posisjon.
7 Spesifikasjoner
Total lengde 81 cm (31,9 in)
Nyttbar lengde 65 cm (25,6 in)
Indre diameter 3,3 mm (10 Fr) (0,13 in)
Ytre diameter 4,3 mm (13 Fr) (0,17 in)
Dilatatorens lengde 86 cm (33,9 in)
Røntgentett markør 5 mm (0,2 in) proksimalt for hylsens tupp
Kompatibel guidewire 0,81 mm (0,032 in) til 0,89 mm (0,035 in)
Kompatibel transseptal nål 89 cm (35,0 in) eller lenger
Miljømessige parametere
Anbefalt forsendelsestemperatur
Anbefalt oppbevaringstemperatur
Bruk 15°C til 30°C (59°F til 86°F) ved høyder under 2400 m (8000 ft)
−35°C til 58°C (−31°F til 136°F), 85 % relativ fuktighet (ikkekondenserende)
Gjennomsnittlig 22°C (72°F) med et standardavvik på 2,7°C
(4,86°F) og handlingskrevende kontrollgrenser på 15°C til
30°C (59°F til 86°F)
over havet
8 Ansvarsfraskrivelse fra Medtronic
Du finner fullstendig garantiinformasjon i den medfølgende ansvarsfraskrivelsen.
9 Service
Medtronic har høyt kvalifiserte, opplærte representanter og ingeniører over hele verden som står
til tjeneste for deg, og som ved forespørsel gir kvalifisert sykehuspersonell opplæring i bruk av
produkter fra Medtronic. Medtronic har også en rekke profesjonelle medarbeidere som kan gi
teknisk veiledning til brukerne av produktene. Ved behov for ytterligere informasjon kan du
kontakte den lokale Medtronic-representanten eller ringe eller skrive til Medtronic på
telefonnummeret eller adressen som er oppgitt på bakpermen.
Norsk
40

1 Opis
65 cm
(25,6 cala)
16 cm
(6,3 cala)
86 cm
(33,9 cala)
Osłona sterowalna FlexCath™ Select firmy Medtronic jest przezskórnym introduktorem cewnika
wyposażonym w zastawkę, umożliwiającym wprowadzanie, wycofywanie i wymianę cewników i
prowadników, a jednocześnie minimalizującym utratę krwi. Wbudowany port boczny z kranikiem
umożliwia podawanie ciągłych wlewów kroplowych, iniekcję przez kanał środkowy,
przepłukiwanie, aspirację, pobieranie próbek krwi i monitorowanie ciśnienia.
Rycina 1. Osłona sterowalna FlexCath Select
Razem z osłoną sterowalną FlexCath Select, w tym samym opakowaniu, dostarczane jest
rozszerzadło. Poniższa tabela zawiera informacje dotyczące osłony:
Model
990065 3,3 mm (10 Fr)
Osłona może być wyginana w celu usprawnienia manewrowania cewnikami wprowadzanymi
przez nią do prawej lub lewej jamy serca.
Osłony sterowalnej FlexCath Select rozmiar 10 Fr można używać z cewnikami diagnostycznymi
i ablacyjnymi firmy Medtronic o maksymalnym rozmiarze 9 Fr.
Rozszerzadło osłony sterowalnej FlexCath Select rozmiar 10 Fr jest zgodne z igłami
transseptalnymi HeartSpan firmy Merit Medical o długości 89 cm lub większej.
Średnica wewnętrzna Średnica zewnętrzna Długość użytkowa
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Zawartość opakowania
Dostarczana osłona sterowalna FlexCath Select jest jałowa. Opakowanie zawiera następujące
elementy:
• 1 osłona sterowalna;
• 1 rozszerzadło;
• dokumentacja produktu.
2 Wskazania do stosowania
Osłona sterowalna FlexCath Select jest przeznaczona do przezskórnego wprowadzania cewnika
do układu naczyń i do jam serca, w tym do lewych jam serca przez przegrodę
międzyprzedsionkową. Możliwość odchylania osłony ułatwia umieszczanie cewnika w żądanym
położeniu.
3 Przeciwwskazania
Umieszczanie osłony sterowalnej FlexCath Select w lewym przedsionku lub lewej komorze serca
jest przeciwwskazane, jeśli u pacjenta występuje którykolwiek z poniższych stanów:
• U pacjenta występuje łatka lub okluder przegrody międzyprzedsionkowej lub
przeprowadzono inną interwencję chirurgiczną w obrębie lub w bezpośrednim sąsiedztwie
przegrody międzyprzedsionkowej.
• U pacjenta występuje skrzeplina w lewym przedsionku serca.
• U pacjenta stwierdzono lub podejrzewa się śluzaka przedsionka serca.
4 Ostrzeżenia i środki ostrożności
Energia ablacji – Gdy osłona jest używana w trakcie ablacji, wszystkie elementy używane do
ablacji muszą znajdować się poza osłoną.
Aspiracja powietrza – Przed zaaspirowaniem roztworu i przepłukiwaniem osłony należy wyjąć
prowadnik i rozszerzadło z osłony. Ta czynność minimalizuje ryzyko zaaspirowania powietrza
przez zastawkę osłony.
Terapia przeciwkrzepliwa – Pacjentom poddawanym zabiegom po lewej stronie serca lub
zabiegom przezprzegrodowym oraz wybranym pacjentom przechodzącym zabiegi po prawej
stronie serca należy w okresie okołozabiegowym podawać odpowiednie dawki leków
przeciwkrzepliwych. Aby zminimalizować krwawienie i powikłania zakrzepowe, należy w okresie
okołozabiegowym podawać pacjentowi leki przeciwkrzepliwe zgodnie z normami
obowiązującymi w placówce.
Wypływ krwi – Upewnić się, że kranik jest zamknięty po przepłukaniu lub aspiracji, aby zapobiec
niezamierzonemu wypływowi krwi przez port boczny.
Usuwanie odpadów stwarzających zagrożenie biologiczne – Wszystkie zużyte urządzenia
i komponenty sterylne należy usunąć zgodnie z procedurami obowiązującymi w szpitalu.
Wstrzyknięcie środka cieniującego – Nie należy wstrzykiwać roztworu środka cieniującego do
osłony za pomocą mechanicznego systemu iniekcyjnego.
Skręcanie rozszerzadła – Nie skręcać rozszerzadła podczas blokowania w łączniku zastawki
lub po zablokowaniu w łączniku zastawki. Może to spowodować przemieszczenie końcówki
rozszerzadła na końcu dystalnym w stosunku do portu bocznego na końcu proksymalnym.
Nie sterylizować ponownie – Urządzenia nie należy ponownie sterylizować w celu ponownego
użycia. Resterylizacja może naruszyć integralność mechaniczną urządzenia lub wywołać ryzyko
skażenia urządzenia prowadzące do urazu, zachorowania lub zgonu pacjenta.
Ryzyko zatoru – Wprowadzenie jakiegokolwiek cewnika lub osłony do układu krążenia wiąże się
z ryzykiem powstania zatoru powietrznego, który może doprowadzić do zamknięcia naczyń i
zawału tkanki o poważnych konsekwencjach. Stosowanie z tym urządzeniem cewników o
rozmiarze mniejszym niż 9 Fr może skutkować zwiększonym ryzykiem wystąpienia zatoru
powietrznego. Elementy należy zawsze wprowadzać i wycofywać powoli oraz stosować
przepłukiwanie, aby zminimalizować wytwarzane podciśnienie, a tym samym ryzyko zatoru
powietrznego.
Data ważności – Należy sprawdzić, czy nie upłynął termin przydatności osłony do użycia. Nie
należy używać produktu, którego termin przydatności minął.
Uszkodzenie żyły udowej – Należy zachować ostrożność, aby zminimalizować uszkodzenia
żyły udowej i miejsca dostępu w trakcie wprowadzania osłony, manipulowania osłoną i
wycofywania jej. Do powikłań cewnikowania żyły udowej należą krwiak i zakrzepica.
Wymóg stosowania fluoroskopii przy umieszczaniu osłony – Zdecydowanie zaleca się
stosowanie fluoroskopii podczas manipulowania osłoną i umieszczania jej. Manipulowanie
osłoną bez obserwacji fluoroskopowej może doprowadzić do uszkodzenia struktur serca i
naczyń.
Tylko do jednorazowego użycia – Urządzenie jest przeznaczone tylko do jednorazowego
użycia u jednego pacjenta. Urządzenia nie należy ponownie używać, poddawać ponownej
obróbce ani ponownie sterylizować w celu ponownego użycia. Ponowne użycie, obróbka lub
resterylizacja może naruszyć integralność mechaniczną urządzenia lub wywołać ryzyko
skażenia urządzenia prowadzące do urazu, zachorowania lub śmierci pacjenta.
Częste przepłukiwanie – Zaleca się regularne przepłukiwanie osłony:
• Aby zapobiec zastojowi krwi, powstawaniu skrzepów, zatorów i wystąpieniu poważnych
urazów u pacjenta.
• Każdorazowo po wstrzyknięciu środka cieniującego, aby uniknąć zatrzymania roztworu
środka cieniującego w kanale.
Obchodzenie się z osłoną i środki ostrożności – Podczas obsługiwania urządzenia:
41
Polski

• Podczas manipulowania urządzeniem należy zachować szczególną ostrożność. Nieuwaga
może doprowadzić do urazu, takiego jak perforacja, tamponada, indukcja arytmii lub blok
serca.
• Nie należy używać nadmiernej siły przy wprowadzaniu lub wycofywaniu urządzenia,
zwłaszcza w razie napotkania oporu.
• Należy unikać umieszczania urządzenia wokół strun ścięgnistych, ponieważ zwiększałoby to
ryzyko uwięźnięcia w sercu, a w konsekwencji powodowałoby konieczność interwencji
chirurgicznej lub naprawy uszkodzonych tkanek.
• Nie należy używać osłony, jeśli jest ona załamana lub uszkodzona.
Dojście do lewego przedsionka – Aby uniknąć wprowadzania rozszerzadła lub osłony do
niepożądanego miejsca, nie należy wprowadzać rozszerzadła lub osłony przez przegrodę
międzyprzedsionkową bez wcześniejszego potwierdzenia odpowiedniego dojścia do lewego
przedsionka.
Niezbędne wyposażenie szpitalne – Podczas stosowania zespołu osłony sterowalnej w
pobliżu powinien znajdować się zestaw do defibrylacji zewnętrznej gotowy do natychmiastowego
użycia.
Inne cewniki, urządzenia lub prowadniki – Należy unikać splątania osłony z innymi
cewnikami, urządzeniami lub prowadnikami. Takie splątanie może spowodować konieczność
interwencji chirurgicznej.
Sztuczne zastawki serca – Nie należy przeprowadzać urządzenia przez sztuczną zastawkę
serca (mechaniczną lub biologiczną). Urządzenie może uwięznąć w zastawce, uszkadzając ją
i powodując niewydolność zastawek lub przedwczesną awarię sztucznej zastawki.
Wykwalifikowani użytkownicy – To urządzenie powinno być używane wyłącznie przez lub pod
nadzorem lekarzy przeszkolonych w zabiegach cewnikowania serca.
Wymagane środowisko stosowania – Zabiegi cewnikowania serca powinny być wykonywane
wyłącznie w kompletnie wyposażonej placówce medycznej.
Aspiracja przez port boczny – Przeprowadzić aspirację przez port boczny podczas
wycofywania rozszerzadła, cewnika, igły, prowadników lub innych urządzeń.
Niedrożność portu bocznego – Należy zachować ostrożność, aby nie dopuścić do
niedrożności portu bocznego i zapewnić skuteczne przepłukiwanie roztworem soli fizjologicznej.
Większy wyciek krwi – W trakcie zabiegu należy zwracać uwagę, czy przez zastawkę
hemostatyczną nie wycieka znaczna ilość krwi.
Kontrola sterylnego opakowania – Przed użyciem należy obejrzeć sterylne opakowanie i
urządzenie. Jeśli sterylne opakowanie lub urządzenie nosi ślady uszkodzenia, nie należy używać
urządzenia. Należy skontaktować się z miejscowym przedstawicielem firmy Medtronic.
Narażenie na promieniowanie RTG i fluoroskopię – Stosowanie fluoroskopii podczas
zabiegów ablacji serca za pomocą cewnika stanowi ryzyko narażenia pacjentów i członków
personelu laboratorium na intensywne promieniowanie RTG. Intensywne narażenie na
promieniowanie może doprowadzić do ostrych urazów popromiennych i zwiększone ryzyko
skutków somatycznych i genetycznych. Przeprowadzanie ablacji za pomocą cewnika powinno
być poprzedzone stosowną analizą ekspozycji na promieniowanie w związku z zabiegiem i
podjęciem kroków mających na celu zminimalizowanie tej ekspozycji. Przed zastosowaniem
urządzenia u kobiet w ciąży należy starannie rozważyć potencjalne ryzyko oraz unikać ekspozycji
na promieniowanie rentgenowskie.
5 Zdarzenia niepożądane
Do potencjalnych zdarzeń niepożądanych związanych z kaniulacją naczyń obwodowych i
umieszczaniem osłony oraz rozszerzadła w sercu należą między innymi:
• Powikłania w miejscu wprowadzenia
(krwiak, zakażenie, zakrzepica, wybroczyny, przetoka tętniczo-żylna, krwawienie
w miejscu wkłucia, krwotok)
• Zator powietrzny
• Arytmia (migotanie przedsionków, trzepotanie przedsionków, częstoskurcz komorowy)
• Zatrzymanie akcji serca
• Uczucie dyskomfortu, ból lub ucisk w
klatce piersiowej
• Skurcz, rozwarstwienie, zakrzepica tętnic
wieńcowych
• Zgon
• Zapalenie wsierdzia
• Blok serca stwarzający konieczność stosowania stałej stymulacji serca
• Krwiak opłucnej
• Zawał mięśnia sercowego
• Perforacja serca lub otaczającej tkanki
• Wysięk osierdziowy, tamponada
• Zapalenie osierdzia
• Wysięk opłucnowy
• Odma opłucnowa
• Tętniak rzekomy
• Obrzęk płuc
• Zator tętnicy płucnej
• Udar
• Skrzeplina
• Przemijający atak niedokrwienny (TIA)
• Reakcja wazowagalna
6 Instrukcja użytkowania
Uwaga: Przed wprowadzeniem osłony do ciała pacjenta należy przetestować mechanizm
wyginania, aby upewnić się, że działa on poprawnie.
1. Stosując technikę aseptyczną, utworzyć dojście do układu naczyń, korzystając z
odpowiedniego introduktora.
2. Wprowadzić zgodny prowadnik (patrz „Dane techniczne”) do układu naczyń i do żądanego
miejsca, stosując standardowe techniki dostępu naczyniowego.
3. Przepłukać port boczny i kanał rozszerzadła sterylnym roztworem soli.
4. Upewnić się, że osłona znajduje się w pozycji neutralnej (wyprostowanej) i przed
wprowadzeniem rozszerzadła przez zastawkę hemostatyczną zwilżyć jego trzon sterylnym
roztworem soli.
5. Rozpocząć montaż zespołu rozszerzadła i osłony, wprowadzając dystalną końcówkę
rozszerzadła do zastawki hemostatycznej w taki sposób, aby zakrzywiona krawędź
rozszerzadła znajdowała się prostopadle do zastawki hemostatycznej (patrz Ryc. 2).
Rycina 2. Osłona sterowalna FlexCath Select
6. Kontynuować wprowadzanie rozszerzadła do osłony, do momentu aż łącznik rozszerzadła
zostanie zablokowany w łączniku osłony.
Uwaga: Etykieta na łączniku rozszerzadła powinna znajdować się w jednej linii z etykietą na
uchwycie osłony, aby zakrzywienie rozszerzadła było wyrównane w tym samym kierunku co
odchylenie osłony i portu bocznego (patrz Ryc. 3).
Rycina 3. Osłona sterowalna FlexCath Select
7. Delikatnym ruchem skręcającym nasunąć rozszerzadło zmontowane z osłoną na prowadnik
i wprowadzić do układu naczyń przez żyłę główną górną.
Polski
42

8. Wyjąć prowadnik.
9. Wprowadzić odpowiednio przygotowaną igłę transseptalną do zespołu rozszerzadła i
osłony tak, aby wskaźnik zakrzywienia na igle transseptalnej był zrównany z portem
bocznym.
Uwaga: Igła transseptalna powinna być używana wraz z mandrynem, aby nie dochodziło do
zdzierania powierzchni wewnętrznej kanału rozszerzadła.
10. Umieścić zmontowany zestaw w prawym przedsionku, aby przygotować urządzenie do
wykonania nakłucia transseptalnego.
11. Pod kontrolą fluoroskopową wykonać nakłucie transseptalne, przeprowadzając pomiar y
ciśnienia i/lub iniekcje środka cieniującego. Potwierdzić poprawne umiejscowienie
urządzenia w lewym przedsionku.
12. Wciągnąć igłę transseptalną do rozszerzadła i delikatnie usunąć zespół rozszerzadła i igły z
osłony.
Uwaga: Rozszerzadło wyjmować powoli, aby zmniejszyć ryzyko wytworzenia podciśnienia
w osłonce. Powinna być możliwa swobodna aspiracja krwi przez port boczny. Jeśli tak nie
jest, należy wycofać osłonę, ponieważ być może jej końcówka przylega do ściany
przedsionka lub żyły płucnej.
13. Zaaspirować krew przez port boczny i upewnić się, że w osłonie nie ma powietrza. Przed
wprowadzeniem cewnika do osłony przeprowadzić aspirację lub umożliwić spontaniczne
cofnięcie się krwi.
Uwaga: Wykonać ten krok po każdej wymianie cewnika.
14. Po uzyskaniu dostępu za pomocą osłony stale stosować leki przeciwkrzepliwe.
15. Przygotować cewnik zgodnie z instrukcją stosowania dostarczoną przez producenta.
16. Wprowadzić cewnik i umieścić osłonę w żądanym położeniu.
Uwagi:
• Zwilżenie trzonu cewnika może ułatwić wprowadzenie.
• Zastawka hemostatyczna wyposażona jest w dodatni ogranicznik, który zapobiega
otwieraniu uszczelki przez osłony matrycy.
• Elementy należy zawsze wprowadzać i wycofywać powoli, aby zminimalizować
wytwarzane podciśnienie.
• Przepłukiwanie osłony należy przeprowadzać także przy wprowadzonym cewniku.
17. Przed wycofaniem osłony należy upewnić się, że znajduje się ona w pozycji neutralnej
(niewygiętej).
7 Dane techniczne
Długość całkowita
Długość użytkowa 65 cm (25,6 in)
Średnica wewnętrzna 3,3 mm (10 Fr) (0,13 in)
Średnica zewnętrzna 4,3 mm (13 Fr) (0,17 in)
Długość rozszerzadła 86 cm (33,9 in)
Znacznik radiocieniujący 5 mm (0,2 in) proksymalnie względem końcówki osłony
Zgodne prowadniki Od 0,81 mm (0,032 in) do 0,89 mm (0,035 in)
Zgodne igły transseptalne 89 cm (35,0 in) lub dłuższe
Parametry środowiskowe
Zalecana temperatura transportu
Zalecana temperatura przechowywania
Użytkowanie Od 15°C do 30°C (od 59°F do 86°F) na wysokości mniejszej
81 cm (31,9 in)
Od -35°C do 58°C (od -31°F do 136°F); wilgotność względna
85% (bez kondensacji)
Średnio 22°C (72°F) z odchyleniem standardowym 2,7°C
(4,86°F). W przypadku temperatury wykraczającej poza
zakres od 15°C do 30°C (od 59°F do 86°F) należy podjąć
działania zapobiegawcze
niż 2400 m (8000 stóp) nad poziomem morza
8 Wyłączenie gwarancji firmy Medtronic
Pełne informacje na temat gwarancji zawiera dołączony dokument wyłączenia gwarancji.
9 Obsługa techniczna
Firma Medtronic zatrudnia na całym świecie wysoko wykwalifikowanych przedstawicieli
i inżynierów gotowych służyć pomocą użytkownikom, a na życzenie prowadzących również
szkolenia z zakresu użytkowania produktów firmy Medtronic dla wykwalifikowanego personelu
szpitalnego. Firma Medtronic zatrudnia ponadto zespół konsultantów zapewniających
użytkownikom profesjonalne konsultacje techniczne. W celu uzyskania dodatkowych informacji
należy skontaktować się bezpośrednio z miejscowym przedstawicielem firmy Medtronic bądź
skontaktować się telefonicznie lub listownie z firmą Medtronic, używając numeru telefonu lub
danych adresowych zamieszczonych na tylnej stronie okładki.
43
Polski

1 Descrição
65 cm
(25,6 pol.)
16 cm
(6,3 pol.)
86 cm
(33,9 pol.)
A bainha direcionável FlexCath™ Select da Medtronic é um introdutor de cateter percutâneo
equipado com uma válvula para permitir a introdução, remoção e troca de cateteres e fios, ao
mesmo tempo que minimiza a perda de sangue. Possui uma porta lateral com torneira de
passagem integrada para permitir a perfusão contínua, injeção através do lúmen central,
irrigação, aspiração, coleta de sangue e monitoramento da pressão.
Figura 1. Bainha direcionável FlexCath Select
A bainha direcionável FlexCath Select é fornecida com um dilatador. A bainha está descrita na
tabela seguinte:
Modelo
990065 3,3 mm (10 Fr)
A bainha pode ser defletida para proporcionar capacidade de manobra adicional aos cateteres
que são avançados através da bainha até a câmara direita ou esquerda do coração.
A bainha direcionável FlexCath Select de 10 Fr pode ser utilizada com cateteres de diagnóstico
e de ablação da Medtronic de tamanho até 9 Fr.
O dilatador da bainha direcionável FlexCath de 10 Fr é compatível com as agulhas transeptais
Merit Medical HeartSpan de 89 cm e maiores.
Diâmetro interno Diâmetro externo Comprimento útil
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Conteúdo da embalagem
A bainha direcionável FlexCath Select é fornecida esterilizada. A embalagem contém os
seguintes componentes:
• 1 bainha direcionável
• 1 dilatador
• Documentação do produto
2 Indicações de utilização
A bainha direcionável FlexCath Select se destina a ser utilizada na introdução percutânea de
cateteres na vasculatura e nas câmaras do coração, incluindo o lado esquerdo do coração
através do septo interatrial. A deflexão da bainha facilita o posicionamento do cateter.
3 Contraindicações
A bainha direcionável FlexCath Select é contraindicada para colocação no átrio ou ventrículo
esquerdos, se alguma das seguintes condições se aplicar ao paciente:
• O paciente tem um patch ou oclusor septal intra-atrial ou foi submetido a outra intervenção
cirúrgica no septo intra-atrial ou perto dele.
• O paciente tem um trombo no átrio esquerdo.
• O paciente teve um diagnóstico de mixoma atrial ou suspeita do mesmo.
4 Avisos e precauções
Energia de ablação – No caso de utilizar a bainha na presença de energia de ablação, deve-se
proceder com cuidado para garantir que todos os elementos de ablação estão fora da bainha.
Aspiração de ar – Retire o fio-guia da bainha antes de aspirar e irrigar a bainha. Essa ação
minimiza a aspiração de ar através da válvula da bainha.
Terapia anticoagulante – Administre os níveis adequados de terapia anticoagulante
perioperatória aos pacientes submetidos a procedimentos cardíacos do lado esquerdo e
transeptais e aos pacientes selecionados submetidos a procedimentos do lado direito. Para
minimizar as hemorragias e as complicações trombóticas, administre terapia anticoagulante
perioperatória de acordo com as normas da instituição.
Hemorragia retrógrada – Certifique-se de que a torneira de passagem está na posição fechada
após a irrigação ou aspiração para evitar uma hemorragia retrógrada acidental através da por ta
lateral.
Eliminação de resíduos biológicos – Descarte todos os dispositivos e componentes estéreis
utilizados de acordo com os procedimentos hospitalares.
Injeção de contraste – Não utilize um sistema de injeção elétrico para injetar solução de
contraste na bainha.
Torção do dilatador – Não torça o dilatador durante ou após encaixá-lo no conector da válvula.
Tal ação pode provocar desalinhamento da ponta do dilatador na extremidade distal em relação
à porta lateral na extremidade proximal.
Não reesterilizar – Não reesterilize este dispositivo com o fim de reutilizá-lo. A reesterilização
poderá comprometer a integridade estrutural do dispositivo ou originar um risco de
contaminação do dispositivo, o que poderá causar lesões, doença ou mesmo a morte do
paciente.
Risco de embolia – A inserção de qualquer cateter ou bainha no sistema circulatório acarreta o
risco de embolia gasosa, o que pode obstruir vasos e causar um infarto tecidual com graves
consequências. A utilização de cateteres menores do que 9 Fr pode produzir um risco acrescido
de embolia gasosa. Em todas as circunstâncias, avance e retire lentamente os componentes e
utilize irrigação para minimizar o vácuo criado e assim minimizar o risco de embolia gasosa.
Data de validade – Verifique se a bainha se encontra dentro da respectiva data de validade. Não
utilize o produto caso a data de validade tenha expirado.
Lesão da veia femoral – Deve-se proceder com cuidado para minimizar as lesões da veia
femoral e do local de acesso durante a inserção, a manipulação ou a remoção da bainha. As
complicações associadas à cateterização da veia femoral incluem hematomas e trombose.
É necessária fluoroscopia para a colocação da bainha – A utilização de fluoroscopia durante
a manipulação e a colocação da bainha é fortemente recomendada. A manipulação da bainha
sem fluoroscopia poderá causar danos nas estruturas cardíacas e vasculares.
Exclusivamente para utilização única – Este dispositivo deve ser utilizado uma única vez em
um único paciente. Não reutilize, reprocesse nem reesterilize este dispositivo com o objetivo de
reutilizá-lo. A reutilização, o reprocessamento ou a reesterilização poderão comprometer a
integridade estrutural do dispositivo ou originar um risco de contaminação do dispositivo, o que
poderia causar lesões, doença ou mesmo a morte do paciente.
Irrigação frequente – É recomendável a irrigação regular da bainha:
• para evitar a estagnação sanguínea, coágulos, êmbolos e lesões graves no paciente;
• para evitar que a solução de contraste adira ao interior do lúmen após cada injeção de
contraste.
Manuseio e cuidados – Quando manusear o dispositivo:
• Proceda com extremo cuidado ao manipular o dispositivo. Caso contrário, pode resultar em
lesões como perfuração, tamponamento, indução de arritmia ou bloqueio cardíaco.
• Não utilize força excessiva para avançar ou recuar o dispositivo, especialmente se encontrar
resistência.
Português (Brasil)
44

• Evite posicionar o dispositivo em torno das cordas tendinosas, uma vez que isso aumenta a
probabilidade de aprisionamento dentro do coração e pode obrigar à realização de uma
intervenção cirúrgica ou ao reparo dos tecidos lesionados.
• Não utilize a bainha caso esta se encontre torcida ou danificada.
Acesso atrial esquerdo – Não avance o dilatador ou a bainha através do septo interatrial sem
primeiro confirmar o acesso atrial esquerdo, para evitar o avanço desses componentes em um
local indesejado.
Equipamentos hospitalares necessários – Tenha equipamento de desfibrilação externo
disponível para utilização imediata durante a utilização do conjunto da bainha direcionável.
Outros cateteres, dispositivos ou fios – Evite o emaranhamento da bainha com outros
cateteres, dispositivos ou fios. Esse emaranhamento poderá necessitar de intervenção cirúrgica.
Válvulas cardíacas protéticas – Não passe o dispositivo através de uma válvula cardíaca
prostética (mecânica ou de tecido). O dispositivo poderá ficar preso na válvula, danificando-a e
causando insuficiência valvular ou falha prematura da válvula prostética.
Usuários qualificados – Este equipamento apenas deve ser utilizado por ou sob a supervisão
de médicos com treinamento em procedimentos de cateterismo cardíaco.
Ambiente de utilização necessário – Os procedimentos de cateterismo cardíaco devem ser
efetuados apenas em instalações totalmente equipadas.
Aspiração pela porta lateral – Aspire a porta lateral quando retirar o dilatador, o cateter, a
agulha, fios ou outros dispositivos.
Obstrução da porta lateral – Deve-se proceder com cuidado para evitar obstruir de alguma
forma a porta lateral e assim garantir a eficácia da irrigação com soro fisiológico.
Derrame sanguíneo significativo – Deve-se proceder com cuidado para garantir que não
ocorra um derrame sanguíneo significativo através da válvula hemostática durante o
procedimento.
Inspeção da embalagem estéril – Antes de utilizar, inspecione a embalagem e o dispositivo
estéreis. Caso a embalagem ou o dispositivo estéril apresente danos, não utilize o dispositivo.
Entre em contato com o seu representante local da Medtronic.
Exposição fluoroscópica e aos raios X – A utilização de fluoroscopia durante procedimentos
de cateterismo de ablação acarreta riscos de exposição significativa aos raios X, tanto para os
pacientes como para o pessoal do laboratório. A exposição extensa pode causar lesões agudas
por radiação e um risco aumentado de efeitos somáticos e genéticos. Efetue o cateterismo de
ablação somente após der dado a devida atenção à potencial exposição à radiação associada ao
procedimento e após ter tomado medidas para minimizar essa exposição. Pondere
cuidadosamente e evite a exposição a raios X antes de utilizar o dispositivo em mulheres
grávidas.
5 Efeitos adversos
Os potenciais efeitos adversos associados à canulação da vasculatura periférica e à inserção
intracardíaca da bainha e do dilatador podem incluir, entre outras, as seguintes patologias:
• Complicações no local de acesso (hematoma, infecção, trombose, equimose, fístula AV, hemorragia no local de punção,
hemorragia)
• Embolia gasosa
• Arritmia (fibrilação atrial, flutter atrial, taquicardia ventricular)
• Parada cardíaca
• Desconforto, dor ou pressão torácica
• Espasmo, dissecação ou trombose das
coronárias
• Morte
• Endocardite
• Bloqueio cardíaco, necessitando de
marca-passo permanente
• Hemotórax
• Infarto do miocárdio
• Perfuração do tecido cardíaco ou circundante
• Efusão, tamponamento pericárdico
• Pericardite
• Efusão pleural
• Pneumotórax
• Pseudoaneurisma
• Edema pulmonar
• Embolia pulmonar
• Derrame
• Trombos
• Ataque isquêmico transitório (AIT)
• Reação vasovagal
6 Instruções de utilização
Observação: Antes de inserir a bainha no paciente, teste o mecanismo de deflexão de forma a
garantir que está operacional.
1. Utilizando uma técnica asséptica, crie um acesso vascular com um introdutor adequado.
2. Utilizando técnicas de acesso vascular padrão, insira um fio-guia compatível (consulte as
Especificações) através da vasculatura até a posição pretendida.
3. Irrigue a por ta lateral da bainha e o lúmen do dilatador com soro fisiológico estéril.
4. Cer tifique-se de que a bainha se encontra em uma posição neutra (não defletida) e
umedeça a haste do dilatador com soro fisiológico estéril antes de inseri-la através da
válvula hemostática.
5. Comece a montagem do dilatador e da bainha introduzindo a ponta distal do dilatador na
válvula hemostática, de modo que a borda curva do dilatador fique perpendicular à válvula
hemostática (consulte a Figura 2).
Figura 2. Bainha direcionável FlexCath Select
6. Continue avançando o dilatador para dentro da bainha até que o conector do dilatador
encaixe completamente no conector da bainha.
Observação: A etiqueta do conector do dilatador deve ficar alinhada com a etiqueta do
cabo da bainha, de modo que a curva do dilatador fique alinhada na mesma orientação da
direção de deflexão da bainha e da porta lateral (consulte Figura 3).
Figura 3. Bainha direcionável FlexCath Select
7. Passe o conjunto dilatador/bainha sobre o fio-guia e insira-o na vasculatura com um ligeiro
movimento de torção na veia cava superior (VCS).
8. Retire o fio-guia.
9. Introduza a agulha transeptal devidamente preparada no conjunto dilatador/bainha, de
modo que o indicador de curvatura da agulha transeptal fique alinhado com a porta lateral.
Observação: A agulha transeptal deve ser utilizada em conjunto com um estilete a fim de
evitar a raspagem do lúmen interno do dilatador.
10. Puxe o conjunto para baixo, até o átrio direito, para preparar para a punção transeptal.
11. Sob orientação fluoroscópica, realize a punção transeptal utilizando medições de pressão,
injeção de contraste ou ambas. Confirme a colocação correta no átrio esquerdo.
12. Puxe a agulha transeptal para dentro do dilatador e remova lentamente o conjunto de
dilatador e agulha da bainha.
45
Português (Brasil)

Observação: Remova o dilatador lentamente para reduzir a possibilidade de criação de
vácuo na bainha. Deve ser possível aspirar o sangue livremente através da porta lateral. Se
isso não acontecer, retire a bainha, pois a respectiva ponta poderá estar encostada à parede
do átrio ou de uma veia pulmonar.
13. Aspire o sangue através da porta lateral e certifique-se de que a bainha não possui ar. Antes
de inserir um cateter na bainha, aspire ou permita o refluxo sanguíneo espontâneo.
Observação: Efetue este passo após qualquer troca de cateter.
14. Após o acesso com a bainha, mantenha a terapia anticoagulante.
15. Prepare o cateter de acordo com as instruções de utilização do fabricante.
16. Insira o cateter e posicione a bainha.
Observações:
• O umedecimento do eixo do cateter pode ajudar a facilitar a introdução.
• O válvula hemostática tem uma parada positiva para evitar que quaisquer dispositivos
de captura abram a vedação.
• Para minimizar o vácuo criado, insira e retire sempre os componentes lentamente.
• A bainha também deve ser irrigada durante a inserção de um cateter.
17. Antes de retirar a bainha, certifique-se de que esta está na posição neutra (não defletida).
7 Especificações
Comprimento total
Comprimento útil 65 cm (25,6 in)
Diâmetro interno 3,3 mm (10 Fr) (0,13 in)
Diâmetro externo 4,3 mm (13 Fr) (0,17 in)
Comprimento do dilatador 86 cm (33,9 in)
Marcador radiopaco 5 mm (0,2 in) proximal em relação à ponta da bainha
Compatibilidade do fio-guia 0,81 mm (0,032 in) a 0,89 mm (0,035 in)
Agulha transeptal compatível 89 cm (35,0 in) ou maior
Parâmetros ambientais
Temperatura de transporte
recomendada
Temperatura de armazenamento recomendada
Operação 15°C a 30°C (59°F a 86°F) para altitudes inferiores a 2400 m
81 cm (31,9 in)
−35°C a 58°C (−31°F a 136°F); 85% de umidade relativa (sem
condensação)
Média de 22°C (72°F) com um desvio padrão de 2,7°C
(4,86°F) e limites de controle acionáveis de 15°C a 30°C (59°F
a 86°F)
(8000 pés) acima do nível do mar
8 Renúncia de garantia da Medtronic
Para obter informações completas sobre a garantia, consulte o documento de renúncia de
garantia anexo.
9 Assistência técnica
A Medtronic possui representantes e engenheiros altamente treinados localizados ao redor do
mundo para atendê-lo, e mediante solicitação, fornecer treinamento para a equipe qualificada do
hospital sobre o uso dos produtos da Medtronic. Além disso, a Medtronic dispõe de uma equipe
profissional de consultores para oferecer consultoria técnica aos usuários dos produtos. Para
mais informações, entre em contato com o representante local da Medtronic, telefone ou escreva
para a Medtronic no número de telefone ou endereço apropriado indicado na contracapa.
Português (Brasil)
46

1 Descrição
65 cm
(25,6 pol.)
16 cm
(6,3 pol.)
86 cm
(33,9 pol.)
A bainha direcionável Medtronic FlexCath™ Select é um introdutor de cateter percutâneo
equipado com uma válvula para permitir a introdução, remoção e troca de cateteres e fios, ao
mesmo tempo que minimiza a perda de sangue. Possui integrada uma porta lateral com torneira
de passagem para permitir a perfusão contínua, injeção através do lúmen central, irrigação,
aspiração, colheita de sangue e monitorização da pressão.
Figura 1. Bainha direcionável FlexCath Select
A bainha direcionável FlexCath Select é fornecida com um dilatador. A bainha está descrita na
tabela seguinte:
Modelo
990065 3,3 mm (10 Fr) (0,13 in
A bainha pode ser fletida para proporcionar capacidade de manobra adicional aos cateteres que
são avançados através da bainha até à câmara direita ou esquerda do coração.
A bainha direcionável FlexCath Select de 10 Fr pode ser utilizada com cateteres de diagnóstico
e de ablação da Medtronic até ao tamanho de 9 Fr.
O dilatador da bainha direcionável FlexCath Select de 10 Fr é compatível com as agulhas
transeptais HeartSpan da Merit Medical de 89 cm de comprimento e superiores.
Diâmetro interno Diâmetro externo Comprimento útil
[pol.])
4,3 mm (13 Fr) (0,17 in
[pol.])
65 cm (25,6 in [pol.])
1.1 Conteúdo da embalagem
A bainha direcionável FlexCath Select é fornecida esterilizada. A embalagem contém os
seguintes componentes:
• 1 bainha direcionável
• 1 dilatador
• Documentação do produto
2 Indicações de utilização
A bainha direcionável FlexCath Select destina-se a ser utilizada na introdução percutânea de
cateteres na vasculatura e nas câmaras do coração, incluindo o lado esquerdo do coração
através do septo interauricular. A flexão da bainha facilita o posicionamento do cateter.
3 Contraindicações
A bainha direcionável FlexCath Select está contraindicada para colocação na aurícula ou no
ventrículo esquerdo se alguma das seguintes condições se aplicar ao doente:
• O doente tem um "patch" ou oclusor septal intra-auricular ou foi submetido a outra
intervenção cirúrgica no septo intra-auricular ou perto deste.
• O doente tem um trombo na aurícula esquerda.
• o doente tiver um diagnóstico de mixoma auricular ou suspeita do mesmo.
4 Avisos e precauções
Energia de ablação – No caso de utilizar a bainha na presença de energia de ablação, deve
proceder com cuidado para garantir que todos os elementos de ablação estão fora da bainha.
Aspiração de ar – Retire o fio-guia da bainha antes de aspirar e irrigar a bainha. Esta ação
minimiza a aspiração de ar através da válvula da bainha.
Terapêutica anticoagulante – Administre os níveis adequados de terapêutica anticoagulante
perioperatória aos doentes submetidos a procedimentos cardíacos do lado esquerdo e
transeptais e a doentes selecionados submetidos a procedimentos do lado direito. Para
minimizar as hemorragias e as complicações trombóticas, administre terapêutica anticoagulante
perioperatória de acordo com as normas da instituição.
Hemorragia retrógrada – Certifique-se de que a torneira de passagem está numa posição
fechada após a irrigação ou aspiração, para evitar uma hemorragia retrógrada não desejada
através da porta lateral.
Eliminação de resíduos biológicos – Elimine todos os dispositivos e componentes
esterilizados usados de acordo com os procedimentos hospitalares.
Injeção de contraste – Não utilize um sistema de injeção potente para injeção da solução de
contraste na bainha.
Torção do dilatador – Não torça o dilatador quando o encaixar, ou depois, no conector da
válvula. Caso contrário, poderá causar o desalinhamento da ponta do dilatador na extremidade
distal em relação à porta lateral na extremidade proximal.
Não reesterilizar – Não reesterilize este dispositivo com o fim de o reutilizar. A reesterilização
poderá comprometer a integridade estrutural do dispositivo ou originar um risco de
contaminação do dispositivo, o que poderá causar lesões, doença ou mesmo a morte do doente.
Risco de embolia – A introdução de qualquer cateter ou bainha no sistema circulatório acarreta
o risco de embolia gasosa, o que pode obstruir vasos e causar um enfarte tecidular com graves
consequências. A utilização de cateteres de tamanho inferior a 9 Fr com este dispositivo poderá
representar um risco acrescido de embolia gasosa. Em todas as circunstâncias, avance e retire
os componentes lentamente e utilize irrigação para minimizar o vácuo criado e assim minimizar
o risco de embolia gasosa.
Prazo de validade – Verifique se a bainha se encontra dentro do respetivo prazo de validade.
Não utilize caso o prazo de validade do produto tenha expirado.
Lesão da veia femoral – Deve proceder-se com cuidado para minimizar as lesões da veia
femoral e do local de acesso durante a inserção, a manipulação ou a remoção da bainha. As
complicações associadas à cateterização da veia femoral incluem hematomas e trombose.
É necessária fluoroscopia para a colocação da bainha – A utilização de fluoroscopia durante
a manipulação e a colocação da bainha é vivamente recomendada. A manipulação da bainha
sem fluoroscopia poderá causar danos nas estruturas cardíacas e vasculares.
Destina-se apenas a uma utilização – Este dispositivo destina-se a ser utilizado uma única vez
num único doente. Não reutilize, reprocesse ou reesterilize este dispositivo com o fim de o
reutilizar. A reutilização, o reprocessamento ou a reesterilização poderão comprometer a
integridade estrutural do dispositivo ou originar um risco de contaminação do dispositivo, o que
poderia causar lesões, doença ou mesmo a morte do doente.
Irrigação frequente – Recomenda-se a irrigação regular da bainha:
• para prevenir a estagnação sanguínea, coágulos, êmbolos e lesões graves do doente;
• para evitar que a solução de contraste adira ao interior do lúmen após cada injeção de
contraste.
Manuseamento e cuidados – Quando manusear o dispositivo:
• Proceda com extremo cuidado ao manipular o dispositivo. Caso contrário, pode resultar em
lesões tais como perfuração, tamponamento, indução de arritmia ou bloqueio cardíaco.
• Não utilize força excessiva para fazer avançar ou recuar o dispositivo, especialmente se
encontrar resistência.
47
Português (Portugal)

• Evite posicionar o dispositivo em torno das cordas tendinosas, uma vez que isso aumenta a
probabilidade de encarceramento dentro do coração e pode obrigar à realização de uma
intervenção cirúrgica ou à reparação dos tecidos lesionados.
• Não utilize a bainha caso esta se encontre torcida ou danificada.
Acesso à aurícula esquerda – Não avance o dilatador ou a bainha através do septo
interauricular sem confirmar primeiro o acesso à aurícula esquerda, para evitar avançar estes
componentes para um local indesejado.
Equipamento hospitalar necessário – Tenha disponível equipamento de desfibrilhação
externa para utilização imediata durante a utilização do conjunto da bainha direcionável.
Outros cateteres, dispositivos ou fios – Evite o emaranhamento da bainha com outros
cateteres, dispositivos ou fios. Esse emaranhamento poderá necessitar de intervenção cirúrgica.
Válvulas cardíacas protéticas – Não passe o dispositivo através de uma válvula cardíaca
protésica (mecânica ou de tecido). O dispositivo poderá ficar preso na válvula, danificando-a e
causando insuficiência valvular ou falha prematura da válvula protésica.
Utilizadores qualificados – Este equipamento apenas deve ser utilizado por ou sob a
supervisão de médicos com formação em procedimentos de cateterismo cardíaco.
Ambiente de utilização necessário – Os procedimentos de cateterismo cardíaco devem ser
efetuados apenas em instalações totalmente equipadas.
Aspiração da porta lateral – Aspire a porta lateral quando remover o dilatador, cateter, agulha,
fios ou outros dispositivos.
Obstrução da porta lateral – Deve proceder-se com cuidado para evitar obstruir de alguma
forma a porta lateral e assim garantir a eficácia da irrigação com soro fisiológico.
Derrame sanguíneo significativo – Deve proceder-se com cuidado para garantir que não
ocorre um derrame sanguíneo significativo através da válvula hemostática durante o
procedimento.
Inspeção da embalagem estéril – Antes de utilizar, inspecione a embalagem e o dispositivo
esterilizados. Caso a embalagem ou o dispositivo esterilizados apresentem danos, não utilize o
dispositivo. Contacte o seu representante local da Medtronic.
Exposição fluoroscópica e aos raios X – A utilização de fluoroscopia durante procedimentos
de cateterismo de ablação acarreta riscos de exposição significativa aos raios X, tanto para os
doentes como para o pessoal do laboratório. A exposição extensa pode causar lesões agudas
por radiação e um risco aumentado de efeitos somáticos e genéticos. Efetue o cateterismo de
ablação somente após der dado a devida atenção à potencial exposição a radiação associada
com o procedimento e após ter tomado medidas para minimizar essa exposição. Pondere
cuidadosamente e evite a exposição a raios X antes de utilizar o dispositivo em mulheres
grávidas.
5 Efeitos adversos
Os potenciais efeitos adversos associados à canulação da vasculatura periférica e à colocação
intracardíaca da bainha e do dilatador podem incluir, entre outras, as seguintes patologias:
• Complicações no local de acesso (hematoma, infecção, trombose, equimose, fístula AV, hemorragia no local de punção,
hemorragia)
• Embolia gasosa
• Arritmia (fibrilhação auricular, flutter auricular, taquicardia ventricular)
• Paragem cardíaca
• Desconforto, dor ou pressão torácica
• Espasmo, dissecção ou trombose das
coronárias
• Morte
• Endocardite
• Bloqueio cardíaco, necessitando de pacemaker permanente
• Hemotórax
• Enfarte do miocárdio
• Perfuração do tecido cardíaco ou circundante
• Efusão, tamponamento pericárdico
• Pericardite
• Efusão pleural
• Pneumotórax
• Pseudoaneurisma
• Edema pulmonar
• Embolia pulmonar
• AVC
• Trombos
• Ataque isquémico transitório (AIT)
• Reação vasovagal
6 Instruções de utilização
Nota: Antes de introduzir a bainha no doente, teste o mecanismo de deflexão de forma a
certificar-se de que está operacional.
1. Utilizando uma técnica assética, crie um acesso vascular com um introdutor adequado.
2. Utilizando técnicas de acesso vascular padrão, insira um fio-guia compatível (consulte as
Especificações) através da vasculatura até à posição pretendida.
3. Irrigue a por ta lateral da bainha e o lúmen do dilatador com soro fisiológico esterilizado.
4. Cer tifique-se de que a bainha se encontra numa posição neutra (não fletida) e humedeça a
haste do dilatador com soro fisiológico esterilizado antes de a inserir através da válvula
hemostática.
5. Comece a montar o dilatador com a bainha introduzindo a ponta distal do dilatador na
válvula hemostática, de forma que a extremidade curvada do dilatador fique perpendicular
à válvula hemostática (consulte a Figura 2).
Figura 2. Bainha direcionável FlexCath Select
6. Continue a avançar o dilatador para o interior da bainha até que o conector do dilatador
encaixe completamente no conector da bainha.
Nota: A etiqueta do conector do dilatador deve ficar alinhada com a etiqueta do manípulo da
bainha, para que a curva do dilatador fique alinhada no mesmo sentido que o sentido de
deflexão da bainha e porta lateral (consulte a Figura 3).
Figura 3. Bainha direcionável FlexCath Select
7. Passe o conjunto dilatador e bainha sobre o fio-guia e introduza-o na vasculatura com um
ligeiro movimento de torção na veia cava superior (VCS).
8. Retire o fio-guia.
9. Insira a agulha transeptal convenientemente preparada no conjunto dilatador da bainha, de
modo a que o indicador da curvatura da agulha transeptal fique alinhado com a porta lateral.
Nota: A agulha transeptal deve ser utilizada em conjunto com um estilete a fim de evitar o
descarnamento do lúmen interno do dilatador.
10. Puxe o conjunto para baixo, até à aurícula direita, para preparar para a punção transeptal.
11. Sob orientação fluoroscópica, realize a punção transeptal utilizando medições de pressão,
injeção de contraste ou ambas. Confirme a colocação correta na aurícula esquerda.
12. Insira a agulha transeptal no dilatador e retire lentamente o conjunto dilatador e agulha da
bainha.
Português (Portugal)
48

Nota: Retire o dilatador lentamente para reduzir a possibilidade de criação de vácuo na
bainha. Deve ser possível aspirar o sangue livremente através da porta lateral. Se isto não
acontecer, retire a bainha pois a respetiva ponta poderá estar encostada à parede da
aurícula ou de uma veia pulmonar.
13. Aspire o sangue através da porta lateral e certifique-se de que a bainha não possui ar. Antes
de inserir um cateter na bainha, aspire ou permita o refluxo sanguíneo espontâneo.
Nota: Execute este passo após todas as trocas de cateter.
14. Após o acesso com a bainha ter sido conseguido, mantenha a terapêutica anticoagulante.
15. Prepare o cateter de acordo com as instruções de utilização do fabricante.
16. Insira o cateter e posicione a bainha.
Notas:
• Humedeça a haste do cateter pode facilitar a inserção.
• A válvula hemostática possui uma paragem total para evitar que os dispositivos de
captura abram o selo.
• Para minimizar o vácuo criado, insira e retire sempre os componentes lentamente.
• A bainha também deve ser irrigada durante a inserção de um cateter.
17. Antes de retirar a bainha, certifique-se de que esta está na posição neutra (não fletida).
7 Especificações
Comprimento total
Comprimento útil 65 cm (25,6 in [pol.])
Diâmetro interno 3,3 mm (10 Fr) (0,13 in [pol.])
Diâmetro externo 4,3 mm (13 Fr) (0,17 in [pol.])
Comprimento do dilatador 86 cm (33,9 in [pol.])
Marcador radiopaco 5 mm (0,2 in [pol.]) proximal em relação à ponta da bainha
Fio-guia compatível 0,81 mm (0,032 in [pol.]) a 0,89 mm (0,035 in [pol.])
Agulha transeptal compatível 89 cm (35,0 in [pol.]) ou superior
Parâmetros ambientais
Temperatura de transporte
recomendada
Temperatura de armazenamento recomendada
Funcionamento 15°C a 30°C (59°F a 86°F) para altitudes inferiores a 2400 m
81 cm (31,9 in [pol.])
-35°C a 58°C (-31°F a 136°F); 85% de humidade relativa (sem
condensação)
Média de 22°C (72°F) com um desvio padrão de 2,7°C
(4,86°F) e limites de controlo acionáveis de 15°C a 30°C (59°F
a 86°F)
(8000 pés) acima do nível do mar
8 Termos gerais da garantia da Medtronic
Para obter informações completas sobre a garantia, consulte o documento de renúncia de
garantia anexo.
9 Assistência técnica
A Medtronic dispõe de engenheiros e representantes altamente qualificados dispersos por todo
o mundo para o servir e, a pedido, ministrar formação a pessoal hospitalar qualificado
relativamente à utilização dos produtos da Medtronic. A Medtronic dispõe igualmente de uma
equipa profissional para fornecer consultoria técnica aos utilizadores dos produtos. Para mais
informações, contacte o seu representante local da Medtronic, telefone ou escreva para a
Medtronic, utilizando a morada ou o número de telefone indicados na contracapa.
49
Português (Portugal)

1 Описание
65 см
(25,6 дюй
ма)
16 см
(6,3 дюйм
а)
86 см
(33,9 дюйм
Управляемый интродьюсер FlexCath™ Select компании Medtronic представляет собой
интродьюсер для чрескожного введения катетера, оснащенный клапаном, который
позволяет вводить, извлекать и заменять катетеры и проводники, минимизируя
кровопотерю. Встроенный в него боковой порт с трехходовым краником позволяет
выполнять непрерывное капельное и струйное введение через центральный просвет,
промывание, аспирацию, забор образцов крови и мониторинг давления.
Рисунок 1. Управляемый интродьюсер FlexCath Select
Управляемый интродьюсер FlexCath Select укомплектован дилататором. Описание
интродьюсера приведено в таблице ниже:
Модель
990065 3,3 mm (10 Fr)
Интродьюсер можно изгибать, что обеспечивает дополнительную маневренность
катетерам, которые проводятся через интродьюсер в правую или левую камеры сердца.
Управляемый интродьюсер FlexCath Select размером 10 Fr можно использовать с
диагностическими катетерами и катетерами для абляции компании Medtronic размерами
до 9 Fr.
Дилататор управляемого интродьюсера FlexCath Select диаметром 10 Fr совместим с
транссептальными иглами HeartSpan компании Merit Medical длиной не менее 89 cm.
Внутренний диаметр Внешний диаметр Полезная длина
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Содержимое упаковки
Управляемый интродьюсер FlexCath Select поставляется стерильным. Одна упаковка
содержит:
• 1 (один) управляемый интродьюсер;
• 1 (один) дилататор;
• документацию по продукту.
2 Показания к применению
Управляемый интродьюсер FlexCath Select предназначен для чрескожного введения
катетера в сосудистое русло и камеры сердца, в том числе в левый отдел сердца через
межпредсердную перегородку. Изгибание интродьюсера облегчает позиционирование
катетера.
3 Противопоказания
Размещение управляемого интродьюсера FlexCath Select в левом предсердии или
желудочке противопоказано, если к пациенту применима хотя бы одна из следующих
ситуаций:
• Наличие на межпредсердной перегородке заплатки, окклюдера или другие
хирургические вмешательства на межпредсердной перегородке или прилегающих
участках.
• Обнаружен тромб в левом предсердии.
• Подтвержденная миксома предсердия или подозрение на нее.
4 Предостережения и меры предосторожности
Источник энергии для абляции – При использовании интродьюсера в присутствии
источника энергии для абляции необходимо следить, чтобы все элементы, участвующие в
абляции, были снаружи интродьюсера.
Аспирация воздуха – Перед выполнением аспирации и промывания интродьюсера
извлеките из него проводник. Это сведет к минимуму аспирацию воздуха через клапан
интродьюсера.
Антикоагуляционная терапия – До процедуры необходимо назначить подходящие
уровни антикоагуляционной терапии для пациентов, планирующих перенести
транссептальную процедуру и процедуру на левых отделах сердца, а также для отдельных
пациентов, переносящих процедуры на правых отделах сердца. Во избежание
геморрагических и тромботических осложнений антикоагуляционная терапия должна
назначаться согласно стандартам, принятым в данном лечебном учреждении.
Обратный ток крови – Во избежание непреднамеренного обратного тока крови через
боковой порт после промывания или аспирации трехходовой краник необходимо
перевести в закрытое положение.
Утилизация биологически опасных отходов – Все использованные устройства и
стерильные компоненты должны утилизироваться согласно процедурам, принятым в
данном лечебном учреждении.
Введение контрастного вещества — не используйте для введения контрастного
раствора в интродьюсер системы автоматического введения.
Перекручивание дилататора – Не скручивайте дилататор во время или после его
фиксации со щелчком во входе клапана. Это может привести к смещению кончика
дилататора на дистальном конце относительно бокового порта на проксимальном конце.
Не подлежит повторной стерилизации – Устройство не подлежит повторной
стерилизации для повторного использования. Повторная стерилизация может привести к
нарушению структурной целостности устройства или создать опасность заражения от
устройства, что способно вызвать травму, заболевание или смерть пациента.
Риск развития эмболии – Введение в кровеносную систему любого катетера или
интродьюсера влечет за собой риск развития воздушной эмболии, результатом чего
может стать закупорка сосудов, что в свою очередь может привести к некрозу ткани с
серьезными последствиями. Использование с этим устройством катетеров диаметром
менее 9 Fr несет повышенный риск воздушной эмболии. Введение и извлечение
компонентов должны всегда производиться медленно, а так же должно проводиться
промывание, чтобы не создавалось отрицательного давления и, следовательно, риска
развития воздушной эмболии.
Срок годности – Убедитесь, что срок годности интродьюсера не истек. Не используйте
продукт после окончания срока годности.
Повреждение бедренной вены – Следует предпринять меры предосторожности, чтобы
свести к минимуму повреждение бедренной вены и места доступа при введении,
перемещении и извлечении интродьюсера. Катетеризация бедренной вены может
привести к гематоме и тромбозу.
Для правильного размещения интродьюсера необходимо проведение
рентгеноскопии – Размещение и манипуляции с интродьюсером рекомендуется
производить под рентгеноскопическим контролем. Манипуляции с интродьюсером без
рентгеноскопического контроля могут привести к повреждениям тканей сердца и
сосудов.
Устройство предназначено только для одноразового применения – Данное
устройство предназначено только для одноразового применения у одного пациента.
Устройство не предназначено для повторного использования, обработки или повторной
стерилизации в целях повторного использования. Повторное использование, обработка
или повторная стерилизация могут привести к нарушению структурной целостности
На русском языке
50

устройства или создать опасность заражения от устройства, что способно вызвать
травму, заболевание или смерть пациента.
Частое промывание – Рекомендуется регулярное промывание интродьюсера:
• Во избежание застоя крови, образования сгустков, эмболии и серьезной травмы
пациента.
• После каждого введения контрастного вещества, чтобы не допустить его адгезии в
просвете.
Обращение и меры предосторожности – При обращении с устройством:
• При манипуляциях с устройством нужно соблюдать предельную осторожность.
Недостаточно осторожное обращение может привести к перфорации, тампонаде,
индуцированию аритмии или блокаде сердца.
• Не следует прилагать слишком большие усилия при введении или извлечении
устройства, особенно если на его пути ощущается сопротивление.
• Избегайте позиционирования устройства в зоне сухожильных корд, так как это
увеличивает вероятность его застревания в тканях сердца, что может вызвать
необходимость хирургического вмешательства или восстановления поврежденных
тканей.
• Не пользуйтесь интродьюсером, если он перекручен или поврежден.
Доступ в левое предсердие – Не продвигайте дилататор или интродьюсер через
межпредсердную перегородку без предварительного подтверждения доступа в левое
предсердие, чтобы не допустить неправильного размещения этих компонентов.
Необходимое медицинское оборудование – Во время использования сборки
управляемого интродьюсера держите наготове внешний дефибриллятор.
Другие катетеры, устройства или проводники – Следите за тем, чтобы интродьюсер
не зацепился за другие катетеры, устройства или проводники. Это может вызвать
необходимость хирургического вмешательства.
Искусственные клапаны сердца – Не следует пропускать устройство через
искусственные клапаны сердца (механические или биологические). Устройство может
застрять в клапане, повредить его и стать причиной недостаточности клапана или
преждевременного выхода искусственного клапана из строя.
Квалифицированные пользователи – Эксплуатация данного оборудования должна
производиться только врачами, обученными катетеризации сердца, или под их
наблюдением.
Условия эксплуатации – Процедуры катетеризации сердца должны проводиться только
в полностью оборудованном для этого помещении.
Аспирация через боковой порт – При извлечении дилататора, катетера, игл,
проводников или других устройств выполняйте аспирацию через боковой порт.
Обструкция бокового порта – Следует принять меры предосторожности для
предотвращения обструкции бокового порта, чтобы убедиться в эффективности
промывания физиологическим раствором.
Значительная кровопотеря – Следует принять меры предосторожности, чтобы не
допустить значительной кровопотери через гемостатический клапан во время
процедуры.
Осмотр стерильной упаковки – Перед использованием осмотрите стерильную
упаковку и устройство. Если стерильная упаковка или устройство имеют признаки
повреждения, устройство использовать нельзя. Обратитесь в региональное
представительство компании Medtronic.
Облучение при рентгенографии и рентгеноскопии – Во время рентгеноскопии при
процедурах катетерной абляции пациенты и сотрудники лаборатории могут подвергаться
значительному радиационному облучению. Чрезмерное облучение может повлечь за
собой острое радиационное поражение и повышенный риск соматического и
генетического воздействия. Катетерную абляцию следует выполнять только после того,
как будут приняты во внимание все возможные риски радиационного облучения,
связанные с выполнением данной процедуры, и приняты все меры, чтобы свести это
облучение к минимуму. Перед применением устройства у беременных женщин следует
тщательно проанализировать возможные риски и избегать воздействия рентгеновского
излучения.
5 Нежелательные явления
К числу возможных побочных эффектов, связанных с катетеризацией периферических
сосудов и внутрисердечным введением интродьюсера и дилататора, относятся
следующие (перечень неисчерпывающий):
осложнения в месте доступа (гематома,
•
инфицирование, тромбообразование,
подкожное кровоизлияние, артериовенозная фистула, кровотечение в месте
прокола, геморрагия)
• воздушная эмболия
• аритмия (фибрилляция предсердий,
трепетание предсердий, желудочковая
тахикардия)
• остановка сердца
• дискомфорт, боль или чувство сдавливания в грудной клетке
• спазм, рассечение, тромбоз коронарной артерии
• смерть
• эндокардит
• блокада сердца, требующая установки
постоянного кардиостимулятора
• гемоторакс
• инфаркт миокарда
• перфорация сердечных или окружающих тканей
• перикардиальный выпот, тампонада
• перикардит
• плевральный выпот
• пневмоторакс
• ложная аневризма
• отек легких
• легочная эмболия
• инсульт
• тромбоз
• транзиторная ишемическая атака
(ТИА)
• вазовагальная реакция
6 Инструкция по эксплуатации
Примечание: Перед введением управляемого интродьюсера в тело пациента нужно
убедиться в исправности поворотного механизма.
1. Соблюдая правила асептики, подготовьте сосудистый доступ с помощью
соответствующего интродьюсера.
2. Введите совместимый проводник (см. «Технические характеристики») через
сосудистое русло в целевую позицию, используя стандартный метод сосудистого
доступа.
3. Промойте боковой порт интродьюсера и просвет для дилататора стерильным
физиологическим раствором.
4. Перед введением дилататора через гемостатический клапан убедитесь, что
интродьюсер находится в нейтральном (неизогнутом) положении и смочите корпус
дилататора стерильным физиологическим раствором.
5. Начните сборку дилататора и интродьюсера, вставив дистальный кончик дилататора
через гемостатический клапан так, чтобы изогнутый край дилататора располагался
перпендикулярно к гемостатическому клапану (см. Рис. 2).
51
На русском языке

Рисунок 2. Управляемый интродьюсер FlexCath Select
6. Продолжайте продвижение дилататора в интродьюсер, чтобы вход дилататора
зафиксировался со щелчком во входе интродьюсера.
Примечание: Маркировку на входе дилататора следует совместить с маркировкой
на входе интродьюсера так, чтобы изгиб дилататора имел одинаковую ориентацию с
направлением отклонения интродьюсера и боковым портом (см. Рис. 3).
Рисунок 3. Управляемый интродьюсер FlexCath Select
7. Легкими вращательными движениями проведите сборку дилататора и интродьюсера
по проводнику через сосудистое русло в ВПВ.
8. Извлеките проводник.
9. Вставьте правильно подготовленную транссептальную иглу в сборку дилататора и
интродьюсера так, чтобы индикатор изгиба на транссептальной игле совместился с
боковым портом.
Примечание: Транссепта льную иглу следует использовать совместно со стилетом
для предотвращения повреждения внутреннего просвета дилататора.
10. Протолкните сборку дилататора и интродьюсера в правое предсердие для
подготовки к выполнению транссептальной пункции.
11. Под рентгеноскопическим контролем направления выполните транссептальную
пункцию с измерением давления, введением контрастного вещества или и того, и
другого. Убедитесь в правильном расположении иглы в левом предсердии.
12. Потяните транссептальную иглу в дилататор и медленно извлеките сборку
дилататора и иглы из интродьюсера.
Примечание: Для уменьшения вероятности создания вакуума в интродьюсере
дилататор следует извлекать медленно. Через боковой порт кровь должна
аспирироваться свободно. В противном случае интродьюсер следует оттянуть назад,
поскольку его кончик мог упереться в стенку предсердия или легочной вены.
13. Чтобы убедиться в том, что в интродьюсере нет воздуха, аспирируйте кровь через
боковой порт. Перед введением катетера в интродьюсер выполните аспирацию или
создайте условия для самопроизвольного обратного тока крови.
Примечание: Выполняйте это действие после каждой замены катетера.
14. После осуществления доступа к интродьюсеру проведите антикоагуляционную
терапию.
15. Подготовьте катетер в соответствии с инструкциями по эксплуатации от
производителя.
16. Введите катетер и установите интродьюсер в нужное положение.
Примечания:
• Для облегчения введения катетера можно увлажнить его корпус.
• Гемостатический клапан оснащен упором-ограничителем, чтобы устройства
захвата не нарушили герметичное соединение.
• Чтобы минимизировать создание вакуума, всегда вводите и извлекайте
компоненты системы медленно.
• При введении катетера также необходимо промывать интродьюсер.
17. Перед извлечением интродьюсера убедитесь, что он находится в нейтральном
(неизогнутом) положении.
7 Технические характеристики
Общая длина
Полезная длина 65 cm (25,6 in)
Внутренний диаметр 3,3 mm (10 Fr) (0,13 in)
Внешний диаметр 4,3 mm (13 Fr) (0,17 in)
Длина дилататора 86 cm (33,9 in)
Рентгеноконтрастный мар-
кер
Совместимость с проводни-
ками
Совместимость с транссеп-
тальными иглами
Параметры окружающей
среды
Рекомендуемая температура при транспортировке
Рекомендуемая температура хранения
Эксплуатация От 15°C до 30°C (от 59°F до 86°F) на высоте менее 2400 m
81 cm (31,9 in)
5 mm (0,2 in) проксимальнее кончика интродьюсера
От 0,81 mm (0,032 in) до 0,89 mm (0,035 in)
89 cm (35,0 in) или длиннее
От −35°C до 58°C (от −31°F до 136°F); 85 % относительной
влажности (без конденсации)
Средняя температура 22°C (72°F) со стандартным отклонением 2,7°C (4,86°F) и рабочими контрольными пределами от 15°C до 30°C (от 59°F до 86°F)
(8000 футов) над уровнем моря
8 Ограниченная гарантия компании Medtronic
Для получения подробной информации по гарантии см. прилагаемый документ отказа от
гарантии.
9 Обслуживание
В компании Medtronic по всему миру работают высококвалифицированные
представители и инженеры, готовые предоставить вам помощь, а также, при
необходимости, обучить специалистов лечебных учреждений использованию продукции
компании Medtronic. Кроме того, в компании Medtronic работают квалифицированные
специалисты по консультированию пользователей продуктов компании. Для получения
дополнительной информации обратитесь в региональное представительство компании
Medtronic либо позвоните или напишите в компанию Medtronic. Соответствующий номер
телефона и адрес приведен на задней обложке.
На русском языке
52

1 Popis
65 cm
(25,6 palca)
16 cm
(6,3 palca)
86 cm
(33,9 palca)
Ovládateľné puzdro Medtronic FlexCath™ Select je perkutánny zavádzač katétra vybavený
ventilom, ktorý umožňuje zavedenie, vytiahnutie a výmenu katétrov a drôtov, pričom súčasne
minimalizuje stratu krvi. Obsahuje integrovaný bočný port s uzatváracím ventilom, ktorý
umožňuje nepretržitú kvapkaciu infúziu, vstrekovanie látok cez centrálny lúmen, preplachovanie,
aspiráciu, odber vzoriek krvi a monitorovanie tlaku.
Obrázok 1. Ovládateľné puzdro FlexCath Select
K ovládateľnému puzdru FlexCath Select je pribalený dilatátor. Informácie o puzdre sú uvedené
v nasledujúcej tabuľke:
Model
990065 3,3 mm (10 Fr)
Puzdro sa dá ohnúť, čo uľahčuje manévrovanie s katétrami, ktoré sa zavádzajú cez puzdro do
pravej alebo ľavej dutiny srdca.
Ovládateľné puzdro FlexCath Select s veľkosťou 10 Fr sa môže používať s diagnostickými
a ablačnými katétrami od spoločnosti Medtronic s veľkosťami do 9 Fr.
Dilatátor ovládateľného puzdra FlexCath Select s veľkosťou 10 Fr je kompatibilný
s transseptálnymi ihlami Merit Medical HeartSpan s dĺžkou najmenej 89 cm.
Vnútorný priemer Vonkajší priemer Použiteľná dĺžka
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Obsah balenia
Ovládateľné puzdro FlexCath Select sa dodáva sterilné. Balenie obsahuje nasledovné súčasti:
• 1 ovládateľné puzdro
• 1 dilatátor
• dokumentácia k produktu
2 Indikácie na použitie
Ovládateľné puzdro FlexCath Select je určené na perkutánne zavedenie katétra do vaskulatúry
a do dutín srdca vrátane ľavej strany srdca cez medzipredsieňovú priehradku. Ohnutie puzdra
uľahčuje umiestnenie katétra.
3 Kontraindikácie
Umiestnenie ovládateľného puzdra FlexCath Select v ľavej predsieni alebo komore je
kontraindikované, ak sa na pacienta vzťahuje niektorá z nasledujúcich podmienok:
• Pacient má intraatriálnu septálnu záplatu alebo okluzor, alebo podstúpil iný chirurgický
zákrok na predsieňovom septe alebo v jeho blízkosti.
• Pacient má trombus v ľavej predsieni.
• Pacient má, alebo má podozrenie na atriálny myxóm.
4 Varovania a preventívne opatrenia
Ablačná energia – Keď používate puzdro za prítomnosti ablačnej energie, musíte zabezpečiť,
aby boli všetky ablačné prvky mimo puzdra.
Aspirácia vzduchu – Vyberte vodiaci drôt z puzdra predtým, ako aspirujete a prepláchnete
puzdro. Minimalizuje sa tým aspirácia vzduchu cez ventil puzdra.
Antikoagulačná liečba – Podajte vhodnú dávku periprocedurálnej antikoagulačnej liečby pre
pacientov, ktorí podstupujú ľavostranné a transseptálne kardiologické zákroky a pre vybratých
pacientov podstupujúcich pravostranné procedúry. Podajte periprocedurálnu antikoagulačnú
liečbu v súlade s normami príslušnej inštitúcie, aby ste minimalizovali krvácanie a trombotické
komplikácie.
Spätné krvácanie – Zabezpečte, aby bol uzatvárací ventil po prepláchnutí alebo aspirácii
v zavretej polohe, čím sa zabráni neželanému spätnému krvácaniu cez bočný port.
Likvidácia biologicky nebezpečného odpadu – Všetky použité zariadenia a sterilné súčasti
zlikvidujte v súlade s nemocničnými pravidlami.
Injekčné podanie kontrastnej látky – na injekčné podanie roztoku kontrastnej látky do puzdra
nepoužívajte systém automatického injektora.
Otáčanie dilatátorom – Neotáčajte dilatátorom počas jeho zacvakávania do ventilovej objímky
ani po ňom. Môže tým prísť k nesprávnemu zarovnaniu hrotu dilatátora na distálnom konci
vzhľadom na bočný port na proximálnom konci.
Opakovane nesterilizujte – Toto zariadenie opakovane nesterilizujte za účelom opätovného
použitia. Opakovaná sterilizácia môže mať negatívny vplyv na štrukturálnu integritu zariadenia
alebo môže spôsobiť riziko vzniku kontaminácie zo zariadenia. To môže mať za následok
zranenie, ochorenie alebo smrť pacienta.
Riziko embolizácie – Zavádzanie akéhokoľvek katétra alebo puzdra do obehového systému
predstavuje riziko vzniku vzduchovej embólie, ktorá môže spôsobiť upchatie ciev a viesť k infarktu
tkaniva so závažnými dôsledkami. Použitie katétrov menších než 9 Fr s týmto zariadením môže
zvýšiť riziko vzduchovej embólie. Súčasti vždy zavádzajte a vyťahujte pomaly a preplachujte ich,
aby sa minimalizovalo vzniknuté vákuum, a tým aj riziko vzduchovej embólie.
Dátum exspirácie – Skontrolujte, či neuplynul dátum exspirácie puzdra. Nepoužívajte, ak
uplynul dátum spotreby zariadenia.
Poškodenie femorálnej žily – Je potrebné zabezpečiť minimalizáciu poškodenia femorálnej žily
a miesta prístupu počas vkladania puzdra, manipulácie alebo odstránenia. Komplikácie
súvisiace s katetrizáciou femorálnej žily zahŕňajú hematóm a trombózu.
Skiaskopia potrebná na umiestnenie puzdra – Dôrazne sa odporúča použitie skiaskopie
počas manipulácie a umiestňovania puzdra. Manipulácia s puzdrom bez skiaskopického
zobrazenia môže viesť k poškodeniu srdcových a vaskulárnych štruktúr.
Len na jednorazové použitie – Toto zariadenie je určené na jednorazové použitie výlučne u
jedného pacienta. Toto zariadenie opätovne nepoužívajte, neupravujte, ani nesterilizujte za
účelom opätovného použitia. Opätovné používanie, upravovanie alebo sterilizovanie môže mať
negatívny vplyv na štrukturálnu integritu zariadenia alebo môže spôsobiť riziko kontaminácie
zariadenia. To môže mať za následok zranenie, ochorenie alebo smrť pacienta.
Časté preplachovanie – Odporúča sa pravidelne preplachovať puzdro:
• aby sa zabránilo stagnácii krvi, krvným zrazeninám, embolom a závažnému poraneniu
pacienta,
• po každom injekčnom podaní kontrastnej látky, aby sa zabránilo zachytávaniu roztoku
kontrastnej látky vnútri kanála.
Pokyny na manipuláciu a starostlivosť – Pri manipulácii so zariadením:
• Pri manipulácii so zariadením postupujte mimoriadne opatrne. Neopatrnosť môže mať za
následok poranenie, ako napríklad perforáciu, tamponádu, indukciu arytmie alebo blokádu
srdca.
• Počas posúvania alebo vyťahovania zariadenia nevyvíjajte nadmernú silu, obzvlášť v
prípade, ak pocítite odpor.
53
Slovenčina

• Zariadenie neumiestňujte okolo chordae tendineae, keďže tým sa zvyšuje pravdepodobnosť
zachytenia v srdci. To môže následne vyžadovať chirurgickú intervenciu alebo revíziu
poškodených tkanív.
• Puzdro nepoužívajte, ak je zalomené alebo poškodené.
Prístup do ľavej predsiene – Nezavádzajte dilatátor ani puzdro cez medzipredsieňové septum
bez toho, aby ste najprv neoverili prístup do ľavej predsiene, a tak zabránili zavedeniu týchto
komponentov do nežiaducej polohy.
Potrebné nemocničné vybavenie – Počas používania súpravy ovládateľného puzdra
uchovávajte v blízkosti externý defibrilátor pripravený na okamžité použitie.
Iné katétre, zariadenia alebo drôty – Dávajte pozor, aby sa puzdro nezamotalo do iných
katétrov, zariadení alebo drôtov. Takéto zamotanie si môže následne vyžadovať chirurgickú
intervenciu.
Protetické srdcové chlopne – Nezavádzajte zariadenie cez protetickú srdcovú chlopňu
(mechanickú alebo tkanivovú). Zariadenie by sa mohlo zachytiť v chlopni, a tým ju poškodiť a
spôsobiť chlopňovú nedostatočnosť alebo predčasné zlyhanie protetickej chlopne.
Kvalifikovaní používatelia – Toto zariadenie by mali používať, alebo na jeho používanie by mali
dozerať, iba lekári, ktorí boli vyškolení v oblasti procedúr katetrizácie srdca.
Požiadavky na prostredie, v ktorom sa katéter použije – Procedúry kardiálnej katetrizácie by
sa mali vykonávať iba v plne vybavenom stredisku.
Aspirácia bočného portu – Bočný port aspirujte pri vyťahovaní dilatátora, katétra, ihly, drôtov
alebo iných zariadení.
Obštrukcia bočného portu – Je potrebné zabrániť obštrukcii bočného portu, aby sa
zabezpečilo efektívne preplachovanie fyziologickým roztokom.
Významný únik krvi – Je potrebné sledovať, aby počas procedúr y nedošlo k významnému úniku
krvi cez hemostatický ventil.
Kontrola sterilného balenia – Pred použitím dôkladne skontrolujte sterilné balenie a zariadenie.
Ak sú sterilné balenie alebo zariadenie poškodené, zariadenie nepoužívajte. Obráťte sa na
miestneho zástupcu spoločnosti Medtronic.
Pôsobenie röntgenu a skiaskopie – Použitie skiaskopie počas ablačných procedúr pomocou
katétra predstavuje významné riziko expozície pôsobeniu röntgenu, rovnako pre pacienta, ako aj
pre laboratórnych pracovníkov. Rozsiahla expozícia môže viesť k akútnemu poškodeniu zdravia
v dôsledku žiarenia a k zvýšenému riziku somatického a genetického poškodenia. Ablačné
procedúry vykonávajte len po dôkladnom zvážení rizika vyplývajúceho z expozície žiareniu, ktoré
je spojené s procedúrou. Na minimalizáciu expozície žiareniu vykonajte príslušné kroky. Pred
použitím zariadenia u tehotných žien dôkladne zvážte uvedené skutočnosti a vyhýbajte sa
vystaveniu röntgenovému žiareniu.
5 Nežiaduce príhody
Potenciálne nežiaduce príhody súvisiace s kanyláciou periférnej vaskulatúry a intrakardiálneho
umiestnenia puzdra a dilatátora môžu, okrem iného, zahŕňať aj nasledujúce stavy:
• komplikácie v mieste prístupu (hematóm,
infekcia, trombóza, ekchymóza, arteriovenózna fistula, krvácanie v mieste vpichu,
hemorágia),
• vzduchová embólia,
• arytmia (predsieňová fibrilácia, predsieňový flutter, komorová tachykardia),
• zástava srdca,
• nepríjemné pocity v hrudníku, bolesť alebo
tlak,
• spazmus koronárnych ciev, disekcia, trombóza,
• smrť,
• endokarditída,
• blokáda srdca vyžadujúca permanentný
kardiostimulátor,
• hemothorax,
• infarkt myokardu,
• perforácia tkaniva srdca alebo okolitého
tkaniva,
• perikardiálny výpotok, tamponáda,
• perikarditída,
• pleurálny výpotok,
• pneumotorax,
• pseudoaneuryzma,
• pľúcny edém,
• pľúcna embolizácia,
• mozgový iktus,
• trombus,
• prechodný ischemický záchvat (TIA),
• vazovagálna reakcia.
6 Návod na použitie
Poznámka: Pred zavedením puzdra do tela pacienta otestujte ohýbací mechanizmus, aby ste
overili jeho funkčnosť.
1. Aseptickým postupom vykonajte vaskulárny prístup pomocou príslušného zavádzača.
2. Vložte kompatibilný vodiaci drôt (pozrite časť Špecifikácie) cez vaskulatúru do požadovanej
polohy pomocou štandardných techník pre cievny prístup.
3. Prepláchnite lúmen bočného portu puzdra a dilatátora sterilným fyziologickým roztokom.
4. Zabezpečte, aby puzdro bolo v neutrálnej (nevychýlenej) polohe a navlhčite driek dilatátora
sterilným fyziologickým roztokom predtým, než ho zasuniete cez hemostatický ventil.
5. Začnite spoločným zostavením dilatátora a puzdra zavedením distálneho hrotu dilatátora do
hemostatického ventilu tak, aby zakrivený okraj dilatátora bol kolmý na hemostatický ventil
(pozrite si Obr. 2).
Obrázok 2. Ovládateľné puzdro FlexCath Select
6. Pokračujte v zavádzaní dilatátora do puzdra tak, aby objímka dilatátora zapadla do objímky
puzdra.
Poznámka: Označenie na objímke dilatátora musí byť zarovnané s označením na rukoväti
puzdra tak, aby zakrivenie dilatátora bolo zarovnané v rovnakej orientácii so smerom ohybu
puzdra, a na bočnom porte (pozrite si Obr. 3).
Obrázok 3. Ovládateľné puzdro FlexCath Select
7. Navlečte súpravu dilatátora puzdra na vodiaci drôt a do vaskulatúry a jemne krúživým
pohybom ju zaveďte do hornej dutej žily (SVC).
8. Vyberte vodiaci drôt.
9. Do súpravy dilatátora puzdra zasuňte dôkladne pripravenú transseptálnu ihlu tak, aby
indikátor zakrivenia na transseptálnej ihle bol zarovnaný s bočným portom.
Poznámka: Transseptálna ihla sa musí používať spolu s vodičom, aby sa zabránilo
poškodeniu vnútorného lúmenu dilatátora.
10. Potiahnite súpravu do pravej predsiene, aby bola pripravená na transseptálnu punkciu.
11. Pod skiaskopickým dohľadom vykonajte transseptálnu punkciu za pomoci merania tlaku,
vstrekovania kontrastnej látky alebo použitím oboch možností. Overte správne umiestnenie
v ľavej predsieni.
12. Potiahnite transseptálnu ihlu do dilatátora a pomaly vyťahujte súpravu dilatátora a ihly
z puzdra.
Slovenčina
54

Poznámka: Dilatátor vyberajte pomaly, aby sa znížila možnosť vytvorenia podtlaku
v puzdre. Krv by mala voľne vytekať cez bočný port. Ak sa tak nestane, puzdro vytiahnite,
keďže hrot puzdra sa môže opierať o stenu predsiene alebo pľúcnej žily.
13. Aspirujte krv cez bočný port a zabezpečte, aby v puzdre nebol žiadny vzduch. Aspiráciu kr vi
alebo spontánne spätné krvácanie vykonajte pred vložením katétra do puzdra.
Poznámka: Tento krok vykonajte po všetkých výmenách katétrov.
14. Po získaní prístupu pomocou puzdra udržiavajte antikoagulačnú terapiu.
15. Pripravte katéter podľa pokynov na používanie od výrobcu.
16. Vložte katéter a umiestnite puzdro.
Poznámky:
• Zavedenie môžete uľahčiť navlhčením drieku katétra.
• Hemostatický ventil obsahuje pozitívnu zarážku zabraňujúcu otvoreniu tesnenia
zachytávacím zariadením.
• Ak chcete minimalizovať vytváranie podtlaku, súčasti zasúvajte a vyberajte vždy
pomaly.
• Puzdro by sa malo tiež prepláchnuť, keď je katéter zavedený.
17. Pred vybratím puzdra overte, či je v neutrálnej (neohnutej) polohe.
7 Špecifikácie
Celková dĺžka
Použiteľná dĺžka 65 cm (25,6 in)
Vnútorný priemer 3,3 mm (10 Fr) (0,13 in)
Vonkajší priemer 4,3 mm (13 Fr) (0,17 in)
Dĺžka dilatátora 86 cm (33,9 in)
Röntgenkontrastný marker 5 mm (0,2 in) proximálne od hrotu puzdra
Kompatibilita vodiaceho drôtu 0,81 mm (0,032 in) až 0,89 mm (0,035 in)
Kompatibilita transseptálnej ihly 89 cm (35,0 in) alebo dlhšia
Podmienky prostredia
Odporúčaná teplota pri preprave
Odporúčaná skladovacia
teplota
Pri prevádzke 15°C až 30°C (59°F až 86°F) pri nadmorských výškach
81 cm (31,9 in)
−35°C až 58°C (−31°F až 136°F); relatívna vlhkosť 85 %
(nekondenzujúca)
Priemerná teplota 22°C (72°F) so štandardnou odchýlkou 2,7°C (4,86°F) a záväznými kontrolnými limitmi 15°C
až 30°C (59°F až 86°F)
do 2 400 m (8 000 stôp)
8 Odmietnutie záruky spoločnosťou Medtronic
Úplné informácie o záruke nájdete v priloženom dokumente o odmietnutí záruky.
9 Servis
Spoločnosť Medtronic zamestnáva po celom svete dôkladne vyškolených zástupcov
a technických pracovníkov, na ktorých sa môžete obrátiť a ktorí v prípade potreby poskytnú
kvalifikovanému nemocničnému personálu školenie týkajúce sa používania produktov
spoločnosti Medtronic. Spoločnosť Medtronic zamestnáva aj odborníkov, ktorí poskytujú
technickú podporu pre používateľov produktov. Ďalšie informácie získate od miestneho zástupcu
spoločnosti Medtronic, prípadne sa písomne alebo telefonicky obráťte na spoločnosť Medtronic,
ktorej kontaktné informácie nájdete na zadnej strane.
55
Slovenčina

1 Beskrivning
65 cm
(25,6 in)
16 cm
(6,3 in)
86 cm
(33,9 in)
Medtronic FlexCath™ Select styrbar skida är en perkutan kateterintroducer som utrustats med en
ventil för att medge introduktion, avlägsnande och byte av katetrar och ledare samtidigt som den
minimerar blodförlust. En sidoport med avstängningskran är integrerad för att medge kontinuerlig
droppinfusion, injektion genom centerlumen, spolning, aspiration, blodprov och
tryckövervakning.
Figur 1. FlexCath Select styrbar skida
En dilatator är förpackad med FlexCath Select styrbar skida. Skidan beskrivs i följande tabell:
Modell
990065 3,3 mm (10 Fr)
Skidan kan böjas för att ge y tterligare styrförmåga till de katetrar som förs fram genom skidan och
in i höger eller vänster hjärtrum.
FlexCath Select styrbar skida på 10 Fr kan användas med Medtronic-katetrar för diagnostik och
ablation i storlekar upp till 9 Fr.
Dilatatorn till FlexCath Select styrbar skida på 10 Fr är kompatibel med Merit Medical HeartSpan
transseptalnålar med en längd på 89 cm eller mer.
Inre diameter Yttre diameter Användbar längd
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Förpackningens innehåll
FlexCath Select styrbara skida levereras steril. Förpackningen innehåller följande delar:
• 1 styrbar skida
• 1 dilatator
• Produktdokumentation
2 Indikationer för användning
FlexCath Select styrbara skida är avsedd för perkutan kateterintroduktion i kärl och hjärtrum,
inklusive vänster sida av hjärtat genom skiljeväggen mellan förmaken. Möjligheten att böja skidan
underlättar placering av katetern.
3 Kontraindikationer
FlexCath Select styrbar skida är kontraindicerad för placering i vänster förmak eller kammare om
något av följande tillstånd gäller för patienten:
• Patienten har en intraatriell septal patch eller ockluder, eller har haft annan kirurgisk
intervention i eller nära intraatriella septum.
• Patienten har en trombos i vänster förmak.
• Patienten har känt eller misstänkt myxom i förmaket.
4 Varningar och försiktighetsåtgärder
Ablationsenergi – När skidan används vid ablationsenergi är det viktigt att säkerställa att
samtliga ablationskomponenter är utanför skidan.
Luftaspiration – Avlägsna styrtråden från skidan innan aspirering och spolning av skidan utförs.
Denna åtgärd minimerar aspireringen av luft genom skidans ventil.
Antikoaguleringsbehandling – För patienter som genomgår vänstersidiga och transseptala
ingrepp i hjärtat, och för utvalda patienter som genomgår högersidiga ingrepp, ska lämplig
omfattning av antikoagulationsbehandling under ingreppet administreras. Minimera blödningar
och trombotiska komplikationer genom att administrera antikoagulationsbehandling i samband
med ingreppet enligt inrättningens riktlinjer.
Backflöde av blod – Kontrollera att avstängningskranen är stängd efter spolning eller aspiration
för att undvika oavsiktligt backflöde av blod genom sidoporten.
Kassering av riskavfall – Kassera alla använda enheter och sterila tillbehör i enlighet med
sjukhusets föreskrifter.
Injektion av kontrastmedel – Använd inte ett automatiskt injektionssystem för att injicera
konstrastmedelslösning i skidan.
Vridning av dilatatorn – Vrid inte dilatatorn under eller efter fastsnäppningen i ventilfattningen.
Detta kan orsaka felaktig inriktning av dilatatorspetsen i den distala änden i förhållande till
sidoporten i den proximala änden.
Får ej omsteriliseras – Enheten får ej omsteriliseras i återanvändningssyfte. Omsterilisering kan
påverka enhetens strukturella integritet eller orsaka skada, sjukdom eller dödsfall hos patienten.
Risk för embolism – En kateter eller skida som förs in i cirkulationssystemet medför en risk för
luftemboli, som kan blockera blodkärl och ge upphov till vävnadsinfarkt med allvarliga
konsekvenser. Användning av katetrar som är mindre än 9 Fr tillsammans med denna enhet kan
innebära förhöjd risk för luftemboli. För alltid in eller dra ut komponenter långsamt och spola för att
minimera risken för vakuum och därmed också risken för luftemboli.
Utgångsdatum – Kontrollera att skidans utgångsdatum inte har passerat. Produkten får inte
användas om utgångsdatum har passerats.
Skada på femoralven – Var noga med att minimera skador på femoralvenen och åtkomstplatsen
vid införande, manipulation eller avlägsnande av skidan. Komplikationer som kan uppstå i
samband med kateterisering av femoralvenen innefattar hematom och trombos.
Genomlysning krävs vid placering av skidan – Användning av fluoroskopi rekommenderas
kraftfullt vid användning och placering av skidan. Om skidan används utan fluoroskopisk ledning
kan skador uppstå på hjärt- och kärlstrukturer.
Endast för engångsbruk – Enheten är endast avsedd för användning en gång på en patient.
Enheten får ej återanvändas, omarbetas eller omsteriliseras. Återanvändning, omarbetning eller
omsterilisering kan påverka enhetens strukturella integritet eller orsaka skada, sjukdom eller
dödsfall hos patienten.
Regelbunden och frekvent spolning – Regelbunden spolning av skidan rekommenderas av
följande skäl:
• För att förhindra blodstockning, blodproppar, emboli och allvarlig patientskada.
• För att förhindra att kontrastmedel fastnar inuti lumen efter varje injektion av kontrastmedel.
Hantering och försiktighetsåtgärder – Vid hantering av enheten:
• Var mycket försiktig när enheten används. Om inte försiktighet iakttas kan skador som
perforering, tamponad, framkallade arytmi eller hjärtblock uppstå.
• För inte in eller dra ut enheten med alltför stor kraft, speciellt om motstånd uppstår.
• Undvik att placera enheten i närheten av chordae tendineae, vilket ökar risken för att katetern
fastnar i hjärtat. Vid denna komplikation kan det bli nödvändigt att utföra ett kirurgiskt ingrepp
eller reparera skadad vävnad.
• Använd inte en skida som är vikt eller skadad.
Åtkomst till vänster förmak – För inte fram dilatatorn eller skidan genom förmaksseptum utan
att först bekräfta åtkomst till vänster förmak, för att förhindra att dessa komponenter förs fram till
en oönskad position.
Erforderlig sjukhusutrustning – Håll extern defibrilleringsutrustning nära till hands för
omedelbart bruk under användning av den styrbara skidenheten.
Svenska
56

Andra katetrar, enheter eller ledare – Undvik att skidan fastnar i andra katetrar, enheter eller
ledare. Om detta inträffar kan ett kirurgiskt ingrepp bli nödvändigt.
Hjärtklaffsproteser – Låt inte enheten passera genom klaffproteser (varken mekaniska eller
biologiska). Det finns risk för att enheten fastnar och/eller att klaffprotesen skadas, med
klaffinsufficiens eller förtida funktionsbortfall hos klaffen som följd.
Kvalificerade användare – Utrustningen får endast användas av läkare, eller under
överinseende av läkare, som har utbildning i hjärtkateteriseringsingrepp.
Krav på användningsmiljö – Hjärtkateteriseringsingrepp får endast utföras i fullständigt
utrustade operationssalar.
Aspiration genom sidoport – Aspirera genom sidoporten medan du drar ut dilatatorn, katetern,
nålen, ledarna eller andra enheter.
Blockering i sidoport – Försiktighet måste iakttas för att förhindra att sidoporten blockeras för
att säkerställa att spolningen med koksaltlösning är effektiv.
Signifikant blodläckage – Observera noggrant att inget signifikant blodläckage uppstår genom
hemostasventilen under ingreppet.
Inspektion av den sterila förpackningen – Inspektera den sterila förpackningen och enheten
före användning. Om den sterila förpackningen eller enheten har skadats får enheten inte
användas. Kontakta en Medtronic-representant.
Röntgen och fluoroskopi – Användning av fluoroskopi under kateterablationsingrepp ökar
risken för betydande exponering för röntgenstrålning för både patienter och sjukvårdspersonal.
Långvarig exponering för röntgenstrålning kan resultera i akuta strålskador och ökad risk för
somatiska och genetiska effekter. Kateterablation bör endast utföras efter noggrant övervägande
av möjliga strålningsrisker som hör samman med ingreppet. Åtgärder bör vidtas för att minska
exponeringen. Överväg noga och undvik röntgenexponering innan enheten används på gravida
kvinnor.
5 Biverkningar
Potentiella biverkningar relaterade till införandet av kanyler i kranskärlen och placering av skidan
och dilatatorn i hjärtat omfattar, men är inte begränsade till, följande:
• Komplikationer vid åtkomststället (hematom, infektioner, trombos, ekkymos, AV-fistel, blödningar från ingångsstället, hemorragi)
• Luftemboli
• Arytmi (förmaksflimmer, förmaksfladder,
kammartakykardi)
• Hjärtstillestånd
• Obehagskänslor, smärta eller tryck över
bröstkorgen
• Kranskärlskramp, dissektion, trombos
• Dödsfall
• Endokardit
• Hjärtblock som kräver permanent användning av pacemaker
• Blödning i lungsäcken
• Hjärtinfarkt
• Perforering av hjärtvävnad eller omgivande vävnad
• Perikardiell utgjutning, tamponad
• Perikardit
• Pleuralvätskeutgjutning
• Pneumotorax
• Pseudoaneurysm
• Lungödem
• Lungemboli
• Stroke
• Blodpropp
• Transitorisk ischemisk attack (TIA)
• Vasovagal reaktion
6 Bruksanvisning
Observera: Innan skidan förs in i patienten ska deflektionsmekanismen testas för att kontrollera
att den fungerar.
1. Använd en aseptisk teknik och skapa kärlaccess med en lämplig introducer.
2. För in en kompatibel styrtråd (se Specifikationer) genom kärlsystemet och in till önskad plats
via standardmetoder för kärlaccess.
3. Spola skidans sidopor t och dilatatorlumen med steril koksaltlösning.
4. Säkerställ att skidan är i ett neutralt (icke-böjt) läge och blöt dilatatorns skaft med steril
koksaltlösning innan den förs in genom hemostasventilen.
5. Börja montera ihop dilatatorn och skidan genom att föra in dilatatorns distala spets i
hemostasventilen, så att dilatatorns krökta kant är vinkelrät mot hemostasventilen (se
Figur 2).
Figur 2. FlexCath Select styrbar skida
6. Fortsätt att föra in dilatatorn i skidan tills dilatatorfattningen snäpper på plats ordentligt i
skidfattningen.
Observera: Etiketten på dilatatorfattningen ska vara i linje med etiketten på skidans handtag
så att dilatatorns krökning riktas in med samma orientering som skidans böjningsriktning och
sidoporten (se Figur 3).
Figur 3. FlexCath Select styrbar skida
7. Trä enheten bestående av skida och dilatator över styrtråden och in i kärlsystemet med hjälp
av en lätt vridande rörelse in i övre hålvenen (SVC).
8. Avlägsna styrtråden.
9. För in den korrekt förberedda transseptalnålen i enheten bestående av skida och dilatator så
att krökningsindikatorn på transseptalnålen riktas in mot sidoporten.
Observera: Transseptalnålen ska användas tillsammans med en mandräng för att förhindra
spaltning av dilatatorns innerlumen.
10. För ned enheten till höger förmak för att förbereda en transseptal punktion.
11. Utför den transseptala punktionen under fluoroskopisk vägledning och med hjälp av
tryckmätningar, injektion av kontrastmedel eller båda. Bekräfta korrekt placering i vänster
förmak.
12. Dra in transseptalnålen i dilatatorn och avlägsna långsamt enheten bestående av dilatator
och nål från skidan.
Observera: Avlägsna dilatatorn långsamt för att undvika undertryck i skidan. Blod ska
aspireras fritt genom sidoporten. Om det inte sker ska skidan dras tillbaka något eftersom
skidspetsen kan ligga an mot förmaksväggen eller en lungven.
13. Aspirera blod genom sidoporten och säkerställ att skidan inte innehåller någon luft. Utför
aspiration eller låt blodet spontant rinna tillbaka innan en kateter förs in i skidan.
Observera: Utför detta steg efter varje kateterbyte.
14. Upprätthåll antikoaguleringsbehandling när åtkomst till skidan har uppnåtts.
15. Förbered katetern enligt tillverkarens bruksanvisning.
16. För in katetern och placera skidan.
57
Svenska

Observera:
• Införandet kan underlättas av att kateterskaftet blöts.
• Hemostasventilen har ett säkert stopp för att förhindra att eventuella
infångningsanordningar öppnar förseglingen.
• Komponenter ska alltid föras in eller avlägsnas långsamt för att minimera det vakuum
som skapas.
• Skidan ska även spolas medan en kateter är införd.
17. Säkerställ att skidan är i neutralt (oböjt) läge innan den dras bort.
7 Tekniska data
Sammanlagd längd
Användbar längd 65 cm (25,6 in)
Inre diameter 3,3 mm (10 Fr) (0,13 in)
Yttre diameter 4,3 mm (13 Fr) (0,17 in)
Dilatatorns längd 86 cm (33,9 in)
Röntgentät markering 5 mm (0,2 in) proximalt om skidans spets
Kompatibilitet hos ledare 0,81 mm (0,032 in) till 0,89 mm (0,035 in)
Kompatibilitet hos transseptal-
nål
Miljöparametrar
Rekommenderad transporttemperatur
Rekommenderad förvaringstemperatur
Drift 15°C till 30°C (59°F till 86°F) på en maximal höjd av 2 400 m
81 cm (31,9 in)
89 cm (35,0 in) eller längre
−35°C till 58°C (−31°F till 136°F), 85 % relativ luftfuktighet
(icke-kondenserande)
Medelvärde på 22°C (72°F) med en standardavvikelse på
2,7°C (4,86°F) och tillåtna gränsvärden på 15°C till 30°C (59°F
till 86°F)
(8 000 fot) över havet
8 Medtronic ansvarsfriskrivning
I det bifogade dokumentet med friskrivningsklausulen finns fullständig information om garantier.
9 Service
Medtronic har välutbildade representanter och tekniker över hela världen som kan stå till tjänst
och, på begäran, erbjuda utbildning till behörig sjukhuspersonal i användningen av
Medtronic-produkterna. Medtronic har professionella konsulter som kan hjälpa
produktanvändarna med tekniska frågor. Ytterligare information kan lämnas av Medtronic eller fås
genom att ringa eller skriva till Medtronic på det telefonnummer eller den adress som anges på
manualens baksida.
Svenska
58

1 Tanım
65 cm
(25,6 inç)
16 cm
(6,3 inç)
86 cm
(33,9 inç)
Medtronic FlexCath™ Select Yönlendirilebilir Kılıf, kan kaybını en aza indirerek kateterlerin
yerleştirilmesini, çekilmesini ve değiştirilmesini sağlayan bir valf ile donatılmış bir perkütan kateter
introdüseridir. Sürekli olarak damlalar halinde infüzyon, ortadaki lumenden enjeksiyon, yıkama,
aspirasyon, kan numunesi alımı ve basınç izleme işlemlerine izin vermek üzere, vanası olan bir yan
port entegre edilmiştir.
Şekil 1. FlexCath Select Yönlendirilebilir Kılıf
FlexCath Select Yönlendirilebilir Kılıf ile birlikte bir dilatör de verilmiştir. Kılıf aşağıdaki tabloda
açıklanmaktadır:
Model
990065 3,3 mm (10 Fr)
Kılıf, kılıfın içinden kalbin sağ veya sol odacığına ilerletilen kateterlere ek manevra yeteneği
sağlayarak farklı yönlere çevrilebilir.
10 Fr FlexCath Select Yönlendirilebilir Kılıf, boyutları 9 Fr’ye kadar olan
Medtronic diyagnostik ve ablasyon kateterleri ile kullanılabilir.
10 Fr FlexCath Select Yönlendirilebilir Kılıf dilatörü 89 cm ve daha uzun olan
Merit Medical HeartSpan Transseptal İğneleri ile uyumludur.
İç çapı Dış çapı Kullanılabilir uzunluğu
(0,13 in)
4,3 mm (13 Fr) (0,17 in) 65 cm (25,6 in)
1.1 Ambalajın içindekiler
FlexCath Select Yönlendirilebilir Kılıf steril olarak tedarik edilir. Ambalaj aşağıdaki öğeleri içerir:
• 1 adet yönlendirilebilir kılıf
• 1 adet dilatör
• Ürünle ilgili belgeler
2 Kullanım endikasyonları
FlexCath Select Yönlendirilebilir Kılıf, perkütan kateterin vaskülatüre ve interatriyal septum yoluyla
kalbin sol tarafı dahil olmak üzere kalbin odacıklarına yerleştirilmesine yöneliktir. Kılıfın yön
değiştirme özelliği kateterin konumlandırılmasını kolaylaştırır.
3 Kontrendikasyonlar
FlexCath Select Yönlendirilebilir Kılıfın aşağıdaki durumlardan herhangi birinin hasta için geçerli
olması durumunda sol atriyuma veya ventriküle yerleştirilmesi kontrendikedir:
• Hastada intra-atriyal septal yama veya tıkayıcı bulunmaktadır veya hasta intra-atriyal septum
içinde veya yanında başka bir cerrahi müdahale geçirmiştir.
• Hastada sol atriyal trombüs vardır.
• Hastada bilinen veya şüphe edilen atriyal miksom vardır.
4 Uyarılar ve önlemler
Ablasyon enerjisi – Kılıf ablasyon enerjisinin olduğu bir durumda kullanılırken, tüm ablasyon
öğelerinin kılıfın dışında olduğundan emin olunması için dikkat gösterilmelidir.
Hava aspirasyonu – Kılıfı aspire edip yıkamadan önce kılavuz teli kılıftan çıkarın. Böylelikle kılıf
valfinin içinden hava aspirasyonunu en aza indirmiş olursunuz.
Antikoagülasyon tedavisi – Sol taraftaki ve transseptal kardiyak prosedürlerden geçen hastalar
ve sağ taraftaki prosedürlerden geçen seçilmiş hastalar için, prosedür öncesinde, esnasında ve
sonrasında uygun düzeylerde antikoagülasyon tedavisi uygulanmalıdır. Kanamayı ve trombotik
komplikasyonları en aza indirmek için prosedür öncesinde, esnasında ve sonrasında kurumun
standartlarına uygun olarak antikoagülasyon tedavisi uygulanmalıdır.
Kanın Geriye Doğru Sızması – Kanın istenmeyen biçimde yan porttan geriye doğru sızmasını
önlemek için yıkamadan veya aspirasyondan sonra vananın kapalı konumda olduğundan emin
olun.
Biyolojik risk oluşturan atıkların bertaraf edilmesi – Tüm kullanılmış cihazları ve steril
bileşenleri hastane prosedürlerine uygun şekilde atın.
Kontrast enjeksiyonu – Kılıfa kontrast çözeltisi enjeksiyonu için elektrikli bir enjeksiyon sistemi
kullanmayın.
Dilatörün döndürülmesi – Dilatörü valf göbeğine oturttuktan sonra döndürmeyin. Bu durum,
distal kenardaki dilatör ucunun proksimal kenardaki yan porta göre yanlış hizalanmasına neden
olabilir.
Yeniden sterilize etmeyin – Bu cihazı tekrar kullanım amacıyla yeniden sterilize etmeyin.
Yeniden sterilize edilmesi, cihazın yapısal bütünlüğünü tehlikeye düşürebilir veya cihazda,
hastanın yaralanması, hastalanması veya ölümüyle sonuçlanabilecek bir kontaminasyon riski
oluşturabilir.
Embolizm riski – Dolaşım sistemi içine herhangi bir kateterin veya kılıfın yerleştirilmesi hava
embolizmi riski içerir ; bu durum damarları tıkayabilir ve ciddi sonuçlar doğuran doku enfarktüsüne
yol açabilir. Bu cihazla birlikte 9 Fr’den daha küçük kateterlerin kullanılması hava embolizmi riskini
artırabilir. Hava oluşumunu en aza indirmek için, bileşenleri daima yavaşça ilerletin, çekin ve
yıkamadan yararlanın, böylece hava embolizmi riskini en aza indirmiş olursunuz.
Son kullanma tarihi – Son kullanma tarihinin geçmediğini doğrulamak için kılıfı kontrol edin. Son
kullanma tarihi geçmişse ürünü kullanmayın.
Femoral ven hasarı – Kılıfın yerleştirilmesi, hareket ettirilmesi veya çekilmesi üzerine femoral
vene ve erişim bölgesine verilebilecek hasarın en aza indirilmesine özen gösterilmelidir. Femoral
ven kateterizasyonuna ilişkin komplikasyonlar hematom ve trombozu içerir.
Kılıfın yerleştirilmesi için gerekli floroskopi – Kılıfın hareket ettirilmesi ve yerleştirilmesi
sırasında floroskopi kullanılması özellikle tavsiye edilmektedir. Kılıfın floroskopi kullanılmadan
hareket ettirilmesi kardiyak ve vasküler yapılarda zarara yol açabilir.
Yalnızca tek kullanımlıktır – Bu cihaz yalnızca tek bir hastada bir kez kullanılmaya yöneliktir. Bu
cihazı yeniden kullanmayın, işleme tabi tutmayın veya tekrar kullanım amacıyla yeniden sterilize
etmeyin. Yeniden kullanılması, işleme tabi tutulması veya sterilize edilmesi, cihazın yapısal
bütünlüğünü tehlikeye düşürebilir veya cihazda, hastanın yaralanması, hastalanması veya
ölümüyle sonuçlanabilecek bir kontaminasyon riski oluşturabilir.
Sık sık yıkama – Kılıfın düzenli olarak yıkanması tavsiye edilmektedir:
• Kan durgunluğunun, pıhtıların, emboli ve ciddi hasta yaralanmasının önlenmesi için.
• Her kontrast enjeksiyonundan sonra, kontrast çözeltinin lümenin içine yapışmasını önlemek
için.
Kullanım ve bakım – Cihazı kullanırken:
• Cihazı hareket ettirirken son derece dikkatli olun. Yeterli özenin gösterilmemesi perforasyon,
tamponad, aritmilerin indüklenmesi veya kalp bloğu gibi yaralanmalarla sonuçlanabilir.
• Özellikle dirençle karşılaşılan durumlarda, cihazı ilerletmek veya çekmek için aşırı güç
uygulamayın.
• Cihazın kalp içinde sıkışma olasılığını artırdığından ve cerrahi müdahaleyi veya zedelenen
dokuların onarılmasını gerektirebildiğinden cihazı korda tendinea’lar etrafında
konumlandırmaktan kaçının.
• Eğilmişse veya hasar görmüşse kılıfı kullanmayın.
59
Türkçe

Sol atriyal erişim – Dilatör veya kılıfın istenmeyen bir konuma ilerletilmesini engellemek için,
öncelikle sol atriyal erişimi teyit etmeden bu bileşenleri interatriyal septum içerisinden
ilerletmeyin.
Gerekli hastane ekipmanı – Yönlendirilebilir kılıf tertibatının kullanımı sırasında, hemen kullanım
için yakınınızda harici defibrilasyon ekipmanı bulundurun.
Diğer kateterler, cihazlar veya teller – Kılıfın diğer kateterler, cihazlar veya tellere
dolaşmasından kaçınılmalıdır. Bu tür bir dolaşıklık cerrahi müdahale gerektirebilir.
Prostetik kalp kapakları – Cihazı prostetik kalp kapağının (mekanik veya doku) içinden
geçirmeyin. Cihaz kapakta sıkışarak kapağa zarar verebilir ve valvüler yetmezliğe veya prostetik
kapağın erken arızalanmasına neden olabilir.
Yetkili kullanıcılar – Bu ekipman yalnızca kardiyak kateterizasyon prosedürleri konusunda
eğitim almış olan hekimler tarafından ve onların gözetimi altında kullanılmalıdır.
Gerekli kullanım ortamı – Kardiyak kateterizasyon prosedürleri yalnızca tam donanımlı bir
tesiste gerçekleştirilmelidir.
Yan port aspirasyonu – Dilatörü, kateteri, iğneyi, telleri veya diğer cihazları geri çekerken yan
portu aspire edin.
Yan portun tıkanması – Salinle yıkama işleminin etkili olduğundan emin olmak için yan portun
tıkanmamasına dikkat edilmelidir.
Önemli kan sızıntısı – Prosedür esnasında hemostatik valften önemli kan sızıntısı olmadığının
gözlenmesine özen gösterilmelidir.
Steril ambalajın incelenmesi – Kullanmadan önce steril ambalajı ve cihazı inceleyin. Steril
ambalajda veya cihazda hasar göze çarpıyorsa cihazı kullanmayın. Bulunduğunuz yerdeki
Medtronic temsilcisiyle irtibata geçin.
Röntgen ve floroskopi maruziyeti – Kateter ablasyon prosedürleri sırasında floroskopinin
kullanılması hem hastalar hem de laboratuar çalışanları açısından röntgen ışınlarına anlamlı
ölçüde maruz kalınması olasılığı teşkil eder. Yaygın ölçüde maruz kalınması, radyasyon nedeniyle
akut yaralanma ile somatik ve genetik etkiler açısından risk artışına neden olabilir. Kateterle
ablasyonu, sadece prosedürle bağlantılı olan olası radyasyon maruziyetine yeterli ölçüde dikkat
ettikten ve bu maruz kalma oranını en aza indirme yönünde adımlar attıktan sonra gerçekleştirin.
Cihaz gebe kadınlarda kullanılmadan önce dikkatlice değerlendirme yapılmalı ve röntgen
maruziyetinden kaçınılmalıdır.
5 Advers olaylar
Periferik vaskülatür kanülasyonuyla ve kılıf ile dilatörün kalp içine yerleştirilmesiyle bağlantılı olan
olası advers olaylar, bunlarla sınırlı olmamakla birlikte aşağıdaki durumları içerebilir:
• Erişim bölgesi komplikasyonları (hematom, enfeksiyon, tromboz, ekimoz, AV fistül, ponksiyon bölgesinde kanama, hemoraji)
• Hava embolizmi
• Aritmi (atriyal fibrilasyon, atriyal flatter, ventriküler taşikardi)
• Kalbin durması
• Göğüste rahatsızlık, ağrı veya basınç
• Koroner arter spazmı, diseksiyon, tromboz
• Ölüm
• Endokardit
• Kalıcı pacemaker gerektiren kalp bloğu
• Hemotoraks
• Miyokard enfarktüsü
• Kardiyak dokuda veya çevreleyen dokuda
perforasyon
• Perikardiyal efüzyon, tamponad
• Perikardit
• Plevral efüzyon
• Pnömotoraks
• Psödoanevrizma
• Pulmoner ödem
• Pulmoner embolizm
• İnme
• Trombüs
• Geçici iskemik atak (GİA)
• Vazovagal reaksiyon
6 Kullanım talimatları
Not: Kılıfı hastaya yerleştirmeden önce, çalıştığından emin olmak için yön değiştirme
mekanizmasını test edin.
1. Aseptik teknik kullanarak uygun bir introdüser ile vasküler erişim oluşturun.
2. Standar t vasküler erişim tekniklerini kullanarak uyumlu bir kılavuz teli (bkz. Teknik Özellikler)
vaskülatürün içinden, istenilen konuma yerleştirin.
3. Kılıfın yan portunu ve dilatör lumenini steril salin çözeltisi ile yıkayın.
4. Kılıfın nötr (yönü değiştirilmemiş) konumda olduğundan emin olun ve dilatör şaftını,
hemostaz valfinin içinden geçirmeden önce steril salin çözeltisi ile ıslatın.
5. Dilatörün kavisli kenarı hemostaz valfine dik olacak şekilde, dilatörün distal ucunu hemostaz
valfine yerleştirerek dilatör ve kılıfı birleştirme işlemine başlayın (bkz. Şekil 2).
Şekil 2. FlexCath Select Yönlendirilebilir Kılıf
6. Dilatör göbeği kılıf göbeğine tam olarak geçene kadar dilatörü kılıf içine ilerletmeye devam
edin.
Not: Dilatör göbeğindeki etiket kılıf sapındaki etiket ile aynı hizada olmalıdır; böylece dilatör
kavisi, kılıfın saptığı yönle ve yan portla aynı yönde hizalanmış olur (bkz. Şekil 3).
Şekil 3. FlexCath Select Yönlendirilebilir Kılıf
7. SVC içine doğru hafif bir döndürme hareketiyle kılıf-dilatör tertibatını kılavuz tel üzerinden
vaskülatüre geçirin.
8. Kılavuz teli çıkarın.
9. Doğru şekilde hazırlanmış olan transseptal iğneyi kılıf-dilatör tertibatına, transseptal iğnedeki
eğrilik göstergesi yan port ile hizalanacak şekilde geçirin.
Not: Dilatörün iç lumeninin sıyrılmasının engellenmesi için, stile ile birlikte transseptal iğne
kullanılmalıdır.
10. Transseptal ponksiyon için hazırlamak üzere tertibatı sağ atriyuma doğru aşağıya çekin.
11. Floroskopi rehberliğinde, basınç ölçümleri, kontrast enjeksiyonu ya da her ikisini de
kullanarak transseptal ponksiyon gerçekleştirin. Sol atriyuma doğru bir şekilde
yerleştirildiğini doğrulayın.
12. Transseptal iğneyi dilatör içine çekin ve dilatör ile iğne tertibatını kılıftan yavaşça çıkarın.
Not: Kılıfın içinde vakum oluşması olasılığını azaltmak için dilatörü yavaşça çıkarın. Kan yan
porttan rahat bir şekilde aspire edilmelidir. Aspirasyon rahatça gerçekleştirilemiyorsa, kılıf
ucu atriyum duvarına veya pulmoner vene yaslanıyor olabileceğinden kılıfı çekin.
13. Kanı yan porttan aspire edin ve kılıfın içinde hava olmadığından emin olun. Kateteri kılıfa
yerleştirmeden önce, aspirasyon uygulayın veya kendiliğinden biraz kan gelmesini sağlayın.
Not: Bu adımı tüm kateter değiştirme işlemlerinden sonra uygulayın.
14. Kılıfla erişim sağlanmasının ardından antikoagülasyon tedavisini sürdürün.
15. Kateteri imalatçının kullanım talimatlarına uygun olarak hazırlayın.
16. Kateteri yerleştirin ve kılıfı konumlandırın.
Türkçe
60

Notlar:
• Kateter şaftının ıslatılması geçirme işleminin kolaylaştırılmasına yardımcı olabilir.
• Hemostaz valfinde, yakalama cihazlarının (varsa) mührü açmasını engellemeye yönelik,
pozitif bir durdurucu vardır.
• Vakum oluşumunu en aza indirmek için bileşenleri daima yavaşça yerleştirin ve çekin.
• Kılıf bir kateter takılıyken de yıkanmalıdır.
17. Kılıfı çekmeden önce kılıfın nötr (yönü değiştirilmemiş) konumda olduğundan emin olun.
7 Teknik Özellikler
Tam uzunluğu
Kullanılabilir uzunluğu 65 cm (25,6 in)
İç çapı 3,3 mm (10 Fr) (0,13 in)
Dış çapı 4,3 mm (13 Fr) (0,17 in)
Dilatör uzunluğu 86 cm (33,9 in)
Radyopak belirteci 5 mm (0,2 in) kılıf ucuna proksimal
Kılavuz tel uyumluluğu 0,81 mm (0,032 in) ila 0,89 mm (0,035 in)
Transseptal iğne uyumluluğu 89 cm (35,0 in) veya daha uzun
Ortam parametreleri
Önerilen taşıma sıcaklığı −35°C ila 58°C (−31°F ila 136°F); %85 bağıl nem (yoğunlaş-
Önerilen saklama sıcaklığı 2,7°C (4,86°F) standart sapmayla ortalama 22°C (72°F) ve
Çalıştırma Deniz seviyesinin üzerinde 2400 m’den (8000 fit) daha düşük
81 cm (31,9 in)
mayan)
15°C ila 30°C (59°F ila 86°F) işleme geçilebilecek kontrol limitleri
olan rakımlarda 15°C ila 30°C (59°F ila 86°F)
8 Medtronic garantiden feragat beyannamesi
Garanti bilgilerinin tamamı için ekteki garantiden feragat beyannamesine bakın.
9 Servis
Medtronic, size hizmet sağlamaları ve istendiğinde Medtronic ürünlerini kullanan vasıflı hastane
personeline eğitim vermeleri amacıyla, dünyanın her yerinde iyi eğitimli temsilciler ve mühendisler
istihdam etmektedir. Medtronic ayrıca ürün kullanıcılarına teknik danışmanlık sağlamak üzere
uzman bir kadro ile çalışmaktadır. Daha fazla bilgi için, bulunduğunuz yerdeki Medtronic
temsilcinizle veya arka kapakta yer alan listeden uygun telefon numarası veya adresi seçerek,
telefon veya posta yoluyla Medtronic ile irtibat kurun.
61
Türkçe



Medtronic, Inc.
*M426693B001*
710 Medtronic Parkway
Minneapolis, MN 55432
USA
www.medtronic.com
+1 763 514 4000
Medtronic CryoCath LP
9000 Autoroute Transcanadienne
Pointe-Claire, Quebec H9R 5Z8
Canada
+1 514 694 1212
Technical Support +1 877 464 2796
Authorized Representative in the
European Community
Medtronic B.V.
Earl Bakkenstraat 10
6422 PJ Heerlen
The Netherlands
+31 45 566 8000
Europe/Middle East/Africa
Medtronic International Trading Sàrl
Route du Molliau 31
Case Postale 84
CH-1131 Tolochenaz
Switzerland
+41 21 802 7000
Australia
Medtronic Australasia Pty Ltd
5 Alma Road
Macquarie Park, NSW 2113
Australia
1800 668 670
Canada
Medtronic of Canada Ltd
99 Hereford Street
Brampton, Ontario L6Y 0R3
Canada
+1 905 460 3800
Technical manuals
www.medtronic.com/manuals
© 2017 Medtronic
M426693B001 1B
2017-02-13
 Loading...
Loading...