Page 1

High Range Heparinase Test Cartridge (HR HTC)
Cartouche de test héparinase valeurs élevées (HR HTC)
High Range Heparinase-Testkartusche (HR HTC)
Cartucho de prueba de heparinasa de rango alto (HR HTC)
Testcartridge voor hoog bereik heparinase (HR-HTC)
Cartuccia per test con eparinasi ad ampio range (HR HTC)
High Range -heparinaasitestiputki (HR HTC)
Testbehållare för heparinas med högt värde (HR HTC)
Φύσιγγα δοκιμασίας ηπαρινάσης υψηλού εύρους (HR HTC)
HR HTC-testkassette (højområdeheparinase)
Cartucho para teste com heparinase - valores altos (HR HTC)
Instructions for Use • Mode d’emploi • Gebrauchsanweisung •
Instrucciones de uso • Gebruiksaanwijzing •
Istruzioni per l’uso • Käyttöohjeet • Bruksanvisning •
Οδηγίες χρήσης • Brugsanvisning • Instruções de utilização
Caution: Federal law (USA) restricts
this device to sale by or on the order of a
physician.
Page 2

Trademarks may be registered and are the property of their respective owners.
Les marques commerciales mentionnées peuvent être déposées et appartiennent à
leurs propriétaires respectifs.
Marken sind eventuell eingetragen und sind das Eigentum ihrer jeweiligen Inhaber.
Las marcas comerciales pueden estar registradas y pertenecen a sus respectivos
propietarios.
Handelsmerken kunnen zijn geregistreerd en zijn het eigendom van de desbetreffende
eigenaars.
I marchi di fabbrica possono essere registrati e sono di proprietà dei rispettivi titolari.
Tavaramerkit voivat olla rekisteröityjä, ja ne ovat omistajiensa omaisuutta.
Varumärken kan vara registrerade och tillhör respektive ägare.
Τα εμπορικά σήματα μπορεί να είναι καταχωρημένα και είναι ιδιοκτησία των αντίστοιχων
κατόχων τους.
Varemærker kan være registrerede og tilhører deres respektive ejere.
As marcas comerciais podem ser registadas e são propriedade dos respetivos
detentores.
Page 3

Explanation of symbols on package labeling. /
Explication des symboles des étiquettes sur
l’emballage. / Erläuterung der Symbole auf der
Verpackung / Explicación de los símbolos que
aparecen en la documentación del envase. /
Verklaring van de symbolen op de productlabels. /
Spiegazione dei simboli presenti sulle etichette
della confezione. / Pakkausetiketin symbolien
selitykset / Förklaring av symboler på
förpackningsmärkningen. / Επεξήγηση των
συμβόλων στη σήμανση της συσκευασίας. /
Forklaring til symbolerne på mærkaterne på
emballagen. / Explicação dos símbolos na
documentação da embalagem.
Conformité Européenne (European Conformity).
This symbol means that the device fully
complies with European Council Directive
IVDD: 98/79/EC. / Conformité Européenne. Ce
symbole signifie que le dispositif est entièrement
conforme à la Directive européenne relative aux
dispositifs médicaux de diagnostic in vitro
IVDD 98/79/CE. / Conformité Européenne
(Europäische Konformität). Dieses Symbol
besagt, dass das Gerät die Anforderungen der
Richtlinie 98/79/EG des Europäischen Rats über
In-vitro-Diagnostika (IVDD) vollständig erfüllt. /
Conformité Européenne (Conformidad
Europea). Este símbolo indica que el dispositivo
cumple totalmente la Directiva 98/79 CEE del
Consejo Europeo sobre dispositivos de
diagnóstico in vitro. / Conformité Européenne
(Europese Conformiteit). Dit symbool betekent
dat het product volledig voldoet aan de richtlijn
van de Europese Raad IVDD: 98/79/EG. /
Conformité Européenne (Conformità europea).
Questo simbolo significa che il dispositivo è
conforme alla Direttiva del Consiglio Europeo
IVDD 98/79/CE. / Conformité Européenne
(eurooppalainen vaatimustenmukaisuus). Tämä
symboli tarkoittaa, että laite on kaikilta osin in
vitro -diagnostiikkaan tarkoitetuista
lääkinnällisistä laitteista annetun Euroopan
unionin neuvoston direktiivin 98/79/EY
mukainen. / Conformité Européenne (Europeisk
standard). Denna symbol betyder att enheten
helt följer Europarådets direktiv
IVDD 98/79/EG. / Conformité Européenne
(Ευρωπαϊκή Συμμόρφωση). Το σύμβολο αυτό
σημαίνει ότι το προϊόν συμμορφώνεται πλήρως
με την Οδηγία του Ευρωπαϊκού Συμβουλίου
περί ιατροτεχνολογικών βοηθημάτων που
χρησιμοποιούνται στη διάγνωση in
vitro: 98/79/ΕΚ. / Conformité Européenne
(Europæisk Standard). Dette symbol betyder, at
enheden fuldt ud overholder det Europæiske
1
Page 4

Råds Direktiv om medicinsk udstyr til in vitrodiagnostik: 98/79/EF. / Conformité Européenne
(Conformidade Europeia). Este símbolo significa
que o dispositivo está em total conformidade
com a Diretiva do Conselho Europeu relativa
aos dispositivos médicos de diagnóstico in
vitro: 98/79/CE.
Do Not Reuse / Ne pas réutiliser / Nicht
wiederverwenden / No reutilizar / Niet opnieuw
gebruiken / Non riutilizzare / Älä käytä
uudelleen / Endast för engångsbruk / Μην
επαναχρησιμοποιείτε / Må ikke genbruges / Não
reutilizar
Use-By Date / À utiliser jusqu'au / Zu verwenden
bis einschließlich / No utilizar después de /
Uiterste gebruiksdatum / Utilizzare entro /
Viimeinen käyttöpäivämäärä / Sista
förbrukningsdatum / Ημερομηνία «Χρήση έως» /
Sidste anvendelsesdato / Utilizar antes da data
Manufactured In / Lieu de fabrication /
Hergestellt in / Fabricado en / Vervaardigd in /
Fabbricato in / Valmistuspaikka / Tillverkad i /
Κατασκευάστηκε σε / Fremstillet i / Fabricado
em
Lot Number / Numéro de lot / Chargennummer /
Número de lote / Partijnummer / Numero di
lotto / Eränumero / Lotnummer / Αριθμός
παρτίδας / Partinummer / Número de lote
Quantity / Quantité / Menge / Cantidad / Aantal /
Quantità / Määrä / Antal / Ποσότητα / Antal /
Quantidade
Consult Instructions for Use / Consulter le mode
d'emploi / Gebrauchsanweisung beachten /
Consultar las instrucciones de uso / Raadpleeg
gebruiksaanwijzing / Consultare le istruzioni per
l'uso / Katso käyttöohjeet / Läs
bruksanvisningen / Συμβουλευτείτε τις Οδηγίες
χρήσης / Se brugsanvisningen / Consultar
instruções de utilização
For US Audiences Only / Uniquement pour les
États-Unis / Gilt nur für Leser in den USA / Solo
aplicable en EE. UU. / Alleen van toepassing
voor de VS / Esclusivamente per il mercato
statunitense / Koskee vain Yhdysvaltoja / Gäller
endast i USA / Μόνο για πελάτες εντός των
ΗΠΑ / Gælder kun i USA / Apenas aplicável aos
EUA
Temperature Limit / Limite de température /
Temperaturbereich / Límite de temperatura /
Temperatuurbereik / Limiti di temperatura /
Lämpötilaraja / Temperaturgräns / Όριο
θερμοκρασίας / Temperaturgrænse / Limites de
temperatura
Fragile, Handle with Care / Fragile, manipuler
avec précaution / Vorsicht, zerbrechlich / Frágil,
2
Page 5
manipular con cuidado / Breekbaar, voorzichtig
hanteren / Fragile, maneggiare con cura /
Helposti särkyvä, käsittele varovasti / Ömtålig,
hanteras varsamt / Εύθραυστο, χειριστείτε με
προσοχή / Fragilt, behandles varsomt / Frágil,
manusear com cuidado
Catalog Number / Numéro de référence /
Katalognummer / Número de catálogo /
Catalogusnummer / Numero di catalogo /
Luettelonumero / Katalognummer / Αριθμός
καταλόγου / Katalognummer / Número de
catálogo
Manufacturer / Fabricant / Hersteller /
Fabricante / Fabrikant / Fabbricante /
Valmistaja / Tillverkare / Κατασκευαστής /
Fabrikant / Fabricante
Authorized Representative in the European
Community / Représentant agréé dans la
Communauté européenne / Autorisierter
Repräsentant in der Europäischen
Gemeinschaft / Representante autorizado en la
Comunidad Europea / Geautoriseerd
vertegenwoordiger in de Europese
Gemeenschap / Rappresentante autorizzato
nella Comunità europea / Valtuutettu edustaja
Euroopan yhteisön alueella / Auktoriserad
representant inom EG / Εξουσιοδοτημένος
αντιπρόσωπος στην Ευρωπαϊκή Κοινότητα /
Autoriseret repræsentant i EF / Representante
autorizado na Comunidade Europeia
Open Here / Ouvrir ici / Hier öffnen / Abrir aquí /
Hier openen / Aprire qui / Avaa tästä / Öppna
här / Ανοίξτε εδώ / Åbnes her / Abrir aqui
This Way Up / Placer ce côté vers le haut /
Diese Seite oben / Este lado hacia arriba / Deze
zijde boven / Questa parte rivolta verso l'alto /
Tämä puoli ylöspäin / Denna sida upp / Προς τα
πάνω / Denne side opad / Manter esta parte
virada para cima
In Vitro Diagnostic Medical Device / Dispositif
médical de diagnostic in vitro / Medizinisches
Gerät zur In-vitro-Diagnostik / Dispositivo
médico para diagnóstico in vitro / In-vitro
diagnostisch medisch apparaat / Dispositivo
medico diagnostico in vitro / In vitro diagnostinen lääkinnällinen laite /
Medicinteknisk produkt för in vitro-diagnostik /
Ιατροτεχνολογικό βοήθημα που χρησιμοποιείται
στη διάγνωση in vitro / Medicinsk udstyr til in
vitrodiagnostik / Dispositivo médico de
diagnóstico in vitro
Biological Risks / Risques biologiques /
Biogefährdung / Riesgos biológicos / Biologisch
gevaar / Rischi biologici / Biologiset riskit /
Biologiska risker / Βιολογικοί κίνδυνοι /
Biologiske risici / Riscos biológicos
3
Page 6

1. Intended Use
For use in identifying the presence of heparin using an activated clotting
time.
For in vitro diagnostic use.
Caution: Due to the unique nature of this product, care must be taken to
ensure that heparinase is not inadvertently transferred from the "HR HTC"
channel to the "HR" channel of the cartridge. For additional information,
see Section 8 and Section 10.
2. Summary
The Medtronic high range heparinase test cartridge, or HR HTC, is a
modification of the high range activated clotting time cartridge (HR ACT)
for the Medtronic automated coagulation timers. The activated clotting
time test was originally described by Hattersley in 19669. The test and its
variations have been widely used to monitor the anticoagulant effect of
3,4,7,8,13,14
heparin
does the HR ACT cartridge. The difference in the cartridge is that one
channel contains a purified bacterial heparinase (HR HTC). The
heparinase rapidly and specifically destroys the heparin present in the
blood sample
6 units/mL of heparin. The heparinase channel will produce a clotting time
reflective of the baseline, unheparinized clotting time of the sample, even
though the sample contains heparin. The other channel of the cartridge is
a standard HR ACT and the clotting time obtained is that of the
heparinized activated clotting time of the sample. Using this cartridge
allows: 1) verification of the presurgical presence of heparin,
2) assessment of the effect of bypass on the baseline activated clotting
time, 3) confirmation of heparin reversal following protamine
administration, 4) identification of postsurgical "heparin rebound," and
5) identification of the presence of heparin in patients who bleed
excessively postsurgically. A CLOTtrac™ HTC Control is available for
verification that the cartridge is performing to specifications.
. The HR HTC uses a freshly drawn whole blood sample, as
1,6,10,16
. The amount of heparinase present will rapidly remove
3. Principles
The activated clotting time test measures the clotting time of freshly drawn
whole blood activated by surface contact. Hattersley's original procedure
used diatomaceous earth as the activating agent. Diatomaceous earth
exhibits differing degrees of contact activation depending on its purity, the
source of the deposit, and the particle size and shape. Medtronic
activated clotting time cartridges use kaolin as the activating agent. Kaolin
exhibits superior characteristics in contact activation of blood coagulation.
The HR ACT and the HR HTC exhibit a decreased sensitivity to heparin,
allowing high levels of heparin to be monitored with the activated clotting
time test.
The endpoint of the test is the detection of clot formation. Medtronic
automated coagulation timers detect the formation of a clot by monitoring
the fall rate of the plunger/flag mechanism contained in each channel of
the cartridge. The plunger assembly falls rapidly through unclotted blood.
When a fibrin network forms, the fall of the plunger assembly is impeded.
This decrease in the fall rate is detected by the photo optical system in the
cover assembly of the instrument. Clot formation is indicated by an audio
signal and the clot timer is stopped. The instruments can perform
2 simultaneous tests using the 2-channel cartridge. Clotting times for each
channel are displayed in seconds following completion of the test. With
the HR HTC, the instrument displays 2 results, one for the sample with
heparinase and one for the sample without heparinase. The front panel
display can be used to alternate between the individual channel clotting
times, or the average and difference between the two channels. When
4 Instructions for Use English
Page 7

using the HR HTC, the averaged reading has little significance, however,
the difference between the two results is the extension of the clotting time
due to the presence of heparin in the sample.
4. Reagents
Each cartridge reagent chamber contains 0.1 mL of
hydroxyethylpiperazineethanesulfonic acid (HEPES) buffer, kaolin,
calcium chloride, and sodium azide as a bacteriostatic agent. The channel
labeled with "HR HTC" contains lyophilized, highly purified heparinase
with stabilizing agents and sodium azide as a bacteriostatic agent.
The HR HTC cartridge can be prewarmed for a maximum of 2 hours.
Once the sample is introduced into the prewarmed cartridge, the test must
be initiated immediately.
5. Storage
The HR HTC should be stored in a stable environment, either at
2°C to 10°C (36°F to 50°F), or 10°C to 25°C (50°F to 77°F). The
cartridges are packaged in sealed trays of 2 cartridges. The cartridges are
stable for the time period indicated on the tray label. Do not use the
cartridges after the Use-By Date. Do not use the cartridge if it appears
discolored, cracked or disfigured, or if the reagent appears to have
evaporated or be contaminated.
Once the seal on the tray lid has been broken, the cartridges are stable
for 24 hours at refrigerator temperatures.
Note: Do not use if there is evidence of freezing.
6. Instrument
The HR HTC is specifically designed for use in Medtronic automated
coagulation timers. Consult the instrument's Operator's Manual for
instructions.
To ensure proper instrument performance, it is important to clean the
instrument a minimum of every 30 days, or more if required.
Note: If blood gets into the actuator cover, clean the instrument as soon
as possible. An actuator cleaning kit (catalog #303-58) is provided with
each instrument. Use the materials provided in each cleaning kit to
perform the cleaning procedure. See the package insert included in the
cleaning kit for details.
7. Specimen Collection and Preparation
Improperly handled samples can yield erroneous coagulation test results;
therefore, samples must be collected carefully and handling techniques
must be consistent.
If blood is obtained by venipuncture, the venipuncture should be clean.
Discard the first several milliliters of blood to avoid contaminating the
sample with tissue thromboplastin.
Note: Do not take blood from heparinized indwelling catheters or other
anticoagulated lines without thoroughly flushing the line.
In testing freshly drawn whole blood, immediately transfer the sample to
the cartridge and initiate the test.
8. Instructions for Use
This product is intended for use only by trained individuals.
Materials supplied:
■
High range heparinase test cartridge (HR HTC), catalog #402-07
Materials required, not supplied
■
Medtronic automated coagulation timer
■
Plastic syringe with needle (preferably 18 or 19 gauge)
Instructions for Use English 5
Page 8

1
2
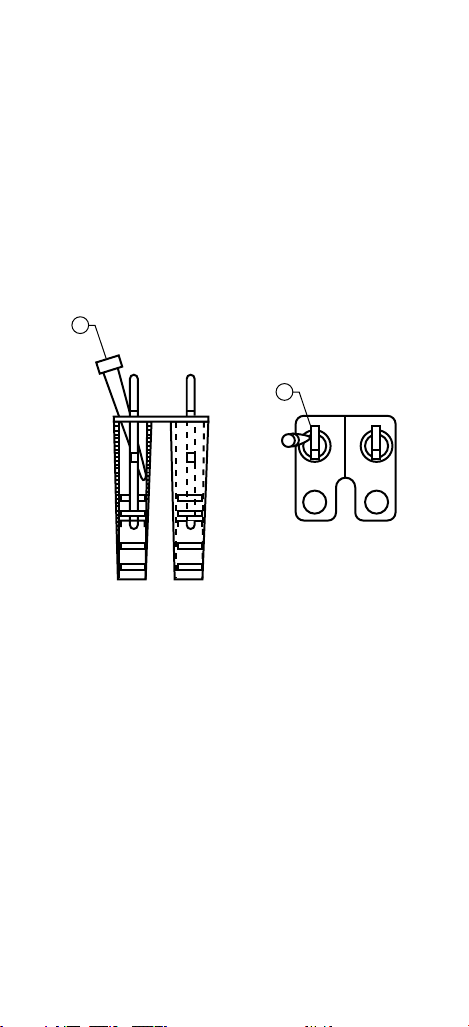
Figure 1. Filling the HR HTC Cartridge
1. Sample (side view)
2. Sample (view from the top)
To use with ACT Plus™ Instrument, follow the steps below:
1. From the Main Menu, select "Cartridge Type," and press the key until
"HTC" is displayed. Press "Enter" to confirm selection.
Note: Lot Numbers and Use-By Date for cartridges and controls must
be entered prior to running a test.
2. From the Main Menu, enter the "Patient ID" and "User ID" numbers.
Press "Enter" to confirm.
3. Prewarm the cartridge for 3 to 5 minutes before collecting the test
sample.
4. Tap the cartridge to resuspend the reagent.
5. Fill each chamber with 0.4 mL of sample.
Note: Always fill the HR channel first and the HR HTC channel
second to ensure heparinase does not contaminate the HR channel.
6. Insert the cartridge into the ACT Plus instrument and close the
actuator heat block to start the test.
7. Clot formation is signaled when an audible tone sounds, the actuator
heat block opens, and the results are displayed.
Following termination of the test, dispose of the cartridge, syringe, and
needle in approved biohazard disposal containers.
9. Results
The response of the activated clotting time to heparin varies considerably
from individual to individual12. Various drugs affect the activated clotting
time, in particular drugs that inhibit platelet activation15. A number of other
factors can affect the response of an individual's activated clotting time to
heparin, eg, antithrombin III levels, heparin potency, coagulation factor
deficiencies, sample activation, consumptive coagulopathies, excessive
sample dilution, and sample temperature. These should be taken into
account when interpreting the results of activated clotting time test
The heparinase in the HR HTC channel of the cartridge is extremely
specific for heparin. Sufficient heparinase is present to ensure that
6 units/mL of heparin is rapidly removed from the sample to bring it back
to a baseline or unheparinized condition. The baseline time may or may
not be at or near the normal range. If the baseline is not within the normal
range in the HR HTC channel, it indicates that some condition other than
2,5,11
.
6 Instructions for Use English
Page 9

the presence of heparin is responsible for extending the baseline clotting
time.
Example for interpreting HR HTC results:
Ch 1 Ch 2 Interpretation
120 120 Patient at baseline, no heparin present in
120 260 Patient has heparin in blood. Extension due
260 260 Patient has underlying coagulopathy unrela-
260 360 Patient has heparin in blood and patient has
60 200 Patient has heparin in blood and patient's
sample.
to effect of heparin only.
ted to heparin.
underlying coagulopathy (probably hemodilution).
coagulation system is activated.
10. Limitations of the Procedure
To obtain accurate and consistent activated clotting times with the
HR HTC, the following conditions must be observed:
■
The instrument heat block and cartridge temperature should be at
37°C ± 0.5°C (98.6°F ± 0.9°F). The cartridge will come to temperature
in 3 to 5 minutes in the instrument heat block.
■
The kaolin activator must be thoroughly resuspended.
■
Blood must be free of tissue thromboplastin. Run the test as soon as
possible after drawing the blood sample.
■
Patient diagnosis and medications should be noted. Medications can
alter clotting times. Samples that give unexplained abnormal values
should be redrawn and retested. If the results are still abnormal and
no cause is apparent, a sample should be citrated and sent to a
clinical lab for special coagulation analysis.
■
To optimize precision, all technique variables should be held constant
from test to test.
■
When the sample is placed in the cartridge, the test should be run as
quickly as possible. The removal of heparin from the sample occurs
rapidly. Contact activation will occur in the cartridge when the sample
has no heparin in it. This will result in shorter clotting times as
activation of the sample proceeds.
■
Methodologies used in cardiopulmonary bypass surgery continually
change as do the characteristics of the patient population. The
conditions that can influence activated clotting time test results may
include, but are not limited to:
■
patient's sensitivity to heparin
■
dilution of clotting factors by the extracorporeal circuit
■
the use of citrated blood products
■
the use of antiplatelet drugs
■
hypothermia
■
fluctuating calcium levels
■
a change in platelet function or count
■
unknown coagulopathies
Excessive blood dilution during bypass, frequently due to a desire to
limit the use of heterologous blood products, can lead to postoperative
bleeding. In severe instances, the dilution may be so great that
clotting, as measured by the activated clotting time, does not occur.
The adequacy of plasma clotting factors cannot be determined by
correlating the extent of dilution with the patient's hematocrit.
Frequently, washed cells have been administered to the patient
Instructions for Use English 7
Page 10

without compensating for lost plasma. If the HR HTC fails to clot in the
heparinase channel (channel #1), following reversal of patient heparin
with protamine, a dilutional coagulopathy is a strong possibility.
Warning: Due to the formulation of the HR HTC, it should not be used
to monitor regional anticoagulation achieved by infusing citrate.
Caution: Extreme care should be taken to ensure that heparinase in
the HR HTC channel is not inadvertently transferred to the sample in
the HR channel of the cartridge. If this occurs, the heparinized clotting
time in the "HR" channel would no longer be representative of the
amount of heparin in the sample, but would indicate less heparin,
depending on how much heparinase was transferred. For this reason,
it is strongly suggested that the "HR" channel be filled first to minimize
the possibility of heparinase transfer.
For precautions and limitations of the instrument, consult the
Operator's Manual.
11. Expected Values
The heparinase channel effectively provides a baseline activated clotting
time on heparinized freshly drawn whole blood. During bypass, the
baseline activated clotting time value may drift upwards, reflecting
hemodilution of the patient's blood. The baseline clotting time correlates
with the dilution of plasma clotting factors, which does not necessarily
correlate with the hematocrit of the patient. Red blood cells added back to
a patient from a cell saver do not compensate for lost plasma coagulation
factors. If the baseline activated clotting time remains extended, a
dilutional coagulopathy (lack of sufficient coagulation factors) may occur
and postoperative bleeding may be observed. The HR HTC can monitor
the development of this situation and allow remedial action before serious
dilution of coagulation factors occurs.
12. Specific Performance Characteristics
Activated clotting time cartridges, in the clotting range of
0 to 600 seconds, typically do not exceed a variation of 12% between
duplicate samples for any one individual. At high heparin levels and
clotting times in excess of 600 seconds, an activated clotting time is
generally not considered to be adequately reliable for determining heparin
levels.
The HR HTC is formulated to produce a normal HR ACT in the channel
labeled "HR", which corresponds closely to the responses originally
reported by Bull, et al (1975). The kaolin activator in each lot of cartridges
has been calibrated to reduce variations in activity between lots to less
than 10%, and to minimize long term drift.
The performance of the "baseline" channel of the cartridge is dependent
on the activity of the heparinase in the channel labeled "HR HTC". The
heparinase has been purified and stabilized to remove 6 units/mL of
heparin in a time span short enough to return the heparinized blood to a
baseline clotting time. The stability of the heparinase is ensured by
maintaining the cartridges at a constant temperature. The ranges in which
the cartridges may be stored are either at 2°C to 10°C (36°F to 50°F), or
10°C to 25°C (50°F to 77°F). Cartridge performance may diminish if the
product is not stored in a stable environment. Repeated movement of
product from refrigerated to ambient or ambient to refrigerated conditions
is not recommended.
13. Quality Control
Two levels of controls should be run for the HTC test to ensure adequate
performance of the instrument and cartridges.
Results should fall within the ranges specified by the manufacturer or
within those determined by the user.
8 Instructions for Use English
Page 11

Controls for the high range heparinase test include: the CLOTtrac™ HR
coagulation control (catalog #550-07) and the CLOTtrac HTC control
(catalog #550-12).
The CLOTtrac HTC control gives a baseline HR ACT in the HR HTC
channel and will time out (>999) in the HR ACT channel.
This control is a lyophilized control which contains 6 units/mL of heparin.
The performance of the HR HTC is verified by running the control in a
cartridge and obtaining a baseline HR ACT value in the channel labeled
"HR HTC" and a timeout (999 seconds) in the channel labeled "HR". This
indicates that the heparinase-containing channel of the cartridge is
properly functioning.
14. References
1. Baugh RF, Deemar KA, Zimmerman JJ. Heparinase in the activated
clotting time assay: Monitoring heparin-independent alterations in
coagulation function. Anesth Analg. 1992;74:201.
2. Bode AP, Eick L. Lysed platelets shorten the activated coagulation
time (ACT) of heparinized blood. Am J Clin Pathol. 1989;91:430.
3. Bull BS, Korpman RA, Huse WM, Briggs BD. Heparin therapy during
extracorporeal circulation. I. Problems inherent in existing heparin
protocols. J Thorac Cardiovasc Surg. 1975;69:674.
4. Bull BS, Huse WM, Brauer FS, Korpman RA. Heparin therapy during
extracorporeal circulation. II. The use of a dose-response curve to
individualize heparin and protamine dosage. J Thorac Cardiovasc
Surg. 1975;69:685.
5. Culliford AT, Gitel SN, Starr N, Thomas ST, Baumann FG, Wessler S,
Spencer FC. Lack of correlation between activated clotting time and
plasma heparin during cardiopulmonary bypass. Ann Surg.
1981;193:105.
6. Dietrich CP, Silva ME, Michelacci YM. Sequential degradation of
heparin in Flavobacterium heparinum. Purification and properties of
five enzymes involved in heparin degradation. J Biol Chem.
1973;248:6408.
7. Effeney DJ, Goldstone J, Chin D, Krupski WC, Ellis RJ. Intraoperative
anticoagulation in cardiovascular surgery. Surgery. 1981;90:1068.
8. Forman WB, Bayer G. A simplified method for monitoring heparin
therapy at the bedside: The activated whole blood clotting time. Am J
Hematol. 1981;11:277.
9. Hattersley PG. Progress report: The activated coagulation time of
whole blood (ACT). Am J Clin Pathol. 1976;66:899.
10. Hutt ED, Kingdon HS. Use of heparinase to eliminate heparin
inhibition in routine coagulation assays. J Lab Clin Med.
1972;79:1027.
11. Kesteven PJ, Pasaoglu I, Williams BT, Savidge GG. Significance of
the whole blood activated clotting time in cardiopulmonary bypass. J
Cardiovasc Surg. 1986;27:85.
12. Mabry CD, Read RC, Thompson BW, Williams GD, White HJ.
Identification of heparin resistance during cardiac and vascular
surgery. Arch Surg. 1979;114:129.
13. Mabry CD, Thompson BW, Read RC. Activated clotting time (ACT)
monitoring of intraoperative heparinization in peripheral vascular
surgery. Am J Surg. 1979;138:894.
14. Mabry CD, Thompson, BW, Read RC, Campbell GS. Activated
clotting time monitoring of intraoperative heparinization: Our
experience and comparison with two techniques. Surgery.
1981;90:889.
Instructions for Use English 9
Page 12

15. Moorehead MT, Westengard JC, Bull BS. Platelet involvement in the
activated coagulation time of heparinized blood. Anesth Analg.
1984;63:394.
16. Yang VC, Linhardt RJ, Bernstein H, Cooney CL, Langer R.
Purification and characterization of heparinase from Flavobacterium
heparinum. J Biol Chem. 1985;260:1849.
15. Disclaimer of Warranty
THE FOLLOWING DISCLAIMER OF WARRANTY APPLIES
TO UNITED STATES CUSTOMERS ONLY:
ALTHOUGH THE HIGH RANGE HEPARINASE TEST CARTRIDGE,
HEREAFTER REFERRED TO AS "PRODUCT," HAS BEEN
MANUFACTURED UNDER CAREFULLY CONTROLLED CONDITIONS,
MEDTRONIC HAS NO CONTROL OVER THE CONDITIONS UNDER
WHICH THIS PRODUCT IS USED. MEDTRONIC, THEREFORE,
DISCLAIMS ALL WARRANTIES, BOTH EXPRESS AND IMPLIED,
WITH RESPECT TO THE PRODUCT, INCLUDING, BUT NOT LIMITED
TO, ANY IMPLIED WARRANTY OF MERCHANTABILITY OR FITNESS
FOR A PARTICULAR PURPOSE. MEDTRONIC SHALL NOT BE
LIABLE TO ANY PERSON OR ENTITY FOR ANY MEDICAL
EXPENSES, OR ANY DIRECT, INCIDENTAL, OR CONSEQUENTIAL
DAMAGES CAUSED BY ANY USE, DEFECT, FAILURE, OR
MALFUNCTION OF THE PRODUCT, WHETHER A CLAIM FOR SUCH
DAMAGES IS BASED UPON WARRANTY, CONTRACT, TORT, OR
OTHERWISE. NO PERSON HAS ANY AUTHORITY TO BIND
MEDTRONIC TO ANY REPRESENTATION OR WARRANTY WITH
RESPECT TO THE PRODUCT.
The exclusions and limitations set out above are not intended to, and
should not be construed so as to, contravene mandatory provisions of
applicable law. If any part or term of this Disclaimer of Warranty is held to
be illegal, unenforceable, or in conflict with applicable law by a court of
competent jurisdiction, the validity of the remaining portions of this
Disclaimer of Warranty shall not be affected, and all rights and obligations
shall be construed and enforced as if this Disclaimer of Warranty did not
contain the particular part or term held to be invalid.
16. Disclaimer of Warranty
THE FOLLOWING DISCLAIMER OF WARRANTY APPLIES
TO CUSTOMERS OUTSIDE THE UNITED STATES:
ALTHOUGH THE HIGH RANGE HEPARINASE TEST CARTRIDGE,
HEREAFTER REFERRED TO AS "PRODUCT," HAS BEEN
CAREFULLY DESIGNED, MANUFACTURED, AND TESTED PRIOR TO
SALE, THE PRODUCT MAY FAIL TO PERFORM ITS INTENDED
FUNCTION SATISFACTORILY FOR A VARIETY OF REASONS. THE
WARNINGS CONTAINED IN THE PRODUCT LABELING PROVIDE
MORE DETAILED INFORMATION AND ARE CONSIDERED AN
INTEGRAL PART OF THIS DISCLAIMER OF WARRANTY.
MEDTRONIC, THEREFORE, DISCLAIMS ALL WARRANTIES, BOTH
EXPRESS AND IMPLIED, WITH RESPECT TO THE PRODUCT.
MEDTRONIC SHALL NOT BE LIABLE FOR ANY INCIDENTAL OR
CONSEQUENTIAL DAMAGES CAUSED BY ANY USE, DEFECT OR
FAILURE OF THE PRODUCT, WHETHER THE CLAIM IS BASED ON
WARRANTY, CONTRACT, TORT, OR OTHERWISE.
The exclusions and limitations set out above are not intended to, and
should not be construed so as to, contravene mandatory provisions of
10 Instructions for Use English
Page 13

applicable law. If any part or term of this Disclaimer of Warranty is held by
any court of competent jurisdiction to be illegal, unenforceable, or in
conflict with applicable law, the validity of the remaining portion of the
Disclaimer of Warranty shall not be affected, and all rights and obligations
shall be construed and enforced as if this Disclaimer of Warranty did not
contain the particular part or term held to be invalid.
Instructions for Use English 11
Page 14

1. Indication
À utiliser pour identifier la présence d'héparine à l'aide du temps de
coagulation activée.
Pour utilisation diagnostique in vitro.
Attention : En raison de la nature unique de ce produit, il faut veiller à ne
pas transférer l'héparinase accidentellement du canal "HR HTC" vers le
canal "HR" de la cartouche. Voir section 8 et section 10 pour plus de
détails.
2. Résumé
La cartouche de test héparinase valeurs élevées, ou HR HTC, de
Medtronic est une version modifiée de la cartouche pour temps de
coagulation activée valeurs élevées (HR ACT), destinée aux
chronomètres de coagulation automatisés de Medtronic. Le test de temps
de coagulation activée a initialement été décrit par Hattersley en 19669.
Ce test et ses variantes sont largement utilisés pour contrôler l'effet
anticoagulant de l'héparine
échantillon de sang total fraîchement prélevé, tout comme la cartouche
HR ACT. La différence est que l'un des canaux de la cartouche contient
une héparinase d'origine bactérienne purifiée (HR HTC). L'héparinase
détruit l'héparine présente dans l'échantillon de sang, de manière rapide
et spécifique
6 unités/ml d'héparine. Le canal d'héparinase génère un temps de
coagulation reflétant le temps de coagulation sans héparine de référence
de l'échantillon, bien que ce dernier contienne de l'héparine. L'autre canal
de la cartouche est un HR ACT standard et le temps de coagulation
obtenu est celui du temps de coagulation activée avec héparine de
l'échantillon. L'utilisation de cette cartouche permet : 1) la vérification de la
présence d'héparine avant une intervention chirurgicale, 2) l'évaluation de
l'effet du pontage sur le temps de coagulation activée de référence, 3) la
confirmation de l'antagonisation de l'héparine suite à l'administration de
protamine, 4) l'identification du "rebond d'héparine" postchirurgical et
5) l'identification de la présence d'héparine chez les patients ayant perdu
beaucoup de sang après une intervention chirurgicale. Un contrôle
HTC CLOTtrac™ est disponible pour vérifier que la cartouche fonctionne
conformément aux spécifications.
1,6,10,16
3,4,7,8,13,14
. La cartouche HR HTC utilise un
. La quantité d'héparinase présente élimine rapidement
3. Principes
Le test de temps de coagulation activée mesure le temps de coagulation
du sang total fraîchement prélevé, activée par contact avec la surface. La
procédure originale d'Hattersley utilisait de la terre de diatomées en tant
qu'agent activant. La terre de diatomées présente différents degrés
d'activation par contact en fonction de sa pureté, de la source du dépôt
ainsi que de la taille et de la forme des particules. Les cartouches de
temps de coagulation activée de Medtronic utilisent du kaolin comme
agent activant. Le kaolin présente des caractéristiques supérieures dans
l'activation par contact de la coagulation sanguine. Les cartouches
HR ACT et HR HTC présentent une sensibilité moindre à l'héparine,
permettant de surveiller des taux élevés d'héparine grâce au test de
temps de coagulation activée.
Le but final du test est la détection de la formation de caillots. Les
chronomètres de coagulation automatisés de Medtronic détectent la
formation d'un caillot en surveillant la vitesse de descente du mécanisme
de piston-drapeau présent dans chaque canal de la cartouche. Le piston
descend rapidement dans du sang non coagulé. Lorsqu'un réseau de
fibrine se forme, la descente du piston est gênée. Cette réduction de la
vitesse de descente est détectée par le système photo-optique qui se
trouve dans le capot de l'instrument. La formation de caillots est indiquée
12 Mode d’emploi Français
Page 15

par un signal sonore et le chronomètre de coagulation s'arrête. Les
instruments peuvent réaliser 2 tests simultanés grâce à la cartouche à
2 canaux. Les temps de coagulation de chaque canal sont affichés, en
secondes, à la fin du test. Avec la cartouche HR HTC, l'instrument affiche
2 résultats, l'un pour l'échantillon avec l'héparinase et l'autre pour
l'échantillon sans héparinase. L'écran du panneau avant peut être utilisé
pour faire alterner les temps de coagulation de chaque canal, ou la
moyenne et la différence entre les deux canaux. Lorsque la cartouche
HR HTC est utilisée, la moyenne relevée a peu de signification ;
cependant, la différence entre les deux résultats correspond au
prolongement du temps de coagulation en raison de la présence
d'héparine dans l'échantillon.
4. Réactifs
La chambre à réactifs de chaque cartouche contient 0,1 ml de
tampon HEPES (acide hydroxyéthyl-pipérazine éthane sulfonique), du
kaolin, du chlorure de calcium et de l'azoture de sodium comme agent
bactériostatique. Le canal étiqueté "HR HTC" contient de l'héparinase
lyophilisée hautement purifiée avec des agents stabilisants et de l'azoture
de sodium comme agent bactériostatique.
La cartouche HR HTC peut être préchauffée pendant un maximum de
2 heures. Une fois l'échantillon introduit dans la cartouche préchauffée, le
test doit être lancé immédiatement.
5. Stockage
La cartouche HR HTC doit être stockée dans un environnement stable,
soit entre 2 °C et 10 °C (36 °F et 50 °F), soit entre 10 °C et 25 °C
(50 °F et 77 °F). Les cartouches sont conditionnées dans des plateaux
hermétiquement fermés de 2 cartouches. Les cartouches sont stables
pendant la période indiquée sur l'étiquette du plateau. Ne pas utiliser les
cartouches après la date de péremption. Ne pas utiliser si la cartouche est
décolorée, fissurée ou abîmée ou si le réactif semble s’être évaporé ou
avoir été contaminé.
Une fois le couvercle du plateau ouvert, les cartouches sont stables
pendant 24 heures au réfrigérateur.
Remarque : Ne pas utiliser en cas de preuve de la congélation des
cartouches.
6. Instrument
La cartouche HR HTC est spécifiquement conçue pour être utilisée dans
les chronomètres de coagulation automatisés de Medtronic. Consulter le
manuel d'utilisation de l'instrument pour les instructions.
Pour garantir les bonnes performances de l'instrument, il est important de
nettoyer l'instrument au moins tous les 30 jours, ou plus souvent si
nécessaire.
Remarque : En présence de sang sur le capot de l'organe de commande,
nettoyer l'instrument aussi vite que possible. Un kit de nettoyage de
l'organe de commande (référence catalogue 303-58) est fourni avec
chaque instrument. Utiliser le matériel fourni dans chaque kit de nettoyage
pour procéder au nettoyage. Se reporter à la notice accompagnant le kit
de nettoyage pour plus de détails.
7. Prélèvement et préparation d’échantillons
La manipulation incorrecte d'échantillons peut entraîner des résultats de
test de coagulation erronés ; les échantillons doivent donc être recueillis
avec soin et les techniques de manipulation doivent demeurer régulières.
Mode d’emploi Français 13
Page 16
Si le sang est obtenu par ponction veineuse, la ponction veineuse doit
1
2
être propre. Jeter les premiers millilitres de sang afin d’éviter la
contamination du sang avec de la thrombokinase tissulaire.
Remarque : Ne pas prélever de sang à partir de cathéters pré-héparinés
ou d’autres lignes avec anticoagulant sans un rinçage rigoureux.
Lors du test de sang total fraîchement prélevé, transférer immédiatement
l'échantillon vers la cartouche et commencer le test.
8. Mode d'emploi
Ce produit ne doit être utilisé que par des personnes spécialisées.
Matériels fournis :
■
Cartouche de test héparinase valeurs élevées (HR HTC), référence
catalogue 402-07
Matériels nécessaires, non fournis
■
Chronomètre de coagulation automatisé de Medtronic
■
Seringue en plastique avec aiguille (calibre 18 ou 19 de préférence)
Figure 1. Remplissage de la cartouche HR HTC
1. Échantillon (vue latérale)
2. Échantillon (vue de dessus)
Pour une utilisation avec l'instrument ACT Plus™, procéder comme suit :
1. Dans le Menu principal, sélectionner "Type de cartouche" et appuyer
sur la touche jusqu'à ce que "HTC" apparaisse. Appuyer sur "Entrée"
pour confirmer la sélection.
Remarque : Les numéros de lots et la date de péremption des
cartouches et des contrôles doivent être saisis avant d'effectuer un
test.
2. À partir du Menu principal, saisir les numéros d'"ID patient" et
d'"ID utilisateur" Appuyer sur "Entrée" pour confirmer.
3. Préchauffer la cartouche pendant 3 à 5 minutes avant de prélever
l'échantillon.
4. Taper légèrement sur la cartouche pour remettre le réactif en
suspension.
5. Placer 0,4 ml d'échantillon dans chaque chambre.
Remarque : Toujours procéder au remplissage du canal HR avant de
remplir le canal HR HTC afin d'éviter toute contamination du canal HR
par l'héparinase.
14 Mode d’emploi Français
Page 17

6. Insérer la cartouche dans l'instrument ACT Plus et fermer le bloc
thermique pour démarrer le test.
7. Lorsque la formation de caillots est détectée, une sonnerie retentit, le
bloc thermique s'ouvre et les résultats sont affichés.
Une fois le test terminé, jeter la cartouche, la seringue et l’aiguille
dans un conteneur pour objets contaminés approuvé.
9. Résultats
La réponse du temps de coagulation activée à l’héparine varie
considérablement d’un individu à l’autre12. Divers médicaments affectent
le temps de coagulation activée, notamment les médicaments qui inhibent
l'activation des plaquettes15. Un certain nombre d’autres facteurs peuvent
affecter la réponse du temps de coagulation activée à l’héparine d’un
individu (par exemple, les niveaux de l’antithrombine III, la teneur de
l’héparine, les déficiences du facteur de coagulation, l’activation de
l’échantillon, les coagulopathies de consommation, la dilution excessive
de l’échantillon et la température de l’échantillon). Ces facteurs doivent
être pris en compte lors de l'interprétation des résultats du test de temps
de coagulation activée
L'héparinase dans le canal HR HTC de la cartouche est hautement
spécifique à l'héparine. L'héparinase présente est suffisante pour garantir
l'élimination rapide de 6 unités/ml d'héparine de l'échantillon et le retour à
une condition de référence ou non héparinée. Le temps de référence peut
être ou ne pas être au niveau ou proche de la plage normale. Si la
référence n'est pas dans la plage normale dans le canal HR HTC, cela
indique qu'une condition autre que la présence d'héparine est
responsable du prolongement du temps de coagulation de référence.
Exemple d'interprétation des résultats HR HTC :
C1 C2 Interprétation
120 120 Patient à la référence, aucune présence
120 260 Présence d'héparine dans le sang du
260 260 Coagulopathie sous-jacente du patient sans
260 360 Présence d'héparine dans le sang du patient
60 200 Présence d'héparine dans le sang du patient
2,5,11
.
d'héparine dans l'échantillon.
patient. Prolongement uniquement dû à l'effet de l'héparine.
lien avec l'héparine.
et coagulopathie sous-jacente (probablement hémodilution).
et système de coagulation activé.
10. Limites de la procédure
Respecter les conditions suivantes pour obtenir des temps de coagulation
activée précis et cohérents avec la cartouche HR HTC :
■
La température du bloc thermique de l'instrument et celle de la
cartouche doivent être de 37 °C ± 0,5 °C (98,6 °F ± 0,9 °F). La
cartouche atteint cette température après 3 à 5 minutes passées dans
le bloc thermique de l'instrument.
■
L'activateur kaolin doit être complètement remis en suspension.
■
Le sang doit être exempt de thrombokinase tissulaire. Effectuer le test
aussi rapidement que possible après le prélèvement de l'échantillon
de sang.
■
Le diagnostic et la médication du patient doivent être notés. Les
médications peuvent modifier les temps de coagulation. Les
échantillons qui donnent des valeurs anormales inexpliquées doivent
faire l'objet d'un nouveau prélèvement et d'un nouveau test. Si les
Mode d’emploi Français 15
Page 18

résultats demeurent anormaux sans aucune cause apparente, citrater
un échantillon et l’envoyer au laboratoire clinique pour une analyse
spéciale de la coagulation.
■
Pour une précision optimale, toutes les variables techniques doivent
être maintenues constantes d’un test à l’autre.
■
Lorsque l'échantillon est placé dans la cartouche, le test doit être
effectué aussi rapidement que possible. L'élimination de l'héparine de
l'échantillon se produit rapidement. L'activation par contact se produit
dans la cartouche lorsque l'échantillon ne contient pas d'héparine.
Cela résultera en des temps de coagulation plus courts à mesure que
l'activation de l'échantillon se poursuit.
■
Les méthodologies utilisées dans la chirurgie de pontage
cardiopulmonaire changent en permanence, de même que les
caractéristiques de la population de patients. Les conditions
susceptibles d'influencer les résultats du test de temps de coagulation
activée incluent notamment :
■
sensibilité du patient à l'héparine
■
dilution des facteurs de coagulation par le circuit extracorporel
■
utilisation de produits sanguins citratés
■
utilisation de médicaments antiplaquettaires
■
hypothermie
■
taux de calcium fluctuants
■
changement dans la fonction ou la numération plaquettaire
■
coagulopathies inconnues
Une dilution sanguine excessive au cours du pontage, fréquemment
due à la volonté de limiter l'utilisation de produits sanguins
hétérologues, peut conduire à une hémorragie postopératoire. Dans
les cas les plus graves, la dilution est si importante que la coagulation,
telle que mesurée par le temps de coagulation activée, n'a pas lieu.
L'adéquation des facteurs de coagulation plasmatique ne peut pas
être déterminée par la corrélation entre l'ampleur de la dilution et
l'hématocrite du patient. Souvent, des cellules lavées ont été
administrées au patient sans compensation pour la perte de plasma.
Si la coagulation de la cartouche HR HTC échoue dans le canal
héparinase (canal 1), suite à la réversion de l'héparine du patient par
la protamine, une coagulopathie dilutionnelle est fort probable.
Avertissement : En raison de sa formulation, la cartouche HR HTC
ne doit pas être utilisée pour surveiller l'anticoagulation régionale
obtenue par perfusion de citrate.
Attention : Il faut particulièrement veiller à ce que l'héparinase dans
le canal HR HTC ne soit pas transférée par inadvertance vers
l'échantillon dans le canal HR de la cartouche. Si cela se produisait, le
temps de coagulation avec héparine dans le canal "HR" ne serait plus
représentatif de la quantité d'héparine dans l'échantillon, mais
indiquerait une quantité inférieure d'héparine, en fonction de la
quantité d'héparinase transférée. Pour cette raison et afin de réduire
la possibilité de transfert d'héparinase, il est fortement suggéré que le
canal "HR" soit rempli en premier.
Pour les précautions et les limites de l'instrument, consulter le manuel
de l'utilisateur.
11. Valeurs prévues
Le canal d'héparinase fournit de manière efficace un temps de
coagulation activée de référence sur du sang total fraîchement prélevé
hépariné. Au cours du pontage, la valeur du temps de coagulation activée
de référence peut augmenter, reflétant l'hémodilution du sang du patient.
Le temps de coagulation de référence est corrélé avec la dilution des
facteurs de coagulation plasmatique qui n'est pas nécessairement en
16 Mode d’emploi Français
Page 19

corrélation avec l'hématocrite du patient. Les globules rouges ajoutés à un
patient à partir d'un récupérateur de sang ne compensent pas les facteurs
de coagulation du plasma perdu. Si le prolongement du temps de
coagulation activée de référence se maintient, une coagulopathie
dilutionnelle (facteurs de coagulation insuffisants) peut se produire et une
hémorragie postopératoire peut être observée. La cartouche HR HTC
peut surveiller le développement de cette situation et permettre de
prendre les mesures pour y remédier avant qu'une dilution grave des
facteurs de coagulation ne se produise.
12. Caractéristiques de performances spécifiques
Les cartouches de temps de coagulation activée, dans la plage de
coagulation de 0 à 600 secondes, ne diffèrent généralement pas de plus
de 12% entre les échantillons dupliqués pour un individu donné. À des
taux d'héparine élevés et des temps de coagulation de plus de
600 secondes, un temps de coagulation activée n’est généralement pas
considéré comme suffisamment fiable pour déterminer les taux
d’héparine.
La cartouche HR HTC est formulée pour produire un HR ACT normal
dans le canal étiqueté "HR", qui correspond étroitement aux réponses
dont Bull, et al (1975) ont initialement fait état. L'activateur kaolin dans
chaque lot de cartouches a été étalonné de manière à réduire les
variations d'activité entre les lots à moins de 10%, et à atténuer la dérive à
long terme.
Les performances du canal "de référence" de la cartouche dépendent de
l'activité de l'héparinase dans le canal étiqueté "HR HTC". L'héparinase a
été purifiée et stabilisée pour éliminer 6 unités/ml d'héparine dans un laps
de temps suffisamment court pour ramener le sang hépariné à un temps
de coagulation de référence. La stabilité de l'héparinase est garantie en
maintenant les cartouches à température constante. Les plages
auxquelles les cartouches peuvent être stockées sont comprises soit
entre 2 °C et 10 °C (36 °F et 50 °F), soit entre 10 °C et 25 °C
(50 °F et 77 °F). Les performances des cartouches peuvent diminuer si le
produit n'est pas stocké dans un environnement stable. Les passages
répétés du produit des conditions réfrigérées aux conditions ambiantes et
inversement ne sont pas recommandés.
13. Contrôle de qualité
Deux niveaux de contrôles doivent être appliqués pour le test HTC afin de
garantir les performances adéquates de l'instrument et des cartouches.
Les résultats doivent être dans les plages spécifiées par le fabricant ou
celles déterminées par l'utilisateur.
Les contrôles pour le test héparinase valeurs élevées comprennent : le
contrôle de coagulation HR CLOTtrac™ (référence catalogue 550-07) et
le contrôle HTC CLOTtrac (référence catalogue 550-12).
Le contrôle HTC CLOTtrac donne un HR ACT de référence dans le canal
HR HTC et sera sujet à temporisation (>999) dans le canal HR ACT.
Ce contrôle est un contrôle lyophilisé qui contient 6 unités/ml d'héparine.
Les performances du HR HTC sont vérifiées par l'exécution du contrôle
dans une cartouche et l'obtention d'une valeur HR ACT de référence dans
le canal étiqueté "HR HTC" et d'une temporisation (999 secondes) dans le
canal étiqueté "HR". Cela indique que le canal de la cartouche contenant
l'héparinase fonctionne correctement.
14. Références
1. Baugh RF, Deemar KA, Zimmerman JJ. Heparinase in the activated
clotting time assay: Monitoring heparin-independent alterations in
coagulation function. Anesth Analg. 1992;74:201.
Mode d’emploi Français 17
Page 20

2. Bode AP, Eick L. Lysed platelets shorten the activated coagulation
time (ACT) of heparinized blood. Am J Clin Pathol. 1989;91:430.
3. Bull BS, Korpman RA, Huse WM, Briggs BD. Heparin therapy during
extracorporeal circulation. I. Problems inherent in existing heparin
protocols. J Thorac Cardiovasc Surg. 1975;69:674.
4. Bull BS, Huse WM, Brauer FS, Korpman RA. Heparin therapy during
extracorporeal circulation. II. The use of a dose-response curve to
individualize heparin and protamine dosage. J Thorac Cardiovasc
Surg. 1975;69:685.
5. Culliford AT, Gitel SN, Starr N, Thomas ST, Baumann FG, Wessler S,
Spencer FC. Lack of correlation between activated clotting time and
plasma heparin during cardiopulmonary bypass. Ann Surg.
1981;193:105.
6. Dietrich CP, Silva ME, Michelacci YM. Sequential degradation of
heparin in Flavobacterium heparinum. Purification and properties of
five enzymes involved in heparin degradation. J Biol Chem.
1973;248:6408.
7. Effeney DJ, Goldstone J, Chin D, Krupski WC, Ellis RJ. Intraoperative
anticoagulation in cardiovascular surgery. Surgery. 1981;90:1068.
8. Forman WB, Bayer G. A simplified method for monitoring heparin
therapy at the bedside: The activated whole blood clotting time. Am J
Hematol. 1981;11:277.
9. Hattersley PG. Progress report: The activated coagulation time of
whole blood (ACT). Am J Clin Pathol. 1976;66:899.
10. Hutt ED, Kingdon HS. Use of heparinase to eliminate heparin
inhibition in routine coagulation assays. J Lab Clin Med.
1972;79:1027.
11. Kesteven PJ, Pasaoglu I, Williams BT, Savidge GG. Significance of
the whole blood activated clotting time in cardiopulmonary bypass. J
Cardiovasc Surg. 1986;27:85.
12. Mabry CD, Read RC, Thompson BW, Williams GD, White HJ.
Identification of heparin resistance during cardiac and vascular
surgery. Arch Surg. 1979;114:129.
13. Mabry CD, Thompson BW, Read RC. Activated clotting time (ACT)
monitoring of intraoperative heparinization in peripheral vascular
surgery. Am J Surg. 1979;138:894.
14. Mabry CD, Thompson, BW, Read RC, Campbell GS. Activated
clotting time monitoring of intraoperative heparinization: Our
experience and comparison with two techniques. Surgery.
1981;90:889.
15. Moorehead MT, Westengard JC, Bull BS. Platelet involvement in the
activated coagulation time of heparinized blood. Anesth Analg.
1984;63:394.
16. Yang VC, Linhardt RJ, Bernstein H, Cooney CL, Langer R.
Purification and characterization of heparinase from Flavobacterium
heparinum. J Biol Chem. 1985;260:1849.
15. Déni de garantie
LE DÉNI DE GARANTIE SUIVANT S'APPLIQUE AUX
CLIENTS SITUÉS HORS DES ÉTATS-UNIS :
BIEN QUE LA CARTOUCHE DE TEST HÉPARINASE VALEURS
ÉLEVÉES, CI-APRÈS LE "PRODUIT" AIT ÉTÉ SOIGNEUSEMENT
CONÇUE, FABRIQUÉE ET TESTÉE AVANT SA MISE EN VENTE, LE
PRODUIT PEUT, POUR DIVERSES RAISONS, CONNAÎTRE DES
DÉFAILLANCES. LES AVERTISSEMENTS FIGURANT SUR LES
ÉTIQUETTES DU PRODUIT CONTIENNENT DES INFORMATIONS
18 Mode d’emploi Français
Page 21

PLUS DÉTAILLÉES ET SONT CONSIDÉRÉS COMME FAISANT
PARTIE INTÉGRANTE DU PRÉSENT DÉNI DE GARANTIE. EN
CONSÉQUENCE, MEDTRONIC DÉCLINE TOUTE RESPONSABILITÉ,
EXPLICITE OU IMPLICITE, RELATIVE AU PRODUIT. MEDTRONIC NE
SERA PAS TENU RESPONSABLE DE TOUS DOMMAGES FORTUITS
OU INDIRECTS QUI SERAIENT PROVOQUÉS PAR TOUS USAGES,
DÉFECTUOSITÉS OU DÉFAILLANCES DU PRODUIT ET CE, QUE LA
PLAINTE SOIT FONDÉE SUR UNE GARANTIE, UNE
RESPONSABILITÉ CONTRACTUELLE, DÉLICTUEUSE OU AUTRE.
Les exclusions et les limitations de garantie mentionnées ci-dessus ne
sont pas et ne doivent pas être interprétées comme contraires aux
dispositions obligatoires des lois applicables. Si une partie ou une
disposition du présent déni de garantie devait être considérée illégale,
non applicable ou contraire à la loi en vigueur par un tribunal compétent,
la validité des autres dispositions du présent déni de garantie n'en sera
pas affectée et tous les autres droits et obligations seront interprétés et
appliqués, sans tenir compte de la partie ou de la disposition considérée
comme non valide.
Mode d’emploi Français 19
Page 22

1. Vorgesehene Verwendung
Zur Verwendung bei der Bestimmung des Vorhandenseins von Heparin
mithilfe einer aktivierten Gerinnungszeit.
Zur In-vitro-Diagnostik.
Vorsicht: Aufgrund der besonderen Eigenschaften dieses Produkts ist
darauf zu achten, dass die Heparinase nicht versehentlich von dem
„HR HTC“-Kanal in den „HR“-Kanal der Kartusche verschleppt wird.
Weitere Informationen finden Sie unter Abschnitt 8 und Abschnitt 10.
2. Kurzbeschreibung
Bei der Medtronic High Range Heparinase-Testkartusche, oder HR HTC,
handelt es sich um eine Abwandlung der High Range Kartusche zur
Bestimmung der aktivierten Gerinnungszeit (HR ACT) für die
automatischen Gerinnungszeitmesser von Medtronic. Die Bestimmung
der aktivierten Gerinnungszeit wurde erstmals 1966 von Hattersley
beschrieben.9 Der Test und seine Varianten werden seitdem in großem
Umfang zur Überwachung der gerinnungshemmenden Wirkung von
Heparin eingesetzt.
abgenommenen Vollblutprobe eingesetzt, genau wie die HR ACTKartusche. Der Unterschied gegenüber dieser Kartusche besteht darin,
dass ein Kanal eine aufgereinigte Heparinase bakteriellen Ursprungs
enthält (HR HTC). Die Heparinase zerstört rasch und spezifisch das in der
Blutprobe vorliegende Heparin.
Heparinase werden rasch 6 Einheiten/ml an Heparin entfernt. Somit wird
in dem Heparinase-Kanal eine Gerinnungszeit erzielt, die der nicht
heparinisierten Referenzgerinnungszeit der Probe entspricht, wenngleich
die Probe Heparin enthält. Bei dem anderen Kanal der Kartusche handelt
es sich um einen standardmäßigen HR ACT-Kanal, und die damit erzielte
Gerinnungszeit entspricht der heparinisierten aktivierten Gerinnungszeit
der Probe. Die Verwendung dieser Kartusche ermöglicht: 1) den
Nachweis des präoperativen Vorliegens von Heparin; 2) die Beurteilung
der Wirkung eines Bypasses auf die Referenzzeit für die aktivierte
Gerinnung; 3) die Bestätigung der Umkehrung der Heparinwirkung nach
Protamin-Gabe; 4) die Identifikation eines postoperativen „HeparinRebounds“ und 5) die Bestimmung des Vorhandenseins von Heparin bei
Patienten mit starken postoperativen Blutungen. Zur Verifikation der
spezifikationsgemäßen Funktion der Kartusche ist eine CLOTtrac™ HTC
Kontrolle erhältlich.
3,4,7,8,13,14
Die HR HTC wird mit einer frisch
1,6,10,16
Durch die vorliegende Menge an
3. Anwendungsprinzip
Bei der Bestimmung der aktivierten Gerinnungszeit wird die
Gerinnungszeit von frisch abgenommenem Vollblut gemessen, das durch
Oberflächenkontakt aktiviert wird. Im Originalverfahren von Hattersley
wurde Diatomeenerde als Aktivator verwendet. Diatomeenerde zeigt
allerdings eine unterschiedlich ausgeprägte Kontaktaktivierung, jeweils
abhängig von ihrer Reinheit, der Quelle der Ablagerung sowie der Größe
und Form der Partikel. Die Medtronic Kartuschen zur Bestimmung der
aktivierten Gerinnungszeit verwenden Kaolin als Aktivator. Kaolin zeigt
überlegene Eigenschaften bei der Kontaktaktivierung im Rahmen der
Blutgerinnung. Die HR ACT und die HR HTC weisen eine herabgesetzte
Empfindlichkeit gegenüber Heparin auf, sodass mit dem Test zur
Bestimmung der aktivierten Gerinnungszeit eine Überwachung hoher
Heparinspiegel möglich ist.
Der Endpunkt des Test ist erreicht, sobald eine Gerinnungsbildung
erkannt wird. Die automatischen Gerinnungszeitmessgeräte von
Medtronic erkennen die Gerinnungsbildung durch die Überwachung der
Sinkgeschwindigkeit des Kolbens bzw. des Fähnchenmechanismus in
den einzelnen Kartuschenkanälen. Bei nicht geronnenem Blut senkt sich
20 Gebrauchsanweisung Deutsch
Page 23

der Kolben rasch. Bei Bildung eines Fibrinnetzes sinkt der Kolben mit
geringerer Geschwindigkeit. Diese Abnahme der Sinkgeschwindigkeit
wird von dem fotooptischen System in dem Gehäuse des Geräts
registriert. Die Gerinnungsbildung wird durch ein akustisches Signal
angezeigt, und der Gerinnungszeitmesser wird angehalten. Mit der
Zweikanalkartusche können die Geräte gleichzeitig zwei Tests
durchführen. Nach Abschluss des Tests werden die Gerinnungszeiten der
einzelnen Kanäle in Sekunden angezeigt. Bei der HR HTC zeigt das
Gerät zwei Ergebnisse an, eines für die Probe mit Heparinase und eines
für die Probe ohne Heparinase. Über die Anzeige an der Vorderseite kann
zwischen den Gerinnungszeiten für die einzelnen Kanäle oder dem
Mittelwert und dem Unterschied zwischen den zwei Kanälen gewechselt
werden. Bei Verwendung der HR HTC hat der gemittelte Messwert nur
geringe Bedeutung. Der Unterschied zwischen den zwei Ergebnissen
hingegen stellt die Verlängerung der Gerinnungszeit infolge des
Vorhandenseins von Heparin in der Probe dar.
4. Reagenzien
Jede Kartuschenreagenzkammer enthält 0,1 ml HydroxyethylpiperazinEthansulfonsäure(HEPES)-Puffer, Kaolin, Calciumchlorid und Natriumazid
als Bakteriostatikum. Der mit „HR HTC“ gekennzeichnete Kanal enthält
lyophilisierte, hochaufgereinigte Heparinase mit Stabilisierungsmitteln und
Natriumazid als Bakteriostatikum.
Die HR HTC-Kartusche kann für maximal 2 Stunden vorgewärmt werden.
Sobald die Probe in die vorgewärmte Kartusche eingebracht wurde, muss
sofort mit dem Test begonnen werden.
5. Lagerung
Die HR HTC muss in einer stabilen Umgebung gelagert werden, entweder
bei 2 °C bis 10 °C (36 °F bis 50 °F) oder bei 10 °C bis 25 °C
(50 °F bis 77 °F). Die Kartuschen sind in versiegelten Schalen zu je
2 Kartuschen verpackt. Die Kartuschen sind für den auf der Schale
angegebenen Zeitraum (siehe Etikett) stabil. Nach Ablauf des
Verfallsdatums („Zu verwenden bis einschließlich“) dürfen die Kartuschen
nicht mehr verwendet werden. Kartuschen, die Verfärbungen, Risse oder
Verformungen aufweisen oder deren Reagenz verdampft oder
verunreinigt zu sein scheint, dürfen nicht verwendet werden.
Nach dem Öffnen der Folie auf der Schale sind die Kartuschen bei
Kühlschranktemperatur 24 Stunden stabil.
Hinweis: Nicht verwenden, wenn Anzeichen dafür vorliegen, dass die
Kartuschen eingefroren war.
6. Gerät
Die HR HTC wurde speziell für die Verwendung in automatischen
Gerinnungszeitmessgeräten von Medtronic entwickelt. Anweisungen sind
der Bedienungsanleitung des Geräts zu entnehmen.
Um eine ordnungsgemäße Geräteleistung sicherzustellen, muss das
Gerät mindestens alle 30 Tage, bei Bedarf auch öfters, gereinigt werden.
Hinweis: Wenn Blut in die Abdeckung des Betätigungselements gelangt,
ist das Gerät so bald wie möglich zu reinigen. Ein Reinigungskit für das
Betätigungselement (Katalognummer 303-58) wird mit jedem Gerät
geliefert. Verwenden Sie die im Reinigungskit enthaltenen Materialien, um
das Reinigungsverfahren durchzuführen. Ausführliche Informationen
finden Sie in der dem Reinigungskit beiliegenden Packungsbeilage.
7. Probennahme und -vorbereitung
Eine unsachgemäße Handhabung der Proben kann zu fehlerhaften
Testergebnissen bei der Bestimmung der Gerinnungsbildung führen. Aus
diesem Grund muss die Probenabnahme mit Sorgfalt erfolgen und es
Gebrauchsanweisung Deutsch 21
Page 24

müssen konsistente Techniken bei der Handhabung der Proben zur
1
2
Anwendung gelangen.
Bei einer Blutabnahme per Venenpunktion muss sauber gearbeitet
werden. Die ersten paar Milliliter Blut sollten verworfen werden, um eine
Kontamination der Probe mit Gewebethromboplastin auszuschließen.
Hinweis: Das Blut darf nicht aus heparinisierten Verweilkathetern oder
anderen gerinnungshemmend präparierten Zugängen abgenommen
werden, ohne den Zugang vorher gründlich zu spülen.
Bei der Bestimmung in frisch abgenommenem Vollblut muss die Probe
sofort in die Kartusche überführt und der Test begonnen werden.
8. Gebrauchsanweisung
Dieses Produkt darf nur von entsprechend geschulten Personen
verwendet werden.
Im Lieferumfang enthaltene Materialien:
■
High Range Heparinase-Testkartusche (HR HTC),
Katalognummer 402-07
Erforderliche Materialien, nicht im Lieferumfang enthalten:
■
automatisches Gerinnungszeitmessgerät von Medtronic
■
Kunststoffspritze mit Kanüle (vorzugsweise 18 oder 19 Gauge)
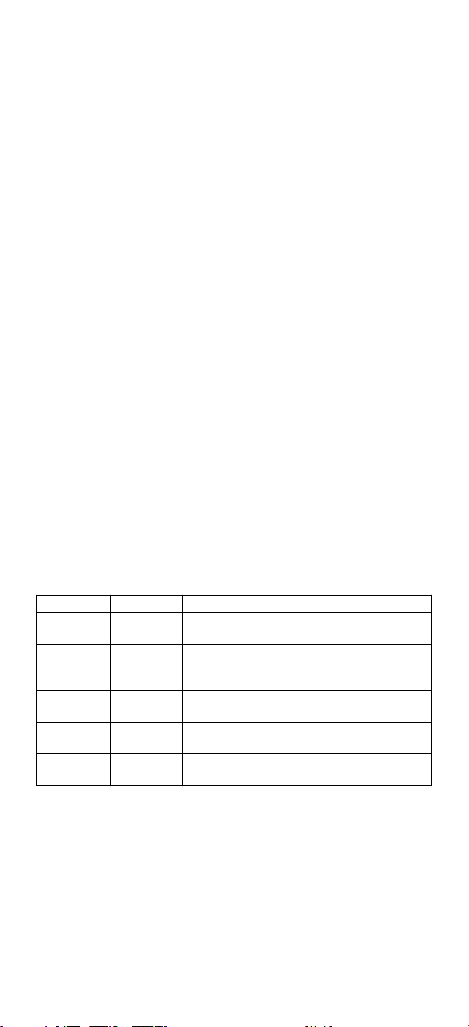
Abbildung 1. Befüllen der HR HTC-Kartusche
1. Probe (Seitenansicht)
2. Probe (Draufsicht)
Bei Verwendung mit dem ACT Plus™ Gerät gehen Sie bitte wie folgt vor:
1. Wählen Sie im Hauptmenü „Kartuschentyp“ und drücken Sie die
Taste, bis „HTC“ angezeigt wird. Drücken Sie zur Bestätigung die
Taste „Eingabe“.
Hinweis: Die Chargennummern und Verfallsdaten („Zu verwenden
bis einschließlich“) der Kartuschen und Kontrollen müssen vor
Testdurchführung eingegeben werden.
2. Geben Sie im Hauptmenü die „Patienten-ID“ und die „BenutzerID“ ein. Drücken Sie zur Bestätigung die Taste „Eingabe“.
3. Wärmen Sie die Kartusche vor Abnahme der Probe für den Test
3 bis 5 Minuten lang vor.
4. Klopfen Sie gegen die Kartusche, um das Reagenz zu
resuspendieren.
22 Gebrauchsanweisung Deutsch
Page 25
5. Füllen Sie jede Kammer mit einer Probenmenge von 0,4 ml.
Hinweis: Befüllen Sie immer zuerst den HR-Kanal und dann den
HR HTC-Kanal, sodass sichergestellt ist, dass der HR-Kanal nicht mit
Heparinase verunreinigt wird.
6. Setzen Sie die Kartusche in das ACT Plus Gerät ein und schließen
Sie den Heizblock des Betätigungselements, um den Test zu starten.
7. Die Gerinnungsbildung wird durch einen akustischen Ton gemeldet,
der Heizblock des Betätigungselements öffnet sich und die
Ergebnisse werden angezeigt.
Entsorgen Sie die Kartusche, Spritze und Kanüle nach Abschluss des
Tests in für biologische Gefahrenstoffe zugelassene
Entsorgungsbehälter.
9. Ergebnisse
Die Reaktion der aktivierten Gerinnungszeit auf Heparin variiert je nach
Patient beträchtlich.12 Verschiedene Arzneimittel wirken sich auf die
aktivierte Gerinnungszeit aus, insbesondere Arzneimittel, die die
Thrombozytenaktivierung hemmen.15 Eine Reihe weiterer Faktoren kann
die patientenspezifische Reaktion der aktivierten Gerinnungszeit auf
Heparin beeinflussen, z. B. die Antithrombin-III-Spiegel, die
Heparinwirksamkeit, ein Mangel an Gerinnungsfaktoren, die
Probenaktivierung, Verbrauchskoagulopathien, eine starke
Probenverdünnung und die Temperatur der Probe. Diese Faktoren sollten
bei der Auswertung der Ergebnisse von Tests zur Bestimmung der
aktivierten Gerinnungszeit berücksichtigt werden.
Die Heparinase in dem HR HTC-Kanal der Kartusche ist hochspezifisch
für Heparin. Die vorhandene Heparinase-Menge ist ausreichend, um
sicherzustellen, dass rasch 6 Einheiten/ml an Heparin aus der Probe
entfernt werden, sodass diese in einen Referenz- oder nicht
heparinisierten Zustand zurückgeführt wird. Die Referenzzeit kann
unmittelbar oder mittelbar dem Normalbereich entsprechen, muss dies
jedoch nicht. Wenn der Referenzwert nicht innerhalb des Normalbereichs
für den HR HTC-Kanal liegt, deutet dies darauf hin, dass ein anderer
Umstand als das Vorhandensein von Heparin für die Verlängerung der
Referenzgerinnungszeit verantwortlich ist.
Auswertung der HR HTC-Ergebnisse – Beispiel:
Kanal 1 Kanal 2 Auswertung
120 120 Referenzwert des Patienten; Probe enthält
120 260 Blut des Patienten enthält Heparin; Verlän-
260 260 Patient hat eine primäre Koagulopathie; kein
260 360 Patient hat Heparin im Blut und eine primäre
60 200 Patient hat Heparin im Blut und das Gerin-
kein Heparin.
gerung geht allein auf die Heparin-Wirkung
zurück.
Bezug zu Heparin.
Koagulopathie (vermutlich Hämodilution).
nungssystem ist aktiviert.
2,5,11
10. Einschränkungen des Verfahrens
Um mit der HR HTC akkurate und konsistente Gerinnungszeiten zu
erzielen, müssen die nachstehenden Bedingungen eingehalten werden:
■
Die Temperatur des Heizblocks des Geräts und der Kartusche sollte
37 °C ± 0,5 °C (98,6 °F ± 0,9 °F) betragen. Im Heizblock des Geräts
wird die Kartusche binnen 3 bis 5 Minuten auf die erforderliche
Temperatur gebracht.
■
Der Kaolin-Aktivator muss gründlich resuspendiert werden.
Gebrauchsanweisung Deutsch 23
Page 26

■
Das Blut darf kein Gewebethromboplastin erhalten. Der Test muss so
schnell wie möglich nach Abnahme der Blutprobe durchgeführt
werden.
■
Die Diagnose des Patienten und die zur Behandlung eingesetzten
Medikamente müssen beachtet werden. Arzneimittel können die
Gerinnungszeiten verändern. Im Falle von Proben mit auffälligen,
nicht erklärbaren Werten ist erneut Blut abzunehmen und zu testen.
Werden erneut auffällige Ergebnisse ohne ersichtlich Ursache erzielt,
sollte eine zitrierte Probe für eine spezielle Gerinnungsuntersuchung
an ein klinisches Labor verschickt werden.
■
Zur Optimierung der Präzision sollten alle Verfahrensvariablen von
Test zu Test konstant gehalten werden.
■
Nach dem Einbringen der Probe in die Kartusche muss der Test so
schnell wie möglich durchgeführt werden. Die Entfernung des
Heparins aus der Probe geschieht rasch. Zur Kontaktaktivierung
innerhalb der Kartusche kommt es, wenn die Probe kein Heparin
enthält. Dies führt durch die fortschreitende Aktivierung der Probe zu
kürzeren Gerinnungszeiten.
■
Die in der kardiopulmonalen Bypasschirurgie verwendeten Verfahren
ändern sich ebenso stetig wie die Merkmale der Patientenpopulation.
Zu den Umständen, die die Ergebnisse der Tests zur Bestimmung der
aktivierten Gerinnungszeit beeinflussen können, zählen unter
anderem:
■
Heparinempfindlichkeit des Patienten
■
Verdünnung der Gerinnungsfaktoren durch den extrakorporalen
Blutkreislauf
■
Anwendung von zitrierten Blutprodukten
■
Anwendung von Thrombozytenhemmern
■
Hypothermie
■
schwankende Calciumspiegel
■
Veränderung der Thrombozytenfunktion oder -zahl
■
nicht bekannte Koagulopathien
Eine übermäßige Blutverdünnung während eines Bypasses, häufig
mit der Bestrebung, die Anwendung von heterologen Blutprodukten zu
beschränken, kann zu postoperativen Blutungen führen. In schweren
Fällen kann die Verdünnung dabei so stark sein, dass eine
Gerinnung, wie sie mit der aktivierten Gerinnungszeit gemessen wird,
nicht mehr eintritt. Ob ausreichend Plasmagerinnungsfaktoren
vorliegen, kann nicht durch Korrelation der Verdünnungsgröße mit
dem Hämatokrit des Patienten bestimmt werden. Häufig wurden den
Patienten gewaschene Zellen verabreicht, ohne dass ein Ausgleich
für das verlorene Plasma erfolgte. Falls es im Heparinase-Kanal der
HR HTC (Kanal Nummer 1) nach der Umkehrung der Wirkung des
patienteneigenen Heparins durch Protamin nicht zu einer Gerinnung
kommt, ist die Wahrscheinlichkeit einer Verdünnungskoagulopathie
groß.
Warnung: Aufgrund der Formulierung der HR HTC sollte diese nicht
zur Überwachung einer regionalen Antikoagulation nach Zitratinfusion
verwendet werden.
Vorsicht: Es muss sorgfältig darauf geachtet werden, dass keine
Heparinase aus dem HR HTC-Kanal versehentlich in die Probe in
dem HR-Kanal der Kartusche verschleppt wird. Wenn dies eintritt,
wäre die heparinisierte Gerinnungszeit des „HR“-Kanals nicht länger
repräsentativ für die Heparinmenge der Probe. Vielmehr würde eine
geringere Menge an Heparin angezeigt, abhängig von der Menge an
verschleppter Heparinase. Aus diesem Grund wird unbedingt
empfohlen, zuerst den „HR“-Kanal zu füllen, um so die Möglichkeit
einer Verschleppung von Heparinase auf ein Minimum zu reduzieren.
24 Gebrauchsanweisung Deutsch
Page 27

Die Vorsichtsmaßnahmen und Einschränkungen für das Gerät
entnehmen Sie bitte der Bedienungsanleitung.
11. Zu erwartende Werte
Der Heparinase-Kanal liefert auf wirksame Weise eine Referenzzeit für
die aktivierte Gerinnung aus frisch abgenommenem heparinisiertem
Vollblut. Während eines Bypasses kann der Referenzwert der aktivierten
Gerinnungszeit nach oben abweichen, wodurch eine Hämodilution des
Blut des Patienten angezeigt wird. Die Referenzgerinnungszeit korreliert
mit der Verdünnung der Plasmagerinnungsfaktoren, die wiederum nicht
zwangsläufig mit dem Hämatokrit des Patienten korreliert. Die
Rückübertragung von Erythrozyten, die in einem Cell Saver
zurückgewonnen wurden, stellt keinen Ausgleich für verlorene
Plasmagerinnungsfaktoren dar. Falls die Referenzzeit der aktivierten
Gerinnung weiterhin verlängert ist, kann es zu einer
Verdünnungskoagulopathie (Mangel an Gerinnungsfaktoren) kommen, in
deren Folge sich postoperative Blutungen zeigen können. Mit der
HR HTC kann die Entwicklung dieser Situation überwacht werden, sodass
vor dem Eintreten einer schwerwiegenden Verdünnung der
Gerinnungsfaktoren Abhilfemaßnahmen getroffen werden können.
12. Spezifische Leistungsmerkmale
Kartuschen zur Bestimmung der aktivierten Gerinnungszeit innerhalb
eines Gerinnungszeitbereichs von 0 bis 600 Sekunden weisen bei der
Doppelmessung von Proben einer Person üblicherweise eine Variation
von maximal 12 % auf. Bei hohen Heparinspiegeln und Gerinnungszeiten
von mehr als 600 Sekunden gilt eine aktivierte Gerinnungszeit
grundsätzlich als nicht zuverlässig genug, um für die Bestimmung der
Heparinspiegel herangezogen werden zu können.
Die Formulierung der HR HTC führt in dem mit „HR“ gekennzeichneten
Kanal zu einer normalen HR ACT und entspricht weitgehend den
Reaktionen, die ursprünglich von Bull et al. (1975) berichtet wurden. Die
Kalibrierung des Kaolin-Aktivators in den einzelnen Kartuschenchargen
reduziert die Wirkungsschwankungen zwischen den Chargen auf weniger
als 10 % und die Langzeitabweichung auf ein Minimum.
Die Leistung des „Referenz“-Kanals der Kartusche ist von der Wirkung
der Heparinase in dem mit „HR HTC“ gekennzeichneten Kanal abhängig.
Die Heparinase wurde aufgereinigt und stabilisiert, sodass sie
6 Einheiten/ml an Heparin innerhalb einer Zeitspanne entfernt, die kurz
genug ist, um das heparinisierte Blut zurück auf eine
Referenzgerinnungszeit zu bringen. Die Stabilität der Heparinase wird
durch die Aufbewahrung der Kartuschen bei einer konstanten Temperatur
gewährleistet. Die Bereiche, in denen die Kartuschen gelagert werden
sollten, liegen entweder bei 2 °C bis 10 °C (36 °F bis 50 °F) oder bei
10 °C bis 25 °C (50 °F bis 77 °F). Bei einer Lagerung in nicht konstant
bleibender Umgebung kann die Kartuschenleistung abnehmen. Eine
wiederholte Überführung des Produkts von Kühl- zu
Umgebungsbedingungen oder umgekehrt wird nicht empfohlen.
13. Qualitätskontrolle
Zur Sicherstellung einer adäquaten Leistung des Geräts und der
Kartuschen sollte der HTC-Test mit Kontrollen in zwei
Konzentrationsstufen kontrolliert werden.
Die Ergebnisse sollten innerhalb der vom Hersteller angegebenen oder
vom Anwender bestimmten Bereiche liegen.
Zu den Kontrollen für den High Range Heparinase-Test gehörendie
CLOTtrac™ HR Gerinnungskontrolle (Katalognummer 550-07) und die
CLOTtrac HTC Kontrolle (Katalognummer 550-12).
Gebrauchsanweisung Deutsch 25
Page 28

Die CLOTtrac HTC Kontrolle führt im HR HTC-Kanal zu einem HR ACTReferenzwert und im HR ACT-Kanal zu einer Zeitüberschreitung (> 999).
Bei dieser Kontrolle handelt es sich um eine lyophilisierte Kontrolle mit
6 Einheiten/ml an Heparin. Die Leistung der HR HTC wird durch den
Testlauf der Kontrolle in einer Kartusche verifiziert, wobei in dem mit
„HR HTC“ gekennzeichneten Kanal ein HR ACT-Referenzwert und in dem
mit „HR“ gekennzeichneten Kanal eine Zeitüberschreitung
(999 Sekunden) zu erzielen ist. Dies zeigt die ordnungsgemäße Funktion
des heparinasehaltigen Kanals der Kartusche an.
14. Literatur
1. Baugh RF, Deemar KA, Zimmerman JJ. Heparinase in the activated
clotting time assay: Monitoring heparin-independent alterations in
coagulation function. Anesth Analg. 1992;74:201.
2. Bode AP, Eick L. Lysed platelets shorten the activated coagulation
time (ACT) of heparinized blood. Am J Clin Pathol. 1989;91:430.
3. Bull BS, Korpman RA, Huse WM, Briggs BD. Heparin therapy during
extracorporeal circulation. I. Problems inherent in existing heparin
protocols. J Thorac Cardiovasc Surg. 1975;69:674.
4. Bull BS, Huse WM, Brauer FS, Korpman RA. Heparin therapy during
extracorporeal circulation. II. The use of a dose-response curve to
individualize heparin and protamine dosage. J Thorac Cardiovasc
Surg. 1975;69:685.
5. Culliford AT, Gitel SN, Starr N, Thomas ST, Baumann FG, Wessler S,
Spencer FC. Lack of correlation between activated clotting time and
plasma heparin during cardiopulmonary bypass. Ann Surg.
1981;193:105.
6. Dietrich CP, Silva ME, Michelacci YM. Sequential degradation of
heparin in Flavobacterium heparinum. Purification and properties of
five enzymes involved in heparin degradation. J Biol Chem.
1973;248:6408.
7. Effeney DJ, Goldstone J, Chin D, Krupski WC, Ellis RJ. Intraoperative
anticoagulation in cardiovascular surgery. Surgery. 1981;90:1068.
8. Forman WB, Bayer G. A simplified method for monitoring heparin
therapy at the bedside: The activated whole blood clotting time. Am J
Hematol. 1981;11:277.
9. Hattersley PG. Progress report: The activated coagulation time of
whole blood (ACT). Am J Clin Pathol. 1976;66:899.
10. Hutt ED, Kingdon HS. Use of heparinase to eliminate heparin
inhibition in routine coagulation assays. J Lab Clin Med.
1972;79:1027.
11. Kesteven PJ, Pasaoglu I, Williams BT, Savidge GG. Significance of
the whole blood activated clotting time in cardiopulmonary bypass. J
Cardiovasc Surg. 1986;27:85.
12. Mabry CD, Read RC, Thompson BW, Williams GD, White HJ.
Identification of heparin resistance during cardiac and vascular
surgery. Arch Surg. 1979;114:129.
13. Mabry CD, Thompson BW, Read RC. Activated clotting time (ACT)
monitoring of intraoperative heparinization in peripheral vascular
surgery. Am J Surg. 1979;138:894.
14. Mabry CD, Thompson, BW, Read RC, Campbell GS. Activated
clotting time monitoring of intraoperative heparinization: Our
experience and comparison with two techniques. Surgery.
1981;90:889.
15. Moorehead MT, Westengard JC, Bull BS. Platelet involvement in the
activated coagulation time of heparinized blood. Anesth Analg.
1984;63:394.
26 Gebrauchsanweisung Deutsch
Page 29

16. Yang VC, Linhardt RJ, Bernstein H, Cooney CL, Langer R.
Purification and characterization of heparinase from Flavobacterium
heparinum. J Biol Chem. 1985;260:1849.
15. Haftungsausschluss
DER FOLGENDE HAFTUNGSAUSSCHLUSS GILT FÜR
KUNDEN AUSSERHALB DER USA:
TROTZ SORGFÄLTIGER KONSTRUKTION, HERSTELLUNG UND VOR
VERKAUF DURCHGEFÜHRTER TESTDURCHLÄUFE IST ES
MÖGLICH, DASS DIE HIGH RANGE HEPARINASETESTKARTUSCHE – IM FOLGENDEN ALS
„PRODUKT“ BEZEICHNET – AUS VERSCHIEDENSTEN GRÜNDEN
NICHT ZUFRIEDENSTELLEND FUNKTIONIERT. DIE WARNHINWEISE
IN DER PRODUKTINFORMATION ENTHALTEN WEITERE
DETAILLIERTE INFORMATIONEN UND SIND ALS BESTANDTEIL
DIESES HAFTUNGSAUSSCHLUSSES ANZUSEHEN. MEDTRONIC
SCHLIESST DAHER JEDE AUSDRÜCKLICHE ODER
STILLSCHWEIGENDE GARANTIE HINSICHTLICH DES PRODUKTS
AUS. MEDTRONIC HAFTET WEDER FÜR UNMITTELBARE NOCH
MITTELBARE ODER FOLGESCHÄDEN, DIE DURCH GEBRAUCH,
DEFEKT ODER STÖRUNG DES PRODUKTS ENTSTEHEN,
UNABHÄNGIG DAVON, OB SICH DER ANSPRUCH AUF
SCHADENSERSATZ AUF EINE GARANTIE, EINEN VERTRAG, EINE
UNERLAUBTE HANDLUNG ODER EINE ANDERE
ANSPRUCHSGRUNDLAGE STÜTZT.
Die hier aufgeführten Haftungsausschlüsse und -beschränkungen sollen
nicht gegen geltendes Recht verstoßen und sind nicht dahingehend
auszulegen. Sollte ein zuständiges Gericht feststellen, dass dieser
Haftungsausschluss ganz oder teilweise unwirksam, nicht durchsetzbar
oder im Widerspruch zu zwingendem Recht ist, berührt dies die Gültigkeit
der restlichen Klauseln nicht und alle Rechte und Pflichten aus diesem
Haftungsausschluss sind so auszulegen und durchzusetzen, als sei der
für ungültig erklärte Teil oder die ungültige Vorschrift in diesem
Haftungsausschluss nicht enthalten.
Gebrauchsanweisung Deutsch 27
Page 30

1. Uso previsto
Para uso en la identificación de presencia de heparina mediante un
tiempo de coagulación activado.
Para utilización en diagnóstico in vitro.
Precaución: Debido a la naturaleza única de este producto, se deben
tomar precauciones para garantizar que no se transfiera heparinasa de
forma accidental desde el canal “HR HTC” al canal “HR” del cartucho.
Para obtener más información, consulte la Sección 8 y la Sección 10.
2. Resumen
El cartucho de prueba de heparinasa de rango alto o HR HTC de
Medtronic, es una modificación del cartucho del tiempo de coagulación
activado de rango alto (HR ACT) para medidores automáticos del tiempo
de coagulación de Medtronic. La prueba de tiempo de coagulación
activado fue descrita por primera vez por Hattersley en 19669. La prueba
y sus variaciones se han utilizado extensamente para controlar el efecto
anticoagulante de la heparina
sangre completa recién extraída, igual que el cartucho HR ACT. La
diferencia entre los cartuchos es que un canal contiene heparinasa
bacteriana purificada (HR HTC). La heparinasa destruye de forma rápida
y específica la heparina presente en la muestra de sangre
cantidad de heparinasa presente eliminará rápidamente 6 unidades/ml de
heparina. El canal de heparina producirá un tiempo de coagulación que
refleja el tiempo de coagulación inicial sin heparina de la muestra, aunque
la muestra contenga heparina. El otro canal del cartucho es un HR ACT
estándar y el tiempo de coagulación obtenido es el tiempo de coagulación
activado con heparina de la muestra. El uso de este cartucho permite:
1) verificar la presencia prequirúrgica de heparina; 2) evaluar el efecto de
un bypass en el tiempo de coagulación activado inicial; 3) confirmar la
inversión de la heparina tras la administración de protamina; 4) identificar
un “rebote posquirúrgico de heparina” y 5) identificar la presencia de
heparina en pacientes que sangran excesivamente tras una intervención
quirúrgica. Hay disponible un control CLOTtrac™ HTC para verificar que
el cartucho funciona según sus especificaciones.
3,4,7,8,13,14
. HR HTC utiliza una muestra de
1,6,10,16
. La
3. Principios
La prueba del tiempo de coagulación activado mide el tiempo de
coagulación de sangre completa recién extraída activada por contacto en
la superficie. El procedimiento original de Hattersley utilizaba tierra
diatomácea como agente activador. La tierra diatomácea muestra
diferentes grados de activación en función de su pureza, el origen del
depósito y el tamaño y la forma de las partículas. Los cartuchos de
tiempo de coagulación activado de Medtronic utilizan caolín como agente
activador. El caolín posee características superiores en la activación por
contacto de la coagulación de sangre. Los cartuchos HR ACT y HR HTC
poseen una menor sensibilidad a la heparina, lo que permite supervisar
niveles altos de heparina con la prueba de tiempo de coagulación
activado.
El criterio de valoración de la prueba es la detección de la formación de
coágulos. Los medidores automáticos del tiempo de coagulación de
Medtronic detectan la formación de un coágulo mediante la supervisión
de la velocidad de caída del mecanismo de émbolo/marca contenido en
cada canal del cartucho. El conjunto del émbolo desciende rápidamente a
través de sangre sin coagular. Cuando se forma una red de fibrina la
caída del conjunto del émbolo se ve impedida. Un sistema fotoóptico
ubicado en la tapa del sistema detecta este cambio de la velocidad de
caída. La formación de un coágulo se indica mediante una señal auditiva
y se detiene el temporizador. El instrumento puede realizar 2 pruebas
28 Instrucciones de uso Español
Page 31

simultáneas con el cartucho de 2 canales. Una vez finalizada la prueba,
se muestran en segundos los tiempos de coagulación de cada canal. Con
el HR HTC, el instrumento muestra 2 resultados, uno para la muestra con
heparinasa y uno para la muestra sin heparinasa. La pantalla del panel
frontal se puede utilizar para cambiar entre los tiempos de coagulación de
cada canal, o la media y la diferencia entre los dos canales. Cuando se
utiliza el cartucho HR HTC, la media de las lecturas tiene poca
importancia, pero la diferencia entre los dos resultados es la extensión del
tiempo de coagulación debido a la presencia de heparina en la muestra.
4. Reactivos
Cada cámara de reactivo del cartucho contiene 0,1 ml de caolín
suspendido en una solución amortiguadora de ácido hidroxietil piperazine
etanosulfónico (HEPES), cloruro cálcico y azida sódica como agente
bacteriostático. El canal etiquetado como “HR HTC” contiene heparinasa
liofilizada altamente purificada con agentes estabilizadores y azida de
sodio como agente bacteriostático.
El cartucho HR HTC se puede precalentar durante un máximo de 2 horas.
Una vez se introduce la muestra en el cartucho precalentado, la prueba
se debe iniciar inmediatamente.
5. Almacenamiento
El cartucho HR HTC debe conservarse en un entorno estable, a una
temperatura de 2 °C a 10 °C (de 36 °F a 50 °F) o de 10 °C a 25 °C (de
50 °F a 77 °F). Los cartuchos se envasan en bandejas selladas de
2 cartuchos. Los cartuchos permanecen estables durante el tiempo
indicado en la etiqueta de la bandeja. No utilice los cartuchos después de
la fecha No utilizar después de. No utilice el cartucho si parece estar
descolorido, agrietado o desfigurado o, si el agente parece haberse
evaporado o estar contaminado.
Una vez la tapa de la bandeja se haya roto, los cartuchos permanecen
estables durante 24 horas a temperaturas del refrigerador.
Nota: No utilizar si hay evidencias de congelación.
6. Instrumento
HR HTC está diseñado específicamente para su uso en medidores
automáticos del tiempo de coagulación de Medtronic. Consulte las
instrucciones del Manual del usuario del instrumento.
Para asegurar el rendimiento adecuado del instrumento, es importante
limpiar el instrumento como mínimo cada 30 días o más si es necesario.
Nota: Si se mancha la tapa del actuador, limpie el instrumento en cuanto
pueda. Con cada instrumento se proporciona un kit de limpieza del
actuador (nº de catálogo 303-58). Utilice los materiales del kit de limpieza
para realizar el siguiente procedimiento de limpieza. Consulte el
prospecto incluido en el kit de limpieza si desea más información.
7. Recogida y preparación de las muestras
Las muestras de sangre manipuladas incorrectamente pueden
proporcionar resultados erróneos en la prueba de coagulación; las
muestras deben recogerse con cuidado y deben utilizarse siempre las
mismas técnicas de manipulación.
Si se obtiene sangre por venopunción, esta debe ser limpia. Deseche los
primeros milímetros de sangre para evitar contaminar la muestra con
tromboplastina histológica.
Nota: No recoja sangre de catéteres permanentes heparinizados ni de
otras vías anticoaguladas sin irrigar a fondo la vía.
Si se analiza sangre completa recién extraída, transfiera la muestra
inmediatamente al cartucho e inicie la prueba.
Instrucciones de uso Español 29
Page 32

8. Instrucciones de uso
1
2
Este producto está diseñado para su utilización exclusivamente por
personas con la formación apropiada.
Materiales suministrados:
■
Cartucho de prueba de heparinasa de rango alto (HR HTC), nº de
catálogo 402-07
Materiales necesarios no suministrados
■
Medidor automático del tiempo de coagulación de Medtronic
■
Jeringa de plástico con aguja (preferiblemente calibre 18 o 19)
Figura 1. Llenado del cartucho HR HTC
1. Muestra (vista lateral)
2. Muestra (vista superior)
Para utilizar con el instrumento ACT Plus™, siga los pasos a
continuación:
1. En el menú principal, seleccione “Tipo de cartucho” y pulse hasta que
aparezca la opción “HTC”. Pulse "Intro" para confirmar la selección.
Nota: Antes de realizar una prueba se deben introducir los números
de lote y la fecha de No utilizar después de de los cartuchos y los
controles.
2. En el menú principal, introduzca los números de “ID de paciente” e
“ID de usuario”. Pulse "Intro" para confirmar.
3. Precaliente el cartucho durante unos 3 a 5 minutos antes de recoger
una muestra de prueba.
4. Golpee suavemente el cartucho para desprender el reactivo.
5. Llene cada cámara con 0,4 ml de muestra.
Nota: Siempre llene primero el canal HR y a continuación el canal
HR HTC para que la heparinasa no contamine el canal HR.
6. Inserte el cartucho en el instrumento ACT Plus y cierre el bloque
térmico del accionador para comenzar la prueba.
7. Se indica la coagulación a través de tonos acústicos, el bloque
térmico del accionador se abre y se muestran los resultados.
Una vez terminada la prueba, deseche el cartucho, la jeringa y la
aguja de acuerdo en recipientes adecuados para residuos
biopeligrosos.
30 Instrucciones de uso Español
Page 33

9. Resultados
La respuesta del tiempo de coagulación activado a la heparina varía
considerablemente de persona a persona12. Diversos fármacos afectan al
tiempo de coagulación activados, en particular los que inhiben la
activación de las plaquetas15. Hay otros factores que pueden afectar a la
respuesta del tiempo de coagulación activado a la heparina de una
persona, como los niveles de antitrombina III, la potencia de la heparina,
deficiencias del factor de coagulación, la activación de la muestra,
coagulopatías de consumo, una dilución excesiva de la muestra y
temperatura de la muestra. Estos factores deben tenerse en cuenta al
interpretar los resultados de las pruebas del tiempo de coagulación
2,5,11
activado
La heparinasa en el canal HR HTC del cartucho es extremadamente
específica para la heparina. Hay presente suficiente heparinasa para
garantizar la eliminación rápida de 6 unidades/ml de heparina de la
muestra para llevarla a su estado inicial o sin heparina. El tiempo inicial
puede estar o no en el intervalo normal o cerca de este. Si el tiempo
inicial no está dentro del intervalo normal del canal HR HTC, indica que
otras condiciones, aparte de la presencia de heparina, son las
responsables de ampliar el tiempo coagulación inicial.
Ejemplo para interpretar los resultados de HR HTC:
.
Ca 1 Ca 2 Interpretación
120 120 Paciente con valor inicial, no hay heparina
120 260 El paciente tiene heparina en la sangre.
260 260 El paciente tiene una coagulopatía subya-
260 360 El paciente tiene heparina en la sangre y
60 200 El paciente tiene heparina en la sangre y su
presente en la muestra.
Extensión solo debida al efecto de la heparina.
cente no relacionada con la heparina.
una coagulopatía subyacente (probablemente hemodilución).
sistema de coagulación está activado.
10. Limitaciones del procedimiento
Para obtener tiempos de coagulación activados exactos y homogéneos
con el cartucho HR HTC, deben cumplirse las siguientes condiciones:
■
La temperatura del bloque térmico del instrumento y del cartucho
debe ser de 37 °C ± 0,5 °C (98,6 °F ± 0,9 °F). El cartucho tardará en
alcanzar la temperatura entre 3 y 5 minutos en el bloque térmico del
instrumento.
■
El activador de caolín debe resuspenderse por completo.
■
La sangre debe estar libre de tromboplastina histológica. Ejecute la
prueba en cuanto sea posible después de extraer la muestra de
sangre.
■
Deben tenerse en cuenta el diagnóstico y los medicamentos que esté
tomando el paciente. Los medicamentos pueden alterar los tiempos
de coagulación. Las muestras que dan valores anómalos
inexplicables se deben volver a extraer y analizar. Si los resultados
son anómalos y no existe una causa aparente, podrá recogerse una
muestra citratada y enviarse al laboratorio clínico para un análisis
especial de coagulación.
■
Para optimizar la precisión, deben mantenerse constantes todas las
variables de la técnica en las distintas pruebas.
■
Cuando la muestra se coloca en el cartucho, la prueba se debe
realizar lo antes posible. La eliminación de heparina de la muestra se
Instrucciones de uso Español 31
Page 34

produce rápidamente. La activación por contacto se producirá en el
cartucho cuando la muestra no tenga heparina. Esto resultará en
tiempos más cortos de coagulación mientras prosigue la activación de
la muestra.
■
Las metodologías empleadas en intervenciones quirúrgicas de
bypass cardiopulmonar cambian continuamente, igual que lo hacen
las características de la población de pacientes. Las condiciones que
pueden influir en los resultados de las pruebas de tiempo de
coagulación activado incluyen entre otras:
■
sensibilidad del paciente a la heparina
■
dilución de factores de coagulación en el circuito extracorpóreo
■
el uso de productos hemáticos citrados
■
el uso de tratamientos antiplaquetarios
■
hipotermia
■
niveles fluctuantes de calcio
■
un cambio en la función o recuento plaquetario
■
coagulopatías desconocidas
Una excesiva dilución de sangre durante el bypass, con frecuencia
debido al deseo de limitar productos hemáticos heterólogos, puede
producir una hemorragia posoperativa. En determinados casos la
dilución puede ser tan acusada que no se produzca la coagulación,
medida por el tiempo de coagulación activado. La adecuación de los
factores de coagulación plasmática no se puede determinar
correlacionando la cantidad de dilución con el hematocrito del
paciente. Con frecuencia, se administran células lavadas al paciente
sin compensar por la pérdida de plasma. Si el cartucho HR HTC no
se coagula en el canal de heparinasa (canal nº 1), seguida de la
inversión de la heparina del paciente con protamina, es muy posible
que se trate de una coagulopatía por dilución.
Advertencia: Debido a la formulación del HR HTC, no se debe
utilizar para monitorizar la anticoagulación regional conseguida al
infundir citrato.
Precaución: Se deben extremar las precauciones para asegurar que
la heparinasa del canal HR HTC no se transfiera inadvertidamente a
la muestra del canal HR del cartucho. Si esto sucede, el tiempo de
coagulación con heparina del canal “HR” dejaría de ser representativo
de la cantidad de heparina en la muestra e indicaría una cantidad
menor de heparina en función de cuánta heparinasa se haya
transferido. Por este motivo, es muy recomendable que se llene
primero el canal “HR” para minimizar la posibilidad de transferencia
de heparinasa.
Si desea ver las medidas preventivas y las limitaciones del
instrumento, consulte el Manual del usuario.
11. Valores previstos
El canal de heparinasa proporciona de forma eficaz un tiempo de
coagulación activado inicial en sangre completa recién extraída. Durante
el bypass, el valor de tiempo de coagulación activado inicial puede
desviarse hacia arriba, para reflejar la hemodilución de la sangre del
paciente. El tiempo de coagulación inicial está correlacionado con el
dilución de los factores plasmáticos de coagulación, que no están
necesariamente correlacionados con el hematocrito del paciente. Los
hematíes devueltos a un paciente a través de un sistema de recuperación
de células no compensan los factores plasmáticos de coagulación
perdidos. Si el tiempo de coagulación activado inicial sigue siendo más
prolongado, puede producirse una coagulopatia por dilución (falta de
suficientes factores de coagulación) y se puede observar una hemorragia
posopoeratoria. El HR HTC puede monitorizar el desarrollo de esta
32 Instrucciones de uso Español
Page 35

situación y permitir tomar acciones correctivas antes de que se produzca
una dilución grave de los factores de coagulación.
12. Características específicas de rendimiento
Los cartuchos de tiempo de coagulación activado, en el intervalo de
tiempo de coagulación de 0 a 600 segundos, no suelen superar una
variación del 12 % entre los canales duplicados en una persona. A
niveles elevados de heparina y tiempos de coagulación superiores a
600 segundos, el tiempo de coagulación activado por lo general no se
considera fiable para determinar niveles de heparina.
El cartucho HR HTC está formulado para producir un HR ATC normal en
el canal etiquetado como “HR”, que se corresponde estrechamente con
las respuestas notificadas originalmente por Bull, et al. (1975). El
activador de caolín en cada lote de cartuchos se ha calibrado para reducir
variaciones en la actividad entre lotes inferiores al 10 % y minimizar la
desviación a largo plazo.
El rendimiento del canal “inicial” del cartucho depende de la actividad de
la heparinasa en el canal etiquetado como “HR HTC”. La heparinasa se
ha purificado y estabilizado para eliminar 6 unidades/ml de heparina en
un periodo de tiempo lo suficientemente corto para hacer que la sangre
heparinizada vuelva a un tiempo de coagulación inicial. La estabilidad de
la heparinasa se garantiza manteniendo los cartuchos a temperatura
constante. Los intervalos en los que los cartuchos pueden conservarse
son de 2 °C a 10 °C (de 36 °F a 50 °F) o de 10 °C a 25 °C (de 50 °F a
77 °F). El rendimiento del cartucho puede reducirse si el producto no se
almacena en un entorno estable. No se recomienda el movimiento
repetido del producto refrigerado a temperatura ambiente y viceversa.
13. Control de calidad
Se deben realizar dos niveles de control para la prueba HTC a fin de
asegurar un rendimiento adecuado del instrumento y los cartuchos.
Los resultados deben estar dentro de los intervalos especificados por el
fabricante o determinados por el usuario.
Los controles para la prueba de heparinasa de rango alto: son el control
de coagulación CLOTtrac™ HR (nº de catálogo 550-07) y el control
CLOTtrac HTC (nº de catálogo 550-12).
El control CLOTtrac HTC proporciona un HR ACT inicial en el canal
HR HTC y agota el tiempo de espera (>999) en el canal HR ACT.
Se trata de un control liofilizado que contiene 6 unidades/ml de heparina.
El rendimiento del cartucho HR HTC se verifica procesando el control en
un cartucho y obteniendo un valor de HR ACT inicial en el canal
etiquetado como “HR HTC” y agotándose el tiempo de espera
(999 segundos) en el canal etiquetado como “HR”. Esto indica que el
canal que contiene heparinasa del cartucho funciona adecuadamente.
14. Referencias bibliográficas
1. Baugh RF, Deemar KA, Zimmerman JJ. Heparinase in the activated
clotting time assay: Monitoring heparin-independent alterations in
coagulation function. Anesth Analg. 1992;74:201.
2. Bode AP, Eick L. Lysed platelets shorten the activated coagulation
time (ACT) of heparinized blood. Am J Clin Pathol. 1989;91:430.
3. Bull BS, Korpman RA, Huse WM, Briggs BD. Heparin therapy during
extracorporeal circulation. I. Problems inherent in existing heparin
protocols. J Thorac Cardiovasc Surg. 1975;69:674.
4. Bull BS, Huse WM, Brauer FS, Korpman RA. Heparin therapy during
extracorporeal circulation. II. The use of a dose-response curve to
individualize heparin and protamine dosage. J Thorac Cardiovasc
Surg. 1975;69:685.
Instrucciones de uso Español 33
Page 36

5. Culliford AT, Gitel SN, Starr N, Thomas ST, Baumann FG, Wessler S,
Spencer FC. Lack of correlation between activated clotting time and
plasma heparin during cardiopulmonary bypass. Ann Surg.
1981;193:105.
6. Dietrich CP, Silva ME, Michelacci YM. Sequential degradation of
heparin in Flavobacterium heparinum. Purification and properties of
five enzymes involved in heparin degradation. J Biol Chem.
1973;248:6408.
7. Effeney DJ, Goldstone J, Chin D, Krupski WC, Ellis RJ. Intraoperative
anticoagulation in cardiovascular surgery. Surgery. 1981;90:1068.
8. Forman WB, Bayer G. A simplified method for monitoring heparin
therapy at the bedside: The activated whole blood clotting time. Am J
Hematol. 1981;11:277.
9. Hattersley PG. Progress report: The activated coagulation time of
whole blood (ACT). Am J Clin Pathol. 1976;66:899.
10. Hutt ED, Kingdon HS. Use of heparinase to eliminate heparin
inhibition in routine coagulation assays. J Lab Clin Med.
1972;79:1027.
11. Kesteven PJ, Pasaoglu I, Williams BT, Savidge GG. Significance of
the whole blood activated clotting time in cardiopulmonary bypass. J
Cardiovasc Surg. 1986;27:85.
12. Mabry CD, Read RC, Thompson BW, Williams GD, White HJ.
Identification of heparin resistance during cardiac and vascular
surgery. Arch Surg. 1979;114:129.
13. Mabry CD, Thompson BW, Read RC. Activated clotting time (ACT)
monitoring of intraoperative heparinization in peripheral vascular
surgery. Am J Surg. 1979;138:894.
14. Mabry CD, Thompson, BW, Read RC, Campbell GS. Activated
clotting time monitoring of intraoperative heparinization: Our
experience and comparison with two techniques. Surgery.
1981;90:889.
15. Moorehead MT, Westengard JC, Bull BS. Platelet involvement in the
activated coagulation time of heparinized blood. Anesth Analg.
1984;63:394.
16. Yang VC, Linhardt RJ, Bernstein H, Cooney CL, Langer R.
Purification and characterization of heparinase from Flavobacterium
heparinum. J Biol Chem. 1985;260:1849.
15. Renuncia de responsabilidad
LA SIGUIENTE RENUNCIA DE RESPONSABILIDAD SE
APLICA SOLO A LOS CLIENTES DE FUERA DE LOS
ESTADOS UNIDOS:
AUNQUE EL CARTUCHO DE PRUEBA DE HEPARINASA DE RANGO
ALTO, AL QUE NOS REFERIREMOS DE AHORA EN ADELANTE
COMO “PRODUCTO”, HA SIDO DISEÑADO, FABRICADO Y
PROBADO CUIDADOSAMENTE ANTES DE PONERLO A LA VENTA,
EL PRODUCTO PUEDE NO CUMPLIR SUS FUNCIONES
SATISFACTORIAMENTE POR VARIAS RAZONES. LAS
ADVERTENCIAS QUE CONTIENE LA DOCUMENTACIÓN DEL
PRODUCTO PROPORCIONAN INFORMACIÓN MÁS DETALLADA Y
SE CONSIDERAN PARTE INTEGRANTE DE ESTA RENUNCIA DE
RESPONSABILIDAD. POR TANTO, MEDTRONIC RENUNCIA A
CUALQUIER RESPONSABILIDAD, TANTO EXPRESA COMO
IMPLÍCITA, CON RESPECTO AL PRODUCTO. MEDTRONIC NO
RESPONDERÁ POR LOS DAÑOS FORTUITOS O CAUSADOS POR
CUALQUIER USO, DEFECTO, FALLO O MAL FUNCIONAMIENTO DEL
34 Instrucciones de uso Español
Page 37

PRODUCTO, AUN CUANDO LA RECLAMACIÓN SE BASE EN UNA
GARANTÍA, CONTRATO, RESPONSABILIDAD
EXTRACONTRACTUAL O CUALQUIER OTRO FUNDAMENTO LEGAL.
Las exclusiones y limitaciones descritas anteriormente no pretenden
contravenir las disposiciones obligatorias establecidas por la legislación
vigente, ni deben interpretarse de dicha forma. En el supuesto de que
cualquier parte o término de la presente Renuncia de responsabilidad sea
declarado por cualquier tribunal competente como ilegal, inaplicable o
contrario a la ley, ello no afectará a la validez del resto de la Renuncia de
responsabilidad, interpretándose y aplicándose cuantos derechos y
obligaciones se incluyen en ella como si la presente Renuncia de
responsabilidad no contuviera la parte o término considerado no válido.
Instrucciones de uso Español 35
Page 38

1. Toepassing
Voor het identificeren van de aanwezigheid van heparine door middel van
een geactiveerde stollingstijd.
Voor in-vitro diagnostisch gebruik.
Let op: Vanwege de unieke aard van dit product moet u erop letten dat
heparinase niet onbedoeld van het "HR HTC"-kanaal wordt overgebracht
naar het "HR"-kanaal van de cartridge. Zie Sectie 8 en Sectie 10 voor
aanvullende informatie.
2. Samenvatting
De testcartridge voor hoog bereik heparinase (HR HTC) van Medtronic is
een modificatie van de HR-ACT-cartridge voor de automatische
stollingstijdmeters van Medtronic. De geactiveerde stollingstijdtest (ACTtest) werd in 1966 beschreven door Hattersley.9 Deze test en de variaties
erop worden wijdverbreid gebruikt voor het bewaken van het
antistollingseffect van heparine.
volbloedmonster gebruikt, net als voor de HR-ACT-cartridge. Het verschil
tussen de cartridges is het feit dat één kanaal een gezuiverd bacterieel
heparinase bevat (HR-HTC). Heparinase vernietigt snel en specifiek de
heparine die in het bloedmonster aanwezig is.
hoeveelheid heparinase verwijdert snel 6 eenheden/ml heparine. Het
heparinasekanaal genereert een stollingstijd die de basislijn voor de nietgehepariniseerde stolling van het monster weerspiegelt, hoewel het
monster heparine bevat. Het andere kanaal van de cartridge is een
standaard HR-ACT en de verkregen stollingstijd is die van de
gehepariniseerde geactiveerde stolling van het monster. Met deze
cartridge is het volgende mogelijk: 1) verificatie van de prechirurgische
aanwezigheid van heparine, 2) beoordeling van het effect van een bypass
op de basislijn voor de geactiveerde stollingstijd, 3) bevestiging van
heparinereversie na toediening van protaminen, 4) identificatie van
postchirurgische "heparinerebound" en 5) identificatie van de
aanwezigheid van heparine bij patiënten die na een operatie overmatig
bloeden. Er is een CLOTtrac™ HTC-controlevloeistof verkrijgbaar om te
controleren of de cartridge volgens de specificaties werkt.
3,4,7,8,13,14
Voor de HR-HTC wordt een vers
1,6,10,16
De aanwezige
3. Werking
De ACT-test meet de stollingstijd van vers volbloed dat wordt geactiveerd
door contact met een oppervlakte. Bij de oorspronkelijke procedure van
Hattersley werd diatomeeënaarde als activeringsmiddel gebruikt.
Diatomeeënaarde vertoont verschillende gradaties van contactactivering,
afhankelijk van de zuiverheid, de bron van de afzetting, en de grootte en
vorm van de deeltjes. Bij de ACT-cartridges van Medtronic wordt kaolien
als activeringsmiddel gebruikt. Kaolien vertoont superieure kenmerken bij
contactactivering van bloedstolling. De HR-ACT en HR-HTC zijn minder
gevoelig voor heparine, waardoor met de ACT-test hogere
heparinegehalten kunnen worden bewaakt.
Het eindpunt van de test is de detectie van stolselvorming. De
automatische stollingstijdmeters van Medtronic detecteren stolselvorming
door de daalsnelheid van de stamper/vlag in beide kanalen van de
cartridge te bewaken. De stamper daalt snel door niet-gestold bloed.
Wanneer een fibrinenetwerk wordt gevormd, wordt de val van de stamper
vertraagd. Deze afname in de dalingssnelheid wordt waargenomen door
een foto-optisch systeem in het deksel van het apparaat. Stolselvorming
wordt aangegeven met een geluidssignaal en de stollingstimer stopt. De
apparaten kunnen 2 tests gelijktijdig uitvoeren met gebruikmaking van een
cartridge met 2 kanalen. Per kanaal wordt de stollingstijd na afronding van
de test in seconden weergegeven. Bij de HR-HTC geeft het apparaat
2 resultaten weer: één voor het monster met heparinase en één voor het
36 Gebruiksaanwijzing Nederlands
Page 39

monster zonder heparinase. Het scherm kan worden gebruikt om te
wisselen tussen de stollingstijden van de afzonderlijke kanalen, of het
gemiddelde en het verschil tussen de twee kanalen. Bij gebruik van de
HR-HTC is de gemiddelde waarde niet zo belangrijk. Het verschil tussen
de twee resultaten is echter de verlenging van de stollingstijd vanwege de
aanwezigheid van heparine in het monster.
4. Reagentia
Elke reagenskamer van de cartridge bevat 0,1 ml hydroxyethylpiperazine-ethaansulfonzuur (HEPES-buffer), kaolien, calciumchloride, en
natriumazide als bacteriostatisch middel. Het kanaal met de aanduiding
"HR HTC" bevat gelyofiliseerde, hooggezuiverde heparinase met
stabilisatiemiddelen en natriumazide als bacteriostatisch middel.
De HR-HTC-cartridge kan gedurende maximaal 2 uur worden
voorverwarmd. Zodra het monster in de voorverwarmde cartridge wordt
geplaatst, moet de test onmiddellijk worden gestart.
5. Opslag
Bewaar de HR HTC in een stabiele omgeving bij 2 °C tot 10 °C
(36 °F tot 50 °F) of bij 10 °C tot 25 °C (50 °F tot 77 °F). De cartridges
worden verpakt in verzegelde trays met 2 cartridges. De cartridges zijn
stabiel gedurende de tijdsperiode die op het etiket van de tray staat
aangegeven. De cartridges niet gebruiken als de uiterste gebruiksdatum
verstreken is. Niet gebruiken als de cartridges verkleurd, gebarsten of
vervormd zijn, of als de reagentia opgedroogd zijn of vervuild lijken.
Wanneer de verzegeling van het traydeksel verbroken is, zijn de
cartridges gedurende 24 uur stabiel bij koelkasttemperatuur.
Opmerking: Niet gebruiken als de cartridge tekenen van bevriezing
vertoont.
6. Instrument
De HR-HTC is specifiek ontworpen voor gebruik in automatische
stollingstijdmeters van Medtronic. Raadpleeg de gebruikershandleiding bij
het apparaat voor instructies.
Voor de juiste werking van het apparaat is het van belang het apparaat
minimaal elke 30 dagen, of zo nodig vaker, te reinigen.
Opmerking: Als er bloed in het actuatordeksel terechtkomt, moet u het
apparaat zo snel mogelijk reinigen. Een reinigingskit voor de actuator
(catalogusnummer 303-58) wordt bij elk apparaat meegeleverd. Gebruik
het materiaal in de reinigingskit voor het uitvoeren van de
reinigingsprocedure. Raadpleeg de bijlage in de reinigingskit voor meer
informatie.
7. Monsterafname en bereiding
Als de monsters onjuist worden verwerkt, zijn de resultaten van
bloedstollingstests mogelijk onjuist. De bloedmonsters moeten daarom
zorgvuldig worden afgenomen en de verwerking moet op consistente
wijze gebeuren.
Als het bloed door middel van een venapunctie is verkregen, moet de
venapunctie schoon zijn. De eerste milliliters bloed moeten worden
weggegooid om verontreiniging van het monster met
weefseltromboplastine te voorkomen.
Opmerking: Bloed afnemen uit met heparineoplossing gevulde
verblijfskatheters of andere lijnen met antistollingsmiddel mag alleen
nadat deze eerst grondig zijn doorgespoeld.
Bij het testen van vers volbloed moet u het monster onmiddellijk in de
cartridge plaatsen en de test starten.
Gebruiksaanwijzing Nederlands 37
Page 40

8. Gebruiksaanwijzing
1
2
Dit product is uitsluitend bestemd voor gebruik door daartoe opgeleide
personen.
Geleverde materialen:
■
Testcartridge voor hoog bereik heparinase (HR-HTC),
catalogusnummer 402-07
Benodigd materiaal, niet meegeleverd
■
Automatische stollingstijdmeter van Medtronic
■
Plastic spuit met naald (bij voorkeur 18 of 19 gauge)
1. Monster (zijaanzicht)
2. Monster (bovenaanzicht)
Volg de onderstaande stappen voor gebruik met het ACT Plus™apparaat:
1. Selecteer vanuit het hoofdmenu "Cartridge Type" en druk op de toets
tot "HTC" wordt weergegeven. Druk op "Enter" om de selectie te
bevestigen.
Opmerking: Voordat u een test uitvoert, moet u de partijnummers en
uiterste gebruiksdata van cartridges en controletests invoeren.
2. Vanuit het hoofdmenu voert u "Patient ID" en "User ID" in. Druk op
"Enter" om te bevestigen.
3. Verwarm voordat het testmonster wordt afgenomen de cartridges
3 tot 5 minuten voor.
4. Tik tegen de cartridge om het reagens te hersuspenderen.
5. Vul elke kamer met 0,4 ml van het monster.
Opmerking: Vul altijd eerst het HR-kanaal en daarna het HR-HTC-
kanaal om ervoor te zorgen dat het HR-kanaal niet wordt
verontreinigd met heparinase.
6. Plaats de cartridge in de ACT Plus en sluit het
actuatorverwarmingsblok om de test te starten.
7. Stolselvorming wordt aangegeven met een geluidssignaal; het
actuatorverwarmingsblok gaat open en de resultaten worden
weergegeven.
Na afloop van de test moeten de cartridge, spuit en naald worden
weggegooid in goedgekeurde containers voor biologisch gevaarlijk
afval.
38 Gebruiksaanwijzing Nederlands
Afbeelding 1. De HR-HTC-cartridge vullen
Page 41

9. Resultaten
De reactie van de geactiveerde stollingstijd op heparine varieert
aanzienlijk van persoon tot persoon.12 Verschillende medicijnen
beïnvloeden de geactiveerde stollingstijd, met name geneesmiddelen die
de activering van bloedplaatjes remmen.15 De reactie van de individuele
stollingstijd van een persoon op heparine kan worden beïnvloed door
allerlei andere factoren, bijvoorbeeld antitrombine III-waarden, de sterkte
van de heparine, afwijkingen bij stollingsfactoren, activering van het
monster, consumptieve coagulopathieën, te sterke dilutie van het
monster, de temperatuur van het monster. Bij de interpretatie van de
resultaten van ACT-test moet rekening gehouden worden hiermee.
De heparinase in het HR-HTC-kanaal van de cartridge is buitengewoon
specifiek voor heparine. Er is voldoende heparinase aanwezig om ervoor
te zorgen dat er snel 6 eenheden/ml heparine uit het monster worden
verwijderd, zodat het monster wordt teruggebracht naar de
uitgangssituatie of niet-gehepariniseerde toestand. De uitgangssituatie
voor de tijd ligt al dan niet binnen of nabij het normale bereik. Als de
basislijn niet binnen het normale bereik in het HR HTC-kanaal ligt,
betekent dit dat een andere toestand dan de aanwezigheid van heparine
verantwoordelijk is voor de langere stollingstijd dan bij de basislijn.
Voorbeeld van de interpretatie van HR-HTC-resultaten:
Ch 1 Ch 2 Interpretatie
120 120 Patiënt bij basislijn, geen heparine aanwezig
120 260 Patiënt heeft heparine in bloed. Verlenging
260 260 Patiënt heeft onderliggende coagulopathie
260 360 Patiënt heeft heparine in bloed en patiënt
60 200 Patiënt heeft heparine in bloed en coagula-
in monster.
alleen vanwege effect van heparine.
niet gerelateerd aan heparine.
heeft onderliggende coagulopathie (waarschijnlijk hemodilutie).
tiesysteem van de patiënt is geactiveerd.
2,5,11
10. Beperkingen van de procedure
Om nauwkeurige en consistente geactiveerde stollingstijden met de HRHTC te verkrijgen, moet u op de volgende condities letten:
■
De temperatuur van het hitteblok en de cartridge moet 37 °C ±0,5 °C
(98,6 °F ±0,9 °F) zijn. De cartridge heeft 3 tot 5 minuten nodig om in
het hitteblok van het apparaat op temperatuur te komen.
■
De kaolien-activator moet grondig worden gehersuspendeerd.
■
Het bloed mag geen weefseltromboplastine bevatten. Voer de test zo
snel mogelijk na afname van het bloedmonster uit.
■
De diagnose en het medicijngebruik van de patiënt moeten worden
genoteerd. Geneesmiddelen kunnen de stollingstijden beïnvloeden.
Als een testmonster onverklaarbare abnormale resultaten geeft, moet
een nieuw monster worden afgenomen en getest. Als de resultaten
abnormaal blijven en er geen duidelijke oorzaak is, moet een monster
met citraat worden behandeld en voor speciale coagulatieanalyse
naar een klinisch laboratorium worden gestuurd.
■
Om de precisie te optimaliseren moeten alle technieken bij elke test
op consistente wijze worden uitgevoerd.
■
Wanneer het monster in de cartridge is geplaatst, moet de test zo snel
mogelijk worden uitgevoerd. De heparine wordt snel uit het monster
verwijderd. Wanneer het monster geen heparine bevat, treedt in de
cartridge contactactivering op. Dit leidt tot kortere stollingstijden als de
activering van het monster doorgaat.
Gebruiksaanwijzing Nederlands 39
Page 42

■
De methodologieën gebruikt bij een cardiopulmonale bypassoperatie
veranderen constant, net als de kenmerken van de
patiëntenpopulatie. De condities die van invloed kunnen zijn op de
resultaten van de ACT-test zijn onder meer:
■
gevoeligheid van de patiënt voor heparine
■
dilutie van stollingsfactoren door het extracorporele circuit
■
het gebruik van met citraat behandelde bloedproducten
■
het gebruik van trombocytenaggregatieremmers
■
hypothermie
■
fluctuerend calciumpeil
■
een verandering in trombocytengetal of -functie
■
onbekende coagulopathieën
Als er excessieve bloeddilutie optreedt bij een bypassoperatie
(meestal vanwege de wens het gebruik van heterologe
bloedproducten te beperken), kan dit tot postoperatieve bloedingen
leiden. In ernstige gevallen kan de dilutie zo sterk zijn dat er geen
stolling optreedt, zoals gemeten door de geactiveerde stollingstijd. De
adequaatheid van plasmastollingsfactoren kan niet worden bepaald
door de verlenging van de dilutie te correleren met de
hematocrietwaarde van de patiënt. Vaak werden er gewassen cellen
aan de patiënt toegediend zonder compensatie voor het verloren
plasma. Als de HR-HTC niet stolt in het heparinasekanaal (kanaal 1),
na heparinereversie met protaminen bij de patiënt, is een
dilutiecoagulopathie een zeer grote mogelijkheid.
Waarschuwing: Door de formulering van de HR-HTC mag het
product niet worden gebruikt voor de bewaking van regionale
anticoagulatie die wordt bereikt door de infusie van citraat.
Let op: Ga uiterst voorzichtig te werk om ervoor te zorgen dat
heparinase uit het HR HTC-kanaal niet onbedoeld wordt overgebracht
naar het monster in het HR-kanaal van de cartridge. Als dit gebeurt, is
de gehepariniseerde stollingstijd in het "HR"-kanaal niet langer
representatief voor de hoeveelheid heparine in het monster, maar
wordt minder heparine aangegeven. Dit is afhankelijk van de
hoeveelheid heparinase die is overgebracht. Daarom wordt ten
zeerste aanbevolen eerst het "HR"-kanaal te vullen om de kans op
overdracht van heparinase te minimaliseren.
Voor voorzorgsmaatregelen en beperkingen van het apparaat
raadpleegt u de gebruikershandleiding.
11. Verwachte waarden
Het heparinasekanaal biedt op effectieve wijze een basislijn voor de
geactiveerde stollingstijd op gehepariniseerd vers volbloed. Tijdens de
bypass kan de basislijnwaarde voor de geactiveerde stollingstijd stijgen
als reflectie van hemodilutie in het bloed van de patiënt. De basislijn voor
de stollingstijd correleert met de dilutie van plasmastollingsfactoren, die
niet noodzakelijk correleert met de hematocrietwaarde van de patiënt.
Rode bloedcellen die vanuit een cell saver aan een patiënt worden
teruggegeven, bieden geen compensatie voor de verloren
plasmastollingsfactoren. Als de basislijn voor de geactiveerde stollingstijd
verlengd blijft, kan een dilutiecoagulopathie (gebrek aan voldoende
stollingsfactoren) optreden en moeten postoperatieve bloedingen in de
gaten worden gehouden. De HR-HTC kan de ontwikkeling van deze
situatie bewaken en ervoor zorgen dat de juiste maatregelen worden
getroffen voordat ernstige dilutie van stollingsfactoren optreedt.
12. Specifieke prestatiekenmerken
ACT-cartridges vertonen bij een bepaalde persoon in het
stollingstijdbereik van 0 tot 600 seconden in het algemeen een variatie
40 Gebruiksaanwijzing Nederlands
Page 43

van niet meer dan 12% tussen de twee monsters. Bij hoge
heparinegehalten en stollingstijden van meer dan 600 seconden wordt
een geactiveerde stollingstijd in het algemeen niet beschouwd als een
adequate bepaling van de heparinegehalten.
De formulering van de HR-HTC is bedoeld voor het genereren van een
normale HR-ACT in het kanaal dat is aangeduid met "HR", die het meest
overeenkomt met de reacties die oorspronkelijk werden gemeld door Bull,
et al (1975). De kaolien-activator in elke partij cartridges is gekalibreerd
om variaties in de activiteit tussen partijen te beperken tot minder dan
10% en om verschuiving op lange termijn te minimaliseren.
De werking van het "baseline"-kanaal van de cartridge is afhankelijk van
de activiteit van de heparinase in het kanaal met de aanduiding
"HR HTC". De heparinase is gezuiverd en gestabiliseerd zodat er
6 eenheden/ml heparine worden verwijderd in een tijdsperiode die kort
genoeg is om het gehepariniseerde bloed te laten terugkeren naar de
basislijn voor de stollingstijd. De stabiliteit van de heparinase wordt
gewaarborgd door de cartridges op een constante temperatuur te houden.
Bewaar de cartridges bij 2 °C tot 10 °C (36 °F tot 50 °F) of bij
10 °C tot 25 °C (50 °F tot 77 °F). De werking van de cartridge verslechtert
als het product niet in een omgeving met stabiele temperatuur wordt
bewaard. Het wordt niet aanbevolen het product herhaaldelijk uit de
koeling in een omgeving met kamertemperatuur of andersom te brengen.
13. Quality Control
Voor de HTC-test moeten twee controletestsniveaus worden uitgevoerd
om de adequate werking van het apparaat en de cartridges te
waarborgen.
De resultaten moeten vallen binnen het bereik dat wordt gespecificeerd
door de fabrikant of het bereik dat wordt bepaald door de gebruiker.
Controletests voor de HR-HTC-test omvatten: de CLOTtrac™-HRcontrolevloeistof voor stollingstest (catalogusnummer 550-07) en de
CLOTtrac HTC-controlevloeistof (catalogusnummer 550-12).
De CLOTtrac HTC-controlevloeistof levert een HR-ACT-basislijn in het
HR HTC-kanaal op en geeft een time-out (>999) in het HR-ACT-kanaal.
Deze gelyofiliseerde controlevloeistof bevat 6 eenheden/ml heparine. De
werking van de HR-HTC wordt gecontroleerd door de controlevloeistof in
een cartridge te plaatsen en een HR-ACT-basislijnwaarde te verkrijgen in
het kanaal met de aanduiding "HR HTC" en een time-out (999 seconden)
in het kanaal met de aanduiding "HR". Dit betekent dat het
cartridgekanaal met heparinase naar behoren werkt.
14. Literatuur
1. Baugh RF, Deemar KA, Zimmerman JJ. Heparinase in the activated
clotting time assay: Monitoring heparin-independent alterations in
coagulation function. Anesth Analg. 1992;74:201.
2. Bode AP, Eick L. Lysed platelets shorten the activated coagulation
time (ACT) of heparinized blood. Am J Clin Pathol. 1989;91:430.
3. Bull BS, Korpman RA, Huse WM, Briggs BD. Heparin therapy during
extracorporeal circulation. I. Problems inherent in existing heparin
protocols. J Thorac Cardiovasc Surg. 1975;69:674.
4. Bull BS, Huse WM, Brauer FS, Korpman RA. Heparin therapy during
extracorporeal circulation. II. The use of a dose-response curve to
individualize heparin and protamine dosage. J Thorac Cardiovasc
Surg. 1975;69:685.
5. Culliford AT, Gitel SN, Starr N, Thomas ST, Baumann FG, Wessler S,
Spencer FC. Lack of correlation between activated clotting time and
plasma heparin during cardiopulmonary bypass. Ann Surg.
1981;193:105.
Gebruiksaanwijzing Nederlands 41
Page 44

6. Dietrich CP, Silva ME, Michelacci YM. Sequential degradation of
heparin in Flavobacterium heparinum. Purification and properties of
five enzymes involved in heparin degradation. J Biol Chem.
1973;248:6408.
7. Effeney DJ, Goldstone J, Chin D, Krupski WC, Ellis RJ. Intraoperative
anticoagulation in cardiovascular surgery. Surgery. 1981;90:1068.
8. Forman WB, Bayer G. A simplified method for monitoring heparin
therapy at the bedside: The activated whole blood clotting time. Am J
Hematol. 1981;11:277.
9. Hattersley PG. Progress report: The activated coagulation time of
whole blood (ACT). Am J Clin Pathol. 1976;66:899.
10. Hutt ED, Kingdon HS. Use of heparinase to eliminate heparin
inhibition in routine coagulation assays. J Lab Clin Med.
1972;79:1027.
11. Kesteven PJ, Pasaoglu I, Williams BT, Savidge GG. Significance of
the whole blood activated clotting time in cardiopulmonary bypass. J
Cardiovasc Surg. 1986;27:85.
12. Mabry CD, Read RC, Thompson BW, Williams GD, White HJ.
Identification of heparin resistance during cardiac and vascular
surgery. Arch Surg. 1979;114:129.
13. Mabry CD, Thompson BW, Read RC. Activated clotting time (ACT)
monitoring of intraoperative heparinization in peripheral vascular
surgery. Am J Surg. 1979;138:894.
14. Mabry CD, Thompson, BW, Read RC, Campbell GS. Activated
clotting time monitoring of intraoperative heparinization: Our
experience and comparison with two techniques. Surgery.
1981;90:889.
15. Moorehead MT, Westengard JC, Bull BS. Platelet involvement in the
activated coagulation time of heparinized blood. Anesth Analg.
1984;63:394.
16. Yang VC, Linhardt RJ, Bernstein H, Cooney CL, Langer R.
Purification and characterization of heparinase from Flavobacterium
heparinum. J Biol Chem. 1985;260:1849.
15. Uitsluiting van garantie
DE VOLGENDE UITSLUITING VAN GARANTIE GELDT
VOOR KLANTEN BUITEN DE VERENIGDE STATEN:
HOEWEL DE TESTCARTRIDGE VOOR HOOG BEREIK HEPARINASE,
HIERNA HET "PRODUCT" GENOEMD, MET VEEL ZORG IS
ONTWORPEN, VERVAARDIGD EN VÓÓR DE VERKOOP GETEST,
KUNNEN ER VERSCHILLENDE REDENEN ZIJN WAAROM HET
PRODUCT NIET VOLGENS DE SPECIFICATIES WERKT. DE
WAARSCHUWINGEN IN DE PRODUCTDOCUMENTATIE BIEDEN
MEER GEDETAILLEERDE INFORMATIE EN VORMEN EEN
INTEGRAAL ONDERDEEL VAN DEZE UITSLUITING VAN GARANTIE.
MEDTRONIC VERLEENT DAAROM GEEN ENKELE GARANTIE,
NOCH EXPLICIET NOCH IMPLICIET, MET BETREKKING TOT HET
PRODUCT. MEDTRONIC IS NIET AANSPRAKELIJK VOOR ENIGE
INCIDENTELE OF GEVOLGSCHADE, VEROORZAAKT DOOR OM HET
EVEN WELK GEBRUIK, DEFECT OF FALEN VAN HET PRODUCT,
ONGEACHT OF DE VORDERING IS GEBASEERD OP EEN
GARANTIE, CONTRACT, ONRECHTMATIGE DAAD OF ANDERSZINS.
De uitsluitingen en beperkingen die hierboven uiteengezet zijn, zijn niet
bedoeld, en moeten niet geïnterpreteerd worden als een inbreuk op
dwingende bepalingen van de van toepassing zijnde wet. Indien enig
onderdeel of enige bepaling van deze Uitsluiting van garantie door een
42 Gebruiksaanwijzing Nederlands
Page 45

daartoe bevoegde rechtbank als onrechtmatig, onuitvoerbaar of in strijd
met de van toepassing zijnde wet beschouwd wordt, zal dit de geldigheid
van het overige deel van de Uitsluiting van garantie niet aantasten en
zullen alle rechten en plichten worden uitgelegd en ten uitvoer worden
gebracht alsof deze Uitsluiting van garantie het desbetreffende ongeldig
verklaarde gedeelte niet bevatte.
Gebruiksaanwijzing Nederlands 43
Page 46

1. Uso previsto
Per l'individuazione della presenza di eparina con il test del tempo di
coagulazione attivata.
Per uso diagnostico in vitro.
Attenzione: data la particolare natura di questo prodotto, adottare le
dovute precauzioni per evitare che l'eparinasi venga inavvertitamente
trasferita dal canale "HR HTC" al canale "HR" della cartuccia. Per ulteriori
informazioni, vedere la Sezione 8 e la Sezione 10.
2. Riepilogo
La cartuccia per il test con eparinasi ad ampio range (HR HTC) Medtronic
è una modificazione della cartuccia per il tempo di coagulazione attivata
ad ampio range (HR ACT) utilizzabile con i timer per la coagulazione
automatici Medtronic. Il test del tempo di coagulazione attivata è stato
descritto per la prima volta da Hattersley nel 1966.9 Il test è stato
ampiamente utilizzato, insieme alle sue varianti, per monitorare l'effetto
anticoagulante dell'eparina
cartuccia HR ACT, viene utilizzata con un campione di sangue intero
fresco. La differenza fra le due cartucce consiste nella presenza di
eparinasi batterica purificata in uno dei canali della cartuccia HR HTC.
L'eparina presente nel campione di sangue viene rapidamente e
selettivamente degradata ad opera dell'eparinasi
eparinasi contenuta nella cartuccia è in grado di eliminare rapidamente
6 unità/ml di eparina. Il tempo di coagulazione ottenuto nel canale
contenente l'eparinasi risulta equivalente al tempo di coagulazione basale
di un campione non eparinizzato, anche se il campione analizzato
contiene eparina. L'altro canale della cartuccia è un normale canale
HR ACT e il tempo di coagulazione ottenuto equivale al tempo di
coagulazione attivata del campione eparinizzato. L'utilizzo di questa
cartuccia consente di: 1) verificare la presenza di eparina nella fase
preoperatoria; 2) valutare gli effetti della procedura di bypass sul tempo di
coagulazione attivata basale; 3) confermare la neutralizzazione
dell'eparina in seguito alla somministrazione di protamina; 4) identificare
l'effetto di "rimbalzo" dell'eparina nella fase postoperatoria; e
5) identificare la presenza di eparina in pazienti con eccessivo
sanguinamento postoperatorio. Per verificare l'effettivo funzionamento
della cartuccia secondo le specifiche, è disponibile un controllo
CLOTtrac™ HTC.
3,4,7,8,13,14
. La cartuccia HR HTC, come la
1,6,10,16
. La quantità di
3. Principi
Il test del tempo di coagulazione attivata misura il tempo di coagulazione
del sangue intero fresco attivata dal contatto con una superficie. La
procedura originaria di Hattersley utilizzava terra diatomacea come
agente attivante. Il grado di attivazione da contatto indotta dalla terra
diatomacea differisce in base al grado di purezza, all'origine del deposito
e alla dimensione e alla forma delle particelle. Nelle cartucce per il tempo
di coagulazione attivata Medtronic l'agente attivante utilizzato è il caolino.
Il caolino possiede delle caratteristiche superiori per quanto riguarda
l'attivazione da contatto del processo di coagulazione sanguigna. Le
cartucce HR ACT e HR HTC mostrano una sensibilità ridotta all'eparina;
ciò consente al test del tempo di coagulazione attivata di monitorare
elevati livelli di eparina.
L'obiettivo del test è la rilevazione della formazione di coaguli. I timer per
la coagulazione automatici Medtronic rilevano la formazione di un coagulo
monitorando la velocità di caduta del meccanismo stantuffo/bandierina
contenuto in ogni canale della cartuccia. Lo stantuffo cade rapidamente
attraverso il sangue non coagulato. Quando si forma una rete di fibrina, la
caduta dello stantuffo viene rallentata. Questo rallentamento della velocità
44 Istruzioni per l’uso Italiano
Page 47

di caduta viene rilevato dal sistema foto-ottico situato nel coperchio dello
strumento. La formazione di coaguli viene indicata da un segnale acustico
e il timer di coagulazione si arresta. Lo strumento è in grado di eseguire
simultaneamente 2 test tramite una cartuccia a due canali. I tempi di
coagulazione per ogni canale vengono visualizzati in secondi dopo il
completamento del test. Utilizzando la cartuccia HR HTC, lo strumento
visualizza 2 risultati: uno per il campione con eparinasi e uno per il
campione senza eparinasi. Sul display del pannello anteriore è possibile
alternare la visualizzazione tra i tempi di coagulazione dei singoli canali
oppure tra la media e la differenza dei risultati dei due canali. Quando si
utilizza la cartuccia HR HTC il valore della media ha poca importanza,
mentre la differenza tra i due risultati rappresenta il prolungamento del
tempo di coagulazione dovuto alla presenza di eparina nel campione.
4. Reagenti
Ogni camera del reagente della cartuccia contiene 0,1 ml di buffer HEPES
(acido idrossietil-piperazinil-etansolfonico), caolino, cloruro di calcio e
azoturo di sodio come agente batteriostatico. Il canale denominato
"HR HTC" contiene eparinasi liofilizzata e altamente purificata con agenti
stabilizzanti e azoturo di sodio come agente batteriostatico.
La cartuccia HR HTC può essere preriscaldata per un massimo di 2 ore.
Una volta introdotto il campione nella cartuccia preriscaldata, è
necessario procedere immediatamente all'esecuzione del test.
5. Conservazione
La cartuccia HR HTC deve essere conservata in un ambiente stabile,
nell'intervallo compreso tra 2 °C e 10 °C (36 °F e 50 °F) oppure tra 10 °C
e 25 °C (50 °F e 77 °F). Le cartucce sono confezionate in contenitori
sigillati, contenenti 2 cartucce ciascuno. Le cartucce sono stabili per il
periodo di tempo indicato sull'etichetta del contenitore. Non utilizzare le
cartucce dopo la data di scadenza. Non utilizzare la cartuccia in presenza
di deformazioni, fessure o alterazione del colore oppure se il reagente
sembra evaporato o contaminato.
Una volta rotto il sigillo che si trova sul coperchio del contenitore, le
cartucce rimangono stabili per 24 ore se conservate in frigorifero.
Nota: non utilizzare la cartuccia in presenza di segni di congelamento.
6. Strumento
La cartuccia HR HTC è destinata specificamente per l'uso con i timer di
coagulazione automatici Medtronic. Per le istruzioni, consultare il manuale
dell'operatore dello strumento.
Per garantire un funzionamento corretto dello strumento è importante
pulire lo strumento almeno ogni 30 giorni o più frequentemente, se
necessario.
Nota: se il sangue penetra dentro il coperchio dell'attuatore, pulire lo
strumento il prima possibile. Unitamente ad ogni strumento viene fornito in
dotazione un kit di pulizia per l'attuatore (n. di catalogo 303-58). Utilizzare
i materiali contenuti in ciascun kit per effettuare la procedura di pulizia.
Per informazioni dettagliate, consultare il foglio illustrativo incluso nel kit di
pulizia.
7. Raccolta e preparazione dei campioni
Una manipolazione non corretta dei campioni può portare a risultati errati
dei test di coagulazione; la raccolta dei campioni deve pertanto essere
eseguita con cura, impiegando sempre le stesse tecniche di
manipolazione.
Se il sangue viene prelevato dalla vena, la zona in cui viene effettuata la
venopuntura deve essere disinfettata. I primi millilitri di sangue devono
Istruzioni per l’uso Italiano 45
Page 48

essere eliminati per evitare la contaminazione del campione con la
1
2
tromboplastina tissutale.
Nota: non prelevare il sangue da cateteri permanenti eparinizzati o da
altre linee anticoagulate senza aver prima irrigato accuratamente la linea.
In caso di sangue intero fresco, trasferire immediatamente il campione
nella cartuccia e procedere all'esecuzione del test.
8. Istruzioni per l'uso
Questo prodotto deve essere utilizzato solo da personale addestrato.
Materiali forniti:
■
Cartuccia per test con eparinasi ad ampio range (HR HTC), n. di
catalogo 402-07
Materiali necessari non forniti:
■
Timer di coagulazione automatico Medtronic
■
Siringa di plastica con ago (preferibilmente calibro 18 o calibro 19)
Figura 1. Riempimento della cartuccia HR HTC
1. Campione (vista laterale)
2. Campione (vista dall'alto)
Per l'utilizzo con lo strumento ACT Plus™, attenersi alle fasi descritte di
seguito:
1. Nel menu principale, selezionare "Tipo di cartuccia" e premere il tasto
fino a visualizzare l'opzione "HTC". Premere "Invio" per confermare la
selezione.
Nota: prima di eseguire un test è necessario inserire i numeri di lotto
e la data di scadenza delle cartucce e dei controlli.
2. Nel menu principale, inserire i codici relativi a "ID paziente" e
"ID utente". Premere "Invio" per confermare.
3. Preriscaldare la cartuccia per 3 - 5 minuti prima di prelevare il
campione da sottoporre al test.
4. Picchiettare la cartuccia per rimettere in sospensione il reagente.
5. Introdurre 0,4 ml di campione in ogni camera.
Nota: riempire prima il canale HR e, successivamente, il canale
HR HTC per garantire che il canale HR non venga contaminato
dall'eparinasi.
6. Inserire la cartuccia nello strumento ACT Plus e chiudere il blocco di
riscaldamento dell'attuatore per iniziare il test.
46 Istruzioni per l’uso Italiano
Page 49

7. La formazione di coaguli è indicata dall'emissione di un segnale
acustico; il blocco di riscaldamento dell'attuatore si apre e i risultati
vengono visualizzati sul display.
Alla fine del test, gettare la cartuccia, la siringa e l'ago in contenitori
omologati per lo smaltimento dei rifiuti a rischio biologico.
9. Risultati
La risposta all'eparina del tempo di coagulazione attivata varia
notevolmente da soggetto a soggetto.12 Il tempo di coagulazione attivata è
influenzato da vari farmaci, in particolare dagli inibitori dell'attivazione
piastrinica.15 Il tempo di coagulazione attivata di un soggetto può essere
condizionato da una serie di altri fattori, ad esempio i livelli di antitrombina
III, la potenza dell'eparina, un deficit dei fattori di coagulazione,
l'attivazione del campione, le coagulopatie da consumo, un'eccessiva
diluizione del campione o la temperatura del campione stesso. Tali fattori
devono essere presi in considerazione nell'interpretazione dei risultati del
test per il tempo di coagulazione attivata
L'eparinasi nel canale HR HTC della cartuccia possiede un'estrema
specificità per l'eparina. La quantità di eparinasi è sufficiente a garantire
l'eliminazione rapida di 6 unità/ml di eparina dal campione, in modo da
riportare quest'ultimo a una condizione basale (non eparinizzata). Il tempo
basale può essere più o meno corrispondente ai valori normali. Se il
valore basale ottenuto dal canale HR HTC non rientra nell'intervallo dei
valori normali, ciò indica la presenza di un altro fattore, diverso
dall'eparina, responsabile del prolungamento del tempo di coagulazione
basale.
Esempio di interpretazione dei risultati ottenuti con la cartuccia HR HTC:
Cn 1 Cn 2 Interpretazione
120 120 Paziente con valore basale, campione privo
120 260 Paziente con sangue eparinizzato. Il prolun-
260 260 Il paziente presenta una coagulopatia di
260 360 Paziente con sangue eparinizzato e con una
60 200 Paziente con sangue eparinizzato e sistema
di eparina.
gamento del tempo è dovuto esclusivamente
alla presenza dell'eparina.
base indipendente dalla presenza di eparina.
coagulopatia di base (probabilmente dovuta
ad emodiluizione).
di coagulazione attivato.
2,5,11
.
10. Limitazioni della procedura
Per ottenere tempi di coagulazione attivata accurati e coerenti con la
cartuccia HR HTC, è necessario rispettare le seguenti condizioni:
■
Il blocco di riscaldamento dello strumento e la cartuccia devono avere
entrambi una temperatura di 37 °C ± 0,5 °C (98,6 °F ± 0,9 °F). Una
volta inserita nel blocco di riscaldamento dello strumento, la cartuccia
raggiungerà la temperatura del blocco in 3 - 5 minuti.
■
È necessario procedere alla risospensione completa dell'attivatore
(caolino).
■
Il sangue non deve contenere tromboplastina tissutale. Il test deve
essere eseguito il prima possibile dopo il prelievo di sangue.
■
La diagnosi del paziente e la terapia devono essere annotate. I
farmaci possono alterare i tempi di coagulazione. È necessario
procedere a un nuovo prelievo e ad una nuova analisi qualora si
ottengano risultati anomali inspiegabili per i campioni. Se i risultati
sono ancora anomali senza alcuna causa apparente, prelevare un
Istruzioni per l’uso Italiano 47
Page 50

campione in citrato e inviarlo a un laboratorio clinico per sottoporlo ad
analisi specifiche per la coagulazione.
■
Per ottimizzare la precisione, tutte le variabili tecniche devono essere
mantenute costanti da un test all'altro.
■
Una volta inserito il campione nella cartuccia, il test dovrà essere
eseguito il più rapidamente possibile. L'eliminazione dell'eparina dal
campione avviene rapidamente. L'attivazione da contatto nella
cartuccia avverrà non appena l'eparina è stata eliminata dal
campione. Ciò provocherà una riduzione dei tempi di coagulazione
man mano che avviene l'attivazione del campione.
■
Le metodiche utilizzate durante un bypass cardiopolmonare sono in
continua evoluzione e le caratteristiche dei pazienti sottoposti a
questa procedura possono variare. Le condizioni in grado di
influenzare i risultati di un test del tempo di coagulazione attivata
includono tra l'altro:
■
la sensibilità del paziente all'eparina
■
la diluizione dei fattori della coagulazione dovuta al circuito
extracorporeo
■
l'uso di emoderivati citratati
■
l'uso di farmaci antipiastrinici
■
l'ipotermia
■
la variazione dei livelli di calcio
■
un'alterazione della conta o della funzione piastrinica
■
la presenza di coagulopatie non note
Un'eccessiva emodiluizione durante una procedura di bypass, dovuta
di frequente al desiderio di limitare la somministrazione di emoderivati
eterologhi, può comportare delle emorragie postoperatorie. In casi
gravi, l'entità della diluizione può essere tale da impedire la
coagulazione, come rilevato dalla misurazione del tempo di
coagulazione attivata. La presenza di una quantità sufficiente di fattori
della coagulazione nel plasma non può essere determinata mettendo
in correlazione il grado di diluizione con l'ematocrito del paziente. Di
frequente i pazienti ricevono trasfusioni di concentrati eritrocitari lavati
senza compensare il volume di plasma perduto. Se nel canale
dell'eparinasi della cartuccia HR HTC (canale n. 1), dopo la
neutralizzazione dell'eparina nel sangue del paziente ad opera della
protamina, non si verifica alcuna coagulazione, esistono forti
probabilità che ci si trovi di fronte a una coagulopatia da
emodiluizione.
Avvertenza: la cartuccia HR HTC, data la sua particolare
formulazione, non va utilizzata per monitorare una terapia
anticoagulante regionale ottenuta tramite l'infusione di citrato.
Attenzione: agire con estrema cautela per evitare che l'eparinasi
contenuta nel canale HR HTC venga inavvertitamente trasferita al
campione presente nel canale HR della cartuccia. In tal caso infatti il
tempo di coagulazione del campione eparinizzato nel canale "HR" non
sarebbe più rappresentativo della quantità di eparina contenuta nel
campione, ma indicherebbe una quantità di eparina inferiore, in base
alla quantità di eparinasi trasferita. Per questo motivo si raccomanda
vivamente di procedere per prima cosa al riempimento del canale
"HR", in modo da minimizzare le probabilità di un trasferimento
dell'eparinasi.
Per le precauzioni e i limiti dello strumento, consultare il manuale
dell'operatore.
11. Valori previsti
Il canale con eparinasi fornisce in maniera efficace il tempo di
coagulazione attivata basale su campioni di sangue fresco intero
48 Istruzioni per l’uso Italiano
Page 51

eparinizzato. Durante una procedura di bypass, il valore basale del tempo
di coagulazione attivata può tendere a un innalzamento, che rispecchia
l'emodiluizione del sangue del paziente. Il tempo di coagulazione basale è
correlato alla diluizione dei fattori della coagulazione contenuti nel plasma,
che a sua volta non è necessariamente correlata all'ematocrito del
paziente. Il recupero degli eritrociti tramite un sistema di autotrasfusione
non compensa la perdita dei fattori di coagulazione contenuti nel plasma.
Se il tempo di coagulazione attivata basale rimane maggiore della norma,
si può verificare una coagulazione da emodiluizione (ovvero una
mancanza dei fattori della coagulazione), con possibili emorragie in fase
postoperatoria. Con la cartuccia HR HTC è possibile monitorare
l'insorgenza di questa condizione, consentendo di intraprendere delle
misure correttive prima che la diluizione dei fattori della coagulazione
possa assumere dimensioni gravi.
12. Caratteristiche di prestazione specifiche
Le cartucce per il tempo di coagulazione attivata con un intervallo del
tempo di coagulazione compreso tra 0 e 600 secondi in genere non
superano una variazione del 12% tra campioni in duplicato per lo stesso
soggetto. In caso di livelli elevati di eparina e tempi di coagulazione oltre i
600 secondi, il tempo di coagulazione attivata non viene generalmente
considerato adeguatamente affidabile per determinare i livelli di eparina.
La cartuccia HR HTC è formulata in modo da generare un HR ACT
normale nel canale denominato "HR", che corrisponde in modo accurato
alle risposte rilevate per la prima volta da Bull et al. (1975). Il caolino, che
funge da attivatore in ciascun lotto di cartucce, è stato calibrato in modo
da ridurre la variabilità dell'attività interlotti a meno del 10% e minimizzare
la deriva a lungo termine.
Le prestazioni del canale "basale" della cartuccia sono dipendenti
dall'attività dell'eparinasi nel canale denominato "HR HTC". L'eparinasi è
stata sottoposta a un processo di purificazione e stabilizzazione ed è in
grado di eliminare 6 unità/ml di eparina in un periodo di tempo
sufficientemente breve da riportare il tempo di coagulazione del sangue
eparinizzato al valore basale. La stabilità dell'eparinasi è garantita
mantenendo le cartucce a una temperatura costante. Le cartucce
possono essere conservate agli intervalli seguenti: 2 °C–10 °C
(36 °F–50 °F), o 10 °C–25 °C (50 °F–77 °F). Le prestazioni delle cartucce
possono deteriorarsi se il prodotto non viene conservato in un ambiente
stabile. Si sconsiglia di sottoporre ripetutamente il prodotto al passaggio
da una temperatura di frigorifero a una temperatura ambiente e viceversa.
13. Controllo qualità
Per garantire prestazioni adeguate dello strumento e delle cartucce è
necessario eseguire il test HTC con due livelli di controlli.
I risultati devono rientrare all'interno degli intervalli specifici indicati dal
produttore o all'interno degli intervalli determinati dall'operatore.
I controlli per il test con eparinasi ad ampio range sono: il controllo di
coagulazione CLOTtrac™ HR (n. di catalogo 550-07) e il controllo
CLOTtrac HTC (n. di catalogo 550-12).
Il controllo CLOTtrac HTC fornisce il valore HR ACT basale nel canale
HR HTC e supera il tempo massimo (>999) nel canale HR ACT.
Si tratta di un controllo liofilizzato contenente 6 unità/ml di eparina. Le
prestazioni del canale HR HTC di una cartuccia vengono verificate
eseguendo un test con il controllo e ottenendo un valore HR ACT basale
nel canale denominato "HR HTC" e un valore di tempo massimo
(999 secondi) nel canale denominato "HR". Ciò indica il funzionamento
corretto del canale della cartuccia contenente eparinasi.
Istruzioni per l’uso Italiano 49
Page 52

14. Bibliografia
1. Baugh RF, Deemar KA, Zimmerman JJ. Heparinase in the activated
clotting time assay: Monitoring heparin-independent alterations in
coagulation function. Anesth Analg. 1992;74:201.
2. Bode AP, Eick L. Lysed platelets shorten the activated coagulation
time (ACT) of heparinized blood. Am J Clin Pathol. 1989;91:430.
3. Bull BS, Korpman RA, Huse WM, Briggs BD. Heparin therapy during
extracorporeal circulation. I. Problems inherent in existing heparin
protocols. J Thorac Cardiovasc Surg. 1975;69:674.
4. Bull BS, Huse WM, Brauer FS, Korpman RA. Heparin therapy during
extracorporeal circulation. II. The use of a dose-response curve to
individualize heparin and protamine dosage. J Thorac Cardiovasc
Surg. 1975;69:685.
5. Culliford AT, Gitel SN, Starr N, Thomas ST, Baumann FG, Wessler S,
Spencer FC. Lack of correlation between activated clotting time and
plasma heparin during cardiopulmonary bypass. Ann Surg.
1981;193:105.
6. Dietrich CP, Silva ME, Michelacci YM. Sequential degradation of
heparin in Flavobacterium heparinum. Purification and properties of
five enzymes involved in heparin degradation. J Biol Chem.
1973;248:6408.
7. Effeney DJ, Goldstone J, Chin D, Krupski WC, Ellis RJ. Intraoperative
anticoagulation in cardiovascular surgery. Surgery. 1981;90:1068.
8. Forman WB, Bayer G. A simplified method for monitoring heparin
therapy at the bedside: The activated whole blood clotting time. Am J
Hematol. 1981;11:277.
9. Hattersley PG. Progress report: The activated coagulation time of
whole blood (ACT). Am J Clin Pathol. 1976;66:899.
10. Hutt ED, Kingdon HS. Use of heparinase to eliminate heparin
inhibition in routine coagulation assays. J Lab Clin Med.
1972;79:1027.
11. Kesteven PJ, Pasaoglu I, Williams BT, Savidge GG. Significance of
the whole blood activated clotting time in cardiopulmonary bypass. J
Cardiovasc Surg. 1986;27:85.
12. Mabry CD, Read RC, Thompson BW, Williams GD, White HJ.
Identification of heparin resistance during cardiac and vascular
surgery. Arch Surg. 1979;114:129.
13. Mabry CD, Thompson BW, Read RC. Activated clotting time (ACT)
monitoring of intraoperative heparinization in peripheral vascular
surgery. Am J Surg. 1979;138:894.
14. Mabry CD, Thompson, BW, Read RC, Campbell GS. Activated
clotting time monitoring of intraoperative heparinization: Our
experience and comparison with two techniques. Surgery.
1981;90:889.
15. Moorehead MT, Westengard JC, Bull BS. Platelet involvement in the
activated coagulation time of heparinized blood. Anesth Analg.
1984;63:394.
16. Yang VC, Linhardt RJ, Bernstein H, Cooney CL, Langer R.
Purification and characterization of heparinase from Flavobacterium
heparinum. J Biol Chem. 1985;260:1849.
50 Istruzioni per l’uso Italiano
Page 53

15. Esclusione dalla garanzia
LA SEGUENTE ESCLUSIONE DALLA GARANZIA È VALIDA
SOLO PER I CLIENTI AL DI FUORI DEGLI STATI UNITI:
SEBBENE LA CARTUCCIA PER IL TEST CON EPARINASI AD AMPIO
RANGE, INDICATA DI SEGUITO COME "PRODOTTO", SIA STATA
ACCURATAMENTE PROGETTATA, REALIZZATA E TESTATA PRIMA
DI ESSERE COMMERCIALIZZATA, POTREBBE NON FUNZIONARE IN
MODO SODDISFACENTE PER DIVERSE RAGIONI. LE AVVERTENZE
INDICATE NELLA DOCUMENTAZIONE DEL PRODOTTO
FORNISCONO INFORMAZIONI PIÙ DETTAGLIATE A TALE
RIGUARDO E SONO DA CONSIDERARSI PARTE INTEGRANTE
DELLA PRESENTE ESCLUSIONE DALLA GARANZIA. DI
CONSEGUENZA, MEDTRONIC NON RILASCIA ALCUNA GARANZIA,
NÉ ESPRESSA NÉ TACITA, IN MERITO AL PRODOTTO. MEDTRONIC
NON PUÒ IN ALCUN CASO ESSERE RITENUTA RESPONSABILE
PER DANNI INCIDENTALI O CONSEQUENZIALI CAUSATI DALL'USO,
DA DIFETTI O DA MANCANZE DEL PRODOTTO,
INDIPENDENTEMENTE DAL FATTO CHE LA RICHIESTA DI
RISARCIMENTO DI TALI DANNI SIA BASATA SU GARANZIA,
CONTRATTO, FATTO ILLECITO O ALTRO.
Le esclusioni e le restrizioni di cui sopra non vanno intese, né devono
essere interpretate in quanto tali, come contrarie a norme ritenute
inderogabili dalla legislazione vigente. Nel caso in cui una parte o un
termine della presente Esclusione dalla garanzia venga giudicato illegale,
inefficace o in conflitto con la legge vigente, la validità delle rimanenti parti
della presente Esclusione dalla garanzia non verrà compromessa, e tutti i
diritti e gli obblighi verranno interpretati e applicati come se la presente
Esclusione dalla garanzia non contenesse la parte o i termini ritenuti non
validi.
Istruzioni per l’uso Italiano 51
Page 54

1. Käyttötarkoitus
Hepariinin osoittaminen aktivoidun hyytymisajan perusteella.
In vitro -diagnostiseen käyttöön.
Varoitus: Tuotteen ainutlaatuisen luonteen takia on varmistettava
huolellisesti, ettei heparinaasia siirretä vahingossa testiputken HR HTC
-kanavasta HR-kanavaan. kohta 8 ja kohta 10 sisältävät lisätietoja.
2. Yhteenveto
Medtronic High Range -heparinaasitestiputki eli HR HTC -testiputki on
aktivoidun hyytymisajan mittauksessa käytettävän High Range
-testiputken (HR ACT -testiputken) muunnelma, jota käytetään Medtronic-
yhtiön automaattisten hyytymisaikamittareiden kanssa. Aktivoidun
hyytymisajan testin kuvasi ensimmäisenä Hattersley vuonna 19669. Testiä
ja sen muunnelmia on käytetty laajasti hepariinin
hyytymisenestovaikutuksen tarkkailuun
käytetään tuoretta kokoverinäytettä samoin kuin HR ACT -testiputkessa.
Testiputken erona on se, että yhdessä kanavassa (HR HTC) on
puhdistettua bakteerien tuottamaa heparinaasia. Heparinaasi tuhoaa
nopeasti ja spesifisesti verinäytteessä olevan hepariinin
Testiputkessa oleva heparinaasimäärä poistaa nopeasti 6 yksikköä
hepariinia millilitrassa. Heparinaasikanavasta saadaan hyytymisaika, joka
vastaa lähtötilannetta eli heparinisoimattoman näytteen hyytymisaikaa,
vaikka näyte sisältääkin hepariinia. Testiputken toinen kanava on normaali
HR ACT -kanava, ja siitä saatava hyytymisaika on heparinisoidun
näytteen aktivoitu hyytymisaika. Tätä testiputkea käyttämällä voidaan
1) varmistaa, että näytteessä on hepariinia ennen leikkausta, 2) arvioida
sydän-keuhkokoneen käytön vaikutusta lähtötilanteen aktivoituun
hyytymisaikaan, 3) vahvistaa hepariinin kumoaminen protamiinin annon
jälkeen, 4) osoittaa leikkauksen jälkeinen hepariinin rebound-ilmiö ja
5) osoittaa hepariini potilaissa, joilla on runsasta verenvuotoa leikkauksen
jälkeen. Saatavilla on CLOTtrac™ HTC -kontrolli, jolla voidaan varmistaa,
että testiputki toimii määritysten mukaisesti.
3, 4, 7, 8, 13, 14
. HR HTC -testiputkessa
1, 6, 10, 16
.
3. Periaatteet
Aktivoidun hyytymisajan testillä mitataan pintakontaktin kautta
aktivoituneen tuoreen kokoveren hyytymisaika. Hattersleyn
alkuperäisessä menettelyssä käytettiin aktivoivana aineena piimaata.
Piimaan aikaansaama kontaktiaktivaatio vaihtelee sen puhtauden,
esiintymäpaikan sekä hiukkasten koon ja muodon mukaan. Medtronicyhtiön aktivoidun hyytymisajan testiputkissa käytetään kaoliinia
aktivoivana aineena. Kaoliinilla on erinomaiset veren hyytymisen
kontaktiaktivaatio-ominaisuudet. HR ACT- ja HR HTC -testiputket ovat
vähemmän herkkiä hepariinille, jolloin aktivoidun hyytymisajan testillä
voidaan seurata suuria hepariinipitoisuuksia.
Testi päättyy, kun hyytymän muodostuminen havaitaan. Medtronic-yhtiön
automaattiset hyytymisaikamittarit havaitsevat hyytymän muodostumisen
seuraamalla testiputken kussakin kanavassa olevan mäntälippumekanismin laskunopeutta. Mäntäyksikkö laskeutuu nopeasti
hyytymättömässä veressä. Kun fibriiniverkko muodostuu, mäntäyksikön
laskunopeus hidastuu. Laitteen kansikokoonpanossa oleva valo-optinen
järjestelmä havaitsee tämän laskunopeuden hidastumisen. Hyytymisen
muodostuminen ilmoitetaan äänimerkillä, ja silloin hyytymisaikamittari
pysähtyy. Laitteilla voidaan tehdä samanaikaisesti kaksi testiä käyttämällä
kaksikanavaista testiputkea. Kun testi on päättynyt, kunkin kanavan
hyytymisajat näkyvät näytössä sekunteina. HR HTC -testiputkea
käytettäessä laite näyttää kaksi tulosta: yhden heparinaasia sisältävälle
näytteelle ja yhden näytteelle, jossa ei ole heparinaasia. Etupaneelin
näyttöön voidaan vaihtaa vuorotellen yksittäisten kanavien hyytymisaika
52 Käyttöohjeet Suomi
Page 55

tai kahden kanavan keskiarvo ja niiden välinen ero. HR HTC -testiputkea
käytettäessä keskiarvolla ei ole juuri merkitystä, mutta kahden tuloksen
välinen ero vastaa hyytymisajan pidentymistä näytteessä olevan
hepariinin takia.
4. Reagenssit
Kunkin testiputken reagenssikammiossa on 0,1 ml
hydroksietyylipiperatsiinietaanisulfonihappo- eli HEPES-puskuria,
kaoliinia, kalsiumkloridia ja natriumatsidia bakteriostaattisena aineena.
Kanava, jossa on merkintä HR HTC, sisältää lyofilisoitua,
erityispuhdistettua heparinaasia ja stabilointiaineita sekä natriumatsidia
bakteriostaattisena aineena.
HR HTC -testiputkea voidaan esilämmittää enintään 2 tuntia. Kun näyte
on lisätty esilämmitettyyn testiputkeen, testi on käynnistettävä heti.
5. Säilyttäminen
HR HTC -testiputkea on säilytettävä vakaassa ympäristössä joko
2–10 °C:ssa (36–50 °F:ssa) tai 10–25 °C:ssa (50–77 °F:ssa). Testiputket
on pakattu suljetuille tarjottimille, joilla on kaksi testiputkea. Testiputket
ovat vakaita tarjottimen etikettiin merkityn ajan. Älä käytä testiputkia
viimeisen käyttöpäivämäärän jälkeen. Älä käytä testiputkea, jos sen väri
näyttää muuttuneen, jos se näyttää haljenneen tai vääntyneen tai jos
reagenssi näyttää haihtuneen tai kontaminoituneen.
Kun tarjottimen kannen sinetti on murrettu, testiputket ovat vakaita
24 tuntia jääkaappilämpötilassa.
Huomautus: Älä käytä tuotetta, jos siinä on merkkejä jäätymisestä.
6. Laite
HR HTC -testiputki on suunniteltu käytettäväksi erityisesti Medtronicyhtiön automaattisissa hyytymisaikamittareissa. Katso ohjeet laitteen
käyttöoppaasta.
Jotta laite toimisi asianmukaisesti, se on tärkeää puhdistaa vähintään
30 päivän välein tai tarvittaessa useammin.
Huomautus: Jos verta pääsee toimilaitteen kannelle, puhdista laite
mahdollisimman pian. Kunkin laitteen mukana toimitetaan toimilaitteen
puhdistuspakkaus (luettelonumero 303–58). Käytä puhdistuksessa
kussakin puhdistuspakkauksessa olevia materiaaleja. Katso tarkat tiedot
puhdistuspakkauksen pakkausselosteesta.
7. Näytteen ottaminen ja valmistaminen
Jos näytteitä käsitellään väärin, hyytymistestitulokset voivat olla
virheellisiä. Siksi näytteet on otettava huolellisesti ja niiden käsittelyssä on
käytettävä yhdenmukaisia menetelmiä.
Jos verinäyte otetaan laskimopunktiolla, punktiokohdan on oltava puhdas.
Hävitä monta ensimmäistä verimillilitraa, jotta kudostromboplastiini ei
kontaminoi näytettä.
Huomautus: Älä ota verinäytettä heparinisoiduista pitkäaikaisista
katetreista tai muista antikoaguloiduista letkuista ilman letkun
perusteellista huuhtelua.
Jos testaat tuoretta kokoverta, siirrä näyte heti testiputkeen ja käynnistä
testi.
8. Käyttöohjeet
Tuote on tarkoitettu vain koulutettujen henkilöiden käyttöön.
Toimitetut materiaalit:
■
High Range -heparinaasitestiputki (HR HTC), luettelonumero 402-07.
Tarvittavat materiaalit, jotka eivät sisälly toimitukseen:
Käyttöohjeet Suomi 53
Page 56

■
1
2
Medtronic-yhtiön automaattinen hyytymisaikamittari
■
muoviruisku, jossa on neula (mieluiten 18 tai 19 G).
Kuva 1. HR HTC -testiputken täyttäminen
1. Näyte (sivusta katsottuna)
2. Näyte (ylhäältä katsottuna)
Jos käytät ACT Plus™ -laitetta, noudata seuraavia ohjeita:
1. Valitse Main Menu (Päävalikko) -näytöstä Cartridge Type
(Testiputkityyppi) ja paina näppäintä, kunnes näytössä näkyy HTC.
Vahvista valinta painamalla Enter (Syötä) -näppäintä.
Huomautus: Testiputkien ja kontrollien eränumerot ja viimeiset
käyttöpäivät on syötettävä ennen testin tekemistä.
2. Syötä Main Menu (Päävalikko) -näytöstä Patient ID (Potilastunnus) ja
User ID (Käyttäjätunnus) numeroina. Vahvista painamalla Enter
(Syötä) -näppäintä.
3. Esilämmitä testiputkea 3–5 minuutin ajan ennen testinäytteen
ottamista.
4. Resuspendoi reagenssi taputtamalla testiputkea.
5. Täytä kuhunkin kanavaan 0,4 ml näytettä.
Huomautus: Täytä aina HR-kanava ensin ja HR HTC -kanava sitten,
jotta heparinaasi ei kontaminoi HR-kanavaa.
6. Aseta testiputki ACT Plus -laitteeseen ja käynnistä testi sulkemalla
toimilaitteen lämmitin.
7. Kun hyytymä muodostuu, laite antaa äänimerkin, toimilaitteen
lämmitin avautuu ja tulokset tulevat näyttöön.
Kun testi on päättynyt, hävitä testiputki, ruisku ja neula laittamalla ne
hyväksyttyihin tartuntavaarallisten jätteiden astioihin.
9. Tulokset
Aktivoidun hyytymisajan vaste hepariiniin vaihtelee huomattavasti eri
henkilöillä12. Useat lääkkeet ja etenkin verihiutaleiden aktivaatiota estävät
lääkkeet vaikuttavat aktivoituun hyytymisaikaan15. Henkilön aktivoidun
hyytymisajan vaste hepariiniin voi riippua useista muistakin tekijöistä,
kuten antitrombiini III:n pitoisuudesta, hepariinin vaikutuksen
voimakkuudesta, hyytymistekijöiden puutoksista, näytteen aktivaatiosta,
DIC-oireyhtymästä, näytteen liiasta laimenemisesta ja näytteen
lämpötilasta. Nämä on otettava huomioon tulkittaessa aktivoidun
hyytymisajan testin tuloksia
2, 5, 11
.
54 Käyttöohjeet Suomi
Page 57

Testiputken HR HTC -kanavan heparinaasi on äärimmäisen spesifinen
hepariinille. Heparinaasia on riittävä määrä sen varmistamiseen, että se
poistaa näytteestä nopeasti 6 yksikköä hepariinia millilitrassa niin, että
näyte palaa lähtötilannetta vastaavaan eli heparinisoimattomaan tilaan.
Lähtötilanteen aika saattaa olla normaalilla alueella tai lähellä sitä, mutta
ei välttämättä. Jos lähtötilanteen arvo ei ole normaalilla alueella HR HTC kanavassa, se tarkoittaa, että jokin muu tila kuin veressä oleva hepariini
aiheuttaa lähtötilanteen hyytymisajan pidentymisen.
Esimerkki HR HTC -tulosten tulkinnasta:
Kanava 1
120 120 Potilas lähtötilanteessa; näytteessä ei hepa-
120 260 Potilaan veressä on hepariinia. Pidentymi-
260 260 Potilaalla on koagulopatia, joka ei liity hepa-
260 360 Potilaan veressä on hepariinia, ja hänellä on
60 200 Potilaan veressä on hepariinia, ja hänen hyy-
Kanava 2 Tulkinta
riinia.
nen johtuu vain hepariinin vaikutuksesta.
riiniin.
koagulopatia (todennäköisesti hemodiluutio).
tymisjärjestelmänsä on aktivoitunut.
10. Menettelyn rajoitukset
Noudata seuraavia ohjeita, jotta HR HTC -testiputkella saadut aktivoidut
hyytymisajat olisivat tarkkoja ja yhdenmukaisia:
■
Laitteen lämmittimen ja testiputken lämpötilan on oltava 37 °C
± 0,5 °C (98,6 °F ± 0,9 °F). Testiputki saavuttaa tämän lämpötilan
3–5 minuutissa laitteen lämmittimessä.
■
Kaoliiniaktivaattori on resuspendoitava perusteellisesti.
■
Veressä ei saa olla kudostromboplastiinia. Tee testi mahdollisimman
nopeasti verinäytteen ottamisen jälkeen.
■
Potilaan diagnoosi ja lääkitys on otettava huomioon. Lääkitys voi
muuttaa hyytymisaikoja. Jos näytteillä saadaan epänormaaleja arvoja
selittämättömästä syystä, näytteet on otettava ja testattava uudelleen.
Jos tulokset ovat vieläkin epänormaaleja eikä siihen löydy syytä,
näytteeseen on lisättävä sitraattia ja se on lähetettävä kliiniseen
laboratorioon erityistä hyytymisanalyysia varten.
■
Jotta tarkkuus olisi mahdollisimman hyvä, kaikki tekniset muuttujat on
pidettävä vakioina testistä toiseen.
■
Kun näyte on siirretty testiputkeen, testi on tehtävä mahdollisimman
nopeasti. Hepariini poistuu näytteestä nopeasti. Testiputkessa
tapahtuu kontaktiaktivaatiota, kun näytteessä ei ole hepariinia. Tämä
johtaa lyhyempiin hyytymisaikoihin näytteen aktivaation edetessä.
■
Sydän-keuhkokoneen avulla tehtävien leikkausten menetelmät
muuttuvat jatkuvasti, samoin myös potilaspopulaation ominaisuudet.
Aktivoidun hyytymisajan testin tuloksiin vaikuttavia olosuhteita voivat
olla muun muassa seuraavat:
■
potilaan herkkyys hepariinille
■
hyytymistekijöiden laimeneminen kehonulkoisen verenkierron
vaikutuksesta
■
sitraattiverivalmisteiden käyttäminen
■
antitrombosyyttilääkkeiden käyttäminen
■
hypotermia
■
vaihtelevat kalsiumpitoisuudet
■
muutos trombosyyttien toiminnassa tai määrässä
■
tuntemattomat koagulopatiat.
Käyttöohjeet Suomi 55
Page 58

Veren liiallinen laimeneminen sydän-keuhkokoneen käytön aikana,
johon on usein syynä se, että halutaan rajoittaa heterologisten
verivalmisteiden käyttöä, voi johtaa leikkauksen jälkeiseen
verenvuotoon. Vaikeissa tapauksissa laimeneminen voi olla niin
runsasta, että aktivoidulla hyytymisajalla mitattavissa olevaa
hyytymistä ei tapahdu. Plasman hyytymistekijöiden riittävyyttä ei voi
määrittää korreloimalla laimenemisen astetta potilaan hematokriitin
kanssa. Usein potilaalle on annettu pestyjä soluja korvaamatta
menetettyä plasmaa. Jos HR HTC -testiputken heparinaasikanava
(kanava 1) ei hyydy, kun potilaan hepariini on kumottu protamiinilla,
on erittäin mahdollista, että potilaalla on dilutionaalinen koagulopatia.
Vaara: HR HTC -testiputken koostumuksen takia sitä ei saa käyttää
sitraatti-infuusiolla aikaansaadun paikallisen antikoagulaation
seurantaan.
Varoitus: Erityisen huolellisesti on varmistettava, että HR HTC kanavan heparinaasia ei siirretä vahingossa testiputken HR-kanavan
näytteeseen. Jos näin käy, HR-kanavan heparinisoidun näytteen
hyytymisaika ei enää edusta näytteessä olevaa hepariinimäärää vaan
osoittaa pienempää hepariinipitoisuutta sen mukaan, kuinka paljon
heparinaasia kanavaan siirrettiin. Tästä syystä on erittäin
suositeltavaa täyttää ensin HR-kanava, jotta heparinaasin siirtymisen
mahdollisuus saadaan minimoitua.
Katso laitetta koskevat varotoimet ja rajoitukset käyttöoppaasta.
11. Odotettavissa olevat arvot
Heparinaasikanavan avulla saadaan mitattua tehokkaasti lähtötilanteen
aktivoitu hyytymisaika tuoreesta heparinisoidusta kokoverestä. Sydänkeuhkokoneen käytön aikana lähtötilanteen aktivoitu hyytymisaika saattaa
pidentyä potilaan hemodiluution takia. Lähtötilanteen hyytymisaika korreloi
plasman hyytymistekijöiden laimenemisen kanssa; hyytymistekijöiden
laimeneminen ei välttämättä korreloi potilaan hematokriitin kanssa.
Potilaaseen veripesurista palautetut punasolut eivät korvaa menetettyjä
plasman hyytymistekijöitä. Jos lähtötilanteen aktivoitu hyytymisaika pysyy
pidentyneenä, seurauksena saattaa olla dilutionaalinen koagulopatia
(hyytymistekijöiden riittämättömyys) ja leikkauksen jälkeinen verenvuoto.
HR HTC -testiputken avulla voidaan seurata tämän tilanteen kehittymistä
ja korjata tilanne, ennen kuin hyytymistekijöiden laimeneminen on
vakavaa.
12. Erityiset toiminnalliset ominaisuudet
Käytettäessä aktivoidun hyytymisajan testiputkia, joiden hyytymisaika-alue
on 0–600 sekuntia, yhden henkilön kahden näytteen välinen vaihtelu ei
tavallisesti ole yli 12 %. Jos hepariinipitoisuus on suuri ja hyytymisaika on
yli 600 sekuntia, aktivoitua hyytymisaikaa ei tavallisesti pidetä riittävän
luotettavana hepariinipitoisuuksien määrittämiseen.
HR HTC -testiputken koostumus on valittu niin, että se tuottaa normaalin
HR ACT -hyytymisajan HR-kanavassa, mikä vastaa läheisesti alun perin
lähteessä Bull et al (1975) raportoituja vasteita. Kunkin testiputkierän
kaoliiniaktivaattori on kalibroitu niin, että sen aktiivisuuden vaihtelu eri
erien välillä on alle 10 % ja pitkäaikainen vaihtelu on minimaalinen.
Testiputken lähtötilannetta vastaavan kanavan toiminta riippuu
heparinaasin aktiivisuudesta HR HTC -kanavassa. Heparinaasi on
puhdistettu ja stabiloitu niin, että se poistaa 6 yksikköä hepariinia
millilitrassa ajassa, joka on riittävän lyhyt palauttamaan heparinisoidun
veren hyytymisajan lähtötilanteen hyytymisajaksi. Heparinaasin stabiilius
varmistetaan pitämällä testiputket vakiolämpötilassa. Testiputket voidaan
säilyttää joko 2–10 °C:ssa (36–50 °F:ssa) tai 10–25 °C:ssa
(50–77 °F:ssa). Testiputken toiminta voi heikentyä, jos tuotetta ei säilytetä
56 Käyttöohjeet Suomi
Page 59

vakaassa ympäristössä. Tuotteen toistuvaa siirtämistä jääkaapista
huoneenlämpöön tai huoneenlämmöstä jääkaappiin ei suositella.
13. Laaduntarkkailu
HTC-testille on tehtävä kaksitasoiset kontrollit, jotta laitteen ja testiputkien
asianmukainen toiminta saadaan varmistettua.
Tulosten on oltava valmistajan antamilla tai käyttäjän määrittämillä
alueilla.
High Range -heparinaasitestin kontrolleja ovat CLOTtrac™ HR
-hyytymiskontrolli (luettelonumero 550-07) ja CLOTtrac HTC -kontrolli
(luettelonumero 550-12).
CLOTtrac HTC -kontrollilla saadaan lähtötilanteen HR ACT -aika HR HTC
-kanavasta, ja se saa aikaan aikakatkaisun (> 999) HR ACT -kanavassa.
Tämä kontrolli on lyofilisoitu kontrolli, jossa on hepariinia 6 yksikköä/ml.
HR HTC -testiputken toiminta varmistetaan käyttämällä kontrollia
testiputkessa, jolloin saadaan lähtötilanteen HR ACT -arvo HR HTC
-kanavasta ja aikakatkaisu (999 sekuntia) HR-kanavasta. Tämä osoittaa,
että testiputken heparinaasia sisältävä kanava toimii oikein.
14. Lähteet
1. Baugh, R. F.; Deemar, K. A.; Zimmerman, J. J. Heparinase in the
activated clotting time assay: Monitoring heparin-independent
alterations in coagulation function. Anesth Analg. 1992; 74: 201.
2. Bode, A. P.; Eick, L. Lysed platelets shorten the activated coagulation
time (ACT) of heparinized blood. Am J Clin Pathol. 1989; 91: 430.
3. Bull, B. S., Korpman, R. A., Huse, W. M., Briggs, B. D. Heparin
therapy during extracorporeal circulation. I. Problems inherent in
existing heparin protocols. J Thorac Cardiovasc Surg. 1975; 69: 674.
4. Bull, B. S.; Huse, W. M.; Brauer, F. S.; Korpman, R. A. Heparin
therapy during extracorporeal circulation. II. The use of a doseresponse curve to individualize heparin and protamine dosage. J
Thorac Cardiovasc Surg. 1975; 69: 685.
5. Culliford, A. T.; Gitel, S. N.; Starr, N.; Thomas, S. T.; Baumann, F. G.;
Wessler, S.; Spencer, F. C. Lack of correlation between activated
clotting time and plasma heparin during cardiopulmonary bypass. Ann
Surg. 1981; 193: 105.
6. Dietrich, C. P.; Silva, M. E.; Michelacci, Y. M. Sequential degradation
of heparin in Flavobacterium heparinum. Purification and properties of
five enzymes involved in heparin degradation. J Biol Chem.
1973; 248: 6408.
7. Effeney, D. J.; Goldstone, J.; Chin, D.; Krupski, W. C.; Ellis, R. J.
Intraoperative anticoagulation in cardiovascular surgery. Surgery.
1981; 90: 1068.
8. Forman, W. B.; Bayer, G. A simplified method for monitoring heparin
therapy at the bedside: The activated whole blood clotting time. Am J
Hematol. 1981; 11: 277.
9. Hattersley, P. G. Progress report: The activated coagulation time of
whole blood (ACT). Am J Clin Pathol. 1976; 66: 899.
10. Hutt, E. D.; Kingdon, H. S. Use of heparinase to eliminate heparin
inhibition in routine coagulation assays. J Lab Clin Med.
1972; 79: 1027.
11. Kesteven, P. J.; Pasaoglu, I.; Williams, B. T.; Savidge, G. G.
Significance of the whole blood activated clotting time in
cardiopulmonary bypass. J Cardiovasc Surg. 1986; 27: 85.
12. Mabry, C. D.; Read, R. C.; Thompson, B. W.; Williams, G. D.; White,
H. J. Identification of heparin resistance during cardiac and vascular
surgery. Arch Surg. 1979; 114: 129.
Käyttöohjeet Suomi 57
Page 60

13. Mabry, C. D.; Thompson, B. W.; Read, R. C. Activated clotting time
(ACT) monitoring of intraoperative heparinization in peripheral
vascular surgery. Am J Surg. 1979; 138: 894.
14. Mabry, C. D.; Thompson, B. W.; Read, R. C.; Campbell, G. S.
Activated clotting time monitoring of intraoperative heparinization: Our
experience and comparison with two techniques. Surgery.
1981; 90: 889.
15. Moorehead, M. T.; Westengard, J. C.; Bull, B. S. Platelet involvement
in the activated coagulation time of heparinized blood. Anesth Analg.
1984; 63: 394.
16. Yang, V. C., Linhardt, R. J.; Bernstein, H.; Cooney, C. L.; Langer, R.
Purification and characterization of heparinase from Flavobacterium
heparinum. J Biol Chem. 1985; 260: 1849.
15. Takuuta koskeva vastuuvapauslauseke
SEURAAVA TAKUUTA KOSKEVA
VASTUUVAPAUSLAUSEKE KOSKEE YHDYSVALTOJEN
ULKOPUOLISIA ASIAKKAITA:
VAIKKA HIGH RANGE -HEPARINAASITESTIPUTKI,
JÄLJEMPÄNÄ ”TUOTE”, ON SUUNNITELTU, VALMISTETTU JA
TESTATTU HUOLELLISESTI ENNEN MYYNTIÄ, USEISTA ERI SYISTÄ
SAATTAA JOHTUA, ETTÄ TUOTE EI TOIMI TARKOITETULLA
TAVALLA. TUOTEDOKUMENTAATIOSSA OLEVAT VAROITUKSET
SISÄLTÄVÄT TARKEMPIA LISÄTIETOJA JA KUULUVAT
OLENNAISENA OSANA TÄHÄN TAKUUTA KOSKEVAAN
VASTUUVAPAUSLAUSEKKEESEEN. MEDTRONIC SANOUTUU
SITEN IRTI KAIKISTA TUOTTEESEEN LIITTYVISTÄ
NIMENOMAISISTA JA KONKLUDENTTISISTA TAKUISTA.
MEDTRONIC EI OLE VASTUUSSA MISTÄÄN SATUNNAISESTA TAI
VÄLILLISESTÄ VAHINGOSTA, JOKA ON AIHEUTUNUT TUOTTEEN
KÄYTÖSTÄ, VIASTA TAI TOIMINNAN LAKKAAMISESTA,
RIIPPUMATTA SIITÄ, PERUSTUUKO VAADE TAKUUSEEN,
SOPIMUKSEEN, OIKEUDENLOUKKAUKSEEN TAI MUUHUN
SEIKKAAN.
Yllä mainittuja rajoituksia ei ole tarkoitettu voimassa olevan pakottavan
lainsäädännön vastaisiksi, eikä niitä pidä tällä tavoin tulkita. Mikäli
toimivaltainen tuomioistuin katsoo, että jokin tämän takuuta koskevan
vastuuvapauslausekkeen osa tai ehto on laiton, täytäntöönpanokelvoton
tai ristiriidassa tapaukseen sovellettavan lainsäädännön kanssa, takuuta
koskeva vastuuvapauslauseke säilyy kuitenkin muilta osin voimassa, ja
kaikkia oikeuksia ja velvollisuuksia on tulkittava ja pantava täytäntöön
ikään kuin tämä takuuta koskeva vastuuvapauslauseke ei sisältäisi sitä
erityistä osaa tai ehtoa, joka katsotaan pätemättömäksi.
58 Käyttöohjeet Suomi
Page 61

1. Användningsområde
För användning vid identifiering av närvaro av heparin med användning av
aktiverad koaguleringstid.
För in vitro-diagnostik.
Obs! På grund av denna produkts unika egenskaper måste försiktighet
iakttas för att säkerställa att heparinas inte av misstag överförs från
behållarens ”HR HTC”-kanal till dess ”HR”-kanal. Ytterligare information
finns i Avsnitt 8 och Avsnitt 10.
2. Sammanfattning
Testbehållare för heparinas med högt värde, eller HR HTC, från Medtronic
är en modifiering av behållaren för aktiverad koaguleringstid, högt område
(HR ACT) för den automatiska koaguleringstidtagaren från Medtronic.
Testet för aktiverad koaguleringstid beskrevs ursprungligen av Hattersley
år 19669. Testet och varianter av detta används allmänt vid övervakning
av heparins antikoagulerande effekt
nytaget helblodsprov, precis som i HR ACT-behållaren. Skillnaden med
behållaren är att en kanal innehåller ett renat bakteriellt heparinas
(HR HTC). Detta heparinas förstör snabbt och specifikt det heparin som
finns i blodprovet
6 enheter/ml heparin. Heparinaskanalen producerar en koaguleringstid
som återspeglar provets ohepariniserade koaguleringstid på baslinjen,
trots att provet innehåller heparin. Den andra kanalen i behållaren är en
HR ACT av standardtyp och den koaguleringstid som erhålls är provets
hepariniserade aktiverade koaguleringstid. Användning av behållaren gör
det möjligt att: 1) verifiera närvaron av heparin före en operation,
2) bedöma effekten av bypass på den aktiverade koaguleringstiden på
baslinjen, 3) bekräfta reversering av heparin efter administrering av
protamin, 4) identifiera postkirurgisk ”återaktivering av heparin” samt
5) identifiera närvaron av heparin hos patienter med kraftiga blödningar
efter operationen. En CLOTtrac™ HTC-kontroll finns tillgänglig för att
verifiera att behållaren fungerar enligt specifikationerna.
1,6,10,16
. Mängden närvarande heparinas avlägsnar snabbt
3,4,7,8,13,14
. Vid HR HTC används ett
3. Principer
Testet av aktiverad koaguleringstid mäter koaguleringstiden för nytaget
helblod som aktiverats genom ytkontakt. I Hattersleys ursprungliga metod
användes kiselgur som aktiveringsmedel. Kiselgurhaltig jord uppvisar
olika grader av kontaktaktivering beroende på dess renhetsgrad,
avlagringens källa samt partiklarnas storlek och form. I behållaren för
aktiverad koaguleringstid från Medtronic används kaolin som aktiverande
medel. Kaolin har överlägsna egenskaper för kontaktaktivering av
blodkoagulering. HR ACT och HR HTC uppvisar en minskad känslighet
för heparin, så att höga nivåer av heparin kan övervakas med testet av
aktiverad koaguleringstid.
Testets slutpunkt är detektion av koagelbildning. Den automatiska
koaguleringstidtagaren från Medtronic detekterar koagelbildning genom
att mäta hur snabbt kolven/flaggmekanismen sjunker i respektive kanal i
behållaren. Kolven sjunker snabbt genom blod utan koagel. När ett
fibrinnätverk bildas förhindras kolvens sjunkande. Denna förändring av
sjunkhastigheten detekteras av ett foto-optiskt system i instrumentets
hölje. Koagelbildning indikeras med en ljudsignal och
koaguleringstidtagaren stoppas. Instrumentet kan utföra 2 tester samtidigt
med hjälp av en 2-kanalig behållare. Koaguleringstiderna för varje kanal
visas i sekunder efter avslutat test. Med HR HTC visar instrumentet
2 resultat, ett för provet med heparinas och ett för provet utan heparinas.
Displayen på frontpanelen kan användas för att växla mellan de enskilda
kanalernas koaguleringstider eller medelvärdet och differensen mellan de
båda kanalerna. När HR HTC används har medelvärdesavläsningen liten
Bruksanvisning Svenska 59
Page 62

betydelse, men differensen mellan de båda resultaten är lika med
förlängningen av koaguleringstiden på grund av närvaro av heparin i
provet.
4. Reagens
Varje reagenskammare i behållaren innehåller 0,1 ml
hydroxyetylpiperazinetansulfonsyra (HEPES)-buffert, kaolin, kalciumklorid
och natriumazid som bakteriedödande medel. Kanalen märkt ”HR HTC”
innehåller frystorkat, högrenat heparinas med stabiliseringsmedel och
natriumazid som bakteriehämmande medel.
HR HTC-behållaren kan förvärmas i högst 2 timmar. Så snart provet förs
in i den förvärmda behållaren måste testet startas omedelbart.
5. Förvaring
HR HTC ska förvaras i en stabil omgivning, vid antingen 2 °C till 10 °C
(36 °F till 50 °F) eller 10 °C till 25 °C (50 °F till 77 °F). Behållarna är
förpackade i förseglade brickor med 2 behållare. Behållarna är hållbara
under den tidsperiod som anges på brickans etikett. Använd inte
behållarna efter sista förbrukningsdatum. Använd inte behållaren om den
visar tecken på missfärgning, sprickor eller annan förändring eller om
reagenset verkar ha avdunstat eller förorenats.
Så snart förseglingen på brickans lock har brutits är behållarna hållbara i
24 timmar vid kylskåpstemperatur.
Observera: Använd dem inte om det finns tecken på tidigare nedfrysning.
6. Instrument
HR HTC har utformats specifikt för användning i den automatiska
koaguleringstidtagaren från Medtronic. Se instrumentets bruksanvisning
för instruktioner.
För att säkerställa korrekt instrumentprestanda är det viktigt att rengöra
instrumentet minst var 30:e dag, eller oftare om det behövs.
Observera: Om det kommer blod på aktuatorns hölje ska instrumentet
rengöras så snart som möjligt. En aktuatorrengöringssats
(katalognummer 303-58) medföljer varje instrument. Utför
rengöringsproceduren med hjälp av det material som medföljer i varje
rengöringssats. Se rengöringssatsens bipacksedel för mer information.
7. Provtagning och provberedning
Felaktigt hanterade prover kan ge felaktiga koaguleringstestresultat.
Proverna måste därför tas med omsorg och alla prover måste hanteras på
samma sätt.
Om blodet erhålls genom venpunktion måste venpunktionsstället vara
rent. Kassera de första millilitrarna blod för att undvika att förorena provet
med vävnadstromboplastin.
Observera: Blod får inte tas från hepariniserade kvarkatetrar eller andra
slangar med antikoagulantia utan att slangen först spolas omsorgsfullt.
Vid test av nytaget helblod ska provet omedelbart överföras till behållaren
och testet inledas.
8. Bruksanvisning
Produkten är endast avsedd att användas av utbildade personer.
Material som medföljer:
■
Testbehållare för heparinas med högt värde, (HR HTC),
katalognr 402-07
Material som behövs men inte medföljer
■
Automatisk koaguleringstidtagare från Medtronic
■
Plastspruta med nål (helst 18 eller 19 gauge)
60 Bruksanvisning Svenska
Page 63

1
2
Figur 1. Fylla HR HTC-behållaren
1. Prov (sett från sidan)
2. Prov (sett uppifrån)
För användning med ACT Plus™-instrumentet, följ nedanstående steg:
1. Välj ”Behållartyp” på huvudmenyn och tryck på tangenten tills ”HTC”
visas. Bekräfta valet genom att trycka på ”Enter”.
Observera: Innan ett test kan utföras måste lotnummer och
utgångsdatum för behållare och kontroller anges.
2. Ange ”Patient-ID” och ”Användar-ID” från huvudmenyn. Bekräfta
genom att trycka på ”Enter”.
3. Förvärm behållaren i 3 till 5 minuter innan testprovet tas.
4. Knacka på behållaren för att resuspendera reagenset.
5. Fyll varje kammare med 0,4 ml prov.
Observera: Fyll alltid HR-kanalen först och HR HTC-kanalen därefter
för att säkerställa att heparinas inte förorenar HR-kanalen.
6. Placera behållaren i ACT Plus-instrumentet och starta testet genom
att stänga aktuatorns värmeblock.
7. Koagelbildning anges med en ljudsignal. Aktuatorns värmeblock
öppnas och resultaten visas.
När testet har slutförts ska behållaren, sprutan och nålen kasseras i
godkända behållare för biologiskt riskmaterial.
9. Resultat
Responsen på aktiverad koaguleringstid för heparin varierar avsevärt från
person till person12. Olika läkemedel påverkar den aktiverade
koaguleringstiden, särskilt läkemedel som hämmar trombocytaktivering15.
Ett antal andra faktorer kan påverka responsen på en persons aktiverade
koaguleringstid på heparin, t.ex. antitrombin III-nivåer, heparinpotens,
brist på koaguleringsfaktor, provaktivering, konsumerande koagulopatier,
för stor utspädning av provet samt provets temperatur. Dessa faktorer ska
beaktas vid tolkningen av testresultaten avseende aktiverad
koaguleringstid
Heparinas i behållarens HR HTC-kanal är extremt specifikt för heparin.
Det finns tillräckligt med heparinas för att säkerställa att 6 enheter/ml
heparin snabbt avlägsnas från provet för att återställa det till tillståndet på
baslinjen eller utan heparin. Baslinjetiden kan ligga vid eller i närheten av
normalområdet, eller inte. Om baslinjen inte ligger inom normalområdet i
2,5,11
.
Bruksanvisning Svenska 61
Page 64

HR HTC-kanalen betyder det att något annat tillstånd än närvaro av
heparin orsakar den förlängda baslinje-koaguleringstiden.
Exempel på tolkning av HR HTC-resultat:
K. 1 K. 2 Tolkning
120 120 Patient vid baslinjen, inget heparin närva-
120 260 Patienten har heparin i blodet. Förlängning
260 260 Patienten har en underliggande koagulopati
260 360 Patienten har heparin i blodet och en under-
60 200 Patienten har heparin i blodet och patientens
rande i provet.
endast på grund av heparinets effekt.
som är orelaterad till heparin.
liggande koagulopati (troligen hemodilution).
koaguleringssystem är aktiverat.
10. Procedurbegränsningar
För att korrekta och konsekventa värden för aktiverad koaguleringstid ska
erhållas med HR HTC måste följande villkor vara uppfyllda:
■
Såväl instrumentets värmeblock som behållaren ska hålla en
temperatur på 37 °C ± 0,5 °C (98,6 °F ± 0,9 °F). Behållaren når den
temperatur som instrumentets värmeblock har inom 3 till 5 minuter.
■
Kaolinaktiveraren måste ha resuspenderats ordentligt.
■
Blodet måste vara fritt från vävnadstromboplastin. Kör testet så snart
som möjligt efter att blodprovet tagits.
■
Patientens diagnos och medicinering ska noteras.
Läkemedelsbehandling kan göra att koaguleringstiderna ändras.
Prover som ger oförklarliga onormala värden ska tas om och testas på
nytt. Om resultaten fortfarande är onormala utan någon uppenbar
orsak, kan ett citrerat blodprov tas och skickas till kliniskt laboratorium
för speciell koaguleringsanalys.
■
För att precisionen ska optimeras ska alla teknikvariabler vara
konstanta från test till test.
■
När provet har placerats i behållaren ska testet köras så snart som
möjligt. Avlägsnandet av heparin från provet sker snabbt.
Kontaktaktivering sker i behållaren om provet inte innehåller heparin.
Detta leder till kortare koaguleringstider när aktiveringen av provet
fortskrider.
■
De metoder som används för kardiopulmonär bypasskirurgi förändras
kontinuerligt, liksom även patientpopulationens egenskaper. Tillstånd
som kan påverka testresultaten för aktiverad koaguleringstid kan
inbegripa, men begränsas inte till:
■
patientens känslighet för heparin
■
utspädning av koaguleringsfaktorer i den extrakorporeala kretsen
■
användningen av citrerade blodprodukter
■
användning a trombocythämmande läkemedel
■
hypotermi
■
fluktuerande kalciumnivåer
■
förändring av trombocytfunktionen eller antalet trombocyter
■
okända koagulopatier.
Omfattande utspädning av blodet under bypass, ofta på grund av en
önskan att begränsa användningen av heterologa blodprodukter, kan
leda till postoperativ blödning. I svåra fall kan utspädningen bli så
omfattande att koagulering, mätt genom aktiverad koaguleringstid,
inte sker. Hur adekvata plasmakoaguleringsfaktorerna är kan inte
fastställas genom korrelation av utspädningsgraden med patientens
hematokrit. Tvättade celler har ofta administrerats till patienten utan
62 Bruksanvisning Svenska
Page 65

kompensation för förlorad plasma. Om HR HTC inte koagulerar i
heparinaskanalen (kanal 1) efter omvändning av patientens heparin
med protamin, är en utspädningskoagulopati en sannolik möjlighet.
Varning: På grund av bildandet av HR HTC bör det inte användas för
att övervaka regional antikoagulering som uppnås genom att
infundera citrat.
Obs! Extrem försiktighet bör iakttas för att säkerställa att heparinas i
HR HTC-kanalen inte oavsiktligen överförs till provet i behållarens HRkanal. Om detta inträffar kommer den hepariniserade
koaguleringstiden i ”HR”-kanalen inte längre att vara representativ för
mängden heparin i provet, utan tyda på mindre heparin, beroende på
hur mycket heparinas som överförts. Av detta skäl föreslås bestämt
att ”HR”-kanalen fylls först för att minimera risken för överföring av
heparinas.
Försiktighetsåtgärder och begränsningar för instrumentet finns i
användarmanualen.
11. Förväntade värden
Heparinaskanalen tillhandahåller effektivt en aktiverad koaguleringstid på
baslinjen för hepariniserat nytaget helblod. Under bypass kan värdet för
aktiverad koaguleringstid på baslinjen driva uppåt och återspegla
hemodilutionen av patientens blod. Koaguleringstiden på baslinjen
korrelerar med utspädningen av plasmakoaguleringsfaktorerna som inte
nödvändigtvis korrelerar med patientens hematokrit. Röda blodkroppar
som återförs till patienten från sparade celler kompenserar inte för
förlorade plasmakoaguleringsfaktorer. Om den aktiverade
koaguleringstiden på baslinjen förblir förlängd kan en
utspädningskoagulopati (brist på tillräckligt med koaguleringsfaktorer)
inträffa och postoperativ blödning kan förekomma. HR HTC kan övervaka
utvecklingen av en sådan situation och möjliggöra vidtagandet av åtgärder
innan allvarlig utspädning av koaguleringsfaktorerna inträffar.
12. Specificerad prestanda
Behållarna för aktiverad koaguleringstid uppvisar inom intervallet
0 till 600 sekunders koaguleringstid i normala fall inte en variation mellan
duplicerade prover som överstiger 12 % för en individ. Vid höga
heparinnivåer och koaguleringstider som överstiger 600 sekunder anses
en aktiverad koaguleringstid generellt inte som en tillräckligt tillförlitlig
prediktor för att fastställa heparinnivåerna.
HR HTC har utformats för att ge en normal HR ACT i kanalen märkt ”HR”,
vilken nära motsvarar de reaktioner som ursprungligen rapporterades av
Bull, et al (1975). Kaolinaktiveraren i varje sats med behållare har
kalibrerats för att minska variationerna i aktivitet mellan satserna till
mindre än 10 % samt minimera långsiktig avdrift.
Prestandan för ”baslinje”-kanalen i behållaren beror på aktiviteten för
heparinaset i kanalen märkt ”HR HTC”. Heparinaset har renats och
stabiliserats för att avlägsna 6 enheter/ml heparin inom ett tidsintervall
som är tillräckligt kort för att återställa det hepariniserade blodet till
koaguleringstiden på baslinjen. Heparinasets stabilitet säkerställs genom
att hålla behållarna vid en konstant temperatur. De områden inom vilka
behållarna får förvaras är vid antingen 2 °C till 10 °C (36 °F till 50 °F) eller
10 °C till 25 °C (50 °F till 77 °F). Behållarnas prestanda kan minska om
produkten inte förvaras i en stabil miljö. Upprepad förflyttning av
produkten från kylförvaring till rumstemperatur och vice versa
rekommenderas inte.
13. Kvalitetskontroll
Två nivåer av kontroller ska köras för HTC-testet för att säkerställa
adekvat prestanda på instrument och behållare.
Bruksanvisning Svenska 63
Page 66

Resultaten ska ligga inom de intervall som tillverkaren anger eller inom
intervall som fastställts av användaren.
Kontrollerna för heparinastestet på hög nivå inkluderar: CLOTtrac™ HRkoaguleringskontroll (katalognr 550-07) och CLOTtrac HTC-kontroll
(katalognr 550-12).
CLOTtrac HTC-kontroll ger en HR ACT på baslinjen i HR HTC-kanalen
och når tidsgränsen (>999) i HR ACT-kanalen.
Denna kontroll är en frystorkad kontroll som innehåller 6 enheter/ml
heparin. Prestandan på HR HTC verifieras genom att köra kontrollen i en
behållare och erhålla ett HR ACT-värde på baslinjen i den kanal som är
märkt ”HR HTC” samt nå tidsgränsen (999 sekunder) i kanalen
märkt ”HR”. Detta visar att behållarens kanal som innehåller heparinas
fungerar som den ska.
14. Referenser
1. Baugh RF, Deemar KA, Zimmerman JJ. Heparinase in the activated
clotting time assay: Monitoring heparin-independent alterations in
coagulation function. Anesth Analg. 1992;74:201.
2. Bode AP, Eick L. Lysed platelets shorten the activated coagulation
time (ACT) of heparinized blood. Am J Clin Pathol. 1989;91:430.
3. Bull BS, Korpman RA, Huse WM, Briggs BD. Heparin therapy during
extracorporeal circulation. I. Problems inherent in existing heparin
protocols. J Thorac Cardiovasc Surg. 1975;69:674.
4. Bull BS, Huse WM, Brauer FS, Korpman RA. Heparin therapy during
extracorporeal circulation. II. The use of a dose-response curve to
individualize heparin and protamine dosage. J Thorac Cardiovasc
Surg. 1975;69:685.
5. Culliford AT, Gitel SN, Starr N, Thomas ST, Baumann FG, Wessler S,
Spencer FC. Lack of correlation between activated clotting time and
plasma heparin during cardiopulmonary bypass. Ann Surg.
1981;193:105.
6. Dietrich CP, Silva ME, Michelacci YM. Sequential degradation of
heparin in Flavobacterium heparinum. Purification and properties of
five enzymes involved in heparin degradation. J Biol Chem.
1973;248:6408.
7. Effeney DJ, Goldstone J, Chin D, Krupski WC, Ellis RJ. Intraoperative
anticoagulation in cardiovascular surgery. Surgery. 1981;90:1068.
8. Forman WB, Bayer G. A simplified method for monitoring heparin
therapy at the bedside: The activated whole blood clotting time. Am J
Hematol. 1981;11:277.
9. Hattersley PG. Progress report: The activated coagulation time of
whole blood (ACT). Am J Clin Pathol. 1976;66:899.
10. Hutt ED, Kingdon HS. Use of heparinase to eliminate heparin
inhibition in routine coagulation assays. J Lab Clin Med.
1972;79:1027.
11. Kesteven PJ, Pasaoglu I, Williams BT, Savidge GG. Significance of
the whole blood activated clotting time in cardiopulmonary bypass. J
Cardiovasc Surg. 1986;27:85.
12. Mabry CD, Read RC, Thompson BW, Williams GD, White HJ.
Identification of heparin resistance during cardiac and vascular
surgery. Arch Surg. 1979;114:129.
13. Mabry CD, Thompson BW, Read RC. Activated clotting time (ACT)
monitoring of intraoperative heparinization in peripheral vascular
surgery. Am J Surg. 1979;138:894.
14. Mabry CD, Thompson, BW, Read RC, Campbell GS. Activated
clotting time monitoring of intraoperative heparinization: Our
64 Bruksanvisning Svenska
Page 67

experience and comparison with two techniques. Surgery.
1981;90:889.
15. Moorehead MT, Westengard JC, Bull BS. Platelet involvement in the
activated coagulation time of heparinized blood. Anesth Analg.
1984;63:394.
16. Yang VC, Linhardt RJ, Bernstein H, Cooney CL, Langer R.
Purification and characterization of heparinase from Flavobacterium
heparinum. J Biol Chem. 1985;260:1849.
15. Friskrivning från ansvar
NEDANSTÅENDE GARANTIFRISKRIVNING GÄLLER
KUNDER UTANFÖR USA:
OAKTAT OM TESTBEHÅLLAREN FÖR HEPARINAS MED HÖGT
VÄRDE, NEDAN KALLAD ”PRODUKTEN”, HAR KONSTRUERATS,
TILLVERKATS OCH KONTROLLERATS NOGGRANT FÖRE
FÖRSÄLJNING, KAN DET AV OLIKA SKÄL INTRÄFFA ATT
PRODUKTEN INTE UPPFYLLER SIN AVSEDDA FUNKTION PÅ ETT
TILLFREDSSTÄLLANDE SÄTT. VARNINGSTEXTERNA I
PRODUKTDOKUMENTATIONEN INNEHÅLLER MER DETALJERAD
INFORMATION OCH UTGÖR EN INTEGRERAD DEL AV DENNA
GARANTIFRISKRIVNING. MEDTRONIC FRÅNSÄGER SIG DÄRFÖR
ALLA GARANTIER, SÅVÄL UTTRYCKLIGA SOM
UNDERFÖRSTÅDDA, AVSEENDE PRODUKTEN. MEDTRONIC SKA
DÄRFÖR INTE VARA SKYLDIGT ATT ERSÄTTA NÅGON SKADA,
VARE SIG DIREKT ELLER INDIREKT, SOM UPPKOMMER MED
ANLEDNING AV PRODUKTENS UTFORMNING ELLER DESS
ANVÄNDNING, OAVSETT OM KRAVET GRUNDAR SIG PÅ
PÅSTÅENDE OM GARANTI, AVTALSBROTT, SKADEGÖRANDE
HANDLING ELLER ANNAT.
De undantag och begränsningar som anges ovan är inte avsedda att stå i
strid med tvingande regler i tillämplig lag, och ska inte heller tolkas så. Om
denna garantifriskrivning till någon del av behörig domstol bedöms vara
olaglig, verkningslös eller stå i strid med tillämplig lag, ska övriga delar av
garantifriskrivningen gälla, varvid alla rättigheter och skyldigheter ska
bestå som om garantifriskrivningen inte innehöll den del eller det villkor
som bedömts vara ogiltigt.
Bruksanvisning Svenska 65
Page 68

1. Προτιθέμενη χρήση
Για χρήση στην ταυτοποίηση της παρουσίας ηπαρίνης με χρήση του
ενεργοποιημένου χρόνου πήξης.
Για διαγνωστική χρήση in vitro.
Προσοχή: Λόγω της μοναδικής φύσης αυτού του προϊόντος, απαιτείται
προσοχή προκειμένου να διασφαλιστεί ότι η ηπαρινάση δεν μεταφέρεται
ακουσίως από το κανάλι «HR HTC» στο κανάλι «HR» της φύσιγγας. Για
πρόσθετες πληροφορίες, βλ. Ενότητα 8 και Ενότητα 10.
2. Περίληψη
Η φύσιγγα δοκιμασίας ηπαρινάσης υψηλού εύρους (HR HTC) της
Medtronic είναι μια τροποποιημένη έκδοση της φύσιγγας υψηλού εύρους
ενεργοποιημένου χρόνου πήξης (HR ACT) για τα αυτοματοποιημένα
χρονόμετρα πήξης της Medtronic. Η δοκιμασία ενεργοποιημένου χρόνου
πήξης περιγράφηκε αρχικά από τον Hattersley το 19669. Η δοκιμασία και
οι παραλλαγές της έχουν χρησιμοποιηθεί ευρέως για την παρακολούθηση
της αντιπηκτικής δράσης της ηπαρίνης
χρησιμοποιεί πρόσφατα ληφθέν δείγμα πλήρους αίματος, όπως και η
φύσιγγα HR ACT. Η διαφορά είναι ότι στη φύσιγγα HR HTC το ένα κανάλι
περιέχει κεκαθαρμένη, προερχόμενη από βακτήρια ηπαρινάση. Η
ηπαρινάση καταστρέφει ταχύτατα και ειδικά την ηπαρίνη που υπάρχει στο
δείγμα αίματος
απομακρύνει ταχύτατα 6 μονάδες/mL ηπαρίνης. Το κανάλι ηπαρινάσης
παράγει χρόνο πήξης που αντικατοπτρίζει τον χρόνο πήξης γραμμής
αναφοράς του μη ηπαρινισμένου δείγματος, παρότι το δείγμα περιέχει
ηπαρίνη. Το άλλο κανάλι της φύσιγγας είναι ένα τυπικό κανάλι «HR ACT»
και ο χρόνος πήξης που προκύπτει είναι ο ενεργοποιημένος χρόνος
πήξης του ηπαρινισμένου δείγματος. Η χρήση αυτής της φύσιγγας
επιτρέπει: 1) την επαλήθευση προεγχειρητικής παρουσίας ηπαρίνης,
2) την αξιολόγηση της επίδρασης της παράκαμψης στον ενεργοποιημένο
χρόνο πήξης γραμμής αναφοράς, 3) την επιβεβαίωση αναστροφής της
ηπαρίνης μετά από χορήγηση πρωταμίνης, 4) την ταυτοποίηση
μετεγχειρητικής «επαναληπτικής δράσης της ηπαρίνης (rebound)», και
5) την ταυτοποίηση της παρουσίας ηπαρίνης σε ασθενείς που εμφανίζουν
υπερβολική αιμορραγία μετεγχειρητικά. Διατίθεται ένας μάρτυρας
CLOTtrac™ HTC για να επαληθευτεί ότι η απόδοση της φύσιγγας είναι
σύμφωνα με τις προδιαγραφές.
1,6,10,16
. Η ποσότητα της ηπαρινάσης που υπάρχει στο κανάλι
3,4,7,8,13,14
. Η φύσιγγα HR HTC
3. Αρχές
Η δοκιμασία ενεργοποιημένου χρόνου πήξης μετράει τον χρόνο πήξης
πρόσφατα ληφθέντος δείγματος πλήρους αίματος ενεργοποιημένου μέσω
επιφανειακής επαφής. Η αρχική διαδικασία του Hattersley
χρησιμοποιούσε γη διατόμων ως παράγοντα ενεργοποίησης. Η γη
διατόμων επιδεικνύει διαφορετικούς βαθμούς ενεργοποίησης εξ επαφής
ανάλογα με την καθαρότητά της, την προέλευση του ιζήματος και το
μέγεθος και σχήμα των σωματιδίων. Οι φύσιγγες ενεργοποιημένου
χρόνου πήξης της Medtronic χρησιμοποιούν καολίνη ως παράγοντα
ενεργοποίησης. Η καολίνη επιδεικνύει ανώτερα χαρακτηριστικά στην εξ
επαφής ενεργοποίηση της πήξης του αίματος. Οι φύσιγγες HR ACT και
HR HTC επιδεικνύουν μειωμένη ευαισθησία στην ηπαρίνη, επιτρέποντας
την παρακολούθηση υψηλών επιπέδων ηπαρίνης με τη δοκιμασία
ενεργοποιημένου χρόνου πήξης.
Το τελικό σημείο της δοκιμασίας είναι η ανίχνευση σχηματισμού θρόμβου.
Τα αυτοματοποιημένα χρονόμετρα πήξης της Medtronic ανιχνεύουν τον
σχηματισμό θρόμβου παρακολουθώντας την ταχύτητα πτώσης του
μηχανισμού εμβόλου/δείκτη που υπάρχει σε κάθε κανάλι της φύσιγγας. Η
διάταξη του εμβόλου πέφτει ταχύτατα σε ένα δείγμα αίματος στο οποίο
δεν έχει συντελεστεί πήξη. Όταν σχηματίζεται ένα πλέγμα ινώδους, η
66 Οδηγίες χρήσης Ελληνικά
Page 69

ταχύτητα πτώσης της διάταξης του εμβόλου μειώνεται. Αυτή η μείωση
στην ταχύτητα πτώσης ανιχνεύεται από ένα φωτοοπτικό σύστημα που
βρίσκεται στη διάταξη καλύμματος της συσκευής. Η ανίχνευση
σχηματισμού θρόμβου υποδεικνύεται από ένα ηχητικό σήμα και το
χρονόμετρο πήξης σταματά. Οι συσκευές μπορούν να εκτελέσουν
2 ταυτόχρονες δοκιμασίες, χρησιμοποιώντας τη 2κάναλη φύσιγγα. Οι
χρόνοι πήξης για κάθε κανάλι εμφανίζονται σε δευτερόλεπτα μετά την
ολοκλήρωση της δοκιμασίας. Με την HR HTC, η συσκευή εμφανίζει
2 αποτελέσματα, ένα για το δείγμα που περιέχει ηπαρινάση και ένα για το
δείγμα που δεν περιέχει ηπαρινάση. Η οθόνη του μπροστινού πίνακα
μπορεί να χρησιμοποιηθεί για την εναλλαγή ανάμεσα στους χρόνους
πήξης κάθε καναλιού ή για την εναλλαγή ανάμεσα στον μέσο όρο και τη
διαφορά μεταξύ των δύο καναλιών. Όταν χρησιμοποιείται η HR HTC, η
μεσοτιμημένη ένδειξη έχει μικρή σημασία, ωστόσο, η διαφορά ανάμεσα
στα δύο αποτελέσματα είναι η παράταση του χρόνου πήξης λόγω
παρουσίας ηπαρίνης στο δείγμα.
4. Αντιδραστήρια
Κάθε θάλαμος αντιδραστηρίου της φύσιγγας περιέχει 0,1 mL ρυθμιστικού
διαλύματος υδροξυαιθυλοπιπεραζινο-αιθανοσουλφονικού οξέος (HEPES),
καολίνη, χλωριούχο ασβέστιο και αζίδιο του νατρίου ως βακτηριοστατικό
παράγοντα. Το κανάλι που φέρει τη σήμανση «HR HTC» περιέχει
λυοφιλοποιημένη ηπαρινάση υψηλής καθαρότητας με παράγοντες
σταθεροποίησης και αζίδιο του νατρίου ως βακτηριοστατικό παράγοντα.
Η φύσιγγα HR HTC μπορεί να προθερμανθεί για μέγιστο διάστημα
2 ωρών. Μόλις το δείγμα τοποθετηθεί στην προθερμασμένη φύσιγγα, η
δοκιμασία πρέπει να ξεκινήσει αμέσως.
5. Αποθήκευση
Η φύσιγγα HR HTC θα πρέπει να αποθηκεύεται σε σταθερό περιβάλλον,
είτε στους 2°C έως 10°C (36°F έως 50°F) είτε στους 10°C έως 25°C
(50°F έως 77°F). Οι φύσιγγες διατίθενται συσκευασμένες σε
σφραγισμένους δίσκους 2 φυσίγγων. Οι φύσιγγες παραμένουν σταθερές
για το χρονικό διάστημα που αναγράφεται στην ετικέτα του δίσκου. Μη
χρησιμοποιείτε τις φύσιγγες μετά την ημερομηνία «Χρήση έως». Μη
χρησιμοποιείτε τη φύσιγγα εάν φαίνεται χρωματικά αλλοιωμένη,
ραγισμένη ή παραμορφωμένη, ή εάν το αντιδραστήριο φαίνεται να έχει
εξατμιστεί ή μολυνθεί.
Από τη στιγμή που θα παραβιαστεί η σφράγιση του καλύμματος του
δίσκου, οι φύσιγγες παραμένουν σταθερές για 24 ώρες σε θερμοκρασία
ψυγείου.
Σημείωση: Μη χρησιμοποιείτε εάν υπάρχει ένδειξη κατάψυξης.
6. Συσκευή
Η φύσιγγα HR HTC έχει σχεδιαστεί ειδικά για χρήση με τα
αυτοματοποιημένα χρονόμετρα πήξης της Medtronic. Για οδηγίες,
συμβουλευτείτε το εγχειρίδιο χειριστή της συσκευής.
Για να διασφαλιστεί η κατάλληλη απόδοση της συσκευής, είναι σημαντικό
να καθαρίζετε τη συσκευή τουλάχιστον κάθε 30 ημέρες, ή πιο συχνά εάν
απαιτείται.
Σημείωση: Εάν εισχωρήσει αίμα μέσα στο κάλυμμα του ενεργοποιητή,
καθαρίστε τη συσκευή το συντομότερο δυνατό. Με κάθε συσκευή
παρέχεται ένα κιτ καθαρισμού ενεργοποιητή (αρ. καταλόγου 303-58).
Χρησιμοποιήστε τα υλικά που παρέχονται με κάθε κιτ καθαρισμού για να
εκτελέσετε τη διαδικασία καθαρισμού. Για λεπτομέρειες, βλ. ένθετο
συσκευασίας που περιέχεται στο κιτ καθαρισμού.
Οδηγίες χρήσης Ελληνικά 67
Page 70

7. Συλλογή και παρασκευή δειγμάτων
1
2
Ο ακατάλληλος χειρισμός δειγμάτων μπορεί να οδηγήσει σε λανθασμένα
αποτελέσματα δοκιμασίας πήξης. Κατά συνέπεια, τα δείγματα πρέπει να
συλλέγονται προσεκτικά και οι τεχνικές χειρισμού πρέπει να είναι
σταθερές.
Εάν για τη λήψη του δείγματος αίματος χρησιμοποιείται φλεβοκέντηση, η
φλεβοκέντηση θα πρέπει να είναι καθαρή. Απορρίψτε τα πρώτα
χιλιοστόλιτρα αίματος για να αποφευχθεί η μόλυνση του δείγματος με
ιστική θρομβοπλαστίνη.
Σημείωση: Μη λαμβάνετε αίμα από ηπαρινισμένους μόνιμους καθετήρες
ή άλλες γραμμές όπου έχουν δράσει αντιπηκτικά χωρίς να έχει γίνει
διεξοδική έκπλυση της γραμμής.
Εάν για τη δοκιμασία χρησιμοποιείται πρόσφατα ληφθέν δείγμα πλήρους
αίματος, μεταφέρετε αμέσως το δείγμα στη φύσιγγα και ξεκινήστε τη
δοκιμασία.
8. Οδηγίες χρήσης
Το παρόν προϊόν προορίζεται για χρήση μόνον από εκπαιδευμένα άτομα.
Παρεχόμενα υλικά:
■
Φύσιγγα δοκιμασίας ηπαρινάσης υψηλού εύρους (HR HTC),
αρ. καταλόγου 402-07
Απαιτούμενα υλικά που δεν παρέχονται
■
Αυτοματοποιημένο χρονόμετρο πήξης της Medtronic
■
Πλαστική σύριγγα με βελόνα (κατά προτίμηση 18 ή 19 gauge)
Εικόνα 1. Πλήρωση της φύσιγγας HR HTC
1. Δείγμα (πλαϊνή όψη)
2. Δείγμα (όψη από πάνω)
Για χρήση με τη συσκευή ACT Plus™, ακολουθήστε τα παρακάτω
βήματα:
1. Από το «Main Menu» (Κύριο μενού), επιλέξτε «Cartridge Type»
(Τύπος φύσιγγας) και πιέστε το πλήκτρο μέχρι να εμφανιστεί η ένδειξη
«HTC». Πιέστε «Enter» (Εισαγωγή) για να επιβεβαιώσετε την
επιλογή.
Σημείωση: Οι αριθμοί παρτίδας και η ημερομηνία «Χρήση έως» για
τις φύσιγγες και τους μάρτυρες πρέπει να εισαχθούν πριν από την
εκτέλεση μιας δοκιμασίας.
68 Οδηγίες χρήσης Ελληνικά
Page 71

2. Στο «Main Menu» (Κύριο μενού), εισαγάγετε τους αριθμούς
«Patient ID» (Αναγνωριστικό ασθενούς) και «User ID»
(Αναγνωριστικό χρήστη). Πιέστε «Enter» (Εισαγωγή) για
επιβεβαίωση.
3. Προθερμάνετε τις φύσιγγες για 3 έως 5 λεπτά πριν από τη συλλογή
του δείγματος δοκιμασίας.
4. Χτυπήστε ελαφρά τη φύσιγγα ώστε το αντιδραστήριο να μετατραπεί
ξανά σε εναιώρημα.
5. Γεμίστε κάθε θάλαμο με 0,4 mL δείγματος.
Σημείωση: Γεμίζετε πάντα το κανάλι «HR» πρώτο και το κανάλι
«HR HTC» δεύτερο για να διασφαλίσετε ότι η ηπαρινάση δεν θα
μολύνει το κανάλι «HR».
6. Εισαγάγετε τη φύσιγγα στη συσκευή ACT Plus και κλείστε τη
θερμαινόμενη πλάκα ενεργοποιητή για να ξεκινήσετε τη δοκιμασία.
7. Ο σχηματισμός θρόμβου σηματοδοτείται από έναν ηχητικό τόνο. Η
θερμαινόμενη πλάκα του ενεργοποιητή ανοίγει και εμφανίζονται τα
αποτελέσματα.
Μετά την ολοκλήρωση της δοκιμασίας, απορρίψτε τη φύσιγγα, τη
σύριγγα και τη βελόνα σε εγκεκριμένα δοχεία απόρριψης βιολογικά
επικίνδυνων αποβλήτων.
9. Αποτελέσματα
Η απόκριση του ενεργοποιημένου χρόνου πήξης στην ηπαρίνη διαφέρει
σημαντικά από άτομο σε άτομο12. Ο ενεργοποιημένος χρόνος πήξης
επηρεάζεται από διάφορα φάρμακα, ιδίως από φάρμακα που
αναστέλλουν την ενεργοποίηση των αιμοπεταλίων15. Μια σειρά άλλων
παραγόντων μπορεί να επηρεάσουν την απόκριση του ενεργοποιημένου
χρόνου πήξης ενός ατόμου στην ηπαρίνη, π.χ. επίπεδα αντιθρομβίνης III,
δραστικότητα ηπαρίνης, ανεπάρκειες του παράγοντα πήξης,
ενεργοποίηση δείγματος, διαταραχές της πήξης του αίματος λόγω
κατανάλωσης των παραγόντων πήξης, υπερβολική αραίωση του
δείγματος και θερμοκρασία δείγματος. Αυτοί οι παράγοντες θα πρέπει να
λαμβάνονται υπόψη κατά την ερμηνεία των αποτελεσμάτων της
δοκιμασίας ενεργοποιημένου χρόνου πήξης
Η ηπαρινάση στο κανάλι «HR HTC» της φύσιγγας είναι εξαιρετικά ειδική
για ηπαρίνη. Υπάρχει επαρκής ποσότητα ηπαρινάσης για να διασφαλιστεί
η ταχύτατη απομάκρυνση 6 μονάδων/mL ηπαρίνης από το δείγμα για την
επαναφορά του σε μια κατάσταση γραμμής αναφοράς ή μη ηπαρινισμένη
κατάσταση. Ο χρόνος γραμμής αναφοράς ενδέχεται να είναι ή να μην είναι
κοντά στο φυσιολογικό εύρος. Εάν ο χρόνος γραμμής αναφοράς δεν είναι
εντός του φυσιολογικού εύρους στο κανάλι «HR HTC», αυτό υποδεικνύει
ότι κάποια άλλη κατάσταση, εκτός της παρουσίας ηπαρίνης, ευθύνεται για
την παράταση του χρόνου πήξης γραμμής αναφοράς.
Παράδειγμα ερμηνείας αποτελεσμάτων HR HTC:
Καν. 1 Καν. 2 Ερμηνεία
120 120 Ο ασθενής εμφανίζει τιμές γραμμής αναφο-
120 260 Ο ασθενής έχει ηπαρίνη στο αίμα του. Η
260 260 Ο ασθενής έχει υποκείμενη διαταραχή της
ράς. Απουσία ηπαρίνης από το δείγμα.
παράταση οφείλεται μόνο στη δράση της
ηπαρίνης.
πήξης του αίματος που δεν σχετίζεται με
ηπαρίνη.
2,5,11
.
Οδηγίες χρήσης Ελληνικά 69
Page 72

Καν. 1 Καν. 2 Ερμηνεία
260 360 Ο ασθενής έχει ηπαρίνη στο αίμα και υποκεί-
60 200 Ο ασθενής έχει ηπαρίνη στο αίμα του και το
μενη διαταραχή της πήξης του αίματος
(πιθανόν αιμοαραίωση).
σύστημα πήξης του ασθενούς είναι ενεργοποιημένο.
10. Περιορισμοί της διαδικασίας
Για τη λήψη ορθών και συνεπών αποτελεσμάτων ενεργοποιημένου
χρόνου πήξης με τη φύσιγγα HR HTC, πρέπει να τηρούνται οι ακόλουθες
συνθήκες:
■
Η θερμοκρασία της θερμαινόμενης πλάκας της συσκευής και της
φύσιγγας πρέπει να είναι 37°C ± 0,5°C (98,6°F ± 0,9°F). Η φύσιγγα
αποκτά θερμοκρασία δωματίου σε 3 έως 5 λεπτά μέσα στη
θερμαινόμενη πλάκα της συσκευής.
■
Ο ενεργοποιητής καολίνης πρέπει να ανακινηθεί καλά ώστε να
μετατραπεί ξανά σε εναιώρημα.
■
Το αίμα δεν πρέπει να περιέχει ιστική θρομβοπλαστίνη. Εκτελέστε τη
δοκιμασία το συντομότερο δυνατό μετά τη λήψη του δείγματος
αίματος.
■
Η διάγνωση του ασθενούς και η φαρμακευτική αγωγή πρέπει να
ληφθούν υπόψη. Τα φάρμακα μπορεί να μεταβάλλουν τους χρόνους
πήξης. Όταν τα δείγματα δίνουν ανεξήγητα μη φυσιολογικές τιμές,
πρέπει να επαναλαμβάνεται η λήψη και η ανάλυσή τους. Εάν τα
αποτελέσματα εξακολουθούν να είναι μη φυσιολογικά χωρίς
προφανές αίτιο, το δείγμα πρέπει να υποβληθεί σε επεξεργασία με
κιτρικό νάτριο και να αποσταλεί στο κλινικό εργαστήριο για ειδική
ανάλυση πήξης.
■
Για βελτιστοποίηση της ακρίβειας, όλες οι μεταβλητές της τεχνικής θα
πρέπει να παραμένουν σταθερές από τη μία δοκιμασία στην άλλη.
■
Όταν το δείγμα τοποθετηθεί στη φύσιγγα, η δοκιμασία πρέπει να
εκτελεστεί το συντομότερο δυνατό. Η απομάκρυνση της ηπαρίνης από
το δείγμα λαμβάνει χώρα ταχύτατα. Η ενεργοποίηση εξ επαφής
σημειώνεται στη φύσιγγα όταν το δείγμα δεν περιέχει ηπαρίνη. Αυτό
θα έχει ως αποτέλεσμα βραχύτερους χρόνους πήξης καθώς προχωρά
η ενεργοποίηση του δείγματος.
■
Οι μεθοδολογίες που χρησιμοποιούνται σε χειρουργικές επεμβάσεις
καρδιοπνευμονικής παράκαμψης αλλάζουν διαρκώς, όπως και τα
χαρακτηριστικά του πληθυσμού ασθενών. Οι καταστάσεις που
μπορούν να επηρεάσουν τα αποτελέσματα της δοκιμασίας
ενεργοποιημένου χρόνου πήξης ενδέχεται να περιλαμβάνουν,
ενδεικτικά, τις εξής:
■
ευαισθησία του ασθενούς στην ηπαρίνη
■
αραίωση των παραγόντων πήξης από το κύκλωμα εξωσωματικής
κυκλοφορίας
■
χρήση προϊόντων αίματος που έχουν υποβληθεί σε επεξεργασία
με κιτρικό νάτριο
■
χρήση αντιαιμοπεταλιακών φαρμάκων
■
υποθερμία
■
μεταβαλλόμενα επίπεδα ασβεστίου
■
μεταβολή στη λειτουργία ή στον αριθμό των αιμοπεταλίων
■
μη γνωστές διαταραχές της πήξης του αίματος
Η υπερβολική αραίωση του αίματος κατά την παράκαμψη, που συχνά
οφείλεται στην επιθυμία περιορισμού της χρήσης προϊόντων
ετερόλογου αίματος, μπορεί να οδηγήσει σε μετεγχειρητική
αιμορραγία. Σε σοβαρές περιπτώσεις, η αραίωση αυτή μπορεί να είναι
70 Οδηγίες χρήσης Ελληνικά
Page 73

τόσο μεγάλη ώστε να μην σημειώνεται πήξη, όπως μετράται από τον
ενεργοποιημένο χρόνο πήξης. Η επάρκεια των παραγόντων πήξης
πλάσματος δεν μπορεί να προσδιοριστεί μέσω του συσχετισμού του
βαθμού της αραίωσης με τον αιματοκρίτη του ασθενούς. Συχνά, έχουν
χορηγηθεί εκπλυμένα κύτταρα στον ασθενή χωρίς να αντισταθμίζεται
η απώλεια πλάσματος. Εάν η φύσιγγα HR HTC δεν παράγει πήξη στο
κανάλι ηπαρινάσης (κανάλι 1), μετά την αναστροφή της ηπαρίνης του
ασθενούς με πρωταμίνη, υπάρχουν πολλές πιθανότητες διαταραχής
της πήξης του αίματος από αραίωση.
Προειδοποίηση: Λόγω της σύνθεσής της, η φύσιγγα HR HTC δεν
πρέπει να χρησιμοποιείται για την παρακολούθηση της περιοχικής
αντιπηκτικής δράσης που επιτυγχάνεται μέσω έγχυσης κιτρικού
νατρίου.
Προσοχή: Θα πρέπει να λαμβάνεται άκρα προσοχή ώστε να
διασφαλιστεί ότι η ηπαρινάση στο κανάλι «HR HTC» δεν μεταφέρεται
ακουσίως στο δείγμα στο κανάλι «HR» της φύσιγγας. Εάν συμβεί
αυτό, ο χρόνος πήξης του ηπαρινισμένου δείγματος στο κανάλι «HR»
δεν θα είναι πλέον αντιπροσωπευτικός της ποσότητας ηπαρίνης στο
δείγμα, αλλά θα υποδεικνύει ότι υπάρχει λιγότερη ηπαρίνη, ανάλογα
με το πόση ηπαρινάση μεταφέρθηκε. Για το λόγο αυτό, συνιστάται
ιδιαίτερα να γίνεται πλήρωση πρώτα του καναλιού «HR» προκειμένου
να ελαχιστοποιηθεί η πιθανότητα μεταφοράς ηπαρινάσης.
Για προφυλάξεις και περιορισμούς ως προς τη χρήση της συσκευής,
συμβουλευτείτε το εγχειρίδιο χειριστή.
11. Αναμενόμενες τιμές
Το κανάλι ηπαρινάσης παρέχει αποτελεσματικά έναν ενεργοποιημένο
χρόνο πήξης γραμμής αναφοράς για ηπαρινισμένο, πρόσφατα ληφθέν
δείγμα πλήρους αίματος. Κατά την παράκαμψη, η τιμή του
ενεργοποιημένου χρόνου πήξης γραμμής αναφοράς ενδέχεται να
μετατοπιστεί προς τα επάνω, αντικατοπτρίζοντας αιμοαραίωση στο αίμα
του ασθενούς. Ο χρόνος πήξης γραμμής αναφοράς συσχετίζεται με την
αραίωση παραγόντων πήξης πλάσματος, η οποία δεν συσχετίζεται
απαραίτητα με τον αιματοκρίτη του ασθενούς. Τα ερυθρά αιμοσφαίρια
που μεταγγίζονται πίσω στον ασθενή από ένα σύστημα αυτομετάγγισης
δεν αντισταθμίζουν την απώλεια παραγόντων πήξης πλάσματος. Εάν ο
ενεργοποιημένος χρόνος πήξης γραμμής αναφοράς εξακολουθεί να είναι
παρατεταμένος, ενδέχεται να σημειωθεί διαταραχή της πήξης του αίματος
από αραίωση (έλλειψη επαρκών παραγόντων πήξης) και μπορεί να
παρατηρηθεί μετεγχειρητική αιμορραγία. Με τη φύσιγγα HR HTC μπορεί
να παρακολουθείται η εξέλιξη αυτής της κατάστασης και να ληφθούν
διορθωτικά μέτρα πριν σημειωθεί σοβαρή αραίωση των παραγόντων
πήξης.
12. Ειδικά χαρακτηριστικά απόδοσης
Οι φύσιγγες ενεργοποιημένου χρόνου πήξης, στο εύρος χρόνου πήξης
από 0 έως 600 δευτερόλεπτα, συνήθως δεν εμφανίζουν απόκλιση
μεγαλύτερη από 12% μεταξύ διπλότυπων δειγμάτων για ένα άτομο. Σε
υψηλά επίπεδα ηπαρίνης και χρόνους πήξης άνω των
600 δευτερολέπτων, ο ενεργοποιημένος χρόνος πήξης γενικά δεν
θεωρείται επαρκώς αξιόπιστος για τον προσδιορισμό των επιπέδων
ηπαρίνης.
Η σύνθεση της φύσιγγας HR HTC είναι τέτοια ώστε να παράγει έναν
φυσιολογικό HR ACT στο κανάλι που φέρει τη σήμανση «HR», ο οποίος
αντιστοιχεί σε μεγάλο βαθμό στις αποκρίσεις που αναφέρθηκαν αρχικά
από τον Bull, et al (1975). Ο ενεργοποιητής καολίνης σε κάθε παρτίδα
φυσίγγων έχει βαθμονομηθεί ώστε να μειώνει τις αποκλίσεις στη δράση
μεταξύ των παρτίδων σε λιγότερο από 10%, και να ελαχιστοποιεί την
μακροπρόθεσμη μετατόπιση.
Οδηγίες χρήσης Ελληνικά 71
Page 74

Η απόδοση του καναλιού «γραμμής αναφοράς» της φύσιγγας εξαρτάται
από τη δράση της ηπαρινάσης στο κανάλι με τη σήμανση «HR HTC». Η
ηπαρινάση έχει καθαρθεί και σταθεροποιηθεί ώστε να απομακρύνει
6 μονάδες/mL ηπαρίνης σε χρονικό διάστημα αρκετά βραχύ ώστε να
επανέλθει το ηπαρινισμένο αίμα σε χρόνο πήξης γραμμής αναφοράς. Η
σταθερότητα της ηπαρινάσης διασφαλίζεται με τη διατήρηση των
φυσίγγων σε σταθερή θερμοκρασία. Τα εύρη στα οποία οι φύσιγγες
μπορούν να αποθηκευτούν είναι είτε 2°C έως 10°C (36°F έως 50°F) είτε
10°C έως 25°C (50°F έως 77°F). Η απόδοση των φυσίγγων ενδέχεται να
μειωθεί εάν το προϊόν δεν αποθηκευτεί σε σταθερό περιβάλλον. Η
επανειλημμένη μεταφορά του προϊόντος από συνθήκες ψύξης σε
συνθήκες περιβάλλοντος ή το αντίστροφο δεν συνιστάται.
13. Έλεγχος ποιότητας
Για να διασφαλιστεί η επαρκής απόδοση της συσκευής και των φυσίγγων,
πρέπει να αναλυθούν δύο επίπεδα μαρτύρων για τη δοκιμασία HTC.
Τα αποτελέσματα θα πρέπει να εμπίπτουν εντός του εύρους που έχει
προκαθοριστεί από τον κατασκευαστή ή του εύρους που καθορίζεται από
τον χρήστη.
Στους μάρτυρες για τη δοκιμασία ηπαρινάσης υψηλού εύρους
περιλαμβάνονται: ο μάρτυρας πήξης CLOTtrac™ HR
(αρ. καταλόγου 550-07) και ο μάρτυρας CLOTtrac HTC
(αρ. καταλόγου 550-12).
Ο μάρτυρας CLOTtrac HTC παρέχει HR ACT γραμμής αναφοράς στο
κανάλι «HR HTC» και η λήξη του χρονικού ορίου του (>999) σημειώνεται
στο κανάλι «HR ACT».
Αυτός ο μάρτυρας είναι ένας λυοφιλοποιημένος μάρτυρας που περιέχει
6 μονάδες/mL ηπαρίνης. Η απόδοση της φύσιγγας HR HTC επαληθεύεται
με ανάλυση του μάρτυρα σε μια φύσιγγα και με τη λήψη μιας τιμής
HR ACT γραμμής αναφοράς στο κανάλι με τη σήμανση «HR HTC», και με
λήξη χρονικού ορίου (999 δευτερόλεπτα) στο κανάλι με τη σήμανση
«HR». Αυτό υποδεικνύει ότι το κανάλι της φύσιγγας που περιέχει
ηπαρινάση λειτουργεί καταλλήλως.
14. Αναφορές
1. Baugh RF, Deemar KA, Zimmerman JJ. Heparinase in the activated
clotting time assay: Monitoring heparin-independent alterations in
coagulation function. Anesth Analg. 1992;74:201.
2. Bode AP, Eick L. Lysed platelets shorten the activated coagulation
time (ACT) of heparinized blood. Am J Clin Pathol. 1989;91:430.
3. Bull BS, Korpman RA, Huse WM, Briggs BD. Heparin therapy during
extracorporeal circulation. I. Problems inherent in existing heparin
protocols. J Thorac Cardiovasc Surg. 1975;69:674.
4. Bull BS, Huse WM, Brauer FS, Korpman RA. Heparin therapy during
extracorporeal circulation. II. The use of a dose-response curve to
individualize heparin and protamine dosage. J Thorac Cardiovasc
Surg. 1975;69:685.
5. Culliford AT, Gitel SN, Starr N, Thomas ST, Baumann FG, Wessler S,
Spencer FC. Lack of correlation between activated clotting time and
plasma heparin during cardiopulmonary bypass. Ann Surg.
1981;193:105.
6. Dietrich CP, Silva ME, Michelacci YM. Sequential degradation of
heparin in Flavobacterium heparinum. Purification and properties of
five enzymes involved in heparin degradation. J Biol Chem.
1973;248:6408.
7. Effeney DJ, Goldstone J, Chin D, Krupski WC, Ellis RJ. Intraoperative
anticoagulation in cardiovascular surgery. Surgery. 1981;90:1068.
72 Οδηγίες χρήσης Ελληνικά
Page 75

8. Forman WB, Bayer G. A simplified method for monitoring heparin
therapy at the bedside: The activated whole blood clotting time. Am J
Hematol. 1981;11:277.
9. Hattersley PG. Progress report: The activated coagulation time of
whole blood (ACT). Am J Clin Pathol. 1976;66:899.
10. Hutt ED, Kingdon HS. Use of heparinase to eliminate heparin
inhibition in routine coagulation assays. J Lab Clin Med.
1972;79:1027.
11. Kesteven PJ, Pasaoglu I, Williams BT, Savidge GG. Significance of
the whole blood activated clotting time in cardiopulmonary bypass. J
Cardiovasc Surg. 1986;27:85.
12. Mabry CD, Read RC, Thompson BW, Williams GD, White HJ.
Identification of heparin resistance during cardiac and vascular
surgery. Arch Surg. 1979;114:129.
13. Mabry CD, Thompson BW, Read RC. Activated clotting time (ACT)
monitoring of intraoperative heparinization in peripheral vascular
surgery. Am J Surg. 1979;138:894.
14. Mabry CD, Thompson, BW, Read RC, Campbell GS. Activated
clotting time monitoring of intraoperative heparinization: Our
experience and comparison with two techniques. Surgery.
1981;90:889.
15. Moorehead MT, Westengard JC, Bull BS. Platelet involvement in the
activated coagulation time of heparinized blood. Anesth Analg.
1984;63:394.
16. Yang VC, Linhardt RJ, Bernstein H, Cooney CL, Langer R.
Purification and characterization of heparinase from Flavobacterium
heparinum. J Biol Chem. 1985;260:1849.
15. Αποποιητική δήλωση της εγγύησης
Η ΑΚΟΛΟΥΘΗ ΑΠΟΠΟΙΗΤΙΚΗ ΔΗΛΩΣΗ ΤΗΣ ΕΓΓΥΗΣΗΣ
ΙΣΧΥΕΙ ΓΙΑ ΠΕΛΑΤΕΣ ΕΚΤΟΣ ΤΩΝ ΗΝΩΜΕΝΩΝ ΠΟΛΙΤΕΙΩΝ
ΤΗΣ ΑΜΕΡΙΚΗΣ:
ΠΑΡΟΤΙ Η ΦΥΣΙΓΓΑ ΔΟΚΙΜΑΣΙΑΣ ΗΠΑΡΙΝΑΣΗΣ ΥΨΗΛΟΥ ΕΥΡΟΥΣ,
ΕΦΕΞΗΣ ΑΝΑΦΕΡΟΜΕΝΗ ΩΣ «ΠΡΟΪΟΝ», ΕΧΕΙ ΣΧΕΔΙΑΣΤΕΙ,
ΚΑΤΑΣΚΕΥΑΣΤΕΙ ΚΑΙ ΔΟΚΙΜΑΣΤΕΙ ΠΡΟΣΕΚΤΙΚΑ ΠΡΙΝ ΑΠΟ ΤΗΝ
ΠΩΛΗΣΗ ΤΗΣ, ΤΟ ΠΡΟΪΟΝ ΕΝΔΕΧΕΤΑΙ ΝΑ ΑΠΟΤΥΧΕΙ ΣΤΗΝ
ΙΚΑΝΟΠΟΙΗΤΙΚΗ ΕΚΤΕΛΕΣΗ ΤΗΣ ΠΡΟΟΡΙΖΟΜΕΝΗΣ ΛΕΙΤΟΥΡΓΙΑΣ
ΤΟΥ ΛΟΓΩ ΠΟΙΚΙΛΩΝ ΑΙΤΙΩΝ. ΟΙ ΠΡΟΕΙΔΟΠΟΙΗΣΕΙΣ ΠΟΥ
ΠΕΡΙΕΧΟΝΤΑΙ ΣΤΗ ΣΗΜΑΝΣΗ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΠΑΡΕΧΟΥΝ
ΛΕΠΤΟΜΕΡΕΣΤΕΡΕΣ ΠΛΗΡΟΦΟΡΙΕΣ ΚΑΙ ΘΕΩΡΟΥΝΤΑΙ
ΑΝΑΠΟΣΠΑΣΤΟ ΤΜΗΜΑ ΤΗΣ ΠΑΡΟΥΣΑΣ ΑΠΟΠΟΙΗΤΙΚΗΣ ΔΗΛΩΣΗΣ
ΤΗΣ ΕΓΓΥΗΣΗΣ. ΣΥΝΕΠΩΣ, Η MEDTRONIC, ΑΠΟΠΟΙΕΙΤΑΙ ΟΛΕΣ ΤΙΣ
ΕΓΓΥΗΣΕΙΣ, ΡΗΤΕΣ ΚΑΙ ΣΙΩΠΗΡΕΣ, ΣΕ ΣΧΕΣΗ ΜΕ ΤΟ ΠΡΟΪΟΝ. H
MEDTRONIC ΔΕΝ ΘΑ ΕΙΝΑΙ ΥΠΕΥΘΥΝΗ ΓΙΑ ΟΠΟΙΕΣΔΗΠΟΤΕ
ΠΕΡΙΣΤΑΣΙΑΚΕΣ Ή ΕΠΑΚΟΛΟΥΘΕΣ ΖΗΜΙΕΣ ΠΡΟΚΑΛΟΥΜΕΝΕΣ
ΑΠΟ ΟΠΟΙΑΔΗΠΟΤΕ ΧΡΗΣΗ, ΕΛΑΤΤΩΜΑ Ή ΑΣΤΟΧΙΑ ΤΟΥ
ΠΡΟΪΟΝΤΟΣ, ΕΙΤΕ Η ΔΙΕΚΔΙΚΗΣΗ ΑΠΟΖΗΜΙΩΣΕΩΝ ΒΑΣΙΖΕΤΑΙ ΣΕ
ΕΓΓΥΗΣΗ, ΣΥΜΒΑΣΗ, ΑΔΙΚΟΠΡΑΞΙΑ ΕΙΤΕ ΣΕ ΟΤΙΔΗΠΟΤΕ ΑΛΛΟ.
Οι εξαιρέσεις και οι περιορισμοί που ορίζονται ανωτέρω δεν έχουν ως
σκοπό και δεν θα πρέπει να ερμηνεύονται κατά τέτοιο τρόπο ώστε να
αντιβαίνουν στις υποχρεωτικές διατάξεις της ισχύουσας νομοθεσίας. Εάν
οποιοδήποτε τμήμα ή όρος της παρούσας Αποποιητικής Δήλωσης της
Εγγύησης κριθεί από δικαστήριο αρμόδιας δικαιοδοσίας παράνομο(ς), μη
εκτελεστό(ς) ή συγκρουόμενο(ς) με την ισχύουσα νομοθεσία, η
εγκυρότητα του υπολοίπου τμήματος της Αποποιητικής Δήλωσης της
Εγγύησης δεν θα επηρεαστεί και όλα τα δικαιώματα και οι υποχρεώσεις
Οδηγίες χρήσης Ελληνικά 73
Page 76

θα ερμηνεύονται και θα ισχύουν ως εάν η παρούσα Αποποιητική Δήλωση
της Εγγύησης να μην περιείχε το συγκεκριμένο τμήμα ή όρο που κρίθηκε
άκυρο(ς).
74 Οδηγίες χρήσης Ελληνικά
Page 77

1. Tilsigtet brug
Bruges til identificering af tilstedeværelsen af heparin ved hjælp af en
aktiveret koagulationstid.
Anvendes ved in vitro diagnosticering.
Forsigtig: På grund af produktets enestående art er det vigtigt at sikre, at
heparinasen ikke uforvarende overføres fra kassettens "HR HTC"-kanal til
"HR"-kanalen. Se Afsnit 8 og Afsnit 10 for yderligere oplysninger.
2. Resumé
HR HTC-testkassetten fra Medtronic, eller højområdeheparinasetestkassetten, er en ændring af HR ACT-testkassetten
(højområdeaktiveret koagulationstidskassette) til automatiske
koagulationstidsmålere fra Medtronic. Testen af den aktiverede
koagulationstid blev oprindeligt beskrevet af Hattersley i 19669. Testen og
variationerne af denne har været anvendt i stort omfang til at overvåge
heparins antikoagulerende effekt
fuldblod, som det er tilfældet med HR ACT-testkassetten. Forskellen på
kassetterne er, at én kanal indeholder en renset bakteriel heparinase
(HR HTC). Heparinasen ødelægger hurtigt og specifikt den heparin, der
findes i blodprøven
hurtigt 6 enheder/ml heparin. Heparinasekanalen vil give en
koagulationstid, der afspejler baseline for prøvens ikke-hepariniserede
koagulationstid, selvom prøven indeholder heparin. Kassettens anden
kanal er en standard-HR ACT, og den opnåede koagulationstid svarer til
den aktiverede koagulationstid for den hepariniserede prøve. Brug af
denne kassette gør følgende muligt: 1) Verificering af tilstedeværelsen af
heparin forud for kirurgiske indgreb, 2) vurdering af effekten af bypass ved
baselines aktiverede koagulationstid, 3) bekræftelse af ophævelsen af
heparin som følge af administration af protamin, 4) identificering af
"tilbagevendende heparin" efter kirurgisk indgreb og 5) identificering af
tilstedeværelsen af heparin hos patienter, der bløder meget efter
kirurgiske indgreb. Der er en CLOTtrac™ HTC-kontrolmåling tilgængelig
til verificering af, at kassetten fungerer i henhold til specifikationerne.
1,6,10,16
3,4,7,8,13,14
. HR HTC bruger en frisk prøve af
. Den mængde heparinase, der findes, fjerner
3. Principper
Testen af den aktiverede koagulationstid måler koagulationstiden for
friske prøver af fuldblod, der aktiveres ved overfladekontakt. Hattersleys
oprindelige procedure anvendte diatoméjord som aktiveringsmiddel.
Diatoméjord udviser forskellige grader af kontaktaktivering afhængigt af
renheden, aflejringskilde samt partikelstørrelse og -form. Medtronickassetter til aktiveret koagulationstid bruger kaolin som aktiveringsmiddel.
Kaolin udviser suveræne karakteristika i forbindelse med kontaktaktivering
af blodkoagulation. HR ACT og HR HTC udviser en nedsat følsomhed
over for heparin, hvilket muliggør monitorering af højt heparinindhold i
forbindelse med testen af den aktiverede koagulationstid.
Testens effektmål er detektion af koageldannelse. De automatiske
koagulationstidsmålere fra Medtronic registrerer koageldannelsen ved at
monitorere faldhastigheden for den stempel/flagmekanisme, der er findes
i hver af kassettens kanaler. Stempelsættet falder hurtigt igennem en
blodprøve uden koagler. Når der dannes et fibrinnetværk, hæmmes
stemplets fald. Denne aftagen af faldhastigheden registreres af det
fotooptiske system i instrumentets låg. Koageldannelse indiceres af et
lydsignal, og koagelmåleren standses. Disse instrumenter kan udføre
2 simultane tests ved hjælp af kassetten med 2 kanaler.
Koagulationstiderne for hver kanal vises i sekunder, når testen er afsluttet.
I forbindelse med HR HTC viser instrumentet 2 resultater, ét for prøven
med heparinase og ét for prøven uden heparinase. Frontpaneldisplayet
kan bruges til at skifte mellem koagulationstiderne for hver enkelt kanal,
Brugsanvisning Dansk 75
Page 78

eller mellem gennemsnittet og forskellen mellem de to kanaler. Når
HR HTC bruges, har den gennemsnitlige måling kun lille betydning.
Forskellen mellem de to resultater er dog forlængelsen af
koagulationstiden, der skyldes tilstedeværelsen af heparin i prøven.
4. Reagenser
Hvert reagenskammer i kassetten indeholder 0,1 ml HEPES-buffer
(hydroxyethylpiperazin-ethansulfonsyre), kaolin, kalciumklorid og
natriumazid som bakteriehæmmende middel. Den kanal, der er mærket
"HR HTC", indeholder frysetørret, grundigt renset heparinase med
stabiliseringsmidler og natriumazid som bakteriehæmmende middel.
HR HTC-kassetten kan forvarmes i maksimum 2 timer. Når prøven
indføres i den forvarmede kassette, skal testen straks påbegyndes.
5. Opbevaring
HR HTC skal opbevares under stabile forhold, enten ved 2 °C til 10 °C
(36 °F til 50 °F) eller ved 10 °C til 25 °C (50 °F til 77 °F). Kassetterne er
pakket i forseglede bakker med 2 kassetter. Kassetterne er stabile i den
tidsperiode, der er angivet på bakkens etiket. Kassetterne må ikke bruges
efter sidste anvendelsesdato. Kassetterne må ikke bruges, hvis de er
misfarvede, revnede eller misformede, eller hvis reagenset ser ud til at
være fordampet eller kontamineret.
Når forseglingen på bakkens låg er brudt, er kassetterne stabile i 24 timer
ved køleskabstemperatur.
Bemærk: Kassetterne må ikke anvendes, hvis der er tegn på, at de har
været frosset.
6. Instrument
HR HTC er specifikt beregnet til brug i automatiske
koagulationstidsmålere fra Medtronic. Se betjeningshåndbogen til
instrumentet for at få anvisninger.
Det er vigtigt at rengøre instrumentet mindst hver 30. dag eller hyppigere,
hvis det er nødvendigt, for at sikre korrekt ydeevne for instrumentet.
Bemærk: Hvis der kommer blod i aktuatorlåget, skal instrumentet
rengøres hurtigst muligt. Der leveres en aktuatorrengøringspakke
(katalognummer 303-58) sammen med hvert instrument. Anvend
materialerne i hver enkelt rengøringspakke til at udføre
rengøringsproceduren. Se den medfølgende indlægsseddel i
rengøringspakken for at få yderligere oplysninger.
7. Prøvetagning og klargøring af prøver
Prøver, som ikke håndteres korrekt, kan give fejlagtige testresultater.
Derfor skal prøver indsamles med forsigtighed og håndteres konsekvent.
Hvis blod udtages via venepunktur, skal venepunkturen være ren. Kassér
de første mange ml blod for at undgå kontaminering af prøven med
tromboplastin fra væv.
Bemærk: Tag ikke blod fra hepariniserede permanente katetre eller andre
antikoagulationsbehandlede slanger uden at skylle slangen grundigt.
I forbindelse med test af friske prøver af fuldblod skal prøven straks
overføres til kassetten, og testen skal startes.
8. Brugsanvisning
Dette produkt er kun beregnet til at blive anvendt af dertil uddannet
personale.
Leverede materialer:
■
HR HTC-testkassette (højområdeheparinase), katalog nr. 402-07
Nødvendige materialer, ikke del af leverancen
76 Brugsanvisning Dansk
Page 79

■
1
2
Automatisk koagulationstidsmåler fra Medtronic
■
Plastsprøjte med kanyle (helst 18 eller 19 gauge)
Figur 1. Fyldning af HR HTC-kassetten
1. Prøve (set fra siden)
2. Prøve (set ovenfra)
Benyt nedenstående fremgangsmåde for at bruge kassetten sammen
med ACT Plus™-instrumentet:
1. Vælg "Kassettetype" i hovedmenuen, og tryk på tasten, indtil "HTC"
vises. Tryk på "Enter" for at godkende valget.
Bemærk: Der skal indtastes partinumre og Kan anvendes til og meddatoer for kassetter og kontroller, før der køres en test.
2. Indtast "Patient ID"- og "Bruger ID"-numre i hovedmenuen. Tryk på
"Enter" for at godkende.
3. Forvarm kassetten i mindst 3 til 5 minutter, før testprøverne hentes.
4. Bank på kassetten for at resuspendere reagenset.
5. Fyld hvert kammer med 0,4 ml af prøven.
Bemærk: Fyld altid HR-kanalen først og dernæst HR HTC-kanalen
for at sikre, at heparinasen ikke kontaminerer HR-kanalen.
6. Sæt kassetten i ACT Plus-instrumentet, og luk aktuatorens varmeblok
for at påbegynde testen.
7. Ved koageldannelse lyder der en tone, aktuatorens varmeblok åbner,
og resultaterne vises.
Når testen er fuldført, bortskaffes kassetten, sprøjten og kanylen i
beholdere til bortskaffelse af materiale med biologisk risiko.
9. Resultater
Responsen af den aktiverede koagulationstid på heparin varierer
væsentligt fra person til person12. En række lægemidler påvirker den
aktiverede koagulationstid, særligt lægemidler, der hæmmer
trombocytaktivering15. En række andre faktorer kan påvirke responsen af
en persons aktiverede koagulationstid på heparin, f.eks. antitrombin IIIniveauer, heparinets styrke, koagulationsfaktormangel, prøveaktivering,
dissemineret intravaskulær koagulation, kraftig prøvefortynding samt
prøvens temperatur. Disse skal tages med i betragtning, når resultaterne
af testen af den aktiverede koagulationstid tolkes
Heparinasen i kassettens HR HTC-kanal er yderst specifik for heparin.
Der er tilstrækkelig med heparinase til stede for at sikre, at 6 enheder/ml
2,5,11
.
Brugsanvisning Dansk 77
Page 80

heparin fjernes hurtigt fra prøven for at bringe den tilbage til baseline eller
en ikke-hepariniseret tilstand. Baselinetidspunktet kan være eller er ikke
inden for eller tæt på normalområdet. Hvis baseline ikke er inden for
normalområdet i HR HTC-kanalen, indikerer det, at der foreligger en
anden tilstand ud over tilstedeværelsen af heparin, som forårsager den
forlængede baselinekoagulationstid.
Eksempler på tolkning af HR HTC-resultaterne:
Ka 1
120 120 Patienten ved baseline, ingen heparin i prø-
120 260 Patienten har heparin i blodet. Forlængelsen
260 260 Patienten har underliggende koagulopati, der
260 360 Patienten har heparin i blodet, og patienten
60 200 Patienten har heparin i blodet, og patientens
Ka 2 Tolkning
ven.
skyldes kun heparins virkning.
er ikke relateret til heparin.
har underliggende koagulopati (sandsynligvis hæmofortynding).
koagulationssystem er aktiveret.
10. Procedurens begrænsninger
Følgende forhold skal overholdes for at opnå nøjagtige og konsekvente
koagulationstider med HR HTC:
■
Temperaturen i instrumentets varmeblok og kassette skal være 37 °C
± 0,5 °C (98,6 °F ± 0,9 °F). Kassetten når temperaturen i løbet af 3 5 minutter i instrumentets varmeblok.
■
Kaolinaktivatoren skal resuspenderes grundigt.
■
Blodet må ikke indeholde vævstromboplastin. Foretag testen hurtigst
muligt, efter at blodprøven er taget.
■
Patientens diagnose og medicinering skal noteres. Medicinering kan
ændre koagulationstiderne. Prøver, der giver uforklarede abnorme
værdier, skal tages om og testes igen. Hvis resultaterne er stadig
abnorme, og der ikke findes nogen tydelig årsag, skal en af prøverne
citreres og sendes til det kliniske laboratorium med henblik på en
særlig koagulationsanalyse.
■
For at optimere nøjagtigheden skal alle tekniske variabler være ens
fra test til test.
■
Når prøven er anbragt i kassetten, skal testen foretages hurtigst
muligt. Heparinet fjernes hurtigt fra prøven. Der forekommer
kontaktaktivering i kassetten, når der ikke er mere heparin i prøven.
Dette resulterer i kortere koagulationstider, da aktiveringen af prøven
fortsætter.
■
De metoder, der anvendes til kardiopulmonal bypassoperation,
ændres kontinuerligt ligesom patientpopulationens karasteristik.
Forhold, der kan påvirke testresultaterne af den aktiverede
koagulationstid, omfatter, men er ikke begrænset til:
■
patienten overfølsomhed over for heparin
■
fortynding af koagulationsfaktorer ved det ekstrakorporale
kredsløb
■
brugen af citrerede blodprodukter
■
brugen af trombocytfunktonshæmmende lægemidler
■
hypotermi
■
svingende calciumniveauer
■
en ændring i trombocytfunktionen eller trombocyttallet
■
ukendte koagulopatier.
78 Brugsanvisning Dansk
Page 81

Kraftig blodfortynding under bypass, ofte på grund af et ønske om at
begrænse brugen af heterologe blodprodukter, kan forårsage
postoperativ blødning. I svære tilfælde kan fortyndingen være så
udtalt, at der ikke forekommer koagulationen, der måles som den
aktiverede koagulationstid. Tilstedeværelsen af tilstrækkelige
plasmakoagulationsfaktorer kan ikke bestemmes ved at korrelere
omfanget af fortyndingen med patientens hæmatokritværdi. Ofte har
patienten modtaget udvaskede celler, uden at der er kompenseret for
det mistede plasma. Hvis HR HTC ikke kan koagulere i
heparinasekanalen (kanal nr. 1), efter en ophævelse af patientens
heparin med protamin, er der en stærk indikation på, at der er opstået
fortyndingskoagulopati.
Advarsel: På grund af HR HTC's formel må den ikke ikke bruges til at
overvåge den regionale antikoagulation, der er opnået ved at
infundere citrat.
Forsigtig: Der skal udvises ekstrem forsigtighed for at sikre, at
heparinasen i HR HTC-kanalen, ikke overføres utilsigtet til prøven i
kassettens HR-kanal. Hvis dette sker, er den hepariniserede
koagulationstid i "HR"-kanalen ikke længere repræsentativ for
mængden af heparin i prøven, men ville indikere, at der var mindre
heparin, afhængigt af hvor meget heparinase der var blevet overført.
Det anbefales derfor kraftigt, at "HR"-kanalen fyldes først for at
minimere risikoen for heparinaseoverførsel.
Se betjeningshåndbogen for at få forsigtighedsregler og oplysninger
om instrumentets begrænsninger.
11. Forventede værdier
Heparinasekanalen viser effektivt den aktiverede koagulationstid ved
baseline af friske prøver af hepariniseret fuldblod. Under bypass kan
værdien for den aktiverede koagulationstid ved baseline afvige i
opadgående retning, hvilket afspejler hæmofortyndingen af patientens
blod. Koagulationstiden ved baseline korrelerer med fortyndingen af
plasmakoagulationsfaktorer, som ikke nødvendigvis korrelerer med
patientens hæmatokritværdi. De erytrocytter, der føres tilbage til en
patient fra en cell-saver, kompenserer ikke for mistede
plasmakoagulationsfaktorer. Hvis den aktiverede koagulationstid ved
baseline forbliver forlænget, kan der forekomme fortyndingskoagulopati
(mangel på tilstrækkelige koagulationsfaktorer), og der kan opstå
postoperativ blødning. HR HTC kan overvåge udviklingen af situationen
og muliggøre helbredende behandling, før der forekommer svær
fortynding af koagulationsfaktorerne.
12. Specifikke præstationskarakteristikker
I kassetter med en aktiveret koagulationstid i koagulationsområdet fra 0 600 sekunder er forskellen mellem to prøver for en person normalt ikke
mere end 12%. Ved høje heparinniveauer og koagulationstider på mere
end 600 sekunder anses en aktiveret koagulationstid generelt ikke for at
være tilstrækkelig pålidelig til at bestemme heparinniveauerne.
HR HTC har en formel, der er beregnet på at give en normal HR ACT i
den kanal, der kaldes "HR", hvilket svarer nøje til de svar, der oprindeligt
blev rapporteret af Bull, et al (1975). Kaolinaktivatoren i hvert kassetteparti
er blevet kalibreret til at reducere variationer i aktiviteten mellem partierne
til mindre end 10% og minimere afvigelser på lang sigt.
Ydeevnen af kassettens "baselinekanal" afhænger af aktiviteten af
heparinasen i den kanal, der hedder "HR HTC". Heparinasen er blevet
renset og stabiliseret, så der fjernes 6 enheder/ml heparin i et tidsrum, der
er tilstrækkeligt kort til at returnere det hepariniserede blod til en
baselinekoagulationstid. Stabiliteten af heparinasen sikres ved at sørge
for, at kassetternes temperatur er konstant. Temperaturområderne i hvilke
Brugsanvisning Dansk 79
Page 82

kassetterne må opbevares er enten fra 2 °C til 10 °C (36 °F til 50 °F) eller
fra 10 °C til 25 °C (50 °F til 77 °F). Kassetteydeevnen forringes evt., hvis
produktet ikke opbevares i et stabilt miljø. Det anbefales ikke at flytte
produktet fra kølerum til stuetemperatur eller fra stuetemperatur til
kølerum.
13. Kvalitetskontrol
Der skal udføres to kontrolniveauer i forbindelse med HTC-testen for at
sikre en tilstrækkelig ydevne af instrumentet og kassetterne.
Resultaterne skal ligge inden for de intervaller, som fabrikanten har anført,
eller inden for de intervaller, som brugeren angiver.
Kontrollerne for højområdeheparinasetesten omfatter: CLOTtrac™ HRkoagulationskontrollen (katalog nr. 550-07) og CLOTtrac HTC-kontrollen
(katalog nr. 550-12).
CLOTtrac HTC-kontrollen giver en baseline-HR ACT i HR HTC-kanalen
og foretager en timeout (>999) i HR ACT-kanalen.
Kontrollen er en frysetørret kontrol, der indeholder 6 enheder/ml heparin.
Ydeevnen af HR HTC bekræftes ved at udføre kontrollen i en kassette og
opnå en HR ACT-baselineværdi i den kanal, der hedder "HR HTC" samt
en timeout (999 sekunder) i den kanal, der hedder "HR". Dette angiver, at
den kanal i kassetten, der indeholder heparinase, fungerer korrekt.
14. Henvisninger
1. Baugh RF, Deemar KA, Zimmerman JJ. Heparinase in the activated
clotting time assay: Monitoring heparin-independent alterations in
coagulation function. Anesth Analg. 1992;74:201.
2. Bode AP, Eick L. Lysed platelets shorten the activated coagulation
time (ACT) of heparinized blood. Am J Clin Pathol. 1989;91:430.
3. Bull BS, Korpman RA, Huse WM, Briggs BD. Heparin therapy during
extracorporeal circulation. I. Problems inherent in existing heparin
protocols. J Thorac Cardiovasc Surg. 1975;69:674.
4. Bull BS, Huse WM, Brauer FS, Korpman RA. Heparin therapy during
extracorporeal circulation. II. The use of a dose-response curve to
individualize heparin and protamine dosage. J Thorac Cardiovasc
Surg. 1975;69:685.
5. Culliford AT, Gitel SN, Starr N, Thomas ST, Baumann FG, Wessler S,
Spencer FC. Lack of correlation between activated clotting time and
plasma heparin during cardiopulmonary bypass. Ann Surg.
1981;193:105.
6. Dietrich CP, Silva ME, Michelacci YM. Sequential degradation of
heparin in Flavobacterium heparinum. Purification and properties of
five enzymes involved in heparin degradation. J Biol Chem.
1973;248:6408.
7. Effeney DJ, Goldstone J, Chin D, Krupski WC, Ellis RJ. Intraoperative
anticoagulation in cardiovascular surgery. Surgery. 1981;90:1068.
8. Forman WB, Bayer G. A simplified method for monitoring heparin
therapy at the bedside: The activated whole blood clotting time. Am J
Hematol. 1981;11:277.
9. Hattersley PG. Progress report: The activated coagulation time of
whole blood (ACT). Am J Clin Pathol. 1976;66:899.
10. Hutt ED, Kingdon HS. Use of heparinase to eliminate heparin
inhibition in routine coagulation assays. J Lab Clin Med.
1972;79:1027.
11. Kesteven PJ, Pasaoglu I, Williams BT, Savidge GG. Significance of
the whole blood activated clotting time in cardiopulmonary bypass. J
Cardiovasc Surg. 1986;27:85.
80 Brugsanvisning Dansk
Page 83

12. Mabry CD, Read RC, Thompson BW, Williams GD, White HJ.
Identification of heparin resistance during cardiac and vascular
surgery. Arch Surg. 1979;114:129.
13. Mabry CD, Thompson BW, Read RC. Activated clotting time (ACT)
monitoring of intraoperative heparinization in peripheral vascular
surgery. Am J Surg. 1979;138:894.
14. Mabry CD, Thompson, BW, Read RC, Campbell GS. Activated
clotting time monitoring of intraoperative heparinization: Our
experience and comparison with two techniques. Surgery.
1981;90:889.
15. Moorehead MT, Westengard JC, Bull BS. Platelet involvement in the
activated coagulation time of heparinized blood. Anesth Analg.
1984;63:394.
16. Yang VC, Linhardt RJ, Bernstein H, Cooney CL, Langer R.
Purification and characterization of heparinase from Flavobacterium
heparinum. J Biol Chem. 1985;260:1849.
15. Ansvarsfraskrivelse
FØLGENDE ANSVARSFRASKRIVELSE GÆLDER FOR
KUNDER UDEN FOR USA:
SELVOM HR HTC-TESTKASSETTEN, I DET FØLGENDE KALDET
"PRODUKTET", ER OMHYGGELIGT DESIGNET, FREMSTILLET OG
AFPRØVET FØR SALG, KAN DER AF MANGE GRUNDE VÆRE EN
RISIKO FOR, AT PRODUKTET IKKE FUNGERER
TILFREDSSTILLENDE EFTER HENSIGTEN. ADVARSLERNE, SOM
FREMGÅR AF PRODUKTETS MÆRKATER, GIVER NÆRMERE
OPLYSNINGER OG BETRAGTES SOM EN INTEGRERET DEL AF
DENNE ANSVARSFRASKRIVELSE. MEDTRONIC FRASKRIVER SIG
DERFOR ALLE GARANTIER, UDTRYKKELIGE SÅVEL SOM
UNDERFORSTÅEDE, I FORHOLD TIL PRODUKTET. MEDTRONIC
KAN IKKE HOLDES ANSVARLIG FOR TILFÆLDIGE SKADER ELLER
FØLGESKADER SOM FØLGE AF BRUG AF PRODUKTET, ELLER
DETS DEFEKT ELLER FEJLFUNKTION, UANSET OM KRAVET
BASERES PÅ GARANTIRET, AFTALERET, ERSTATNINGSRET UDEN
FOR KONTRAKT ELLER ANDEN RETSLÆRE.
Ovennævnte undtagelser og begrænsninger har ikke til hensigt at være
og må ikke fortolkes således, at de kommer i modstrid med ufravigelige
bestemmelser i gældende lov. Hvis dele af eller vilkår i denne
ansvarsfraskrivelse af en retsinstans i en kompetent jurisdiktion anses for
ulovlige, uden retskraft eller i konflikt med den relevante lovgivning,
berøres de resterende dele af ansvarsfraskrivelsen ikke, og alle
rettigheder og forpligtelser skal tolkes og håndhæves, som om denne
ansvarsfraskrivelse ikke indeholdt de pågældende dele eller vilkår, der
anses for ugyldige.
Brugsanvisning Dansk 81
Page 84

1. Utilização prevista
Para utilização na identificação da presença de heparina, utilizando um
tempo de coagulação ativada.
Para utilização em diagnóstico in vitro.
Atenção: Devido à natureza única deste produto, proceda com cuidado
para garantir que não ocorre transferência involuntária de heparinase do
canal "HR HTC" para o canal "HR" do cartucho. Para mais informações,
consulte a Secção 8 e a Secção 10.
2. Resumo
O cartucho para teste com heparinase - valores altos da Medtronic, ou
HR HTC, é uma modificação do cartucho de tempo de coagulação
ativada - valores altos (HR ACT) para os medidores automáticos do
tempo de coagulação da Medtronic. O teste do tempo de coagulação
ativada foi descrito originalmente por Hattersley em 1966.9 O teste e as
suas variantes têm sido largamente utilizados para monitorizar o efeito
anticoagulante da heparina.
cartucho HR HTC utiliza uma amostra de sangue total colhido
recentemente. A diferença neste cartucho é que um canal contém uma
heparinase bacteriana purificada (HR HTC). A heparinase destrói de
forma rápida e específica a heparina presente na amostra de sangue.
1,6,10,16
A quantidade de heparinase presente removerá rapidamente
6 unidades/ml de heparina. O canal com heparinase produz um tempo de
coagulação que reflete o tempo de coagulação basal da amostra não
heparinizada, apesar de a amostra conter heparina. O outro canal do
cartucho é um HR ACT padrão e o tempo de coagulação obtido é o
tempo de coagulação ativada da amostra heparinizada. A utilização deste
cartucho permite: 1) a verificação da presença pré-cirúrgica de heparina,
2) a avaliação do efeito do bypass no valor basal do tempo de
coagulação ativada, 3) a confirmação da reversão do efeito da heparina
após administração de protamina, 4) a identificação do "efeito rebound da
heparina" pós-cirúrgico e 5) a identificação da presença de heparina em
doentes com sangramento pós-cirúrgico excessivo. Um controlo
CLOTtrac™ HTC permite verificar se o cartucho está a funcionar de
acordo com as especificações.
3,4,7,8,13,14
Tal como o cartucho HR ACT, o
3. Princípios
O teste do tempo de coagulação ativada mede o tempo de coagulação de
sangue total colhido recentemente, ativada por contacto de superfície. O
procedimento original de Hattersley utilizou terra de diatomáceas como
agente de ativação. A terra de diatomáceas apresenta diferentes graus
de ativação por contacto dependendo da sua pureza, da origem do
depósito e do tamanho e forma das partículas. Os cartuchos de tempo de
coagulação ativada da Medtronic utilizam caulino como agente de
ativação. O caulino possui características superiores na ativação por
contacto da coagulação sanguínea. Os cartuchos HR ACT e HR HTC
apresentam uma sensibilidade reduzida à heparina, o que permite a
monitorização de níveis elevados de heparina com o teste do tempo de
coagulação ativada.
O objetivo final do teste é a deteção da formação de coágulos. Os
medidores automáticos do tempo de coagulação da Medtronic detetam a
formação de um coágulo através da monitorização da velocidade de
descida do êmbolo/mecanismo de sinalização contido em cada canal do
cartucho. A unidade do êmbolo desce rapidamente através de sangue
não coagulado. Quando se forma uma rede de fibrina, a descida da
unidade do êmbolo é dificultada. Esta diminuição da velocidade de
descida é detetada pelo sistema foto-ótico situado na unidade da tampa
do instrumento. A formação do coágulo é indicada por um sinal sonoro e
82 Instruções de utilização Português (PT)
Page 85

o temporizador da coagulação é parado. Os instrumentos podem realizar
2 testes em simultâneo, utilizando o cartucho com 2 canais. Os tempos
de coagulação para cada canal são indicados em segundos após a
conclusão do teste. Com o cartucho HR HTC, o instrumento apresenta
2 resultados: um para a amostra com heparinase e um para a amostra
sem heparinase. O visor do painel frontal pode ser utilizado para alternar
entre os tempos de coagulação dos canais individuais ou entre a média e
a diferença entre os dois canais. Quando se utiliza o cartucho HR HTC, a
leitura média tem pouco significado. No entanto, a diferença entre os dois
resultados é o prolongamento do tempo de coagulação devido à
presença de heparina na amostra.
4. Reagentes
Cada câmara de reagentes do cartucho contém 0,1 ml de tampão HEPES
(ácido 2-[4-(2-hidroxietil)1-piperazinil]-etanosulfónico), caulino, cloreto de
cálcio e azida de sódio como agente bacteriostático. O canal identificado
como "HR HTC" contém heparinase liofilizada de elevada pureza,
juntamente com agentes estabilizadores e azida de sódio como agente
bacteriostático.
O cartucho HR HTC pode ser previamente aquecido durante um período
máximo de 2 horas. Uma vez a amostra introduzida no cartucho
pré-aquecido, o teste deve iniciar-se imediatamente.
5. Armazenamento
O cartucho HR HTC deve ser armazenado num ambiente estável, a uma
temperatura no intervalo de 2 °C a 10 °C (36 °F a 50 °F) ou de
10 °C a 25 °C (50 °F a 77 °F). Os cartuchos são embalados em tabuleiros
selados de 2 cartuchos. Os cartuchos são estáveis pelo período de tempo
indicado na etiqueta do tabuleiro. Não utilize os cartuchos após a data de
validade. Não utilize o cartucho se este parecer descolorado, rachado ou
danificado, ou se o reagente aparentar ter sofrido evaporação ou estar
contaminado.
Depois de o selo na tampa do tabuleiro ser quebrado, os cartuchos são
estáveis durante 24 horas a temperaturas refrigeradas.
Nota: Não utilize se houver evidência de congelamento.
6. Instrumento
O cartucho HR HTC foi especificamente concebido para utilização em
medidores automáticos do tempo de coagulação da Medtronic. Consulte
o manual do operador do instrumento para obter instruções.
Para garantir um desempenho adequado do instrumento, é importante
limpar o instrumento pelo menos uma vez a cada 30 dias, ou mais se
necessário.
Nota: Se entrar sangue na proteção do acionador, limpe o instrumento o
mais rapidamente possível. Cada instrumento é fornecido com um
conjunto de limpeza do acionador (número de catálogo 303-58). Utilize os
materiais disponibilizados em cada conjunto de limpeza para efetuar o
procedimento de limpeza. Consulte o folheto incluído na embalagem do
conjunto de limpeza para obter pormenores.
7. Colheita e preparação das amostras
As amostras manuseadas indevidamente podem fornecer resultados
erróneos do teste de coagulação. Por conseguinte, as amostras devem
ser colhidas com cuidado e as técnicas de manuseamento devem ser
consistentes.
Se o sangue for obtido por punção venosa, a punção deve ser limpa.
Rejeite os primeiros mililitros de sangue para evitar a contaminação da
amostra com tromboplastina tecidual.
Instruções de utilização Português (PT) 83
Page 86

Nota: Não colha sangue de cateteres permanentes heparinizados nem
1
2
de outras vias anticoaguladas sem um enxaguamento prévio completo da
linha.
Ao testar sangue total colhido recentemente, transfira imediatamente a
amostra para o cartucho e inicie o teste.
8. Instruções de utilização
Este produto só deve ser utilizado por técnicos experientes.
Materiais fornecidos:
■
Cartucho para teste com heparinase - valores altos (HR HTC),
número de catálogo 402-07
Materiais necessários, não fornecidos
■
Medidor automático do tempo de coagulação da Medtronic
■
Seringa de plástico com agulha (preferencialmente de
calibre 18 ou 19)
Figura 1. Enchimento do cartucho HR HTC
1. Amostra (vista lateral)
2. Amostra (vista de cima)
Para utilizar com o instrumento ACT Plus™, siga os passos seguintes:
1. A partir de "Main Menu" (Menu principal), selecione "Cartridge Type"
(Tipo de cartucho) e prima a tecla até surgir "HTC". Prima "Enter"
para confirmar a seleção.
Nota: Antes de efetuar uma análise, é necessário introduzir os
números de lote e a data de validade para os cartuchos e os
controlos.
2. A partir de "Main Menu" (Menu principal), introduza os números de
"Patient ID" (ID do doente) e "User ID" (ID do utilizador). Prima
"Enter" para confirmar.
3. Aqueça previamente o cartucho, durante 3 a 5 minutos, antes de
efetuar a colheita da amostra a testar.
4. Bata levemente no cartucho para ressuspender o reagente.
5. Encha cada câmara com 0,4 ml de amostra.
Nota: Encha sempre primeiro o canal HR e depois o canal HR HTC
para garantir que a heparinase não contamina o canal HR.
6. Introduza o cartucho no instrumento ACT Plus e feche o bloco
térmico do acionador para iniciar a análise.
84 Instruções de utilização Português (PT)
Page 87

7. A formação de coágulos é assinalada pela emissão de um sinal
sonoro, o bloco térmico do acionador abre-se e os resultados são
apresentados.
Após conclusão do teste, elimine o cartucho, a seringa e a agulha em
recipientes aprovados para a eliminação de materiais biológicos
perigosos.
9. Resultados
A resposta do tempo de coagulação ativada à heparina varia
consideravelmente de indivíduo para indivíduo.12 Vários fármacos afetam
o tempo de coagulação ativada, em particular os fármacos que inibem a
ativação plaquetária.15 Há uma série de outros fatores que podem afetar a
resposta do tempo de coagulação ativada de um indivíduo à heparina,
por exemplo, os níveis de antitrombina III, a potência da heparina, as
deficiências de fatores de coagulação, a ativação da amostra, as
coagulopatias de consumo, a diluição excessiva da amostra e a
temperatura da amostra. Estes fatores devem ser tomados em
consideração aquando da interpretação dos resultados do teste do tempo
de coagulação ativada.
A heparinase no canal HR HTC do cartucho é extremamente específica
para a heparina. Está presente uma quantidade suficiente de heparinase
para garantir a remoção rápida de 6 unidades/ml de heparina da amostra,
de modo a trazer a amostra de volta para um estado não heparinizado ou
basal. O tempo basal poderá ou não estar dentro do intervalo normal ou
próximo dele. Caso a linha de base não esteja dentro do intervalo normal
no canal HR HTC, esse resultado indica que alguma outra condição que
não a presença de heparina é responsável pelo prolongamento do tempo
de coagulação basal.
Exemplo para interpretar os resultados do cartucho HR HTC:
Canal 1 Canal 2 Interpretação
120 120 Doente na linha de base, não existe hepa-
120 260 Doente tem heparina no sangue. Prolonga-
260 260 Doente tem coagulopatia subjacente não
260 360 Doente tem heparina no sangue e doente
60 200 Doente tem heparina no sangue e sistema
2,5,11
rina na amostra.
mento devido apenas ao efeito da heparina.
relacionada com heparina.
tem coagulopatia subjacente (provavelmente
hemodiluição).
de coagulação do doente está ativado.
10. Limitações do procedimento
Para obter tempos de coagulação ativada consistentes e precisos com o
cartucho HR HTC, é necessário respeitar as seguintes condições:
■
A temperatura do bloco térmico do instrumento e do cartucho deve
rondar os 37 °C ± 0,5 °C (98,6 °F ± 0,9 °F). O cartucho atingirá a
temperatura no espaço de 3 a 5 minutos após colocação no bloco
térmico do instrumento.
■
O agente de ativação caulino deverá ser muito bem ressuspenso.
■
O sangue não pode conter tromboplastina tecidual. Efetue a análise
logo que possível após a colheita da amostra de sangue.
■
O diagnóstico e a medicação do doente devem ser tidos em conta.
Os fármacos podem alterar os tempos de coagulação. As amostras
que forneçam valores anómalos inexplicáveis devem ser novamente
colhidas e analisadas. Caso os resultados ainda sejam anómalos e
não haja causa aparente, uma amostra deverá ser citrada e enviada
Instruções de utilização Português (PT) 85
Page 88

para um laboratório clínico para ser submetida a uma análise de
coagulação especial.
■
No sentido de otimizar a precisão, as variáveis de todas as técnicas
devem ser consistentes de teste para teste.
■
Após a colocação da amostra no cartucho, a análise deve ser
realizada o mais rapidamente possível. A remoção da heparina da
amostra ocorre rapidamente. Quando a amostra não contém
heparina, tem lugar a ativação por contacto no cartucho. Este
procedimento resultará em tempos de coagulação mais curtos à
medida que a ativação da amostra prossegue.
■
As metodologias utilizadas na cirurgia de bypass cardiopulmonar
variam continuamente, assim como as características da população
de doentes. As condições que podem influenciar os resultados do
teste do tempo de coagulação ativada incluem, entre outros:
■
a sensibilidade do doente à heparina
■
a diluição dos fatores de coagulação pelo circuito extracorporal
■
a utilização de produtos sanguíneos citrados
■
a utilização de fármacos antiplaquetários
■
hipotermia
■
níveis de cálcio flutuantes
■
uma alteração da contagem ou da função das plaquetas
■
coagulopatias desconhecidas
Uma diluição excessiva do sangue durante o bypass, frequentemente
devido ao desejo de limitar a utilização de produtos sanguíneos
heterólogos, pode conduzir a sangramento pós-operatório. Em casos
graves, a diluição pode ser tão grande que a coagulação, medida
pelo tempo de coagulação ativada, não se verifica. A adequação dos
fatores de coagulação do plasma não pode ser determinada por
correlação da extensão da diluição com o hematócrito do doente.
Com frequência, as células lavadas foram administradas ao doente
sem que tenha havido compensação do plasma perdido. Se o
cartucho HR HTC não conseguir efetuar a coagulação no canal com
heparinase (canal n.º 1), após reversão do efeito da heparina com
protamina, a existência de uma coagulopatia dilucional é uma forte
possibilidade.
Aviso: Devido à sua formulação, o cartucho HR HTC não deve ser
utilizado para monitorizar a anticoagulação regional obtida através da
infusão de citrato.
Atenção: É necessário um cuidado extremo para garantir que a
heparinase no canal HR HTC não é transferida involuntariamente
para a amostra no canal HR do cartucho. No caso de isso se verificar,
o tempo de coagulação da amostra heparinizada no canal "HR"
deixaria de ser representativo da quantidade de heparina presente na
amostra e indicaria menos heparina, dependendo da quantidade de
heparinase transferida. Por este motivo, recomenda-se vivamente
que o canal "HR" seja cheio em primeiro lugar para minimizar a
possibilidade de transferência de heparinase.
Para ver as precauções e limitações do instrumento, consulte o
manual do operador.
11. Valores esperados
O canal com heparinase fornece efetivamente um tempo de coagulação
ativada basal em sangue total heparinizado colhido recentemente.
Durante o bypass, o valor basal do tempo de coagulação ativada poderá
sofrer flutuações para cima, refletindo a hemodiluição do sangue do
doente. O tempo de coagulação basal está correlacionado com a diluição
dos fatores de coagulação do plasma, que não está necessariamente
correlacionada com o hematócrito do doente. Os glóbulos vermelhos
86 Instruções de utilização Português (PT)
Page 89

devolvidos ao doente a partir de um recuperador de células não fazem a
compensação dos fatores de coagulação do plasma perdidos. Caso o
tempo de coagulação ativada basal permaneça alargado, é possível que
se verifique uma coagulopatia dilucional (ausência de quantidade
suficiente de fatores de coagulação) e se observe sangramento pósoperatório. O cartucho HR HTC pode monitorizar o desenvolvimento
desta situação e permitir uma ação corretiva antes que ocorra uma
diluição grave dos fatores de coagulação.
12. Características específicas de desempenho
Os cartuchos de tempo de coagulação ativada, no intervalo de
coagulação de 0 a 600 segundos, normalmente não excedem uma
variação de 12% entre amostras duplicadas para um determinado
indivíduo. Para níveis elevados de heparina e tempos de coagulação
acima de 600 segundos, um tempo de coagulação ativada geralmente
não é considerado suficientemente fiável para a determinação dos níveis
de heparina.
O cartucho HR HTC foi formulado para produzir um HR ACT normal no
canal identificado como "HR", o que corresponde de perto às respostas
originalmente referidas por Bull, et al (1975). Em cada lote de cartuchos,
o agente de ativação caulino foi calibrado para reduzir as variações de
atividade entre lotes para menos de 10%, bem como para minimizar a
flutuação a longo prazo.
O desempenho do canal "basal" do cartucho depende da atividade da
heparinase no canal identificado como "HR HTC". A heparinase foi
purificada e estabilizada para remover 6 unidades/ml de heparina, num
espaço de tempo suficientemente curto para retornar o sangue
heparinizado a um tempo de coagulação basal. A estabilidade da
heparinase é garantida através da manutenção dos cartuchos a uma
temperatura constante. Os intervalos de temperatura em que os
cartuchos podem ser armazenados são 2 °C a 10 °C (36 °F a 50 °F) ou
10 °C a 25 °C (50 °F a 77 °F). O desempenho do cartucho poderá
diminuir caso o produto não seja armazenado num ambiente estável. A
movimentação repetida do produto de condições refrigeradas para
condições ambientais ou vice-versa não é recomendada.
13. Controlo de qualidade
De modo a garantir um desempenho adequado do instrumento e dos
cartuchos, o teste HTC deve ser submetido a dois níveis de controlos.
Os resultados deverão situar-se dentro dos intervalos especificados pelo
fabricante ou dentro dos intervalos determinados pelo utilizador.
Os controlos para o teste com heparinase - valores altos incluem: o
controlo de coagulação CLOTtrac™ HR (número de catálogo 550-07) e o
controlo CLOTtrac HTC (número de catálogo 550-12).
O controlo CLOTtrac HTC fornece um valor HR ACT basal no canal
HR HTC e excederá o tempo possível (>999) no canal HR ACT.
Este controlo é um controlo liofilizado que contém 6 unidades/ml de
heparina. O desempenho do cartucho HR HTC é verificado mediante
processamento do controlo num cartucho e obtenção de um valor
HR ACT basal no canal identificado como "HR HTC" e de um "timeout"
(999 segundos) no canal identificado como "HR". Este resultado indica
que o canal do cartucho que contém a heparinase está a funcionar
corretamente.
14. Bibliografia
1. Baugh RF, Deemar KA, Zimmerman JJ. Heparinase in the activated
clotting time assay: Monitoring heparin-independent alterations in
coagulation function. Anesth Analg. 1992;74:201.
Instruções de utilização Português (PT) 87
Page 90

2. Bode AP, Eick L. Lysed platelets shorten the activated coagulation
time (ACT) of heparinized blood. Am J Clin Pathol. 1989;91:430.
3. Bull BS, Korpman RA, Huse WM, Briggs BD. Heparin therapy during
extracorporeal circulation. I. Problems inherent in existing heparin
protocols. J Thorac Cardiovasc Surg. 1975;69:674.
4. Bull BS, Huse WM, Brauer FS, Korpman RA. Heparin therapy during
extracorporeal circulation. II. The use of a dose-response curve to
individualize heparin and protamine dosage. J Thorac Cardiovasc
Surg. 1975;69:685.
5. Culliford AT, Gitel SN, Starr N, Thomas ST, Baumann FG, Wessler S,
Spencer FC. Lack of correlation between activated clotting time and
plasma heparin during cardiopulmonary bypass. Ann Surg.
1981;193:105.
6. Dietrich CP, Silva ME, Michelacci YM. Sequential degradation of
heparin in Flavobacterium heparinum. Purification and properties of
five enzymes involved in heparin degradation. J Biol Chem.
1973;248:6408.
7. Effeney DJ, Goldstone J, Chin D, Krupski WC, Ellis RJ. Intraoperative
anticoagulation in cardiovascular surgery. Surgery. 1981;90:1068.
8. Forman WB, Bayer G. A simplified method for monitoring heparin
therapy at the bedside: The activated whole blood clotting time. Am J
Hematol. 1981;11:277.
9. Hattersley PG. Progress report: The activated coagulation time of
whole blood (ACT). Am J Clin Pathol. 1976;66:899.
10. Hutt ED, Kingdon HS. Use of heparinase to eliminate heparin
inhibition in routine coagulation assays. J Lab Clin Med.
1972;79:1027.
11. Kesteven PJ, Pasaoglu I, Williams BT, Savidge GG. Significance of
the whole blood activated clotting time in cardiopulmonary bypass. J
Cardiovasc Surg. 1986;27:85.
12. Mabry CD, Read RC, Thompson BW, Williams GD, White HJ.
Identification of heparin resistance during cardiac and vascular
surgery. Arch Surg. 1979;114:129.
13. Mabry CD, Thompson BW, Read RC. Activated clotting time (ACT)
monitoring of intraoperative heparinization in peripheral vascular
surgery. Am J Surg. 1979;138:894.
14. Mabry CD, Thompson, BW, Read RC, Campbell GS. Activated
clotting time monitoring of intraoperative heparinization: Our
experience and comparison with two techniques. Surgery.
1981;90:889.
15. Moorehead MT, Westengard JC, Bull BS. Platelet involvement in the
activated coagulation time of heparinized blood. Anesth Analg.
1984;63:394.
16. Yang VC, Linhardt RJ, Bernstein H, Cooney CL, Langer R.
Purification and characterization of heparinase from Flavobacterium
heparinum. J Biol Chem. 1985;260:1849.
15. Renúncia de garantia
A SEGUINTE RENÚNCIA DE GARANTIA APLICA-SE A
CLIENTES NO EXTERIOR DOS ESTADOS UNIDOS:
APESAR DE O CARTUCHO PARA TESTE COM HEPARINASE VALORES ALTOS, A PARTIR DAQUI REFERIDO COMO "PRODUTO",
TER SIDO CUIDADOSAMENTE DESENHADO, FABRICADO E
TESTADO ANTES DA COMERCIALIZAÇÃO, O PRODUTO PODE NÃO
DESEMPENHAR SATISFATORIAMENTE A SUA FUNÇÃO DEVIDO A
UMA VARIEDADE DE MOTIVOS. OS AVISOS CONTIDOS NA
88 Instruções de utilização Português (PT)
Page 91

DOCUMENTAÇÃO DO PRODUTO FORNECEM INFORMAÇÕES MAIS
DETALHADAS E SÃO CONSIDERADOS UMA PARTE INTEGRANTE
DESTA RENÚNCIA DE GARANTIA. POR CONSEGUINTE, A
MEDTRONIC RENUNCIA A TODAS AS GARANTIAS, EXPRESSAS OU
IMPLÍCITAS, RELATIVAS AO PRODUTO. A MEDTRONIC NÃO SERÁ
RESPONSÁVEL POR QUAISQUER DANOS ACIDENTAIS OU
INDIRETOS CAUSADOS POR QUALQUER UTILIZAÇÃO, DEFEITO
OU FALHA DO PRODUTO, QUER A QUEIXA SE BASEIE NA
GARANTIA, CONTRATO, DANOS OU OUTROS.
As exclusões e limitações acima definidas não se destinam a infringir
estipulações obrigatórias da lei aplicável e não devem ser interpretadas
como tal. Se alguma parte ou termo desta renúncia de garantia for
considerado ilegal, não executável ou em conflito com a lei aplicável por
parte de um tribunal da jurisdição competente, a validade da restante
porção da renúncia de garantia não será afetada, devendo todos os
direitos e obrigações ser interpretados e executados como se esta
renúncia de garantia não contivesse a parte ou termo particular
considerado inválido.
Instruções de utilização Português (PT) 89
Page 92

Medtronic, Inc.
*M975862A001*
710 Medtronic Parkway
Minneapolis, MN 55432
USA
www.medtronic.com
+1 763 514 4000
LifeLine Technical Support, 24-hour
consultation service:
1 877 526 7890
Customer Service and Product
Orders:
1 800 854 3570
Medtronic Perfusion Systems
18501 E. Plaza Drive
Parker, CO 80134 USA
Medtronic B.V.
Earl Bakkenstraat 10
6422 PJ Heerlen
The Netherlands
+31 45 566 8000
Australia
Medtronic Australasia Pty Ltd
5 Alma Road
Macquarie Park, NSW 2113
Australia
1800 668 670
Canada
Medtronic of Canada Ltd
99 Hereford Street
Brampton, Ontario L6Y 0R3
Canada
1 800 268 5346
© 2004-2017 Medtronic
M975862A001 Rev. 1A
 Loading...
Loading...