Page 1

ThoraTrak™
MICS Retractor System
MICS система за ретрактор
Retraktorový systém MICS
MICS Retraktorsystem
MICS Thoraxsperrer-System
Σύστημα διαστολέα MICS (Ελάχιστα επεμβατικής καρδιοχειρουργικής)
Sistema de retracción para cirugía cardíaca mínimamente invasiva (MICS)
Minimaalselt invasiivse südamekirurgia retraktorsüsteem
MICS-levitinjärjestelmä
Kit écarteur MICS
Sustav retraktora MICS
MICS mellkasterpesz-rendszer
Sistema di divaricazione per cardiochirurgia mininvasiva (MICS)
MICS retraktoriaus sistema
MICS atvilcēja sistēma
MICS-wondspreidingssysteem
Sårhakesystem for minimalt invasiv hjertekirurgi (MICS)
System retraktora MICS
Sistema de retração MICS
Sistema de retração MICS
Sistem retractor MICS
Система ретрактора для мини-инвазивных кардиохирургических
вмешательств
Rozovierací systém MICS
Retraktorski sistem za minimalno invazivno srčno kirurgijo (MICS)
Sistem za retrakciju za MICS
Sårhakesystem för MICS
MICS Ekartör Sistemi
Instructions for Use • Инструкции за употреба • Návod k použití •
Brugsanvisning • Gebrauchsanweisung • Οδηγίες χρήσης • Instrucciones
de uso • Kasutusjuhend • Käyttöohjeet • Mode d'emploi • Upute za
upotrebu • Használati útmutató • Istruzioni per l'uso • Naudojimo
instrukcijos • Lietošanas pamācība • Gebruiksaanwijzing • Bruksanvisning
• Instrukcja użytkowania • Instruções de utilização • Instruções de
utilização • Instrucţiuni de utilizare • Инструкция по эксплуатации •
Pokyny na používanie • Navodila za uporabo • Uputstva za upotrebu •
Bruksanvisning • Kullanım Talimatları
Caution: Federal law (USA) restricts this device to sale
by or on the order of a physician.
Page 2

The following list includes trademarks or registered trademarks of Medtronic in the United States and possibly in other
countries. All other trademarks are the property of their respective owners.
В списъка по-долу са изброени търговски марки или регистрирани търговски марки на Medtronic в САЩ и
други държави. Всички останали търговски марки са притежание на съответните им собственици.
Následující seznam uvádí ochranné známky nebo registrované ochranné známky společnosti Medtronic v USA a
případně v jiných zemích. Všechny ostatní ochranné známky jsou majetkem příslušných vlastníků.
Følgende liste indeholder varemærker eller registrerede varemærker tilhørende Medtronic i USA og muligvis i andre
lande. Alle andre varemærker tilhører de respektive ejere.
Die folgende Liste beinhaltet Marken oder eingetragene Marken von Medtronic in den USA und möglicherweise in
anderen Ländern. Alle anderen Marken sind Eigentum ihrer jeweiligen Inhaber.
Ο ακόλουθος κατάλογος περιλαμβάνει εμπορικά σήματα ή σήματα κατατεθέντα της Medtronic στις Ηνωμένες
Πολιτείες και πιθανόν σε άλλες χώρες. Όλα τα άλλα εμπορικά σήματα είναι ιδιοκτησία των αντίστοιχων κατόχων
τους.
La siguiente lista incluye marcas comerciales o marcas registradas de Medtronic en los Estados Unidos y
posiblemente en otros países. Todas las marcas comerciales son propiedad de sus propietarios respectivos.
Järgmises loendis on toodud Ameerika Ühendriikides ja ka teistes riikides asuvate ettevõtte Medtronic kaubamärgid
või registreeritud kaubamärgid. Kõik teised kaubamärgid on nende vastavate omanike omandid.
Seuraava luettelo sisältää Medtronicin tavaramerkit ja rekisteröidyt tavaramerkit Yhdysvalloissa ja mahdollisesti
muissa maissa. Kaikki muut tavaramerkit ovat niiden omistajien omaisuutta.
La liste suivante inclut des marques commerciales ou des marques déposées de Medtronic aux États-Unis et
eventuellement dans d'autres pays. Toutes les autres marques commerciales sont la propriété de leurs détenteurs
respectifs.
Na sljedećem popisu nalaze se registrirani zaštitni znaci tvrtke Medtronic u Sjedinjenim Američkim Državama i,
eventualno, u drugim zemljama. Svi ostali zaštitni znaci pripadaju svojim vlasnicima.
Az alábbi lista a Medtronic Egyesült Államokban és valószínűleg más országokban érvényes védjegyeit vagy
bejegyzett védjegyeit tartalmazza. Minden egyéb védjegy a megfelelő tulajdonosok tulajdonát képezi.
L'elenco seguente include marchi di fabbrica o marchi registrati della Medtronic negli Stati Uniti ed eventualmente in
altri Paesi. Tutti gli altri marchi di fabbrica sono di proprietà dei rispettivi proprietari.
Tai yra „Medtronic“ prekių ženklai arba registruotieji prekių ženklai JAV ir galimai kitose šalyse. Visi kiti prekių ženklai
yra jų atitinkamų savininkų nuosavybė.
Sarakstā, kas norādīts tālāk, uzskaitītas kompānijas Medtronic preču zīmes vai ASV reģistrētās preču zīmes. Visas
citas preču zīmes ir to attiecīgo īpašnieku īpašums.
In de onderstaande lijst staan de gedeponeerde of geregistreerde handelsmerken van Medtronic in de Verenigde
Staten en mogelijk in andere landen. Alle andere handelsmerken zijn het eigendom van de desbetreffende eigenaar.
Den følgende listen inneholder varemerker eller registrerte varemerker for Medtronic i USA og eventuelt i andre land.
Alle andre varemerker tilhører de respektive eierne.
Poniższa lista zawiera znaki towarowe lub zastrzeżone znaki towarowe firmy Medtronic w Stanach Zjednoczonych i
prawdopodobnie w innych krajach. Wszystkie pozostałe znaki towarowe są własnością ich prawowitych właścicieli.
A lista a seguir inclui marcas comerciais ou marcas comerciais registradas da Medtronic nos Estados Unidos e
possivelmente em outros países.Todas as outras marcas comerciais são propriedade dos seus respectivos
proprietários.
A lista que se segue inclui marcas comerciais ou marcas comerciais registadas da Medtronic nos EUA e
possivelmente noutros países. Todas as outras marcas comerciais são propriedade dos respetivos detentores.
Următoarea listă include mărcile comerciale sau mărcile comerciale înregistrate ale Medtronic în Statele Unite ale
Americii şi, posibil, în alte ţări. Toate celelalte mărci comerciale sunt proprietatea deţinătorilor respectivi.
Следующий список включает товарные знаки или зарегистрированные товарные знаки корпорации
Medtronic в США и, возможно, в других странах. Все другие товарные знаки являются собственностью их
владельцев.
Nasledujúci zoznam obsahuje ochranné známky alebo registrované ochranné známky spoločnosti Medtronic v USA
a prípadne v ďalších krajinách. Všetky ostatné ochranné známky sú majetkom príslušných vlastníkov.
Spodaj so navedene blagovne znamke ali registrirane blagovne znamke družbe Medtronic v Združenih državah
Amerike in drugih državah. Vse druge blagovne znamke so last njihovih lastnikov.
Sledeća lista obuhvata žigove ili registrovane žigove preduzeća Medtronic u SAD i možda u drugim zemljama. Svi
drugi zaštićeni žigovi vlasništvo su odgovarajućih vlasnika.
Följande lista innehåller varumärken eller registrerade varumärken som tillhör Medtronic i USA och möjligen i andra
länder. Alla övriga varumärken tillhör respektive innehavare.
Aşağıdaki liste Medtronic şirketinin Amerika Birleşik Devletleri'nde ve muhtemelen diğer ülkelerdeki ticari markalarını
veya tescilli ticari markalarını içerir. Diğer ticari markaların tümü ilgili sahiplerinin mülkiyetindedir.
Medtronic, ThoraTrak
Page 3

Explanation of symbols on package labeling • Обяснение на символите от
етикетите на опаковката • Vysvětlení symbolů uvedených na štítcích
balení • Forklaring til symbolerne på emballagens mærkater • Erläuterung
der Symbole auf der Verpackung • Επεξήγηση των συμβόλων στη
σήμανση της συσκευασίας • Explicación de los símbolos que aparecen en
la documentación del envase • Pakendi siltidel olevate tingmärkide
tähendus • Pakkausetiketin symbolien selitykset • Explication des symboles
des étiquettes sur l’emballage • Objašnjenje simbola na ambalažnoj etiketi •
A csomag címkéin látható szimbólumok jelentése • Spiegazione dei simboli
presenti sulle etichette della confezione • Pakuotės etiketėse nurodytų
simbolių reikšmės • Uz iepakojuma etiķetes attēloto simbolu skaidrojums •
Verklaring van de symbolen op de verpakkingslabels • Forklaring av
symboler på pakningen • Objaśnienie symboli znajdujących się na
etykietach opakowania • Explicação dos símbolos nas etiquetas da
embalagem • Explicação dos símbolos na documentação da embalagem •
Legenda simbolurilor cuprinse în etichetele de pe ambalaj • Пояснение к
символам на этикетках упаковки • Vysvetlivky k symbolom na označení
balenia • Razlaga simbolov na embalaži • Objašnjenje simbola na oznakama
na pakovanju • Förklaring av symboler på förpackningsmärkningen •
Ambalaj etiketindeki sembollerin açıklamaları
Refer to the outer package label to see which symbols apply to this product. •
Погледнете външния етикет на опаковката, за да видите кои символи се
отнасят за този продукт. • Symboly, které se vztahují k tomuto výrobku, naleznete
na štítku na vnější straně obalu. • Se mærkaten på den ydre emballage for de
symboler, der gælder for dette produkt. • Welche Symbole für dieses Produkt
zutreffen, entnehmen Sie bitte dem Etikett auf der Verpackung. • Ανατρέξτε στην
ετικέτα της εξωτερικής συσκευασίας για να δείτε ποια σύμβολα ισχύουν για το
παρόν προϊόν. • Consulte la etiqueta del envase exterior para comprobar qué
símbolos son aplicables a este producto. • Välispakendi sildilt näete, millised
tingmärgid selle toote puhul kehtivad. • Katso ulkopakkauksen etiketistä, mitkä
symbolit koskevat tätä tuotetta. • Se référer à l’étiquette sur l’emballage extérieur
pour savoir quels symboles s’appliquent à ce produit. • Na etiketama na ambalaži
pogledajte koji se simboli odnose na ovaj proizvod. • A termékre vonatkozó
szimbólumok a csomagoláson találhatók. • Fare riferimento all’etichetta sulla
confezione esterna per sapere quali simboli si applicano a questo prodotto. •
Norėdami sužinoti, kokiu simboliu pažymėtas šis gaminys, žiūrėkite į išorinę
pakuotės etiketę. • Skatiet ārējā iepakojuma marķējumu, lai redzētu simbolus, kas
attiecas uz šo izstrādājumu. • Controleer het label op de buitenverpakking om te
zien welke symbolen op dit product van toepassing zijn. • Se på etiketten på den ytre
pakningen for å fastslå hvilke symboler som gjelder for dette produktet. • Należy
zapoznać się z etykietą na zewnętrznym opakowaniu, aby określić, które symbole
dotyczą niniejszego produktu. • Consulte a etiqueta externa da embalagem para
ver quais símbolos aplicam-se a este produto. • Consultar a etiqueta exterior da
embalagem para ver quais os símbolos que se aplicam a este produto. • Consultaţi
eticheta dispozitivului pentru simbolurile aplicabile acestui produs. •
См. на этикетке внешней упаковки, какие символы применимы к данному
продукту. • Prezrite si označenie na vonkajšom obale a zistite, ktoré symboly sa
vzťahujú na tento produkt. • Na nalepki na zunanji embalaži so navedeni simboli, ki
se nanašajo na ta izdelek. • Pogledajte spoljnu oznaku na pakovanju da biste videli
koji se simboli primenjuju na ovaj proizvod. • Se etiketten på ytterförpackningen för
de symboler som gäller denna produkt. • Bu üründe hangi sembollerin geçerli
olduğunu görmek için dış ambalaj etiketine başvurun.
Conformité Européenne (European Conformity). This symbol means that
the device fully complies with European Council Directive MDD:
93/42/EEC. • Conformité Européenne (European Conformity)
(Европейско съответствие). Този символ означава, че уредът
3
Page 4

отговаря напълно на Директива на Европейския съвет за
медицински изделия: 93/42/ЕИО. • Conformité Européenne (Evropská
shoda). Tento symbol znamená, že zařízení zcela splňuje požadavky
směrnice Evropské rady MDD: 93/42/EHS. • Conformité Européenne
(europæisk standard). Dette symbol betyder, at enheden fuldt ud
overholder Det Europæiske Råds direktiv om medicinsk udstyr:
93/42/EØF. • Conformité Européenne (Europäische Konformität). Dieses
Symbol besagt, dass das Gerät allen Vorschriften der europäischen
Richtlinie 93/42/EWG für Medizinprodukte entspricht. • Conformité
Européenne (Ευρωπαϊκή Συμμόρφωση). Το σύμβολο αυτό σημαίνει ότι
το προϊόν συμμορφώνεται πλήρως με την Ευρωπαϊκή Οδηγία περί
ιατροτεχνολογικών προϊόντων: 93/42/ΕΟΚ. • Conformité Européenne
(Conformidad Europea). Este símbolo indica que el dispositivo cumple
totalmente la Directiva: 93/42/CEE del Consejo Europeo relativa a los
productos sanitarios. • Conformité Européenne (Euroopa standard). See
tingmärk tähendab, et seade vastab täielikult Euroopa Ühenduste
Nõukogu meditsiiniseadmete direktiivi 93/42/EMÜ nõuetele. •
Conformité Européenne (eurooppalainen vaatimustenmukaisuus).
Tämä symboli tarkoittaa, että laite on kaikilta osin Euroopan unionin
neuvoston lääkintälaitedirektiivin 93/42/ETY mukainen. • Conformité
Européenne (conformité européenne). Ce symbole signifie que l’appareil
est entièrement conforme à la Directive du Conseil de l’Union
européenne MDD : 93/42/CEE. • Conformité Européenne (usklađenost s
europskim normama). Taj simbol znači da je uređaj potpuno usklađen s
direktivom Europskog vijeća MDD: 93/42/EEZ. • Conformité Européenne
(Európai Megfelelőség). Ez a szimbólum azt jelenti, hogy az eszköz teljes
mértékben megfelel az Európai Tanács orvostechnikai eszközökről szóló
93/42/EGK irányelvének. • Conformité Européenne (Conformità
europea). Questo simbolo indica che il dispositivo è conforme alla
Direttiva Europea MDD 93/42/CEE. • Conformité Européenne (Europos
atitiktis). Šis simbolis reiškia, kad prietaisas visiškai atitinka Europos
Tarybos direktyvą MDD: 93/42/EEB. • Conformité Européenne (atbilstība
Eiropas prasībām). Šis simbols norāda, ka ierīce pilnībā atbilst Eiropas
Padomes Direktīvas 93/42/EEK par medicīnas ierīcēm prasībām. •
Conformité Européenne (Europese Conformiteit). Dit symbool betekent
dat het product volledig voldoet aan richtlijn van de Europese Raad MDD:
93/42/EEG. • Conformité Européenne (samsvar med europeisk
standard). Dette symbolet betyr at enheten er fullstendig i samsvar med
EU-direktiv MDD: 93/42/EØF. • Conformité Européenne (Zgodność
z normami Unii Europejskiej). Ten symbol oznacza, że urządzenie spełnia
wszystkie wymogi dyrektywy Rady Europejskiej 93/42/EWG w sprawie
wyrobów medycznych. • Conformité Européenne (Conformidade
Europeia). Este símbolo significa que o dispositivo está em total
conformidade com a Diretiva do Conselho Europeu MDD: 93/42/CEE. •
Conformité Européenne (Conformidade Europeia). Este símbolo
significa que o dispositivo está em total conformidade com a Diretiva do
Conselho Europeu MDD: 93/42/CEE. • Conformité Européenne
(Conformitate europeană). Acest simbol indică faptul că dispozitivul este
în deplină conformitate cu Directiva MDD: 93/42/CEE a Consiliului
European. • Conformité Européenne (Европейское соответствие).
Этот символ обозначает, что устройство полностью соответствует
требованиям Директивы Европейского Совета MDD: 93/42/EEC •
Conformité Européenne (Zhoda s požiadavkami EÚ). Tento symbol
znamená, že zariadenie je v plnom súlade s ustanoveniami smernice
Európskej rady MDD: 93/42/EHP. • Conformité Européenne (evropska
skladnost). Ta simbol pomeni, da je pripomoček v celoti skladen z
Direktivo Evropskega sveta o medicinskih pripomočkih: 93/42/EGS. •
4
Page 5

Conformité Européenne (usklađenost sa evropskim standardima). Ovaj
simbol znači da je uređaj u potpunosti usklađen sa Direktivom Saveta
Evrope MDD: 93/42/EEC. • Conformité Européenne (Europeisk
standard). Denna symbol betyder att utrustningen helt följer Europeiska
rådets MDD-direktiv: 93/42/EEG. • Conformité Européenne (Avrupa
Normlarına Uygunluk). Bu sembol, cihazın Avrupa Konseyi Direktifi MDD:
93/42/EEC ile tamamen uyumlu olduğu anlamına gelir.
Nonsterile • Нестерилен • Nesterilní • Ikke-steril • Unsteril • Μη στείρο •
No estéril • Mittesteriilne • Epästeriili • Non stérile • Nije sterilno • Nem
steril • Non sterile • Nesterilus • Nesterila • Niet-steriel • Usteril • Produkt
niejałowy • Não estéril • Não estéril • Nesteril • Нестерильно • Nesterilné
• Nesterilno • Nije sterilno • Icke-steril • Steril Değildir
Catalog number • Каталожен номер • Katalogové číslo •
Katalognummer • Katalognummer • Αριθμός καταλόγου • Número de
catálogo • Kataloogi number • Luettelonumero • Numéro de référence •
Kataloški broj • Katalógusszám • Numero di catalogo • Katalogo numeris
• Kataloga numurs • Catalogusnummer • Artikkelnummer • Numer
katalogowy • Número de catálogo • Número de catálogo • Număr de
catalog • Номер по каталогу • Katalógové číslo • Kataloška številka •
Kataloški broj • Katalognummer • Katalog numarası
Manufacturer • Производител • Výrobce • Fabrikant • Hersteller •
Κατασκευαστής • Fabricante • Tootja • Valmistaja • Fabricant •
Proizvođač • Gyártó • Fabbricante • Gamintojas • Ražotājs • Fabrikant •
Produsent • Producent • Fabricante • Fabricante • Producător •
Производитель • Výrobca • Izdelovalec • Proizvođač • Tillverkare •
Üretici
Manufacturing site • Производствен обект • Místo výroby •
Fabrikationssted • Produktionsstätte • Εργοστάσιο κατασκευής • Lugar
de fabricación • Tootmiskoht • Valmistuspaikka • Site de fabrication •
Mjesto proizvodnje • Gyártóhely • Luogo di fabbricazione • Pagaminimo
vieta • Ražotne • Productieplaats • Produksjonssted • Zakład produkcyjny
• Local de fabricação • Local de fabrico • Locul fabricaţiei • Место
производства • Miesto výroby • Kraj izdelave • Mesto proizvodnje •
Tillverkningsanläggning • Üretim yeri
Date of manufacture • Дата на производство • Datum výroby •
Fabrikationsdato • Herstellungsdatum • Ημερομηνία κατασκευής •
Fecha de fabricación • Tootmiskuupäev • Valmistuspäivämäärä • Date de
fabrication • Datum proizvodnje • Gyártás ideje • Data di fabbricazione •
Pagaminimo data • Ražošanas datums • Productiedatum •
Produksjonsdato • Data produkcji • Data de fabricação • Data de fabrico •
Data fabricării • Дата изготовления • Dátum výroby • Datum izdelave •
Datum proizvodnje • Tillverkningsdatum • Üretim tarihi
Authorized representative in the European Community • Упълномощен
представител в Европейската общност • Autorizovaný zástupce pro
Evropské společenství • Autoriseret repræsentant i EU • Autorisierter
Repräsentant in der Europäischen Gemeinschaft • Εξουσιοδοτημένος
αντιπρόσωπος στην Ευρωπαϊκή Κοινότητα • Representante autorizado
en la Comunidad Europea • Volitatud esindaja Euroopa Ühenduses •
Valtuutettu edustaja Euroopan yhteisön alueella • Représentant autorisé
dans la Communauté européenne • Ovlašteni predstavnik u Europskoj
zajednici • Hivatalos képviselet az Európai Közösségben •
Rappresentante autorizzato nella Comunità europea • Įgaliotasis
atstovas Europos Bendrijoje • Pilnvarotais pārstāvis Eiropas Kopienā •
Geautoriseerd vertegenwoordiger in de Europese Gemeenschap •
Autorisert representant i Det europeiske fellesskap • Autoryzowany
5
Page 6

przedstawiciel w Unii Europejskiej • Representante autorizado na
Comunidade Europeia • Representante autorizado na Comunidade
Europeia • Reprezentanţă autorizată în Comunitatea Europeană •
Уполномоченный представитель в Европейском сообществе •
Autorizovaný zástupca pre Európske spoločenstvo • Pooblaščeni
predstavnik v Evropski skupnosti • Ovlašćeni predstavnik u Evropskoj
zajednici • Auktoriserad representant inom EG • Avrupa Topluluğu’ndaki
yetkili temsilci
Do not use if package is damaged • Не използвайте, ако опаковката е
повредена • Nepoužívejte, je-li obal poškozený • Må ikke anvendes, hvis
emballagen er beskadiget • Nicht verwenden, wenn die Verpackung
beschädigt ist • Μη χρησιμοποιείτε εάν η συσκευασία υποστεί ζημιά • No
utilizar si el envase está dañado • Ärge kasutage, kui pakend on
kahjustatud • Älä käytä, jos pakkaus on vaurioitunut • Ne pas utiliser si
l’emballage est endommagé • Nemojte upotrebljavati ako je ambalaža
oštećena • Ne használja fel, ha a csomagolás sérült • Non utilizzare se
l’imballaggio non è integro • Nenaudokite, jei pakuotė pažeista • Nelietot,
ja iepakojums ir bojāts • Niet gebruiken als de verpakking beschadigd is •
Skal ikke brukes hvis pakningen er skadet • Nie stosować, jeśli
opakowanie jest uszkodzone • Não utilizar se a embalagem estiver
danificada • Não utilizar se a embalagem estiver danificada • Nu folosiţi
dacă ambalajul este deteriorat • Не использовать, если упаковка
повреждена • Nepoužívajte, ak je obal poškodený • Ne uporabljajte, če
je embalaža poškodovana • Ne koristiti ako je pakovanje oštećeno • Får ej
användas om förpackningen är skadad • Ambalaj hasarlıysa kullanmayın
Lot number • Номер на партида • Číslo šarže • Partinummer •
Losnummer • Αριθμός παρτίδας • Número de lote • Partii number •
Eränumero • Numéro de lot • Broj serije • Tételszám • Numero di lotto •
Partijos numeris • Partijas numurs • Partijnummer • Lotnummer • Numer
partii produkcyjnej • Número de lote • Número de lote • Număr de lot •
Номер партии • Číslo šarže • Serijska številka • Broj serije • Lotnummer •
Lot numarası
For US audiences only • Само за САЩ • Pouze pro uživatele v USA •
Gælder kun i USA • Gilt nur für Leser in den USA • Μόνο για πελάτες
εντός των ΗΠΑ • Solo aplicable en EE. UU. • Ainult kasutajatele
Ameerika Ühendriikides • Koskee vain Yhdysvaltoja • Ne s’applique
qu’aux États-Unis • Samo za američko tržište • Csak egyesült államokbeli
felhasználóknak • Esclusivamente per il mercato statunitense • Tik JAV
naudotojams • Tikai pircējiem ASV • Alleen van toepassing voor de VS •
Gjelder kun USA • Dotyczy tylko odbiorców w USA • Aplicável apenas aos
EUA • Aplicável apenas aos EUA • Numai pentru SUA • Только для США
• Len pre používateľov v USA • Samo za uporabnike v ZDA • Samo za
korisnike u SAD • Gäller endast i USA • Yalnızca ABD’deki kullanıcılar için
Quantity • Количество • Množství • Antal • Menge • Ποσότητα • Cantidad
• Kogus • Määrä • Quantité • Količina • Mennyiség • Quantità • Kiekis •
Daudzums • Aantal • Antall • Ilość • Quantidade • Quantidade • Cantitate •
Количество • Množstvo • Količina • Količina • Antal • Miktar
Consult Instructions for Use • Разгледайте инструкциите за употреба •
Viz návod k použití • Se brugsanvisningen • Gebrauchsanweisung
beachten • Συμβουλευτείτε τις Οδηγίες χρήσης • Consultar las
instrucciones de uso • Tutvuge kasutusjuhistega • Katso käyttöohjeet •
Consulter le mode d’emploi • Pogledajte upute za upotrebu • Lásd a
használati útmutatót • Consultare le istruzioni per l’uso • Skaitykite
naudojimo instrukcijose • Skatīt lietošanas instrukciju • Raadpleeg
gebruiksaanwijzing • Se i bruksanvisningen • Należy zapoznać się
6
Page 7

z instrukcją użytkowania • Consultar instruções de utilização • Consultar
instruções de utilização • Consultaţi instrucţiunile de utilizare • См.
инструкцию по эксплуатации • Pozrite pokyny na používanie • Glejte
navodila za uporabo • Pogledajte uputstva za upotrebu • Läs
bruksanvisningen • Kullanım Talimatlarına Bakın
7
Page 8

Figure 1. Retractor rack • Фигура 1. Подложка за ретрактор • Obrázek 1. Tělo
retraktoru • Figur 1. Retraktormonteringspanel • Abbildung 1. Thoraxsperrer •
Εικόνα 1. Σύστημα διαστολέα • Figura 1. Porta-separador •
Joonis 1. Retraktsiooniraam • Kuva 1. Levitinrunko • Figure 1. Crémaillère de
l’écarteur • Sl. 1. Postolje retraktora • 1. ábra. A mellkasterpesz állványa •
Figura 1. Binario del divaricatore • 1 pav. Retraktorius • 1. attēls. Atvilcēja statne •
Afbeelding 1. Wondspreider • Figur 1. Sårhakeramme • Rycina 1. Statyw
retraktora • Figura 1. Suporte do retrator • Figura 1. Suporte do retrator •
Figura 1. Stativul retractorului • Рисунок 1. Рама ретрактора • Obrázok 1. Rám
rozvierača • Slika 1. Držalo retraktorja • Slika 1. Nosač retraktora • Figur 1. Hållare
för sårhake • Şekil 1. Ekartör askısı
Figure 2. LIMA blades, standard • Фигура 2. Остриета за LIMA, стандартни •
Obrázek 2. Lopatky pro levou vnitřní mamární tepnu, standardní •
Figur 2. LIMA-blade, standard • Abbildung 2. LIMA-Blätter, Standard •
Εικόνα 2. Λεπίδες LIMA, συνήθεις • Figura 2. Valvas para AMII, estándares •
Joonis 2. Vasaku arteria thoracica interna (LIMA) labad, standardsed •
Kuva 2. LIMA-lavat, vakiot • Figure 2. Valves AMIG, standard • Sl. 2. Oštrice za
lijevu unutarnju mamarnu arteriju, standardne • 2. ábra. Standard, bal oldali artéria
mammaria interna lapocok • Figura 2. Lame per arteria mammaria interna sinistra,
standard • 2 pav. LIMA mentelės, standartinės • 2. attēls. LIMA lāpstiņas, standarta
• Afbeelding 2. LIMA-bladen, standaard • Figur 2. LIMA-blad, standard •
Rycina 2. Ramiona do lewej tętnicy piersiowej wewnętrznej (standardowe) •
Figura 2. Lâminas para a artéria mamária interna esquerda, padrão •
Figura 2. Lâminas para a artéria mamária interna esquerda, padrão •
Figura 2. Lame LIMA, standard • Рисунок 2. Лезвия ЛВГА, стандартные •
Obrázok 2. Lopatky LIMA (ľavá arteria mammaria interna), štandardné •
Slika 2. Lopatice za levo notranjo prsno arterijo (LIMA), standardne •
Slika 2. Lopatice za LIMA, standardne • Figur 2. Blad för vänster arteria mammaria
interna, standard • Şekil 2. LIMA bıçakları, standart
Figure 3. LIMA blades, deep • Фигура 3. Остриета за LIMA, дълбоки •
Obrázek 3. Lopatky pro levou vnitřní mamární tepnu, hluboké •
Figur 3. LIMA-blade, dybe • Abbildung 3. LIMA-Blätter, tief • Εικόνα 3. Λεπίδες
LIMA, βαθιές • Figura 3. Valvas para AMII, profundas • Joonis 3. Vasaku arteria
thoracica interna (LIMA) labad, sügavad • Kuva 3. LIMA-lavat, syvät •
8
Page 9

Figure 3. Valves AMIG, profondes • Sl. 3. Oštrice za lijevu unutarnju mamarnu
arteriju, duboke • 3. ábra. Mély, bal oldali artéria mammaria interna lapocok •
Figura 3. Lame per arteria mammaria interna sinistra, profonde • 3 pav. LIMA
mentelės, giliosios • 3. attēls. LIMA lāpstiņas, apakšējās •
Afbeelding 3. LIMA-bladen, diep • Figur 3. LIMA-blad, dype • Rycina 3. Ramiona
do lewej tętnicy piersiowej wewnętrznej (głębokie) • Figura 3. Lâminas para a
artéria mamária interna esquerda, profundas • Figura 3. Lâminas para a artéria
mamária interna esquerda, profundas • Figura 3. Lame LIMA, adânci •
Рисунок 3. Лезвия ЛВГА, глубокие • Obrázok 3. Lopatky LIMA (ľavá arteria
mammaria interna), hlboké • Slika 3. Lopatice za levo notranjo prsno arterijo
(LIMA), globoke • Slika 3. Lopatice za LIMA, duboke • Figur 3. Blad för vänster
arteria mammaria interna, djupa • Şekil 3. LIMA bıçakları, derin
Figure 4. Long and short thoracotomy blades, standard • Фигура 4. Дълги и къси
остриета за торакотомия, стандартни • Obrázek 4. Dlouhé a krátké lopatky pro
torakotomii, standardní • Figur 4. Lange og korte thorakotomiblade, standard •
Abbildung 4. Lange und kurze Thorakotomieblätter, Standard •
Εικόνα 4. Μακριές και κοντές λεπίδες θωρακοτομής, συνήθεις • Figura 4. Valvas
para toracotomía largas y cortas, estándares • Joonis 4. Pikad ja lühikesed
torakotoomia labad, standardsed • Kuva 4. Pitkät ja lyhyet torakotomialavat, vakiot
• Figure 4. Valves de thoracotomie longues et courtes, standard • Sl. 4. Duge i
kratke oštrice za torakotomiju, standardne • 4. ábra. Hosszú és rövid, standard
thoracotomiás lapocok • Figura 4. Lame per toracotomia standard lunghe e corte •
4 pav. Ilgos ir trumpos torakotomijos mentelės, standartinės • 4. attēls. Garās un
īsās torakotomijas lāpstiņas, standarta • Afbeelding 4. Lange en korte
thoracotomiebladen, standaard • Figur 4. Lange og korte torakotomiblad, standard
• Rycina 4. Długie i krótkie ramiona do torakotomii (standardowe) •
Figura 4. Lâminas de toracotomia compridas e curtas, padrão • Figura 4. Lâminas
de toracotomia compridas e curtas, padrão • Figura 4. Lame lungi şi scurte pentru
toracotomie, standard • Рисунок 4. Длинные и короткие лезвия для
торакотомии, стандартные • Obrázok 4. Dlhé a krátke torakotomické lopatky,
štandardné • Slika 4. Dolge in kratke lopatice za torakotomijo, standardne •
Slika 4. Duge i kratke lopatice za torakotomiju, standardne • Figur 4. Långa och
korta torakotomiblad, standard • Şekil 4. Uzun ve kısa torakotomi bıçakları, standart
9
Page 10
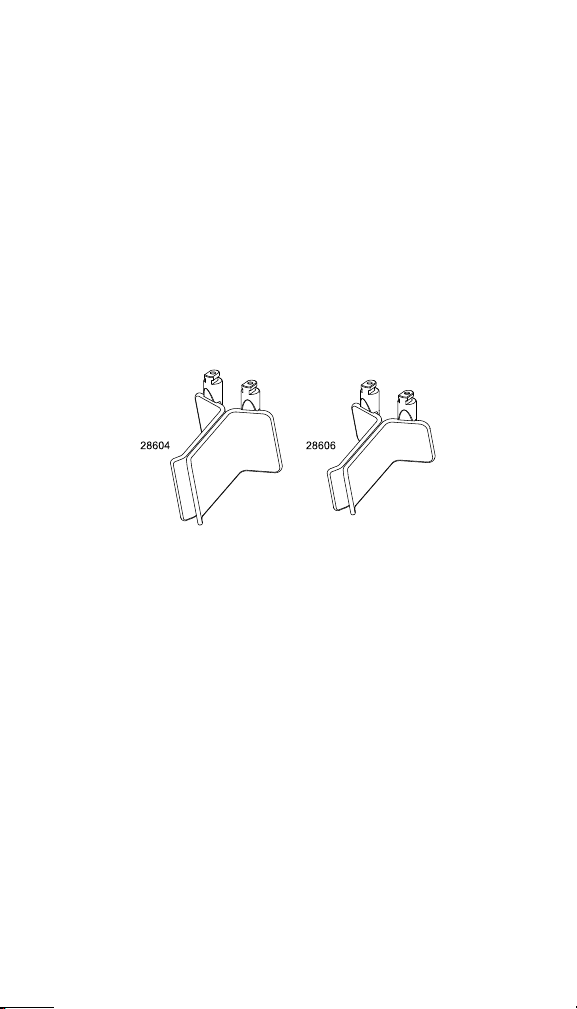
Figure 5. Long and short thoracotomy blades, deep • Фигура 5. Дълги и къси
остриета за торакотомия, дълбоки • Obrázek 5. Dlouhé a krátké lopatky pro
torakotomii, hluboké • Figur 5. Lange og korte thorakotomiblade, dybe •
Abbildung 5. Lange und kurze Thorakotomieblätter, tief • Εικόνα 5. Μακριές και
κοντές λεπίδες θωρακοτομής, βαθιές • Figura 5. Valvas para toracotomía largas
y cortas, profundas • Joonis 5. Pikad ja lühikesed torakotoomia labad, sügavad •
Kuva 5. Pitkät ja lyhyet torakotomialavat, syvät • Figure 5. Valves de thoracotomie
longues et courtes, profondes • Sl. 5. Duge i kratke oštrice za torakotomiju, duboke •
5. ábra. Hosszú és rövid, mély thoracotomiás lapocok • Figura 5. Lame per
toracotomia profonde lunghe e corte • 5 pav. Ilgos ir trumpos torakotomijos
mentelės, giliosios • 5. attēls. Garās un īsās torakotomijas lāpstiņas, apakšējās •
Afbeelding 5. Lange en korte thoracotomiebladen, diep • Figur 5. Lange og korte
torakotomiblad, dype • Rycina 5. Długie i krótkie ramiona do torakotomii (głębokie)
• Figura 5. Lâminas de toracotomia, compridas e curtas, profundas •
Figura 5. Lâminas de toracotomia compridas e curtas, profundas • Figura 5. Lame
lungi şi scurte pentru toracotomie, adânci • Рисунок 5. Длинные и короткие
лезвия для торакотомии, глубокие • Obrázok 5. Dlhé a krátke torakotomické
lopatky, hlboké • Slika 5. Dolge in kratke lopatice za torakotomijo, globoke •
Slika 5. Duge i kratke lopatice za torakotomiju, duboke • Figur 5. Långa och korta
torakotomiblad, djupa • Şekil 5. Uzun ve kısa torakotomi bıçakları, derin
Figure 6. Long and short extended mount inferior blades, standard •
Фигура 6. Дълги и къси удължени монтирани остриета нисш клас,
стандартни • Obrázek 6. Dlouhé a krátké spodní lopatky s prodlouženým čepem,
standardní • Figur 6. Lange og korte forlængede nedre montérblade, standard •
Abbildung 6. Lange und kurze, tiefer greifende Thorakotomieblätter mit
verlängerter Befestigung, Standard • Εικόνα 6. Μακριές και κοντές λεπίδες
μεγαλύτερου βάθους με εκτεινόμενη βάση, συνήθεις • Figura 6. Valvas inferiores
largas y cortas con brazo extendido, estándares • Joonis 6. Pikk ja lühike alumine
pikendatud alusega laba, standardne • Kuva 6. Pitkällä kiinnikkeellä varustetut
pitkät ja lyhyet alemmat lavat, vakiot • Figure 6. Valves inférieures de fixation,
rallongées, longues et courtes, standard • Sl. 6. Duge i kratke oštrice za produženu
donju montažu, standardne • 6. ábra. Hosszú és rövid, standard, nyújtott karú
inferior lapocok • Figura 6. Lame per toracotomia inferiori lunghe e corte, standard,
con attacco esteso • 6 pav. Ilgos ir trumpos pailginto tvirtinimo papildomos
mentelės, standartinės • 6. attēls. Garās un īsās pagarināma stiprinājuma iekšējās
lāpstiņas, standarta • Afbeelding 6. Laag-grijpende, lange en korte bladen met
verlengd montagestuk, standaard • Figur 6. Lange og korte nedre blad med
forlenget feste, standard • Rycina 6. Długie i krótkie ramiona dolne o przedłużonym
mocowaniu (standardowe) • Figura 6. Lâminas inferiores prolongadas de
montagem, compridas e curtas, padrão • Figura 6. Lâminas inferiores prolongadas
de montagem, compridas e curtas, padrão • Figura 6. Lame inferioare lungi şi
scurte, cu montare extinsă, standard • Рисунок 6. Длинные и короткие нижние
лезвия с удлиненным креплением, стандартные • Obrázok 6. Dlhé a krátke
pomocné lopatky s predĺženou násadou, štandardné • Slika 6. Dolge in kratke
spodnje lopatice s podaljšanim nosilcem, standardne • Slika 6. Duge i kratke
10
Page 11

inferiorne lopatice sa produženim postoljem, standardne • Figur 6. Långa och korta
nedre blad med förlängd monteringsstav, standard • Şekil 6. Uzun ve kısa uzatılmış
montajlı inferior bıçaklar, standart
Figure 7. Orientation of blade • Фигура 7. Ориентация на острие •
Obrázek 7. Orientace lopatek • Figur 7. Bladets placering •
Abbildung 7. Ausrichtung des Blatts • Εικόνα 7. Προσανατολισμός της λεπίδας •
Figura 7. Orientación de la valva • Joonis 7. Laba orientatsioon • Kuva 7. Lavan
suunta • Figure 7. Orientation de la valve • Sl. 7. Usmjerenje oštrice •
7. ábra. Lapoc tájolása • Figura 7. Orientamento della lama • 7 pav. Mentelės
orientacija • 7. attēls. Lāpstiņas orientācija • Afbeelding 7. Oriëntatie van het blad •
Figur 7. Bladets orientering • Rycina 7. Orientacja ramienia • Figura 7. Orientação
da lâmina • Figura 7. Orientação da lâmina • Figura 7. Orientarea lamei •
Рисунок 7. Ориентация лезвия • Obrázok 7. Orientácia lopatky •
Slika 7. Orientacija lopatice • Slika 7. Orijentacija lopatice •
Figur 7. Riktningsangivelse för bladen • Şekil 7. Bıçak yönü
EN
BG
CS
DA
DE
EL
1 Depth
2 Length
1 Дълбочина
2 Дължина
1 Hloubka
2 Délka
1 Dybde
2 Længde
1 Tiefe
2 Länge
1 Βάθος
2 Μήκος
11
Page 12

ES
ET
FI
FR
HR
HU
IT
LT
LV
NL
NO
PL
PT-BR
PT-PT
RO
RU
SK
SL
SR
SV
TR
1 Profundidad
2 Longitud
1 Sügavus
2 Pikkus
1 Syvyys
2 Pituus
1 Profondeur
2 Longueur
1 Dubina
2 Duljina
1 Mélység
2 hosszúság
1 Profondità
2 Lunghezza
1 Gylis
2 Ilgis
1 Dziļums
2 Garums
1 Diepte
2 Lengte
1 Dybde
2 Lengde
1 Głębokość
2 Długość
1 Profundidade
2 Comprimento
1 Profundidade
2 Comprimento
1 Adâncime
2 Lungime
1 Глубина
2 Длина
1 Hĺbka
2 Dĺžka
1 Globina
2 Dolžina
1 Dubina
2 Dužina
1 Djup
2 Längd
1 Derinlik
2 Uzunluk
12
Page 13

1 Product description
Model Description
28610 MICS retractor system
28611 Retractor rack
28601 LIMA blades, standard
28602 LIMA blades, deep
28603 Long thoracotomy blades, standard
28604 Long thoracotomy blades, deep
28604B Long extended mount inferior blade, standard
28605 Short thoracotomy blades, standard
28606 Short thoracotomy blades, deep
28606B Short extended mount inferior blade, standard
Note: Model 28601 is the blade most commonly used for left internal mammary
artery (LIMA) harvest. Model 28605 is the blade most commonly used for general
thoracotomy retraction. All other blades were designed to accommodate various
patient anatomies.
Note: Models 28604B and 28606B are inferior blades designed for women and
obese patients. Use these inferior blades with the superior blades (Models 28604
and 28606).
2 Indications for use
The ThoraTrak minimally invasive cardiac surgery (MICS) retractor system is
intended to provide surgical access for minimally invasive cardiothoracic
procedures, including minimally invasive coronary artery bypass grafting (CABG)
surgery and LIMA harvest, by retraction of soft and bony tissue.
3 Precautions
Proper surgical procedures and techniques are the responsibility of the medical
professional. Surgeons must evaluate the appropriateness of any procedure based
on their own medical training and experience.
4 Adverse effects
None known.
5 Processing and reprocessing
Medtronic has validated the following instructions for preparing this medical device
for reuse. It remains the responsibility of the processor to ensure that the
processing, as actually performed using equipment, materials, and personnel in the
processing facility, achieves the desired result. Processing requires validation and
routine monitoring. Likewise, any deviation by the processor from the following
instructions should be properly evaluated for effectiveness and potential adverse
consequences. Cleaning may be done manually, or it may be automated according
to these Instructions for Use or an equivalent, validated method.
5.1 Cleaning
Warning: Thoroughly clean the device to eliminate soil prior to sterilization.
Warning: Do not use solvent-based cleaners (for example, acetone or toluene).
13
English
Page 14
• Do not allow contaminated devices to dry before implementing any cleaning
procedure.
• Reprocess devices within 2 hours after use. If transport to the processing area
will be delayed, place the device in a covered container with an enzymatic
detergent to prevent drying.
• If the device contains multiple components, completely disassemble the
components prior to cleaning per these Instructions for Use.
• Examine the device for cracking or degradation prior to use. Do not use the
device if any components show signs of cracking or degradation.
• Thermal disinfection is not required because the devices are terminally
sterilized.
5.1.1 Manual cleaning
Medtronic has established the following manual cleaning procedure in Table 1.
These steps must be performed within a maximum of 2 hours after use.
Note: If the device has movable parts, ensure that all surface areas have been
thoroughly cleaned.
Table 1. Manual cleaning instructions
Step Process Temperature Cleaning instructions
1 Rinsing >27 °C (>81 °F) Remove gross soil using running water
2 Soaking >28 °C (>82 °F) Submerge the device completely for a
3 Ultrasonic
clean
4 Rinsing >27 °C (>81 °F) Rinse the device with running water for
5 Drying N/A Dry with a clean, lint-free wipe.
6 Inspection N/A Visually inspect each device for any
5.1.2 Automated cleaning
Medtronic has established the following automated cleaning procedure. The steps
in Table 2 must be performed within a maximum of 2 hours after use.
Note: If the device or component has movable parts, ensure that all surface areas
have been thoroughly cleaned.
>27 °C (>81 °F) Submerge the device completely in an
for 1 min. Use a soft-bristle brush (for
example, a nylon toothbrush) to clean
the device thoroughly.
minimum of 5 min with 15.6 mL/1 L (or 2
ounces/1 gallon) of an enzymatic
detergent (for example, ENZOL™) and
water. Remove visible soil with a softbristled brush.
ultrasonic cleaner (for example,
Bransonic™) with 7.8 mL/1 L (or 1
ounce/1 gallon) of an enzymatic detergent (for example, ENZOL) and water.
Sonicate for 10 min.
1 min.
remaining soil or moisture. If soil
remains, repeat the process.
English
14
Page 15

Table 2. Pretreatment instructions
Step Process
1 Rinsing >25 °C (>77 °F) Remove gross soil using running tap
2 Soaking >25 °C (>77 °F) Submerge the device completely for
3 Rinsing >25 °C (>77 °F) Rinse the device for a minimum of
4 Inspection N/A Visually inspect the device for any
Medtronic used the Prolystica™ family of cleaners according to the manufacturer’s
recommendations to validate the automated cleaning process. It is the
responsibility of the processor to ensure that the processing is conducted in
accordance with a validated method. Any deviation by the processor from these
recommendations should be evaluated.
1. Place the device in an automated washer (for example, Steris Reliance™
Genfore™ Washer/Disinfector).
Note: Avoid contact between devices while loading the washer.
2. Set the automated washer to run the parameters identified in Table 3 and allow
the automated washer to complete the wash cycle.
Table 3. Automated washer cleaning parameters
Treatment
Enzymatic
wash
Wash 02:00 ≥60 °C
Rinse 02:00 ≥60 °C
Dry 15:00 ≥82 °C
Inspection N/A N/A Visually inspect each device for any
Water tempera-
ture Cleaning instructions
water.
a minimum of 1 min with 7.8 mL/1 L
(or 1 ounce/1 gallon) of an enzymatic detergent (for example,
ENZOL) and water. Remove visible
soil with a soft-bristled brush (for
example, a nylon toothbrush).
2 min.
remaining soil. If needed, repeat the
process.
Time
(min) Temperature Cleaning agent
04:00 ≥60 °C
(≥140 °F)
(≥140 °F)
(≥140 °F)
(≥180 °F)
Steris Prolystica™ Ultra Concentrate
Enzymatic Cleaner diluted as
1.0 mL/1 L (or 0.125 ounce/1 gallon).
Steris Prolystica™ Ultra Concentrate
Neutral Detergent diluted as
1.0 mL/1 L (or 0.125 ounce/1 gallon).
N/A
N/A
remaining soil or moisture. If soil
remains, repeat the process. If needed, dry the device with filtered, compressed air or a lint-free wipe.
5.2 Steam sterilization and resterilization
• Use standard packaging material. Ensure that the pack is large enough to
contain the device without stressing the seals. When validating the sterilization
processes, Medtronic used the appropriate accessory tray for each device.
15
English
Page 16

• Medtronic validated steam cycles when the devices were wrapped by CSR
(Central Supply Room) wrap. However, the steam sterilization process can be
completed when the devices are either unwrapped or wrapped in steam
sterilization compatible materials.
• When sterilizing multiple devices in 1 autoclave cycle, do not exceed the
sterilizer’s maximum load.
• Examine the device for cracking or degradation prior to use. Do not use the
device if components show signs of cracking or degradation.
• Some non-US health care authorities recommend sterilization cycle
parameters that minimize the potential risk of transmitting Creutzfeldt-Jakob
Disease (CJD). This recommendation is especially important for surgical
instruments that could come into contact with the central nervous system.
Table 4. Sterilization cycle parameters
Cycle type
Prevacuum
(dynamic-air-
removal)
Prevacuum
(dynamic-air-
removal)
Prevacuum (dynamic-
air-removal) for CJD
a
Temperature 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Exposure time 4 min 3 min 18 min
a
Medtronic recommends incinerating devices that have directly contacted patients suspected
or confirmed with Transmissible Spongiform Encephalopathy (TSE)/CJD diagnosis. NHS
Estates HTM 2010 Parts 4 & 6: Appendix 2, Items contaminated with TSE Agents and WHO
Infection Control Guidelines for Transmissible Spongiform Encephalopathies refer to a TSE
decontamination cycle using a steam autoclave at a temperature of 134 °C to 137 °C (273 °F
to 279 °F) for a single cycle of 18 min or multiple cycles totaling 18 min (for example, six 3 min
cycles).
b
The minimum dry times were validated using sterilizers with vacuum drying capabilities. Drying
cycles using ambient atmospheric pressure may require longer dry times. Refer to the sterilizer
manufacturer’s recommendations.
Dry time
b
20 min 16 min 30 min
6 Instructions for use
Note: The blades are marked with a number that corresponds to the last digit of the
model number. For example, 28603 is marked “3”; 28606B is marked “6B.” Each
blade is marked with a unique serial number.
6.1 Blade attachment
1. Attach the blades to the retractor rack by sliding the blade mount into the
retractor rack arm.
2. Remove the blades by sliding the blade mount out of the retractor rack arm.
6.2 LIMA harvest
1. Place the retractor, with LIMA blades attached, into the thoracotomy. The large
LIMA blade with the hole at the end should be oriented cephalad to the smaller
blade.
2. Turn the retractor knob to open the retractor and spread the thoracotomy.
3. Apply upward tension on the large LIMA blade at the hole at the end of the
blade to tilt the retractor upward. This action provides access to the LIMA and
enables harvesting.
Note: The retractor is designed to work with the Rultract™ retractor system to
apply upward tension on the large LIMA blade. Other means or methods for
applying upward tension may be used.
English
16
Page 17

4. Once the LIMA harvest is complete, release upward tension from the large
LIMA blade.
5. Depress the release lever to close the retractor.
6. Remove the retractor from the thoracotomy.
6.3 General thoracotomy retraction
1. Attach thoracotomy blades to the retractor.
2. Place the retractor into the thoracotomy.
3. Turn the retractor knob to open the retractor and spread the thoracotomy.
4. Upon completion of the procedure, depress the release lever to close the
retractor.
5. Remove the retractor from the thoracotomy.
7 Disclaimer of warranty (global)
ALTHOUGH THE PRODUCT HAS BEEN DESIGNED, MANUFACTURED, AND
TESTED PRIOR TO SALE UNDER CAREFULLY CONTROLLED CONDITIONS,
THE PRODUCT MAY FAIL TO PERFORM ITS INTENDED FUNCTION FOR A
VARIETY OF REASONS. MEDTRONIC HAS NO CONTROL OVER THE
CONDITIONS UNDER WHICH THIS PRODUCT IS USED. THE WARNINGS
CONTAINED IN THE PRODUCT LABELING PROVIDE MORE DETAILED
INFORMATION AND ARE CONSIDERED AN INTEGRAL PART OF THIS
DISCLAIMER OF WARRANTY. MEDTRONIC, THEREFORE, DISCLAIMS ALL
WARRANTIES, BOTH EXPRESS AND IMPLIED, WITH RESPECT TO THE
PRODUCT, INCLUDING, BUT NOT LIMITED TO, ANY IMPLIED WARRANTY OF
MERCHANTABILITY OR FITNESS FOR A PARTICULAR PURPOSE.
MEDTRONIC SHALL NOT BE LIABLE TO ANY PERSON OR ENTITY FOR ANY
MEDICAL EXPENSES OR ANY DIRECT, INCIDENTAL, OR CONSEQUENTIAL
DAMAGES CAUSED BY ANY USE, DEFECT, FAILURE, OR MALFUNCTION OF
THE PRODUCT, WHETHER THE CLAIM IS BASED UPON WARRANTY,
CONTRACT, TORT, OR OTHERWISE. EXCEPT AS OTHERWISE AGREED TO
IN WRITING BY AUTHORIZED MEDTRONIC PERSONNEL, NO PERSON HAS
ANY AUTHORITY TO BIND MEDTRONIC TO ANY REPRESENTATION OR
WARRANTY WITH RESPECT TO THE PRODUCT.
The exclusions and limitations set out above are not intended to, and should not be
construed so as to, contravene mandatory provisions of applicable law. If any part
or term of this Disclaimer of Warranty is held by any court of competent jurisdiction
to be illegal, unenforceable, or in conflict with applicable law, the validity of the
remaining portions of this Disclaimer of Warranty shall not be affected, and all rights
and obligations shall be construed and enforced as if this Disclaimer of Warranty did
not contain the particular part or term held to be invalid.
17
English
Page 18

1 Описание на продукта
Модел Описание
28610 MICS система за ретрактор
28611 Подложка за ретрактор
28601 Остриета за LIMA, стандартни
28602 Остриета за LIMA, дълбоки
28603 Дълги остриета за торакотомия, стандартни
28604 Дълги остриета за торакотомия, дълбоки
28604B Дълго удължено монтирано острие, стандартно
28605 Къси остриета за торакотомия, стандартни
28606 Къси остриета за торакотомия, дълбоки
28606B Късо удължено монтирано острие нисш клас, стан-
Забележка: Модел 28601 е острието, което най-често се използва за
отпрепариране на лява вътрешна гръдна артерия (LIMA). Модел 28605 е
острието, което най-често се използва за ретракция при торакотомия.
Всички други остриета са предназначени за използване при различни
вариации на анатомията на пациента.
Забележка: Модели 28604B и 28606B са по-нисш клас остриета,
предназначени за жени и пациенти с наднормено тегло. Използвайте тези
остриета от по-нисш клас с остриетата от по-висш клас (модели 28604 и
28606).
дартно
2 Показания за употреба
Системата за ретрактор за минимална инвазивна сърдечна хирургия (MICS)
на ThoraTrak е предназначена за осигуряване на хирургичен достъп за
минимални инвазивни кардиоторакални процедури, включително при
хирургично поставяне на байпас присадка на коронарна артерия (CABG) и
отпрепариране на LIMA чрез ретракция на меки тъкани и кости.
3 Предпазни мерки
Медицинският специалист носи отговорност за извършване на
хирургическите процедури и техники по правилния начин. Хирурзите трябва
да направят оценка на приложимостта на процедурата въз основа на своя
собствен медицински опит и образование.
4 Странични ефекти
Не са известни.
5 Обработка и повторна обработка
Medtronic са одобрили инструкциите по-долу за подготовка на това
медицинско устройство за повторна употреба. Обработващото лице е
отговорно за постигане на желания резултат чрез действителното
извършване с помощта на оборудването, материалите и персонала в
помещението за обработка. Обработката изисква одобрение и регулярно
проследяване. Всяко отклонение на обработващото лице от посочените
инструкции трябва да бъде правилно оценено за ефективност и възможни
странични последствия. Почистването може да се извърши по ръчен или
Български
18
Page 19

автоматичен начин според тези инструкции за употреба или еквивалентен
одобрен метод.
5.1 Почистване
Предупреждение: Преди стерилизация почистете устройството
внимателно, за да се премахне замърсяването.
Предупреждение: Не използвайте почистващи материали на основата на
разтворители (напр. ацетон или толуен).
• Не позволявайте изсъхването на замърсени устройства преди прилагане
на някаква почистваща процедура.
• Обработвайте повторно устройствата 2 часа след употреба. Ако
преносът до мястото за обработка се забави, поставете устройството в
покрит контейнер с ензимен детергент, за да предотвратите изсушаване.
• Ако устройството съдържа множество компоненти, напълно разглобете
елементите преди почистване според тези инструкции за употреба.
• Преди употреба проверете устройството за напукване и разрушаване. Не
използвайте устройството, ако компонентите показват признаци на
напукване или разрушаване.
• Не се изисква топлинна дезинфекция, защото устройствата са крайно
стерилизирани.
5.1.1 Ръчно почистване
Medtronic са установили следната процедура за ръчно почистване в
Таблица 1. Тези действия трябва да се извършат в рамките на 2 часа след
употреба.
Забележка: Ако устройството притежава подвижни части, се уверете, че
всички повърхности са изцяло почистени.
Таблица 1. Инструкции за ръчно почистване
Дей-
ствие Процес Температура Инструкции за почистване
1 Изплак-
ване
2 Потапяне >28 °C (>82 °F) Потопете напълно устройството за
3 Почистен
с ултра-
звук
4 Изплак-
ване
>27 °C (>81 °F) Отстранете замърсяванията, като
използвате течаща вода за 1 min.
Използвайте мека четка (например
найлонова четка за зъби), за да
почистите устройството щателно.
минимум 5 min в 15,6 mL/1 L (или
2 унции/1 галон) ензимен детергент
(например ENZOL™) и вода. Премахнете видимото замърсяване
чрез мека четка.
>27 °C (>81 °F) Потопете напълно устройството в
ултразвуково почистващо устройство (например Bransonic™) в
7,8 mL/1 L (или 1 унция/1 галон) ензимен детергент (например ENZOL) и
вода. Облъчвайте за 10 min.
>27 °C (>81 °F) Изплакнете устройството с течаща
вода за 1 min.
19 Български
Page 20

Таблица 1. Инструкции за ръчно почистване (продължение)
Дей-
ствие Процес Температура Инструкции за почистване
5 Изсуша-
ване
6 Проверка Не е наличен Визуално огледайте всяко устрой-
5.1.2 Автоматично почистване
Medtronic са установили следната процедура за автоматично почистване.
Стъпките в Таблица 2 трябва да се извършат най-късно 2 часа след употреба.
Забележка: Ако устройството или компонент имат подвижни части, се
уверете, че всички повърхности са изцяло почистени.
Таблица 2. Инструкции преди лечение
Дей-
ствие Процес
1 Изплак-
ване
2 Потапяне > 25 °C (> 77 °F) Потопете напълно устройството
3 Изплак-
ване
4 Проверка Не е наличен Огледайте визуално устрой-
Medtronic използва семейството почистващи препарати Prolystica™ съгласно
препоръките на производителя за одобряване на процеса по автоматично
почистване. Проява на отговорност от страна на обработващото лице е да се
увери, че обработката се провежда според одобрен метод. Всяко отклонение
от процеса спрямо тези препоръки трябва да бъде оценено.
1. Поставете устройството в автоматична миеща машина (например
миеща машина/дезинфекциращ уред Steris Reliance™ Genfore™).
Забележка: Избягвайте контакт между устройствата, докато
зареждате миещата машина.
2. Настройте автоматичната миеща машина да следва параметрите,
посочени в Таблица 3, и оставете на автоматичната миеща машина да
завърши миещия цикъл.
Не е наличен Подсушете с чиста кърпа без вла-
синки.
ство за оставащо замърсяване или
влага. Ако е останало замърсяване,
повторете процедурата.
Температура на
водата Инструкции за почистване
> 25 °C (> 77 °F) Отстранете замърсяванията,
като използвате течаща чешмяна
вода.
за най-малко 1 min в 7,8 mL/1 L
(или 1 унция/1 галон) ензимен
детергент (например ENZOL) и
вода. Премахнете видимото
замърсяване чрез мека четка
(например найлонова четка за
зъби).
> 25 °C (> 77 °F) Изплакнете устройството за поне
2 min.
ството за остатъчно замърсяване. Повторете процеса, ако е
необходимо.
Български
20
Page 21

Таблица 3. Параметри за автоматично измиване на миещата машина
Обработка
Ензимно
измиване
Промиване 02:00 ≥ 60 °C
Изплакване 02:00 ≥ 60 °C
Изсушаване 15:00 ≥ 82 °C
Проверка Не е
Време
(min)
04:00 ≥ 60 °C
наличен
Темпера-
тура Почистващ агент
(≥ 140 °F)
(≥ 140 °F)
(≥ 140 °F)
(≥ 180 °F)
Не е наличен Визуално огледайте всяко устрой-
Ултра концентриран ензимен
почистващ препарат Steris
Prolystica™, разреден като
1,0 mL/1 L (или
0,125 унции/1 галон).
Ултра концентриран неутрален
детергент Steris Prolystica™, разреден като 1,0 mL/1 L (или
0,125 унция/1 галон).
Не е наличен
Не е наличен
ство за оставащо замърсяване или
влага. Ако е останало замърсяване, повторете процедурата. Ако
е необходимо, изсушете устройството с филтриран въздух под
налягане или кърпа без власинки.
5.2 Стерилизация с пара и повторна стерилизация
• Използвайте стандартен материал за опаковане. Уверете се, че
опаковката е достатъчно голяма, за да побере устройството, без да се
създава напрежение върху затварянето. При валидиране на процеса на
стерилизация Medtronic са използвали подходящата допълнителна тава
за всяко устройство.
• Medtronic са валидирали циклите с пара, когато устройствата са обвити с
опаковка CSR (Central Supply Room - Централна стая за снабдяване).
Процесът на стерилизиране с пара може да бъде завършен, когато
устройствата са неопаковани или опаковани с материали, съвместими
със стерилизацията с пара.
• При стерилизирането на множество устройства в 1 автоклавен цикъл не
превишавайте максималния товар на стерилизатора.
• Преди употреба проверете устройството за напукване и разрушаване. Не
използвайте устройството, ако показва признаци на напукване или
разрушаване.
• Някои здравни органи извън САЩ препоръчват цикъл на стерилизиране
с параметри, които ще сведат до минимум потенциалния риск от пренос
на болестта на Кройцфелд-Якоб (CJD). Тази препоръка е особено важна
за хирургическите инструменти, които може да влязат в контакт с
централната нервна система.
21
Български
Page 22

Таблица 4. Параметри на цикъла на стерилизация
Тип на
цикъла
Предварите-
лен вакуум
(динамично
извеждане на
въздуха)
Предварителен
вакуум (дина-
мично изве-
ждане на въз-
духа)
Предварителен
вакуум (динамично
извеждане на въз-
духа) за CJD
a
Температура 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Време на
4 min 3 min 18 min
излагане
Време на
b
сушене
a
Medtronic препоръчва устройствата, влизали в пряк контакт с пациенти с
предполагаема или потвърдена диагноза за трансмисивна спонгиформна
енцефалопатия (TSE)/CJD, да се изгарят. NHS Estates HTM 2010 Parts 4 & 6: Appendix 2,
Items contaminated with TSE Agents and WHO Infection Control Guidelines for Transmissible
Spongiform Encephalopathies (Насоки на СЗО за контрол на инфекциите по отношение
на трансмисивните спонгиформни енцефалопатии) се отнасят за цикъла на
обеззаразяване от трансмисивна спонгиформна енцефалопатия с помощта на парен
автоклав при температура от 134 °C до 137 °C (273 °F до 279 °F) за единичен цикъл от
18 min или за няколко цикъла с обща продължителност от 18 min (например шест
цикъла от 3 min).
b
Минималните времена на сушене са одобрени при употреба на стерилизатори с
възможности за сушене във вакуум. Изсушаващи цикли, използващи околното
атмосферно налягане, може да изискват по-дълги периоди на сушене. Разгледайте
препоръките от производителя на стерилизатора.
20 min 16 min 30 min
6 Инструкции за употреба
Забележка: Остриетата са обозначени с номер, който съответства на
последната цифра на номера на модела. Например 28603 е означен като „3“;
28606B е означен като „6B“. Всяко острие е маркирано с уникален сериен
номер.
6.1 Прикрепване на острие
1. Прикрепете остриетата към подложката за прибиране, като
приплъзнете острието, монтирано на дръжката, на подложката за
прибиране.
2. Отстранете остриетата, като приплъзнете монтираното острие извън
дръжката на подложката за прибиране.
6.2 Отпрепариране на LIMA
1. Използвайте ретрактора с прикрепените остриета за LIMA при
торакотомията. Голямото острие за LIMA с отвора в края трябва да бъде
ориентирано към главата спрямо по-малкото острие.
2. Завъртете копчето на ретрактора, за да отворите ретрактора и да
разширите торакотомията.
3. Приложете натиск нагоре върху голямото острие за LIMA на отвора в
края на острието, за да наклоните ретрактора напред. Това действие
осигурява достъп до LIMA и позволява отпрепариране.
Забележка: Ретракторът е предназначен за работа със системата за
ретрактор Rultract™ с цел прилагане на напрежение нагоре на голямото
острие за LIMA. Могат да бъдат използвани други начини и методи за
прилагане на напрежение в посока нагоре.
Български
22
Page 23

4. При пълно отпрепариране на LIMA освободете напрежението в посока
нагоре от голямото острие за LIMA.
5. Спуснете лоста за освобождаване за затваряне на ретрактора.
6. Отстранете ретрактора от полето на торакотомията.
6.3 Обща ретракция при торакотомия
1. Прикрепете остриетата за торакотомия към ретрактора.
2. Поставете ретрактора в полето за торакотомия.
3. Завъртете копчето на ретрактора, за да отворите ретрактора и да
разширите торакотомията.
4. При завършване на процедурата спуснете лоста за освобождаване, за
да затворите ретрактора.
5. Отстранете ретрактора от полето на торакотомията.
7 Отказ от гаранция (глобално)
ВЪПРЕКИ ЧЕ ПРОДУКТЪТ Е ПРОЕКТИРАН, ПРОИЗВЕДЕН И ТЕСТВАН
ПРЕДИ ПРОДАЖБА ПРИ ВНИМАТЕЛНО КОНТРОЛИРАНИ УСЛОВИЯ,
ПРОДУКТЪТ МОЖЕ ДА НЕ ИЗПЪЛНИ ЗАДОВОЛИТЕЛНО
ПРЕДНАЗНАЧЕНАТА МУ ФУНКЦИЯ ПОРАДИ РЕДИЦА ПРИЧИНИ.
MEDTRONIC НЕ КОНТРОЛИРА УСЛОВИЯТА, ПРИ КОИТО СЕ ИЗПОЛЗВА
ТОЗИ ПРОДУКТ. ПРЕДУПРЕЖДЕНИЯТА, КОИТО СЕ СЪДЪРЖАТ В
ЕТИКЕТИТЕ НА ПРОДУКТА, СЪДЪРЖАТ ПОДРОБНА ИНФОРМАЦИЯ, И
СЕ СЧИТАТ ЗА НЕРАЗДЕЛНА ЧАСТ ОТ ТОЗИ ОТКАЗ ОТ ГАРАНЦИИ.
ПОРАДИ ТАЗИ ПРИЧИНА MEDTRONIC ОТХВЪРЛЯ ВСИЧКИ ГАРАНЦИИ,
ИЗРИЧНИ ИЛИ ПОДРАЗБИРАЩИ СЕ, ПО ОТНОШЕНИЕ НА ПРОДУКТА,
ВКЛЮЧИТЕЛНО, НО НЕ САМО, ВСЯКА ПРОИЗТИЧАЩА ГАРАНЦИЯ ЗА
ПРОДАВАЕМОСТ ИЛИ ГОДНОСТ ЗА ОПРЕДЕЛЕНА ЦЕЛ. MEDTRONIC
НЯМА ДА НОСИ ОТГОВОРНОСТ ПРЕД НИКОЕ ЛИЦЕ ИЛИ СУБЕКТ ЗА
НИКАКВИ МЕДИЦИНСКИ РАЗХОДИ ИЛИ ДИРЕКТНИ, СЛУЧАЙНИ ИЛИ
ПОСЛЕДВАЩИ ЩЕТИ, НАНЕСЕНИ ОТ УПОТРЕБА, ДЕФЕКТ ИЛИ
НЕИЗПРАВНОСТ НА ПРОДУКТА, НЕЗАВИСИМО ДАЛИ ИСКЪТ СЕ
ОСНОВАВА НА ГАРАНЦИЯ, ДОГОВОР, ЗАКОНОВО НАРУШЕНИЕ, ИЛИ
ДРУГО. ОСВЕН ЧРЕЗ ПИСМЕНО СЪГЛАСИЕ ОТ ОТОРИЗИРАН ЕКИП НА
MEDTRONIC, НИКОЙ ЧОВЕК НЯМА ПРАВО ДА ОБВЪРЗВА MEDTRONIC С
КАКВОТО И ДА Е ПРЕДСТАВИТЕЛСТВО ИЛИ ГАРАНЦИЯ ОТНОСНО
ПРОДУКТА.
Изключенията и ограниченията, наложени по-горе, не са предназначени да и
не трябва да се тълкуват като такива, които противоречат на
задължителните разпоредби на съответния закон. Ако някоя част или
условие от този отказ от гаранции се приемат от някой съд с компетентна
юрисдикция за незаконни, неизпълними или в противоречие със
съответното законодателство, валидността на останалите части от този
отказ от гаранции няма да бъде повлияна и всички права и задължения ще
бъдат изтълкувани и изпълнени така, сякаш този отказ от гаранции не е
съдържал частта или условието, счетени за невалидни.
23
Български
Page 24

1 Popis výrobku
Model Popis
28610 Retraktorový systém MICS
28611 Tělo retraktoru
28601 Lopatky pro levou vnitřní mamární tepnu, standardní
28602 Lopatky pro levou vnitřní mamární tepnu, hluboké
28603 Dlouhé lopatky pro torakotomii, standardní
28604 Dlouhé lopatky pro torakotomii, hluboké
28604B Dlouhá spodní lopatka s prodlouženým čepem, stan-
28605 Krátké lopatky pro torakotomii, standardní
28606 Krátké lopatky pro torakotomii, hluboké
28606B Krátká spodní lopatka s prodlouženým čepem, standardní
Poznámka: Model 28601 je lopatka, která se nejčastěji používá k odběru štěpu
z levé vnitřní mamární tepny (LIMA). Model 28605 je lopatka, která se nejčastěji
používá k běžné torakotomické retrakci. Všechny ostatní lopatky jsou
zkonstruovány tak, aby se daly přizpůsobit různým anatomickým poměrům
pacienta.
Poznámka: Modely 28604B a 28606B jsou spodní lopatky určené pro ženy a
obézní pacienty. Tyto spodní lopatky používejte spolu s horními lopatkami
(modely 28604 a 28606).
dardní
2 Indikace k použití
Retraktorový systém ThoraTrak pro minimálně invazivní kardiochirurgii (MICS) je
určen k zajištění chirurgického přístupu při minimálně invazivních kardiotorakálních
výkonech, jako jsou například minimálně invazivní operace koronárního arteriálního
bypassu (CABG) a odběry štěpů z levé vnitřní mamární tepny (LIMA), a to
prostřednictvím retrakce měkké a kostní tkáně.
3 Bezpečnostní opatření
Za použití správných chirurgických postupů a technik zodpovídá odborný lékař.
Vhodnost jednotlivých postupů musí posoudit chirurg na základě vlastní lékařské
praxe a zkušeností.
4 Nežádoucí účinky
Nejsou známy.
5 Ošetření a ošetření při opakovaném použití
Společnost Medtronic validovala pro přípravu tohoto zdravotnického prostředku
k opakovanému použití následující pokyny. Za to, aby se při ošetření skutečně
používalo určené vybavení a materiály, prováděli je k tomu určení pracovníci a bylo
tak při něm dosaženo požadovaných výsledků, je zodpovědná osoba zajišťující
ošetření. Při ošetření se vyžaduje validace a sledování předepsaného postupu.
Stejně tak je třeba v případě, že se osoba provádějící ošetření nějakým způsobem
odchýlí od následujících pokynů, správně vyhodnotit vliv takového odchýlení na
účinnost a možné nežádoucí účinky. Čištění lze provádět ručně nebo
automatizovaně, a to podle tohoto návodu k použití nebo nějakou ekvivalentní
validovanou metodou.
Česky
24
Page 25

5.1 Čištění
Varování: Před provedením sterilizace prostředek důkladně očistěte, aby se
odstranily nečistoty.
Varování: Nepoužívejte čisticí prostředky na bázi rozpouštědel (např. aceton nebo
toluen).
• Před provedením jakéhokoli postupu čištění nenechte kontaminované
prostředky oschnout.
• Ošetření prostředků pro opakované použití provádějte do 2 hodin po použití.
Pokud bude přesun na místo, kde se bude ošetření provádět, trvat déle,
umístěte prostředek do zakryté nádoby obsahující enzymatický čisticí
prostředek, aby neoschl.
• Obsahuje-li prostředek několik komponent, musíte komponenty před
provedením čištění zcela demontovat podle tohoto návodu k použití.
• Před použitím zkontrolujte, zda na prostředku nejsou patrné praskliny nebo
známky opotřebení. Pokud kterákoli komponenta vykazuje známky trhlin nebo
opotřebení, prostředek nepoužívejte.
• Tepelná dezinfekce se nevyžaduje, protože prostředky se v závěrečné fázi
sterilizují.
5.1.1 Ruční čištění
Společnost Medtronic stanovila následující postup ručního čištění (viz Tabulka 1).
Tyto kroky musí být provedeny nejdéle do 2 hodin po použití.
Poznámka: Pokud má prostředek odnímatelné součásti, zajistěte, aby byly
důkladně očištěny všechny povrchové plochy.
Tabulka 1. Pokyny pro ruční čištění
Krok Proces Teplota Pokyny k čištění
1 Oplacho-
2 Namáčení >28 °C (>82 °F) Zdravotnický prostředek zcela ponořte
3 Ultrazvu-
kové
čištění
4 Oplacho-
>27 °C (>81 °F) Pod tekoucí vodou po dobu 1 min opla-
vání
>27 °C (>81 °F) Zdravotnický prostředek zcela ponořte
>27 °C (>81 °F) Oplachujte zdravotnický prostředek
vání
chujte hrubé nečistoty. Prostředek
důkladně očistěte kartáčkem s jemnými štětinkami (např. nylonovým zubním kartáčkem).
minimálně na 5 min do roztoku enzymatického čisticího prostředku (např.
ENZOL™) a vody namíchaného
v poměru 15,6 mL/1 L (nebo
2 unce/1 galon). Kartáčkem s jemnými
štětinkami odstraňte viditelné nečistoty.
do ultrazvukové čističky (např.
Bransonic™) s roztokem enzymatického čisticího prostředku (např.
ENZOL) a vody namíchaným v poměru
7,8 mL/1 L (nebo 1 unce/1 galon).
Čistěte v ultrazvukové lázni po dobu
10 min.
pod tekoucí vodou po dobu 1 min.
25 Česky
Page 26

Tabulka 1. Pokyny pro ruční čištění (pokračování)
Krok Proces Teplota Pokyny k čištění
5 Sušení (Neužívá se) Osušte čistou tkaninou nepouštějící
6 Kontrola (Neužívá se) Vizuálně zkontrolujte všechny pro-
5.1.2 Automatizované čištění
Společnost Medtronic stanovila následující postup automatizovaného čištění.
Kroky, které popisuje Tabulka 2, je nutné provést nejdéle do 2 hodin po použití.
Poznámka: Pokud má prostředek nebo komponenta odnímatelné součásti,
zajistěte, aby byly důkladně očištěny všechny povrchové plochy.
Tabulka 2. Pokyny pro předběžné ošetření
Krok Proces Teplota vody Pokyny k čištění
1 Oplacho-
vání
2 Namáčení >25 °C (>77 °F) Zdravotnický prostředek zcela
3 Oplacho-
vání
4 Kontrola (Neužívá se) Vizuálně zkontrolujte, zda na pro-
Společnost Medtronic použila k validaci procesu automatizovaného čištění čisticí
prostředky řady Prolystica™ (v souladu s doporučeními výrobce). Za to, aby bylo
ošetření provedeno v souladu s validovanou metodou, je zodpovědná osoba
zajišťující ošetření. Pokud se osoba provádějící ošetření od těchto doporučení
jakýmkoli způsobem odchýlí, je třeba provést vyhodnocení.
1. Vložte zdravotnický prostředek do automatické myčky (např.
myčka/dezinfekční přístroj Steris Reliance™ Genfore™).
Poznámka: Při vkládání do myčky zabraňte kontaktu mezi prostředky.
2. Nastavte na automatické myčce parametry, které obsahuje Tabulka 3,
a nechte proběhnout jeden mycí cyklus.
Tabulka 3. Parametry čištění v automatické myčce
Ošetření
Enzymatické
mytí
>25 °C (>77 °F) Pod tekoucí vodou z vodovodního
>25 °C (>77 °F) Oplachujte zdravotnický prostředek
Čas
(min) Teplota Čisticí prostředek
04:00 ≥60 °C
(≥140 °F)
vlákna.
středky, zda na nich nejsou zbytky nečistot nebo zda nejsou vlhké. Pokud na
nich zůstaly nečistoty, zopakujte
postup.
kohoutku odstraňte hrubé nečistoty.
ponořte minimálně na 1 min do roztoku enzymatického čisticího prostředku (např. ENZOL) a vody namíchaného v poměru 7,8 mL/1 L (nebo
1 unce/1 galon). Kartáčkem s jemnými štětinkami (např. nylonovým
zubním kartáčkem) odstraňte viditelné nečistoty.
minimálně 2 min.
středku nezbyly žádné nečistoty.
V případě potřeby postup zopakujte.
Koncentrovaný enzymatický čisticí
prostředek Steris Prolystica™ Ultra
26Česky
Page 27

Tabulka 3. Parametry čištění v automatické myčce (pokračování)
Čas
Ošetření
(min) Teplota Čisticí prostředek
naředěný v poměru 1,0 mL/1 L
(0,125 unce/1 galon).
Mytí 02:00 ≥60 °C
(≥140 °F)
Koncentrovaný neutrální čisticí prostředek Steris Prolystica™ Ultra naředěný v poměru 1,0 mL/1 L
(0,125 unce/1 galon).
Oplachování 02:00 ≥60 °C
(Neužívá se)
(≥140 °F)
Sušení 15:00 ≥82 °C
(Neužívá se)
(≥180 °F)
Kontrola (Neužívá
(Neužívá se) Vizuálně zkontrolujte všechny pro-
se)
středky, zda na nich nejsou zbytky
nečistot nebo zda nejsou vlhké.
Pokud na nich zůstaly nečistoty,
zopakujte postup. V případě potřeby
prostředky osušte filtrovaným stlačeným vzduchem nebo tkaninou nepouštějící vlákna.
5.2 Sterilizace parou a resterilizace
• Použijte standardní obalový materiál. Zkontrolujte, zda je obal dostatečně
velký, aby obsažený zdravotnický prostředek neměl smáčknuté těsnicí spoje.
Společnost Medtronic použila při validaci sterilizačních postupů pro každý
prostředek vhodný podnos na příslušenství.
• Společnost Medtronic validovala parní cykly na zdravotnických prostředcích
zabalených do obalu CSR (Central Supply Room). Postup sterilizace parou
však lze provést i tehdy, nejsou-li zdravotnické prostředky zabaleny nebo jsou-li
zabaleny do materiálů vhodných pro sterilizaci.
• Při sterilizaci více prostředků v 1 cyklu autoklávu nesmí být překročeno
maximální zatížení sterilizátoru.
• Před použitím zkontrolujte, zda na prostředku nejsou patrné praskliny nebo
známky opotřebení. Pokud komponenty vykazují známky trhlin nebo
opotřebení, zdravotnický prostředek nepoužívejte.
• Některé orgány v jiných zemích než v USA, které se zabývají problematikou
zdravotní péče, doporučují sterilizaci s parametry cyklu, které snižují případné
riziko přenosu Creutzfeldt-Jakobovy nemoci (CJD) na minimum. Toto
doporučení je obzvláště důležité pro chirurgické nástroje, které by mohly přijít
do kontaktu s centrálním nervovým systémem.
Tabulka 4. Parametry sterilizačního cyklu
Typ cyklu
Teplota 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Doba působení 4 min 3 min 18 min
Doba sušení
a
Prostředky, které přišly do přímého kontaktu s pacienty se suspektní nebo potvrzenou
diagnózou přenosné spongiformní encefalopatie (TSE)/CJD, doporučuje společnost
Medtronic spálit. Materiály NHS Estates HTM 2010 Parts 4 & 6: Appendix 2, Items
contaminated with TSE Agents (Část 4 a 6: Dodatek 2, Položky kontaminované agens TSE)
Prevakuum
(dynamické
odvzdušnění)
b
20 min 16 min 30 min
Prevakuum
(dynamické
odvzdušnění)
Prevakuum (dynamické
odvzdušnění) pro CJD
a
27
Česky
Page 28

a WHO Infection Control Guidelines for Transmissible Spongiform Encephalopathies
(Směrnice WHO pro kontrolu infekce přenosné spongiformní encefalopatie) uvádějí
dekontaminační cyklus TSE za použití parního autoklávu při teplotě 134 °C až 137 °C (273 °F
až 279 °F) pro jeden cyklus o délce 18 min nebo několik cyklů s celkovou dobou trvání 18 min
(např. šest cyklů o délce 3 min).
b
Minimální doby sušení byly validovány s využitím sterilizačních přístrojů, které umožňují
vakuové sušení. Cykly sušení za použití okolního atmosférického tlaku mohou vyžadovat delší
dobu sušení. Viz doporučení výrobce sterilizačního přístroje.
6 Návod k použití
Poznámka: Lopatky jsou označeny číslicí odpovídající poslední číslici čísla
modelu. Model 28603 je například označen číslicí 3, model 28606B je označen
znaky 6B. Každá lopatka je označena jedinečným sériovým číslem.
6.1 Připevnění lopatek
1. Lopatky k tělu retraktoru připevníte zasunutím čepů lopatek do ramene těla
retraktoru.
2. Pokud chcete lopatky odstranit, vysuňte jejich čepy z ramene těla retraktoru.
6.2 Odběr štěpu z levé vnitřní mamární tepny (LIMA)
1. Umístěte retraktor s nasazenými lopatkami pro levou vnitřní mamární tepnu do
torakálního řezu. Velká lopatka pro levou vnitřní mamární tepnu s otvorem na
konci by měla směřovat cefalicky k menší lopatce.
2. K rozevření retraktoru a torakálního řezu otočte regulátorem retraktoru.
3. Zatlačením na velkou lopatku pro levou vnitřní mamární tepnu směrem nahoru
v místě otvoru na konci lopatky nakloníte retraktor nahoru. Tímto způsobem lze
získat přístup k levé vnitřní mamární tepně (LIMA) a provést odběr štěpu.
Poznámka: Retraktor je určen k použití s retraktorovým systémem Rultract™,
aby bylo možné vyvinout na velkou lopatku pro levou vnitřní mamární tepnu tlak
směrem nahoru. Je možné použít také jiné prostředky a metody pro vyvinutí
tlaku směrem nahoru.
4. Po dokončení odběru štěpu z levé vnitřní mamární tepny uvolněte tlak směrem
nahoru vyvinutý na velkou lopatku pro levou vnitřní mamární tepnu.
5. Stlačením uvolňovací páčky zavřete retraktor.
6. Vyjměte retraktor z torakálního řezu.
6.3 Běžná torakotomická retrakce
1. Připevněte k retraktoru lopatky pro torakotomii.
2. Zaveďte retraktor do torakálního řezu.
3. K rozevření retraktoru a torakálního řezu otočte regulátorem retraktoru.
4. Po dokončení postupu stiskněte uvolňovací páčku pro zavření retraktoru.
5. Vyjměte retraktor z torakálního řezu.
7 Odmítnutí záruk (globální)
AČKOLI BYL VÝROBEK NAVRŽEN, VYROBEN A PŘED PRODEJEM
TESTOVÁN ZA PEČLIVĚ KONTROLOVANÝCH PODMÍNEK, JE MOŽNÉ, ŽE
U VÝROBKU Z RŮZNÝCH DŮVODŮ SELŽE JEHO ZAMÝŠLENÁ FUNKCE.
SPOLEČNOST MEDTRONIC NEMÁ ŽÁDNOU KONTROLU NAD
PODMÍNKAMI, VE KTERÝCH SE VÝROBEK POUŽÍVÁ. VAROVÁNÍ UVEDENÁ
NA ŠTÍTCÍCH VÝROBKU POSKYTUJÍ PODROBNĚJŠÍ INFORMACE A JSOU
POVAŽOVÁNA ZA NEDÍLNOU SOUČÁST TOHOTO ODMÍTNUTÍ ZÁRUK.
Česky
28
Page 29

SPOLEČNOST MEDTRONIC PROTO ODMÍTÁ ODPOVĚDNOST ZA JAKÉKOLI
ZÁRUKY ZA TENTO VÝROBEK, AŤ UŽ PŘÍMÉ NEBO PŘEDPOKLÁDANÉ,
VČETNĚ, ALE NIKOLI S OMEZENÍM NA JAKÉKOLI PŘEDPOKLÁDANÉ
ZÁRUKY PRODEJNOSTI NEBO VHODNOSTI K URČITÉMU ÚČELU.
SPOLEČNOST MEDTRONIC NEODPOVÍDÁ ŽÁDNÉ OSOBĚ ANI PRÁVNÍMU
SUBJEKTU ZA JAKÉKOLI ZDRAVOTNÍ VÝDAJE NEBO PŘÍMÉ, NÁHODNÉ ČI
NÁSLEDNÉ ŠKODY ZPŮSOBENÉ POUŽITÍM, VADOU, SELHÁNÍM NEBO
CHYBNOU FUNKCÍ VÝROBKU, BEZ OHLEDU NA TO, ZDA NÁROK VYPLÝVÁ
ZE ZÁRUKY, SMLOUVY, PROTIPRÁVNÍHO ČINU ČI Z JINÉHO DŮVODU.
POKUD NENÍ AUTORIZOVANÝMI PRACOVNÍKY SPOLEČNOSTI MEDTRONIC
PÍSEMNĚ SCHVÁLENO JINAK, ŽÁDNÁ OSOBA NENÍ OPRÁVNĚNA
ZAVAZOVAT SPOLEČNOST MEDTRONIC K JAKÝMKOLI PROHLÁŠENÍM
NEBO ZÁRUKÁM TÝKAJÍCÍM SE TOHOTO VÝROBKU.
Výjimky a omezení zde uvedená nejsou zamýšlena a nemají být v rozporu s platným
ustanovením rozhodného práva. Pokud bude kterákoli část nebo podmínka tohoto
odmítnutí záruk shledána příslušným soudem jako protiprávní, nevynutitelná nebo
v rozporu s příslušnými právními předpisy, nemá to vliv na platnost zbývající části
tohoto odmítnutí záruk a všechna práva a závazky budou chápány a uplatněny tak,
jako by toto odmítnutí záruk neobsahovalo tuto konkrétní část nebo podmínku, která
byla shledána neplatnou.
29
Česky
Page 30

1 Produktbeskrivelse
Model Beskrivelse
28610 MICS Retraktorsystem
28611 Retraktormonteringspanel
28601 LIMA-blade, standard
28602 LIMA-blade, dybe
28603 Lange thorakotomiblade, standard
28604 Lange thorakotomiblade, dybe
28604B Langt forlænget nedre montérblad, standard
28605 Korte thorakotomiblade, standard
28606 Korte thorakotomiblade, dybe
28606B Kort forlænget nedre montérblad, standard
Bemærk: Model 28601 er det blad, der hyppigst benyttes ved udtagning af venstre
arteria mammaria interna (LIMA). Model 28605 er det blad, der hyppigst benyttes
ved almindelig thorakotomitilbagetrækning. Alle øvrige blade er udformet, så de
passer til forskellige patientanatomier.
Bemærk: Model 28604B og 28606B er nedre blade, der er beregnet til kvinder og
overvægtige patienter. Anvend disse nedre blade med de øvre blade (model 28604
og 28606).
2 Indikationer for brug
ThoraTrak retraktorsystemet til minimalt invasiv hjertekirurgi (MICS) er beregnet til
at give adgang til at udføre minimalt invasiv kardiothorakalkirurgi, herunder minimalt
invasiv koronararterie bypass-transplantationsprocedurer (CABG) og udtagning af
venstre arteria mammaria interna (LIMA), ved tilbagetrækning af blødt og benet
væv.
3 Forholdsregler
Korrekte operationsprocedurer og -teknikker er lægens ansvar. Lægerne må selv
vurdere enhver procedures egnethed på baggrund af egen lægeuddannelse og
egne erfaringer.
4 Bivirkninger
Ingen kendte.
5 Behandling og genbehandling
Følgende instruktioner er blevet valideret af Medtronic til klargøring af denne
medicinske enhed med henblik på genanvendelse. Den rengøringsansvarlige skal
sørge for, at rengøringen, som den udføres ved brug af udstyr, materialer og
personale i rengøringsområdet, giver det ønskede resultat. Rengøringen kræver
validering og rutinemæssig overvågning. Ligeledes skal enhver fravigelse, som den
rengøringsansvarlige foretager i forhold til nedenstående instruktioner, evalueres
grundigt med henblik på at fastslå effektivitet og eventuelle uønskede
konsekvenser. Rengøring kan udføres manuelt eller automatisk i henhold til denne
brugsanvisning eller en tilsvarende valideret metode.
5.1 Rengøring
Advarsel: Rengør enheden grundigt for at fjerne snavs inden sterilisering.
Dansk
30
Page 31

Advarsel: Anvend ikke rensemidler med opløsningsmidler (f.eks. acetone eller
toluen).
• Kontaminerede enheder må ikke tørre inden rengøring.
• Enhederne skal genbehandles inden for 2 timer efter brug. Hvis overførslen til
behandlingsområdet bliver forsinket, skal enheden anbringes i en tildækket
beholder med et enzymholdigt rensemiddel for at forhindre indtørring.
• Hvis enheden består af flere komponenter, skal den skilles helt ad inden
rengøring i henhold til denne brugsanvisning.
• Undersøg enheden for revner eller slitage inden brug. Enheden må ikke bruges,
hvis nogen komponenter viser tegn på revner eller slitage.
• Termisk desinfektion er ikke nødvendig, da enhederne er steriliseret terminalt.
5.1.1 Manuel rengøring
Medtronic har fastlagt følgende procedure for manuel rengøring i Tabel 1. Disse trin
skal udføres inden for maks. 2 timer efter brug.
Bemærk: Hvis enheden har bevægelige dele, skal man sikre sig, at alle
overfladeområder er blevet grundigt rengjort.
Tabel 1. Instruktioner til manuel rengøring
Trin Proces Temperatur Rengøringsvejledning
1 Skylning >27 °C (>81 °F) Fjern det meste snavs med rindende
2 Iblødsæt-
3 Rengøring
ultralyd
4 Skylning >27 °C (>81 °F) Skyl enheden med rindende vand i
5 Tørring Ikke tilgængeligt Tør med en ren, fnugfri klud.
6 Inspektion Ikke tilgængeligt Inspicer hver enhed visuelt for tilbage-
5.1.2 Automatisk rengøring
Medtronic har fastsat følgende procedure for automatisk rengøring. Trinnene i
Tabel 2 skal udføres inden for maks. 2 timer efter brug.
Bemærk: Hvis enheden eller komponenten har bevægelige dele, skal man sikre
sig, at alle overfladeområder er blevet grundigt rengjort.
>28 °C (>82 °F) Nedsænk enheden helt i min. 5 min
ning
>27 °C (>81 °F) Nedsænk enheden helt i et ultralyds-
med
vand i 1 min. Brug en blød børste (f.eks.
en nylontandbørste) til at rengøre enheden grundigt.
med 15,6 mL/1 L (eller 2 oz/1 gallon) af
et enzymholdigt rensemiddel (f.eks.
ENZOL™) og vand. Fjern synligt snavs
med en blød børste.
bad (f.eks. Bransonic™) med
7,8 mL/1 L (eller 1 oz/1 gallon) af et
enzymholdigt rensemiddel (f.eks.
ENZOL) og vand. Udfør ultralydsbehandling i 10 min.
1 min.
værende snavs eller fugt. Hvis komponenten ikke er ren, gentages processen.
31
Dansk
Page 32

Tabel 2. Instruktioner til forbehandling
Trin Proces Vandtemperatur Rengøringsvejledning
1 Skylning >25 °C (>77 °F) Fjern det meste snavs med rin-
2 Iblødsæt-
ning
3 Skylning >25 °C (>77 °F) Skyl enheden i min. 2 min.
4 Inspektion Ikke tilgængeligt Inspicer enheden visuelt for tilbage-
Medtronic brugte rensemidler fra Prolystica™-serien i henhold til fabrikantens
anbefalinger til at validere den automatiske rengøringsproces. Den
rengøringsansvarlige skal sørge for, at rengøringen udføres i henhold til en valideret
metode. Enhver afvigelse, som den rengøringsansvarlige gør fra disse
anbefalinger, skal evalueres.
1. Anbring enheden i en automatisk opvaskemaskine (f.eks. Steris Reliance™
Genfore™ Washer/Disinfector).
Bemærk: Undgå kontakt mellem enhederne, når opvaskemaskinen fyldes.
2. Indstil den automatiske opvaskemaskine til at køre de parametre, der er
angivet i Tabel 3 og lad den automatiske opvaskemaskine fuldføre
vaskecyklussen.
Tabel 3. Parametre ved rengøring i den automatiske opvaskemaskine
Behandling
Enzymatisk
vask
Vask 02:00 ≥60 °C
Skyl 02:00 ≥60 °C
Tør 15:00 ≥82 °C
Inspektion Ikke til-
>25 °C (>77 °F) Nedsænk enheden helt i min. 1 min
Tid
(min) Temperatur Rengøringsmiddel
04:00 ≥60 °C
gænge-
ligt
(≥140 °F)
(≥140 °F)
(≥140 °F)
(≥180 °F)
Ikke tilgænge-
ligt
dende vand fra hanen.
med 7,8 mL/1 L (eller 1 oz/1 gallon)
af et enzymholdigt rensemiddel
(f.eks. ENZOL) og vand. Fjern synligt snavs med en blød børste (f.eks.
en nylontandbørste).
værende snavs. Om nødvendigt
gentages processen.
Steris Prolystica™ Ultra Concentrate
Enzymatic Cleaner fortyndet som
1,0 mL/1 L (eller 0,125 oz/1 gallon).
Steris Prolystica™ Ultra Concentrate
Neutral Detergent fortyndet som
1,0 mL/1 L (eller 0,125 oz/1 gallon).
Ikke tilgængeligt
Ikke tilgængeligt
Inspicer hver enhed visuelt for tilbageværende snavs eller fugt. Hvis
komponenten ikke er ren, gentages
processen. Tør enheden med filtreret
trykluft eller en fnugfri klud, hvis det er
nødvendigt.
5.2 Dampsterilisering og resterilisering
• Anvend standardmateriale til indpakning. Sørg for, at indpakningen er så stor, at
enheden kan være der uden at lægge pres på forseglingerne. Under
valideringen af steriliseringsprocesserne, anvendte Medtronic den relevante
tilbehørsbakke til hver enhed.
Dansk
32
Page 33

• Medtronic validerede dampcyklusser, mens enhederne var indpakket med
CSR (Central Supply Room) indpakning. Dampsteriliseringsprocessen kan
dog udføres, mens enhederne enten er uindpakkede eller pakket i materialer,
som er kompatible med dampsterilisering.
• Når flere enheder steriliseres i 1 autoklaveringscyklus, må sterilisatorens
maksimale kapacitet ikke overskrides.
• Undersøg enheden for revner eller slitage inden brug. Enheden må ikke bruges,
hvis der er tegn på revner eller slitage.
• Nogle sundhedsmyndigheder uden for USA anbefaler
steriliseringscyklusparametre, som minimerer den potentielle risiko for at
overføre Creutzfeldt-Jakob sygdom (CJD). Denne anbefaling er især vigtig for
kirurgiske instrumenter, som kan komme i kontakt med centralnervesystemet.
Tabel 4. Steriliseringscyklusparametre
Cyklustype
Prævakuum
(dynamisk
luftfjernelse)
Prævakuum
(dynamisk luft-
fjernelse)
Prævakuum (dynamisk
luftfjernelse) til CJD
Temperatur 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Eksponerings-
tid
b
Tørretid
a
Medtronic anbefaler, at enheder, som har været i direkte kontakt med patienter, der er under
mistanke for eller har fået bekræftet diagnosen overførbar spongiform encephalopati
(TSE)/CJD, forbrændes. NHS Estates HTM 2010 Parts 4 & 6: Appendix 2, Items contaminated
with TSE Agents, og WHO Infection Control Guidelines for Transmissible Spongiform
Encephalopathies henviser til en TSE-dekontamineringscyklus, der bruger en dampautoklave
med en temperatur på 134 °C til 137 °C (273 °F til 279 °F) for en enkelt cyklus på 18 min eller
flere cyklusser på i alt 18 min (f.eks. seks 3 min cyklusser).
b
Minimumstørretiderne blev valideret med sterilisatorer med vakuumtørrefunktioner. Der kan
være brug for længere tørretider til tørrecyklusser, der foregår ved atmosfærisk tryk. Se
sterilisatorfabrikantens anbefalinger.
4 min 3 min 18 min
20 min 16 min 30 min
6 Brugsanvisning
Bemærk: Bladene er mærket med et tal, der svarer til det sidste ciffer i
modelnummeret. For eksempel er 28603 markeret med “3”; 28606B er markeret
med “6B”. Hvert blad er mærket med et unikt serienummer.
6.1 Bladfastgørelse
1. Fastgør hvert blad til retraktoren ved at skubbe bladmonteringen ind i armen på
retraktormonteringspanelet.
2. Fjern bladene ved at trække bladmonteringen ud af
retraktormonteringspanelet.
6.2 LIMA-udtagning
1. Placér retraktoren, med LIMA-bladene fastgjorte, inde i thorakotomien. De
store LIMA-blade med hul på enden skal vendes cephalt i forhold til det mindre
blad.
2. Drej på retraktordrejeknappen for at åbne retraktoren og sprede
thorakotomien.
3. Tryk opad på det store LIMA-blad ved hullet på bladets ende for at vippe
retraktoren opad. Denne handling giver adgang til LIMA og gøre udtagning
mulig.
a
33
Dansk
Page 34

Bemærk: Retraktoren er konstrueret til at virke sammen med
Rultract™-retraktorsystemet for at udøve opadvendt tryk på det store
LIMA-blad. Der kan anvendes andre midler eller metoder til at udøve
opadvendt tryk.
4. Når udtagning af LIMA er fuldendt, løsnes det opadvendte tryk fra det store
LIMA-blad.
5. Tryk håndtagsudløseren helt ned for at lukke retraktoren.
6. Fjern retraktoren fra thorakotomien.
6.3 Almindelig thorakotomitilbagetrækning
1. Fastgør thorakotomibladene på retraktoren.
2. Anbring retraktoren i thorakotomien.
3. Drej på retraktordrejeknappen for at åbne retraktoren og sprede
thorakotomien.
4. Når indgrebet er gennemført, tryk håndtagsudløseren helt ned for at lukke
retraktoren.
5. Fjern retraktoren fra thorakotomien.
7 Ansvarsfraskrivelse (globalt)
SELVOM PRODUKTET ER BLEVET OMHYGGELIGT KONSTRUERET,
FREMSTILLET OG AFPRØVET INDEN SALG, KAN DER AF FORSKELLIGE
ÅRSAGER VÆRE RISIKO FOR, AT PRODUKTET IKKE FUNGERER EFTER
HENSIGTEN. MEDTRONIC HAR INGEN KONTROL OVER DE FORHOLD, SOM
PRODUKTET ANVENDES UNDER. ADVARSLERNE, SOM FREMGÅR AF
PRODUKTETS MÆRKATER, GIVER YDERLIGERE OPLYSNINGER OG
BETRAGTES SOM EN INTEGRERET DEL AF DENNE
ANSVARSFRASKRIVELSE. MEDTRONIC FRASKRIVER SIG DERFOR ALLE
GARANTIER, BÅDE UDTRYKKELIGE OG UNDERFORSTÅEDE, MED
HENSYN TIL PRODUKTET, HERUNDER, MEN IKKE BEGRÆNSET TIL, ALLE
UNDERFORSTÅEDE GARANTIER FOR SALGBARHED ELLER EGNETHED
TIL ET BESTEMT FORMÅL. MEDTRONIC ER IKKE ANSVARLIG OVER FOR
NOGEN PERSON ELLER ORGANISATION FOR NOGEN SOM HELST
MEDICINSKE UDGIFTER ELLER NOGEN SOM HELST DIREKTE,
TILFÆLDIGE ELLER FØLGESKADER, DER ER FORÅRSAGET AF NOGEN
FORM FOR BRUG, DEFEKT, FEJL ELLER FUNKTIONSVIGT VEDRØRENDE
PRODUKTET, UANSET OM KRAVET BYGGER PÅ GARANTIRET, AFTALERET,
ERSTATNINGSRET ELLER ANDET. MEDMINDRE DER FORELIGGER EN
SKRIFTLIG AFTALE MED BEMYNDIGET MEDTRONIC PERSONALE, HAR
INGEN PERSON NOGEN SOM HELST BEMYNDIGELSE TIL AT BINDE
MEDTRONIC TIL NOGEN ERKLÆRING ELLER GARANTI I FORBINDELSE
MED PRODUKTET.
Ovennævnte undtagelser og begrænsninger har ikke til hensigt at være i modstrid
med ufravigelige bestemmelser i gældende lov, og de må ikke fortolkes således.
Hvis noget afsnit eller vilkår i denne ansvarsfraskrivelse af en kompetent retsinstans
anses for ulovligt, uden retskraft eller i modstrid med gældende lovgivning, berøres
den resterende del af ansvarsfraskrivelsen ikke, og alle rettigheder og forpligtelser
skal tolkes og håndhæves, som om denne ansvarsfraskrivelse ikke indeholdt det
pågældende afsnit eller vilkår, der anses for ugyldigt.
Dansk
34
Page 35

1 Produktbeschreibung
Modell Beschreibung
28610 MICS Thoraxsperrer-System
28611 Thoraxsperrer
28601 LIMA-Blätter, Standard
28602 LIMA-Blätter, tief
28603 Lange Thorakotomieblätter, Standard
28604 Lange Thorakotomieblätter, tief
28604B Tiefer greifendes, langes Blatt mit verlängerter Befesti-
28605 Kurze Thorakotomieblätter, Standard
28606 Kurze Thorakotomieblätter, tief
28606B Tiefer greifendes, kurzes Blatt mit verlängerter Befesti-
Hinweis: Modell 28601 ist das am häufigsten für die Entnahme der linksseitigen
Arteria mammaria interna (LIMA) verwendete Blatt. Modell 28605 ist das am
häufigsten für die allgemeine Retraktion bei einer Thorakotomie verwendete Blatt.
Alle anderen Blätter wurden für verschiedene Patientenanatomien konzipiert.
Hinweis: Bei den Modellen 28604B und 28606B handelt es sich um tiefer greifende
Blätter für Frauen und fettleibige Patienten. Diese tiefer greifenden Blätter sind
zusammen mit den höher greifenden Blättern (Modelle 28604 und 28606) zu
verwenden.
gung, Standard
gung, Standard
2 Indikationen
Das ThoraTrak MICS Thoraxsperrer-System für die minimalinvasive Herzchirurgie
(minimally invasive cardiac surgery, MICS) dient zur Schaffung eines chirurgischen
Zugangs bei minimalinvasiven kardiothorakalen Eingriffen, einschließlich der
minimalinvasiven Venentransplantation beim autologen Koronararterien-Bypass
(CABG) und der Entnahme der linksseitigen Arteria mammaria interna (LIMA)
durch Zurückhalten von weichem und knochigem Gewebe.
3 Vorsichtsmaßnahmen
Die Verantwortung für die Anwendung und Einhaltung geeigneter operativer
Maßnahmen und Techniken obliegt dem Arzt. Chirurgen müssen die Eignung
jeglicher Verfahren auf der Basis der eigenen ärztlichen Ausbildung und Erfahrung
selbst beurteilen.
4 Unerwünschte Nebenwirkungen
Keine bekannt.
5 Aufbereitung und Wiederaufbereitung
Medtronic hat die folgenden Anweisungen für die Vorbereitung dieses
Medizinprodukts zur Wiederverwendung validiert. Es liegt jedoch weiterhin in der
Verantwortung der die Aufbereitung durchführenden Person sicherzustellen, dass
die Aufbereitung in ihrer tatsächlichen Durchführung mit den Geräten, Materialien
und dem Personal der Aufbereitungseinrichtung das erwünschte Ergebnis erzielt.
Diese Aufbereitung erfordert die Validierung und routinemäßige Überwachung des
Vorgangs. Im gleichen Maße müssen alle Abweichungen der durchführenden
Person von den folgenden Anweisungen ordnungsgemäß auf ihre Wirksamkeit und
35
Deutsch
Page 36

potenziell nachteiligen Folgen bewertet werden. Die Reinigung kann manuell oder
automatisiert gemäß der vorliegenden Gebrauchsanweisung oder einer
gleichwertigen validierten Methode durchgeführt werden.
5.1 Reinigung
Warnung: Reinigen Sie das Produkt gründlich, um vor der Sterilisierung
Verschmutzungen zu beseitigen.
Warnung: Verwenden Sie keine Reinigungsmittel auf Lösungsmittelbasis (z. B.
Azeton oder Toluol).
• Lassen Sie kontaminierte Produkte vor Durchführung eines
Reinigungsverfahrens nicht trocknen.
• Die Produkte sind innerhalb von zwei Stunden nach ihrer Verwendung
wiederaufzubereiten. Wenn sich der Transfer zum Aufbereitungsbereich
verzögert, legen Sie die Produkte in einen abgedeckten Behälter mit einem
enzymhaltigen Reinigungsmittel, damit sie nicht austrocknen.
• Wenn das Produkt aus mehreren Komponenten besteht, müssen die
Komponenten komplett zerlegt werden, bevor sie gemäß dieser
Gebrauchsanweisung gereinigt werden.
• Untersuchen Sie das Produkt vor der Verwendung auf Risse oder
Beschädigungen. Verwenden Sie das Produkt nicht, wenn Komponenten
Anzeichen von Rissen oder Beschädigungen aufweisen.
• Eine thermische Desinfektion ist nicht erforderlich, da die Produkte terminal
sterilisiert werden.
5.1.1 Manuelle Reinigung
Medtronic hat das folgende manuelle Reinigungsverfahren in Tabelle 1 für geeignet
befunden. Diese Schritte müssen innerhalb von maximal 2 Stunden nach der
Verwendung durchgeführt werden.
Hinweis: Wenn das Produkt bewegliche Teile besitzt, ist sicherzustellen, dass alle
Oberflächen gründlich gereinigt wurden.
Tabelle 1. Anleitung zur manuellen Reinigung
Schritt Vorgang Temperatur Reinigungsanleitung
1 Abspülen > 27 °C (> 81 °F) Grobe Verschmutzungen 1 min lang
2 Einwei-
3 Ultra-
schallreini-
> 28 °C (> 82 °F) Das Produkt mindestens 5 min lang
chen
> 27 °C (> 81 °F) Das Produkt vollständig in einen Ultra-
gen
unter fließendem Wasser abspülen.
Das Produkt gründlich mit einer Bürste
mit weichen Borsten (z. B. einer Nylonzahnbürste) reinigen.
vollständig in 15,6 mL/1 L (oder
2 Unzen/1 Gallone) enzymatische Reinigungslösung (zum Beispiel
ENZOL™) und Wasser eintauchen.
Sichtbare Verschmutzungen mit einer
Bürste mit weichen Borsten entfernen.
schallreiniger (zum Beispiel
Bransonic™) mit 7,8 mL/1 L (oder
1 Unze/1 Gallone) enzymatischer Reinigungslösung (zum Beispiel ENZOL)
und Wasser eintauchen. 10 min lang
mit Ultraschall reinigen.
36Deutsch
Page 37

Tabelle 1. Anleitung zur manuellen Reinigung (Fortsetzung)
Schritt Vorgang Temperatur Reinigungsanleitung
4 Abspülen > 27 °C (> 81 °F) Das Produkt 1 min lang unter fließen-
5 Trocknen – Mit einem sauberen, fusselfreien Tuch
6 Inspektion – Jedes einzelne Produkt visuell auf
5.1.2 Automatisierte Reinigung
Medtronic hat das folgende automatisierte Reinigungsverfahren für geeignet
befunden. Die in Tabelle 2 aufgeführten Schritte müssen innerhalb von maximal 2
Stunden nach der Verwendung durchgeführt werden.
Hinweis: Wenn das Produkt oder die Komponente bewegliche Teile besitzt, ist
sicherzustellen, dass alle Oberflächen gründlich gereinigt wurden.
Tabelle 2. Anleitung zur Vorbehandlung
Schritt Vorgang
1 Abspülen > 25 °C (> 77 °F) Grobe Verschmutzungen unter
2 Einwei-
chen
3 Abspülen > 25 °C (> 77 °F) Das Produkt mindestens 2 min lang
4 Inspektion – Das Produkt visuell auf eventuelle
Medtronic hat bei der Validierung des automatisierten Reinigungsverfahrens die
Prolystica™ Familie von Reinigungsmitteln gemäß den Empfehlungen des
Herstellers verwendet. Es liegt in der Verantwortung der durchführenden Person
sicherzustellen, dass die Aufbereitung gemäß eines validierten Verfahrens erfolgt.
Jegliche Abweichung, die die Aufbereitung durchführende Person von diesen
Empfehlungen vornimmt, muss überprüft werden.
1. Legen Sie das Produkt in einen automatischen Wäscher (zum Beispiel Steris
Reliance™ Genfore™ Wäscher/Desinfektor).
Hinweis: Vermeiden Sie beim Bestücken des Wäschers jegliche Berührung
zwischen den Produkten.
Wassertempera-
tur Reinigungsanleitung
> 25 °C (> 77 °F) Das Produkt mindestens 1 min lang
dem Wasser abspülen.
abtrocknen.
eventuelle Schmutz- oder Feuchtigkeitsreste überprüfen. Wenn noch
Schmutzreste vorhanden sind, wiederholen Sie den Vorgang.
fließendem Leitungswasser abspülen.
vollständig in 7,8 mL/1 L (oder
1 Unze/1 Gallone) enzymatische
Reinigungslösung (zum Beispiel
ENZOL) und Wasser eintauchen.
Sichtbare Verschmutzungen mit
einer Bürste mit weichen Borsten (z.
B. einer Nylonzahnbürste) entfernen.
abspülen.
Schmutzrückstände überprüfen.
Bei Bedarf den Vorgang wiederholen.
37
Deutsch
Page 38

2. Stellen Sie den automatischen Wäscher auf die in Tabelle 3 angegebenen
Parameter ein und lassen Sie den automatischen Wäscher den Waschzyklus
vollständig durchführen.
Tabelle 3. Reinigungsparameter für den automatischen Wäscher
Behandlung
Enzymatische
Wäsche
Waschen 02:00 ≥ 60 °C
Spülen 02:00 ≥ 60 °C
Trocknen 15:00 ≥ 82 °C
Inspektion – – Jedes einzelne Produkt visuell auf
Zeit
(min) Temperatur Reinigungsmittel
04:00 ≥ 60 °C
(≥ 140 °F)
(≥ 140 °F)
(≥ 140 °F)
(≥ 180 °F)
Steris Prolystica™ Ultra Concentrate
Enzymatic Cleaner, verdünnt im
Mischungsverhältnis 1,0 mL/1 L (oder
0,125 Unzen/1 Gallone).
Steris Prolystica™ Ultra Concentrate
Neutral Detergent, verdünnt im
Mischungsverhältnis 1,0 mL/1 L (oder
0,125 Unzen/1 Gallone).
–
–
eventuelle Schmutz- oder Feuchtigkeitsreste überprüfen. Wenn noch
Schmutzreste vorhanden sind, wiederholen Sie den Vorgang. Das Produkt bei Bedarf mit gefilterter Druckluft oder einem fusselfreien Tuch
trocknen.
5.2 Dampfsterilisation und Resterilisation
• Verwenden Sie ein Standardverpackungsmaterial. Vergewissern Sie sich,
dass die Packung groß genug ist, um das Produkt aufzunehmen, ohne dabei
die Versiegelungen überzubeanspruchen. Bei der Validierung des
Sterilisationsverfahrens hat Medtronic für jedes Produkt die geeignete
Zubehörschale verwendet.
• Bei der Validierung der Dampfzyklen durch Medtronic waren die Produkte in
Sterilisiermaterial aus dem zentralen Versorgungsraum eingewickelt. Die
Dampfsterilisation kann jedoch auch durchgeführt werden, wenn die Produkte
entweder nicht eingewickelt sind oder in für die Dampfsterilisation geeignetes
Material eingewickelt sind.
• Stellen Sie bei der Sterilisation mehrerer Produkte in einem Autoklavierzyklus
sicher, dass die maximale Beladung des Sterilisators nicht überschritten wird.
• Untersuchen Sie das Produkt vor der Verwendung auf Risse oder
Beschädigungen. Verwenden Sie das Produkt nicht, wenn Komponenten
Anzeichen von Rissen oder Beschädigungen aufweisen.
• Einige Gesundheitsbehörden außerhalb der USA empfehlen Parameter für den
Sterilisationszyklus, die das potenzielle Übertragungsrisiko der
Creutzfeldt-Jakob-Krankheit (CJD) minimieren. Diese Empfehlung gilt vor
allem für chirurgische Instrumente, die mit dem Zentralnervensystem in
Berührung kommen könnten.
Deutsch
38
Page 39

Tabelle 4. Parameter für den Sterilisationszyklus
Vorvakuum
Zyklustyp
(Dynamische
Luftentfer-
nung)
Vorvakuum
(Dynamische
Luftentfernung)
Vorvakuum (dynamische Luftentfernung)
für CJD
a
Temperatur 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Expositionszeit 4 min 3 min 18 min
Trocknungs-
b
dauer
a
Medtronic empfiehlt die Verbrennung von Produkten, die in direkten Kontakt mit Patienten mit
vermuteter oder bestätigter transmissibler spongiformer Enzephalopathie (TSE)/CreutzfeldtJakob-Diagnose gekommen sind. In der Veröffentlichung des staatlichen britischen
Gesundheitsdienstes NHS Estates HTM 2010 Parts 4 & 6: Appendix 2, Items contaminated
with TSE Agents und in den Leitlinien der Weltgesundheitsorganisation zur
Infektionsbekämpfung bei transmissiblen spongiformen Enzephalopathien WHO Infection
Control Guidelines for Transmissible Spongiform Encephalopathies wird ein
TSE-Dekontaminierungszyklus mit einem Dampfautoklav bei einer Temperatur von 134 °C bis
137 °C (273 °F bis 279 °F) für einen einzelnen Zyklus von 18 min oder für mehrere Zyklen mit
einer Dauer von insgesamt 18 min (z. B. sechs Zyklen von jeweils 3 min) angegeben.
b
Die Mindesttrocknungsdauer wurde bei Verwendung von Sterilisatoren mit
Vakuumtrocknungsfähigkeiten validiert. Trocknungszyklen unter atmosphärischem
Umgebungsluftdruck erfordern unter Umständen längere Trocknungszeiten. In den
Empfehlungen des Sterilisationsgeräteherstellers nachschlagen.
20 min 16 min 30 min
6 Gebrauchsanweisung
Hinweis: Die Blätter sind mit einer Zahl gekennzeichnet, die der letzten Ziffer der
Modellnummer entspricht. 28603 ist beispielsweise mit „3“ gekennzeichnet;
28606B ist mit „6B“ gekennzeichnet. Jedes Blatt ist mit einer eindeutigen
Seriennummer gekennzeichnet.
6.1 Blattbefestigung
1. Zum Anbringen der Blätter am Thoraxsperrer die Blattbefestigung auf den
Befestigungsarm des Thoraxsperrers schieben.
2. Zum Entfernen der Blätter die Blattbefestigung vom Befestigungsarm des
Thoraxsperrers abziehen.
6.2 Entnahme der linksseitigen Arteria mammaria interna (LIMA)
1. Den Thoraxsperrer mit den daran befestigten LIMA-Blättern in der
Thorakotomie platzieren. Das große LIMA-Blatt mit dem Loch am Ende muss
(im Verhältnis zum kleineren Blatt) kopfwärts ausgerichtet werden.
2. Am Knopf des Thoraxsperrers drehen, um diesen zu öffnen und die
Thorakotomie zu spreizen.
3. Ziehen Sie das gelochte Ende des großen LIMA-Blattes aufwärts, um den
Retraktor aufwärts zu bewegen. Hierdurch erhalten Sie Zugang zur LIMA und
können die Entnahme derselben durchführen.
Hinweis: Der Thoraxsperrer ist zur Verwendung mit dem Rultract™
Thoraxsperrer-System vorgesehen, um die aufwärtsgerichtete Kraft auf das
große LIMA-Blatt auszuüben. Andere Methoden zur Ausübung dieser
Aufwärtskraft sind zulässig.
4. Heben Sie, sobald die LIMA-Entnahme abgeschlossen ist, die auf das große
LIMA-Blatt ausgeübte Aufwärtskraft auf.
39
Deutsch
Page 40

5. Den Lösehebel hinabdrücken, um den Thoraxsperrer zu schließen.
6. Den Thoraxsperrer aus der Thorakotomie herausnehmen.
6.3 Verwendung des Thoraxsperrers bei der Thorakotomie
1. Die Thorakotomieblätter am Thoraxsperrer befestigen.
2. Den Thoraxsperrer in der Thorakotomie platzieren.
3. Am Knopf des Thoraxsperrers drehen, um diesen zu öffnen und die
Thorakotomie zu spreizen.
4. Nach Beendigung des Eingriffs den Lösehebel hinabdrücken, um den
Thoraxsperrer zu schließen.
5. Den Thoraxsperrer aus der Thorakotomie herausnehmen.
7 Haftungsausschluss (weltweit)
TROTZ SORGFÄLTIGER KONSTRUKTION, HERSTELLUNG UND VOR
VERKAUF DURCHGEFÜHRTER TESTDURCHLÄUFE IST ES MÖGLICH,
DASS DAS PRODUKT AUS DEN VERSCHIEDENSTEN GRÜNDEN NICHT
ZUFRIEDENSTELLEND FUNKTIONIERT. MEDTRONIC HAT KEINEN
EINFLUSS AUF DIE BEDINGUNGEN, UNTER DENEN DIESES PRODUKT
VERWENDET WIRD. DIE WARNHINWEISE IN DER PRODUKTINFORMATION
ENTHALTEN WEITERE DETAILLIERTE INFORMATIONEN UND SIND ALS
BESTANDTEIL DIESES HAFTUNGSAUSSCHLUSSES ANZUSEHEN.
MEDTRONIC SCHLIESST DAHER JEDE AUSDRÜCKLICHE ODER
STILLSCHWEIGENDE GARANTIE IN BEZUG AUF DAS PRODUKT AUS. DIES
SCHLIESST JEGLICHE IMPLIZITE GARANTIE AUF MARKTGÄNGIGKEIT
ODER EIGNUNG FÜR EINEN BESTIMMTEN ZWECK EIN. MEDTRONIC
HAFTET NICHT GEGENÜBER NATÜRLICHEN ODER JURISTISCHEN
PERSONEN JEGLICHER ART FÜR MEDIZINISCHE KOSTEN ODER
UNMITTELBARE, BEILÄUFIGE ODER FOLGESCHÄDEN, DIE DURCH
GEBRAUCH, DEFEKT, AUSFALL ODER FEHLFUNKTION DES PRODUKTS
ENTSTEHEN, UNABHÄNGIG DAVON, OB SICH EINE HAFTUNG FÜR
DERARTIGE SCHÄDEN AUF EINE GARANTIE, EINEN VERTRAG, EINE
UNERLAUBTE HANDLUNG ODER EINE ANDERE ANSPRUCHSGRUNDLAGE
STÜTZT. SOWEIT NICHT SCHRIFTLICH MIT ENTSPRECHEND BEFUGTEN
MEDTRONIC MITARBEITERN ETWAS ANDERES VEREINBART WURDE, IST
NIEMAND BERECHTIGT, MEDTRONIC AN IRGENDEINE ZUSICHERUNG
ODER GARANTIE IN BEZUG AUF DAS PRODUKT ZU BINDEN.
Die hier aufgeführten Haftungsausschlüsse und -beschränkungen sollen nicht
gegen geltendes Recht verstoßen und sind nicht dahingehend auszulegen. Sollte
ein zuständiges Gericht feststellen, dass dieser Haftungsausschluss ganz oder
teilweise unwirksam, nicht durchsetzbar oder im Widerspruch zu geltendem Recht
ist, berührt dies die Gültigkeit der restlichen Klauseln nicht. Alle Rechte und
Pflichten aus diesem Haftungsausschluss sind so auszulegen und durchzuführen,
als sei der für ungültig erklärte Teil oder die ungültige Vorschrift in dem
Haftungsausschluss nicht enthalten.
Deutsch
40
Page 41

1 Περιγραφή προϊόντος
Μοντέλο Περιγραφή
28610 Σύστημα διαστολέα MICS (Ελάχιστα επεμβατικής καρ-
28611 Σύστημα διαστολέα
28601 Λεπίδες LIMA, συνήθεις
28602 Λεπίδες LIMA, βαθιές
28603 Μακριές λεπίδες θωρακοτομής, συνήθεις
28604 Μακριές λεπίδες θωρακοτομής, βαθιές
28604B Μακριά λεπίδα μεγαλύτερου βάθους με εκτεινόμενη
28605 Κοντές λεπίδες θωρακοτομής, συνήθεις
28606 Κοντές λεπίδες θωρακοτομής, βαθιές
28606B Κοντή λεπίδα μεγαλύτερου βάθους με εκτεινόμενη
Σημείωση: Η λεπίδα Μοντέλο 28601 είναι αυτή που χρησιμοποιείται συνήθως
για την αφαίρεση (harvest) της αριστερής έσω μαστικής αρτηρίας (LIMA). Η
λεπίδα Μοντέλο 28605 είναι αυτή που χρησιμοποιείται συνήθως για γενική
διαστολή θωρακοτομής. Όλες οι άλλες λεπίδες έχουν σχεδιασθεί για να
εξυπηρετούν διάφορες ανατομίες ασθενών.
Σημείωση: Τα Μοντέλα 28604B και 28606B είναι λεπίδες μεγαλύτερου βάθους
σχεδιασμένες για γυναίκες και παχύσαρκους ασθενείς. Χρησιμοποιήστε αυτές
τις λεπίδες μεγαλύτερου βάθους με τις λεπίδες μικρότερου βάθους
(Μοντέλα 28604 και 28606).
διοχειρουργικής)
βάση, συνήθης
βάση, συνήθης
2 Ενδείξεις χρήσης
Το σύστημα διαστολέα ελάχιστα επεμβατικής καρδιοχειρουργικής (MICS)
ThoraTrak προορίζεται για την παροχή χειρουργικής προσπέλασης σε ελάχιστα
επεμβατικές καρδιοθωρακικές διαδικασίες, περιλαμβανομένης της ελάχιστα
επεμβατικής αορτοστεφανιαίας παράκαμψης με μόσχευμα (CABG) και της
αφαίρεσης (harvest) της αριστερής έσω μαστικής αρτηρίας (LIMA), μέσω της
διαστολής μαλακού και οστέινου ιστού.
3 Προφυλάξεις
Η χρήση κατάλληλων χειρουργικών διαδικασιών και τεχνικών αποτελεί ευθύνη
του επαγγελματία ιατρού. Οι χειρουργοί πρέπει να αξιολογούν την
καταλληλότητα οποιασδήποτε διαδικασίας βασιζόμενοι στην προσωπική τους
ιατρική εκπαίδευση και εμπειρία.
4 Ανεπιθύμητες ενέργειες
Καμία γνωστή.
5 Επεξεργασία και επανεπεξεργασία
Η Medtronic έχει επικυρώσει τις ακόλουθες οδηγίες για την προετοιμασία του
παρόντος ιατροτεχνολογικού προϊόντος για επαναχρησιμοποίηση. Αποτελεί
ευθύνη του υπεύθυνου επεξεργασίας να διασφαλίσει ότι η επεξεργασία όπως
διεξάγεται πραγματικά με χρήση εξοπλισμού, υλικών και προσωπικού στις
εγκαταστάσεις επεξεργασίας επιτυγχάνει το επιθυμητό αποτέλεσμα. Η
επεξεργασία απαιτεί επικύρωση και τακτική παρακολούθηση. Ομοίως, κάθε
41
Ελληνικά
Page 42

απόκλιση του υπεύθυνου επεξεργασίας από τις ακόλουθες οδηγίες θα πρέπει να
αξιολογείται καταλλήλως ως προς την αποτελεσματικότητα και πιθανές
ανεπιθύμητες συνέπειες. Ο καθαρισμός μπορεί να γίνεται μη αυτόματα ή μπορεί
να είναι αυτοματοποιημένος σύμφωνα με τις παρούσες Οδηγίες χρήσης ή με
αντίστοιχη επικυρωμένη μέθοδο.
5.1 Καθαρισμός
Προειδοποίηση: Πριν την αποστείρωση καθαρίστε σχολαστικά το προϊόν για να
απομακρύνετε τα υπολείμματα.
Προειδοποίηση: Μη χρησιμοποιείτε καθαριστικά που έχουν ως βάση διαλύτες
(π.χ. ακετόνη ή τολουόλιο).
• Μην αφήνετε τα μολυσμένα προϊόντα να στεγνώσουν πριν εφαρμόσετε
οποιαδήποτε διαδικασία καθαρισμού.
• Επανεπεξεργαστείτε τα προϊόντα εντός 2 ωρών μετά τη χρήση. Εάν η
μεταφορά στην περιοχή επεξεργασίας πρόκειται να καθυστερήσει,
τοποθετήστε το προϊόν σε καλυμμένο δοχείο με ενζυμικό απορρυπαντικό
ώστε να μη στεγνώσει.
• Εάν το προϊόν περιέχει πολλαπλά εξαρτήματα, αποσυναρμολογήστε
πλήρως τα εξαρτήματα πριν τον καθαρισμό, σύμφωνα με τις παρούσες
Οδηγίες χρήσης.
• Πριν από τη χρήση, εξετάστε το προϊόν για ραγίσματα ή αλλοίωση. Μη
χρησιμοποιήσετε το προϊόν εάν σε οποιαδήποτε εξαρτήματα υπάρχουν
ενδείξεις ραγίσματος ή αλλοίωσης.
• Δεν απαιτείται θερμική απολύμανση επειδή τα προϊόντα είναι τελικά
αποστειρωμένα.
5.1.1 Μη αυτόματος καθαρισμός
Η Medtronic έχει καθιερώσει την ακόλουθη διαδικασία μη αυτόματου καθαρισμού
στον Πίν. 1. Τα συγκεκριμένα βήματα πρέπει να εκτελεστούν εντός το πολύ
2 ωρών μετά τη χρήση.
Σημείωση: Εάν το προϊόν έχει κινητά μέρη, βεβαιωθείτε ότι όλες οι
επιφανειακές περιοχές έχουν καθαριστεί σχολαστικά.
Πίνακας 1. Οδηγίες μη αυτόματου καθαρισμού
Βήμα
Διαδικα-
1 Έκπλυση >27 °C (>81 °F) Απομακρύνετε τα έντονα υπολείμ-
2 Εμβά-
3 Καθαρι-
σία Θερμοκρασία Οδηγίες καθαρισμού
ματα με τη χρήση τρεχούμενου νερού
επί 1 min. Χρησιμοποιήστε μια βούρτσα με μαλακές τρίχες (για παράδειγμα, μια οδοντόβουρτσα με νάιλον
τρίχες) για να καθαρίσετε σχολαστικά
πτιση
>28 °C (>82 °F) Εμβαπτίστε τελείως το προϊόν για
>27 °C (>81 °F) Εμβαπτίστε τελείως το προϊόν σε λου-
σμός με
το προϊόν.
τουλάχιστον 5 min σε διάλυμα
15,6 mL/1 L (ή 2 ουγγιές/1 γαλόνι) από
ενζυμικό απορρυπαντικό (για
παράδειγμα, ENZOL™) και νερό. Απομακρύνετε τα ορατά υπολείμματα με
μια βούρτσα με μαλακές τρίχες.
τρό υπερήχων (για παράδειγμα,
Bransonic™) με διάλυμα 7,8 mL/1 L (ή
42Ελληνικά
Page 43

Πίνακας 1. Οδηγίες μη αυτόματου καθαρισμού (συνέχεια)
Βήμα
5.1.2 Αυτόματος καθαρισμός
Η Medtronic έχει καθιερώσει την ακόλουθη διαδικασία αυτόματου καθαρισμού. Τα
βήματα στον Πίν. 2 πρέπει να εκτελεστούν εντός το πολύ 2 ωρών μετά τη χρήση.
Σημείωση: Εάν το προϊόν ή το εξάρτημα έχει κινητά μέρη, βεβαιωθείτε ότι όλες
οι επιφανειακές περιοχές έχουν καθαριστεί σχολαστικά.
Πίνακας 2. Οδηγίες προεπεξεργασίας
Βήμα
Η Medtronic χρησιμοποίησε την οικογένεια καθαριστικών Prolystica™ σύμφωνα
με τις συστάσεις του κατασκευαστή για να επικυρώσει τη διαδικασία αυτόματου
καθαρισμού. Αποτελεί ευθύνη του υπεύθυνου επεξεργασίας να διασφαλίσει ότι η
επεξεργασία διεξάγεται σύμφωνα με μια επικυρωμένη μέθοδο. Οποιαδήποτε
απόκλιση του υπεύθυνου επεξεργασίας από αυτές τις συστάσεις θα πρέπει να
αξιολογείται.
1. Τοποθετήστε το προϊόν σε μια αυτόματη συσκευή πλύσης (για παράδειγμα
Διαδικα-
σία Θερμοκρασία Οδηγίες καθαρισμού
υπερή-
χους
4 Έκπλυση >27 °C (>81 °F) Εκπλύνετε το προϊόν με τρεχούμενο
5 Στέγνωμα Δ/Ε Στεγνώστε με ένα καθαρό πανί που
6 Επιθεώ-
ρηση
Διαδικα-
σία
1 Έκπλυση >25 °C (>77 °F) Απομακρύνετε τα έντονα υπολείμ-
2 Εμβάπτιση >25 °C (>77 °F) Εμβαπτίστε τελείως το προϊόν για
3 Έκπλυση >25 °C (>77 °F) Εκπλύνετε το προϊόν επί
4 Επιθεώ-
ρηση
τη συσκευή πλύσης/απολύμανσης Steris Reliance™ Genfore™).
Σημείωση: Αποφύγετε την επαφή των προϊόντων μεταξύ τους κατά την
τοποθέτησή τους στη συσκευή πλύσης.
Δ/Ε Επιθεωρήστε οπτικά κάθε προϊόν για
Θερμοκρασία
νερού Οδηγίες καθαρισμού
Δ/Ε Επιθεωρήστε οπτικά το προϊόν για
1 ουγγιά/1 γαλόνι) από ενζυμικό απορρυπαντικό (για παράδειγμα, ENZOL)
και νερό. Καθαρίστε με υπερήχους για
10 min.
νερό επί 1 min.
δεν αφήνει χνούδι.
τυχόν υπολείμματα ή υγρασία. Εάν
παραμένουν υπολείμματα, επαναλάβετε τη διαδικασία.
ματα με τη χρήση τρεχούμενου
νερού βρύσης.
τουλάχιστον 1 min σε διάλυμα
7,8 mL/1 L (ή 1 ουγγιά/1 γαλόνι)
από ενζυμικό απορρυπαντικό (για
παράδειγμα, ENZOL) και νερό.
Απομακρύνετε τα ορατά υπολείμματα με μια βούρτσα με μαλακές
τρίχες (για παράδειγμα, οδοντόβουρτσα με νάιλον τρίχες).
τουλάχιστον 2 min.
τυχόν υπολείμματα. Εάν χρειάζεται, επαναλάβετε τη διαδικασία.
43
Ελληνικά
Page 44

2. Ρυθμίστε την αυτόματη συσκευή πλύσης να λειτουργήσει με τις
παραμέτρους που προσδιορίζονται στον Πίν. 3 και επιτρέψτε στην αυτόματη
συσκευή πλύσης να ολοκληρώσει τον κύκλο πλύσης.
Πίνακας 3. Παράμετροι καθαρισμού αυτόματης συσκευής πλύσης
Επεξεργασία
Ενζυμική
πλύση
Πλύση 02:00 ≥60 °C
Έκπλυση 02:00 ≥60 °C
Στέγνωμα 15:00 ≥82 °C
Επιθεώρηση Δ/Ε Δ/Ε Επιθεωρήστε οπτικά κάθε προϊόν
Χρόνος
(min)
04:00 ≥60 °C
Θερμοκρα-
σία Καθαριστική ουσία
(≥140 °F)
(≥140 °F)
(≥140 °F)
(≥180 °F)
Steris Prolystica™ Ultra Concentrate
Enzymatic Cleaner αραιωμένο ως
1,0 mL/1 L (ή 0,125 ουγγιές/1 γαλόνι).
Steris Prolystica™ Ultra Concentrate
Neutral Detergent αραιωμένο ως
1,0 mL/1 L (ή 0,125 ουγγιές/1 γαλόνι).
Δ/Ε
Δ/Ε
για τυχόν υπολείμματα ή υγρασία.
Εάν παραμένουν υπολείμματα, επαναλάβετε τη διαδικασία. Εάν χρειάζεται, στεγνώστε το προϊόν με φιλτραρισμένο, συμπιεσμένο αέρα ή με
πανί που δεν αφήνει χνούδι.
5.2 Αποστείρωση με ατμό και επαναποστείρωση
• Χρησιμοποιήστε κάποιο σύνηθες υλικό συσκευασίας. Βεβαιωθείτε ότι η
συσκευασία είναι αρκετά μεγάλη ώστε να χωράει το προϊόν χωρίς να
ασκείται πίεση στα σημεία σφράγισης. Κατά την επικύρωση των διαδικασιών
αποστείρωσης, η Medtronic χρησιμοποίησε τον κατάλληλο δίσκο
παρελκομένων για κάθε προϊόν.
• Η Medtronic επικύρωσε κύκλους ατμού όπου τα προϊόντα ήταν τυλιγμένα με
υλικό περιτυλίγματος αποστείρωσης CSR (Central Supply Room: Κεντρικό
τμήμα εφοδιασμού). Ωστόσο, η διαδικασία αποστείρωσης με ατμό μπορεί να
ολοκληρωθεί όταν τα προϊόντα είναι είτε χωρίς περιτύλιγμα είτε τυλιγμένα
με υλικά συμβατά με αποστείρωση με ατμό.
• Κατά την αποστείρωση πολλαπλών προϊόντων σε 1 κύκλο αυτόκαυστου, μην
υπερβαίνετε το μέγιστο φορτίο του αποστειρωτή.
• Πριν από τη χρήση, εξετάστε το προϊόν για ραγίσματα ή αλλοίωση. Μη
χρησιμοποιήσετε το προϊόν εάν σε οποιαδήποτε εξαρτήματα υπάρχουν
ενδείξεις ραγίσματος ή αλλοίωσης.
• Ορισμένες υγειονομικές αρχές εκτός των Η.Π.Α. συνιστούν παραμέτρους
κύκλου αποστείρωσης που ελαχιστοποιούν τον ενδεχόμενο κίνδυνο
μετάδοσης της νόσου Creutzfeldt-Jakob (CJD). Αυτή η σύσταση είναι
ιδιαίτερα σημαντική για χειρουργικά εργαλεία που θα μπορούσαν να έλθουν
σε επαφή με το κεντρικό νευρικό σύστημα.
Ελληνικά
44
Page 45

Πίνακας 4. Παράμετροι κύκλου αποστείρωσης
Προκατεργα-
Τύπος
κύκλου
σία κενού
(δυναμική
αφαίρεση
αέρα)
Προκατεργασία
κενού (δυνα-
μική αφαίρεση
αέρα)
Προκατεργασία κενού
(δυναμική αφαίρεση
αέρα) για CJD
a
Θερμοκρασία 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Χρόνος έκθε-
4 min 3 min 18 min
σης
Χρόνος στε-
γνώματος
a
Η Medtronic συνιστά την αποτέφρωση των προϊόντων που είχαν άμεση επαφή με ασθενείς
με πιθανολογούμενη ή επιβεβαιωμένη διάγνωση μεταδοτικής σπογγώδους
εγκεφαλοπάθειας (ΜΣΕ)/CJD. Στα NHS Estates HTM 2010 Parts 4 & 6: Appendix 2, Items
contaminated with TSE Agents και WHO Infection Control Guidelines for Transmissible
Spongiform Encephalopathies αναφέρεται ένας κύκλος απολύμανσης ΜΣΕ με χρήση
αυτόκαυστου ατμού σε θερμοκρασία 134 °C έως 137 °C (273 °F έως 279 °F) για έναν
μεμονωμένο κύκλο 18 min ή για πολλαπλούς κύκλους συνολικά 18 min (για παράδειγμα
έξι κύκλους 3 min).
b
Οι ελάχιστοι χρόνοι στεγνώματος επικυρώθηκαν με τη χρήση αποστειρωτών με
δυνατότητες στεγνώματος με αρνητική πίεση. Οι κύκλοι στεγνώματος που χρησιμοποιούν
ατμοσφαιρική πίεση περιβάλλοντος μπορεί να απαιτούν μεγαλύτερους χρόνους
στεγνώματος. Ανατρέξτε στις συστάσεις του κατασκευαστή του αποστειρωτή.
20 min 16 min 30 min
b
6 Οδηγίες χρήσης
Σημείωση: Οι λεπίδες φέρουν σήμανση με έναν αριθμό που αντιστοιχεί στο
τελευταίο ψηφίο του αριθμού μοντέλου. Για παράδειγμα, το μοντέλο 28603 είναι
επισημασμένο ως «3», το μοντέλο 28606B ως «6B». Κάθε λεπίδα φέρει έναν
μοναδικό αριθμό σειράς.
6.1 Προσάρτηση λεπίδας
1. Προσαρτήστε τις λεπίδες στο σύστημα διαστολέα σύροντας τη βάση της
λεπίδας μέσα στον βραχίονα του συστήματος διαστολέα.
2. Αφαιρέστε τις λεπίδες σύροντας τη βάση της λεπίδας έξω από τον βραχίονα
του συστήματος διαστολέα.
6.2 Αφαίρεση (harvest) αριστερής έσω μαστικής αρτηρίας (LIMA)
1. Τοποθετήστε το διαστολέα, με προσαρτημένες τις λεπίδες LIMA, στη
θωρακοτομή. Η μεγάλη λεπίδα LIMA με την οπή στο άκρο θα πρέπει να είναι
προσανατολισμένη προς την κεφαλή ως προς τη μικρότερη λεπίδα.
2. Στρέψτε το κομβίο διαστολέα για να ανοίξετε τον διαστολέα και να
διανοίξετε τη θωρακοτομή.
3. Εφαρμόστε ανοδική τάνυση στη μεγάλη λεπίδα LIMA στην οπή στο άκρο
της λεπίδας ώστε ο διαστολέας να αποκτήσει ανοδική κλίση. Η ενέργεια
αυτή παρέχει πρόσβαση στη LIMA και δίνει τη δυνατότητα αφαίρεσης
(harvesting).
Σημείωση: Ο διαστολέας έχει σχεδιασθεί για χρήση με το σύστημα
διαστολέα Rultract™ ώστε να εφαρμόζεται ανοδική τάνυση στη μεγάλη
λεπίδα LIMA. Μπορούν να χρησιμοποιηθούν άλλοι τρόποι ή μέθοδοι
εφαρμογής ανοδικής τάνυσης.
4. Αφού ολοκληρωθεί η αφαίρεση LIMA (harvest), απελευθερώστε την
ανοδική τάνυση από τη μεγάλη λεπίδα LIMA.
45
Ελληνικά
Page 46

5. Πατήστε το μοχλό απελευθέρωσης για να κλείσετε τον διαστολέα.
6. Αφαιρέστε τον διαστολέα από τη θωρακοτομή.
6.3 Γενική διαστολή θωρακοτομής
1. Προσαρτήστε τις λεπίδες θωρακοτομής στον διαστολέα.
2. Τοποθετήστε τον διαστολέα μέσα στη θωρακοτομή.
3. Στρέψτε το κομβίο διαστολέα για να ανοίξετε τον διαστολέα και να
διανοίξετε τη θωρακοτομή.
4. Μόλις ολοκληρωθεί η διαδικασία, πατήστε το μοχλό απελευθέρωσης για να
κλείσετε τον διαστολέα.
5. Αφαιρέστε τον διαστολέα από τη θωρακοτομή.
7 Αποποιητική δήλωση της εγγύησης (παγκόσμια)
ΠΑΡΟΤΙ ΤΟ ΠΡΟΪΟΝ ΕΧΕΙ ΣΧΕΔΙΑΣΤΕΙ, ΚΑΤΑΣΚΕΥΑΣΤΕΙ ΚΑΙ ΔΟΚΙΜΑΣΤΕΙ
ΠΡΙΝ ΑΠΟ ΤΗΝ ΠΩΛΗΣΗ ΥΠΟ ΠΡΟΣΕΚΤΙΚΑ ΕΛΕΓΧΟΜΕΝΕΣ ΣΥΝΘΗΚΕΣ,
ΤΟ ΠΡΟΪΟΝ ΜΠΟΡΕΙ ΝΑ ΑΠΟΤΥΧΕΙ ΣΤΗΝ ΕΚΤΕΛΕΣΗ ΤΗΣ
ΠΡΟΟΡΙΖΟΜΕΝΗΣ ΛΕΙΤΟΥΡΓΙΑΣ ΛΟΓΩ ΠΟΙΚΙΛΩΝ ΑΙΤΙΩΝ. Η MEDTRONIC
ΔΕΝ ΕΧΕΙ ΕΛΕΓΧΟ ΤΩΝ ΣΥΝΘΗΚΩΝ ΥΠΟ ΤΙΣ ΟΠΟΙΕΣ ΧΡΗΣΙΜΟΠΟΙΕΙΤΑΙ ΤΟ
ΠΑΡΟΝ ΠΡΟΪΟΝ. ΟΙ ΠΡΟΕΙΔΟΠΟΙΗΣΕΙΣ ΠΟΥ ΠΕΡΙΕΧΟΝΤΑΙ ΣΤΗ ΣΗΜΑΝΣΗ
ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΠΑΡΕΧΟΥΝ ΛΕΠΤΟΜΕΡΕΣΤΕΡΕΣ ΠΛΗΡΟΦΟΡΙΕΣ ΚΑΙ
ΘΕΩΡΟΥΝΤΑΙ ΑΝΑΠΟΣΠΑΣΤΟ ΤΜΗΜΑ ΤΗΣ ΠΑΡΟΥΣΑΣ ΑΠΟΠΟΙΗΤΙΚΗΣ
ΔΗΛΩΣΗΣ ΤΗΣ ΕΓΓΥΗΣΗΣ. ΣΥΝΕΠΩΣ, Η MEDTRONIC ΑΠΟΠΟΙΕΙΤΑΙ ΟΛΕΣ
ΤΙΣ ΕΓΓΥΗΣΕΙΣ, ΡΗΤΕΣ ΚΑΙ ΣΙΩΠΗΡΕΣ, ΣΕ ΣΧΕΣΗ ΜΕ ΤΟ ΠΡΟΪΟΝ,
ΠΕΡΙΛΑΜΒΑΝΟΜΕΝΗΣ, ΕΝΔΕΙΚΤΙΚΑ, ΟΠΟΙΑΣΔΗΠΟΤΕ ΣΙΩΠΗΡΗΣ
ΕΓΓΥΗΣΗΣ ΠΕΡΙ ΕΜΠΟΡΕΥΣΙΜΟΤΗΤΑΣ Ή ΚΑΤΑΛΛΗΛΟΤΗΤΑΣ ΓΙΑ
ΣΥΓΚΕΚΡΙΜΕΝΟ ΣΚΟΠΟ. H MEDTRONIC ΔΕΝ ΘΑ ΕΙΝΑΙ ΥΠΕΥΘΥΝΗ
ΑΠΕΝΑΝΤΙ ΣΕ ΟΠΟΙΟΔΗΠΟΤΕ ΦΥΣΙΚΟ Ή ΝΟΜΙΚΟ ΠΡΟΣΩΠΟ ΓΙΑ
ΟΠΟΙΕΣΔΗΠΟΤΕ ΙΑΤΡΙΚΕΣ ΔΑΠΑΝΕΣ Ή ΟΠΟΙΕΣΔΗΠΟΤΕ ΑΜΕΣΕΣ,
ΘΕΤΙΚΕΣ Ή ΑΠΟΘΕΤΙΚΕΣ ΖΗΜΙΕΣ ΠΡΟΚΑΛΟΥΜΕΝΕΣ ΑΠΟ ΟΠΟΙΑΔΗΠΟΤΕ
ΧΡΗΣΗ, ΕΛΑΤΤΩΜΑ, ΑΣΤΟΧΙΑ Ή ΔΥΣΛΕΙΤΟΥΡΓΙΑ ΤΟΥ ΠΡΟΪΟΝΤΟΣ, ΕΙΤΕ Η
ΑΞΙΩΣΗ ΒΑΣΙΖΕΤΑΙ ΣΕ ΕΓΓΥΗΣΗ, ΣΥΜΒΑΣΗ, ΑΔΙΚΟΠΡΑΞΙΑ ΕΙΤΕ ΣΕ
ΟΤΙΔΗΠΟΤΕ ΑΛΛΟ. ΕΚΤΟΣ ΑΝ ΕΧΕΙ ΣΥΜΦΩΝΗΘΕΙ ΔΙΑΦΟΡΕΤΙΚΑ
ΕΓΓΡΑΦΩΣ ΑΠΟ ΕΞΟΥΣΙΟΔΟΤΗΜΕΝΟ ΠΡΟΣΩΠΙΚΟ ΤΗΣ MEDTRONIC,
ΚΑΝΕΝΑ ΠΡΟΣΩΠΟ ΔΕΝ ΕΧΕΙ ΤΗ ΔΙΚΑΙΟΔΟΣΙΑ ΝΑ ΔΕΣΜΕΥΣΕΙ ΤΗ
MEDTRONIC ΣΕ ΟΠΟΙΑΔΗΠΟΤΕ ΔΗΛΩΣΗ Ή ΕΓΓΥΗΣΗ ΣΕ ΣΧΕΣΗ ΜΕ ΤΟ
ΠΡΟΪΟΝ.
Οι εξαιρέσεις και οι περιορισμοί που ορίζονται ανωτέρω, δεν έχουν ως σκοπό και
δεν θα πρέπει να ερμηνεύονται κατά τέτοιο τρόπο, ώστε να αντιβαίνουν στις
υποχρεωτικές διατάξεις της ισχύουσας νομοθεσίας. Εάν οποιοδήποτε τμήμα ή
όρος της παρούσας Αποποιητικής Δήλωσης της Εγγύησης κριθεί από
οποιοδήποτε δικαστήριο αρμόδιας δικαιοδοσίας παράνομο(ς), μη εφαρμόσιμο(ς)
ή συγκρουόμενο(ς) με την ισχύουσα νομοθεσία, η εγκυρότητα των υπολοίπων
τμημάτων της παρούσας Αποποιητικής Δήλωσης της Εγγύησης δεν θα
επηρεαστεί, και όλα τα δικαιώματα και οι υποχρεώσεις θα ερμηνεύονται και θα
εφαρμόζονται ως εάν η παρούσα Αποποιητική Δήλωση της Εγγύησης να μην
περιείχε το συγκεκριμένο τμήμα ή όρο που κρίθηκε άκυρο(ς).
Ελληνικά
46
Page 47

1 Descripción del producto
Modelo Descripción
28610 Sistema de retracción para cirugía cardíaca mínimamente
28611 Porta-separador
28601 Valvas para AMII, estándares
28602 Valvas para AMII, profundas
28603 Valvas para toracotomía largas, estándares
28604 Valvas para toracotomía largas, profundas
28604B Valva inferior larga con brazo extendido, estándar
28605 Valvas para toracotomía cortas, estándares
28606 Valvas para toracotomía cortas, profundas
28606B Valva inferior corta con brazo extendido, estándar
Nota: El Modelo 28601 es la valva que se usa más a menudo para la extracción de
la arteria mamaria interna izquierda (AMII). El Modelo 28605 es la valva que se usa
más a menudo para la retracción en una toracotomía general. Todas las demás
valvas se han diseñado para adaptarse a la anatomía de distintos pacientes.
Nota: Los Modelos 28604B y 28606B son valvas inferiores diseñadas para mujeres
y pacientes obesos. Estas valvas inferiores deben utilizarse con las valvas
superiores (Modelos 28604 y 28606).
invasiva (MICS)
2 Indicaciones de uso
El sistema de retracción para cirugía cardíaca mínimamente invasiva (MICS, por su
sigla en inglés) ThoraTrak está indicado para proporcionar acceso quirúrgico en
intervenciones cardiotorácicas mínimamente invasivas, incluidos los
procedimientos mínimamente invasivos de injerto de bypass de arterias coronarias
y de extracción de la AMII, mediante la retracción del tejido blando y óseo.
3 Medidas preventivas
Las técnicas y procedimientos quirúrgicos adecuados son responsabilidad del
profesional médico. El cirujano debe evaluar la conveniencia de cualquier
procedimiento según su propia formación y experiencia médicas.
4 Efectos adversos
No se conocen.
5 Procesamiento y reprocesamiento
Medtronic ha validado las siguientes instrucciones para preparar este dispositivo
médico para su reutilización. Es responsabilidad de la persona encargada del
procesamiento garantizar que se obtengan los resultados deseados del
procesamiento realizado, utilizando el equipo, los materiales y el personal de la
instalación de procesamiento. El procesamiento requiere validación y una
supervisión sistemática. Igualmente, cualquier desviación de las siguientes
instrucciones por parte de la persona encargada del procedimiento se debe
evaluar adecuadamente en lo relativo a la eficacia y las posibles consecuencias
adversas. La limpieza puede realizarse de forma manual o de forma automática de
acuerdo con estas instrucciones de uso o conforme a un método validado
equivalente.
47
Español
Page 48

5.1 Limpieza
Advertencia: Limpie cuidadosamente el dispositivo para eliminar la suciedad
antes de proceder con la esterilización.
Advertencia: No utilice productos de limpieza basados en disolventes (por
ejemplo, acetona o tolueno).
• No deje que los dispositivos contaminados se sequen antes de llevar a cabo
cualquier procedimiento de limpieza.
• Reprocese los dispositivos en las 2 horas siguientes a su uso. Si se va a retrasar
el traslado al área de procesamiento, ponga el dispositivo en un recipiente
cubierto que contenga un detergente enzimático para evitar que se seque.
• Si el dispositivo contiene numerosos componentes, desmóntelos por completo
antes de llevar a cabo el proceso de limpieza siguiendo estas instrucciones de
uso.
• Compruebe que el dispositivo no presente desgaste ni deterioro antes de
utilizarlo. No utilice el dispositivo si alguno de los componentes muestra
señales de desgaste o deterioro.
• La desinfección térmica no es necesaria puesto que los dispositivos se
someten a esterilización terminal.
5.1.1 Limpieza manual
Medtronic ha establecido el siguiente procedimiento de limpieza manual descrito
en la Tabla 1. Estos pasos deben realizarse en un plazo máximo de 2 horas después
de la utilización del dispositivo.
Nota: Si el dispositivo tiene piezas móviles, asegúrese de que se han limpiado
meticulosamente todas las superficies.
Tabla 1. Instrucciones para la limpieza manual
Paso Proceso Temperatura Instrucciones de limpieza
1 Enjuague > 27 °C (> 81 °F) Elimine la suciedad visible con agua
2 Sumersión > 28 °C (> 82 °F) Sumerja completamente el dispositivo
3 Limpieza
ultrasó-
4 Enjuague > 27 °C (> 81 °F) Enjuague el dispositivo con agua
5 Secado N/A (N/D) Séquelos con un paño seco y sin pelu-
6 Inspec-
> 27 °C (> 81 °F) Sumerja completamente el dispositivo
nica
N/A (N/D) Examine visualmente cada dispositivo
ción
corriente durante 1 min. Utilice un cepillo de cerdas suaves (por ejemplo, un
cepillo de dientes de nailon) para limpiar el dispositivo meticulosamente.
durante al menos 5 min en 15,6 mL/1 L
(o 2 onzas/1 galón) de un detergente
enzimático (por ejemplo, ENZOL™) y
agua. Elimine la suciedad visible con
un cepillo de cerdas suaves.
en un limpiador ultrasónico (por ejemplo, Bransonic™) en 7,8 mL/1 L (o
1 onza/1 galón) de un detergente enzimático (por ejemplo, ENZOL) y agua.
Sométalos al ultrasonido durante
10 min.
corriente durante 1 min.
sas.
para detectar cualquier resto de sucie-
48Español
Page 49

Tabla 1. Instrucciones para la limpieza manual (continuación)
Paso Proceso Temperatura Instrucciones de limpieza
5.1.2 Limpieza automática
Medtronic ha establecido el siguiente procedimiento de limpieza automática. Los
pasos descritos en la Tabla 2 deben realizarse en un plazo máximo de 2 horas
después de la utilización del dispositivo.
Nota: Si el dispositivo o componente tiene piezas móviles, asegúrese de que se
han limpiado meticulosamente todas las superficies.
Tabla 2. Instrucciones para el pretratamiento
Paso Proceso
1 Enjuague > 25 °C (> 77 °F) Elimine la suciedad visible con agua
2 Sumersión > 25 °C (> 77 °F) Sumerja completamente el disposi-
3 Enjuague > 25 °C (> 77 °F) Enjuague el dispositivo durante al
4 Inspección N/A (N/D) Examine visualmente el dispositivo
Medtronic utilizó la familia de detergentes Prolystica™ de acuerdo con las
recomendaciones del fabricante para validar el proceso de limpieza automática. Es
responsabilidad de la persona que lleve a cabo el procedimiento asegurarse de que
éste se lleve a cabo de acuerdo con un método validado. Cualquier desviación
respecto de estas recomendaciones por parte de la persona encargada del
procedimiento se debe evaluar.
1. Ponga el dispositivo en un lavador automático (por ejemplo, Steris Reliance™
Genfore™ Washer/Disinfector).
Nota: Evite el contacto entre dispositivos mientras carga el lavador.
2. Configure el lavador automático con los parámetros indicados en la Tabla 3 y
deje que complete el ciclo de lavado.
Tabla 3. Parámetros de limpieza del lavador automático
Tratamiento
Lavado enzi-
mático
Lavado 02:00 ≥ 60 °C
Temperatura del
agua Instrucciones de limpieza
Tiempo
(min) Temperatura Producto de limpieza
04:00 ≥ 60 °C
(≥ 140 °F)
(≥ 140 °F)
dad o humedad. Si continúa habiendo
suciedad, repita el proceso.
corriente.
tivo durante al menos 1 min en
7,8 mL/1 L (o 1 onza/1 galón) de un
detergente enzimático (por ejemplo, ENZOL) y agua. Elimine la
suciedad visible con un cepillo de
cerdas suaves (por ejemplo, un
cepillo de dientes de nailon).
menos 2 min.
para detectar cualquier resto de
suciedad. En caso necesario, repita
el proceso.
Steris Prolystica™ Ultra Concentrate
Enzymatic Cleaner diluido a
1,0 mL/1 L (o 0,125 onzas/1 galón).
Steris Prolystica™ Ultra Concentrate
Neutral Detergent diluido a 1,0 mL/1 L
(o 0,125 onzas/1 galón).
49 Español
Page 50

Tabla 3. Parámetros de limpieza del lavador automático (continuación)
Tiempo
Tratamiento
Enjuagado 02:00 ≥ 60 °C
(min) Temperatura Producto de limpieza
N/A (N/D)
(≥ 140 °F)
Secado 15:00 ≥ 82 °C
N/A (N/D)
(≥ 180 °F)
Inspección N/A
(N/D)
N/A (N/D) Examine visualmente cada disposi-
tivo para detectar cualquier resto de
suciedad o humedad. Si continúa
habiendo suciedad, repita el proceso.
En caso necesario, seque el dispositivo con aire comprimido y filtrado o
con un paño sin pelusas.
5.2 Esterilización y reesterilización con vapor
• Utilice material de empaquetado estándar. Asegúrese de que el paquete es lo
suficientemente grande como para contener el dispositivo sin que los cierres
queden tensos. Para validar los procesos de esterilización, Medtronic utilizó la
bandeja de accesorios adecuada para cada dispositivo.
• Medtronic validó los ciclos de vapor con los dispositivos empaquetados con
material de empaquetado CSR (Central Supply Room). No obstante, el
proceso de esterilización con vapor puede realizarse con dispositivos no
empaquetados o con dispositivos empaquetados en materiales para
esterilización con vapor compatibles.
• Cuando esterilice varios dispositivos en un ciclo de autoclave, asegúrese de no
exceder la carga máxima del esterilizador.
• Compruebe que el dispositivo no presente desgaste ni deterioro antes de
utilizarlo. No utilice el dispositivo si los componentes muestran señales de
desgaste o deterioro.
• Algunas autoridades sanitarias no estadounidenses recomiendan parámetros
para el ciclo de esterilización que reduzcan al mínimo el posible riesgo de
transmisión de la enfermedad de Creutzfeldt-Jakob. Esta recomendación es
especialmente importante para los instrumentos quirúrgicos que pudieran
entrar en contacto con el sistema nervioso central.
Tabla 4. Parámetros del ciclo de esterilización
Tipo de ciclo
Prevacío (eli-
minación diná-
mica de aire)
Prevacío (elimi-
nación dinámica
de aire)
Temperatura 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Tiempo de
4 min 3 min 18 min
exposición
Tiempo de
b
secado
a
Medtronic recomienda incinerar los dispositivos que hayan estado en contacto directo con
pacientes con un diagnóstico sospechoso o confirmado de encefalopatía espongiforme
transmisible (EET)/enfermedad de Creutzfeldt-Jakob. Los documentos NHS Estates HTM
2010 Parts 4 & 6: Appendix 2, Items contaminated with TSE Agents (Memorando técnico de
salud de 2010 del NSH Estates, Partes 4 y 6: Apéndice 2, Elementos contaminados con
agentes de EET) y WHO Infection Control Guidelines for Transmissible Spongiform
Encephalopathies (Directrices de control de infecciones de la OMS para encefalopatías
20 min 16 min 30 min
Prevacío (eliminación
dinámica de aire) para
la enfermedad de
Creutzfeldt-Jakob
a
Español
50
Page 51

espongiformes transmisibles) hacen referencia a un ciclo de descontaminación para EET en
un autoclave de vapor a una temperatura de 134 °C a 137 °C (273 °F a 279 °F) durante un solo
ciclo de 18 min o varios ciclos que sumen un tiempo total de 18 min (por ejemplo, seis ciclos
de 3 min).
b
Los tiempos de secado mínimos se han validado mediante esterilizadores con función de
secado al vacío. Los ciclos de secado que usan presión atmosférica ambiente pueden
necesitar tiempos de secado más largos. Consulte las recomendaciones del fabricante del
esterilizador.
6 Instrucciones de uso
Nota: Las valvas están marcadas con un número que corresponde al último dígito
del número de modelo. Por ejemplo, las hojas del Modelo 28603 están marcadas
con “3”, mientras que las del Modelo 28606B están marcadas con “6B”. Cada valva
está marcada con un número de serie único.
6.1 Acoplamiento de las valvas
1. Acople las valvas al porta-separador deslizando el soporte de la valva en el
brazo del porta-separador.
2. Retire las valvas deslizando el soporte de la valva para extraerlo del brazo del
porta-separador.
6.2 Extracción de la AMII
1. Coloque el separador, con las valvas para AMII acopladas, en la toracotomía.
La valva para AMII larga con un orificio en el extremo debe orientarse con la
parte anterior hacia la valva más corta.
2. Gire el mando del separador para abrir el separador y ampliar la toracotomía.
3. Aplique presión ascendente sobre el orificio en el extremo de la valva para
AMII larga para inclinar el separador hacia arriba. Esta acción proporciona
acceso a la AMII y posibilita la extracción.
Nota: El separador se ha diseñado para funcionar con el sistema separador
Rultract™, que aplica la presión ascendente en la valva para AMII grande.
Pueden utilizarse otros medios o métodos para aplicar presión ascendente.
4. Una vez completada la extracción de la AMII, libere la presión ascendente en
la valva para AMII grande.
5. Presione la palanca de liberación para cerrar el separador.
6. Extraiga el separador de la toracotomía.
6.3 Retracción en una toracotomía general
1. Acople las valvas para toracotomía al separador.
2. Coloque el separador en la toracotomía.
3. Gire el mando del separador para abrir el separador y ampliar la toracotomía.
4. Una vez finalizado el procedimiento, presione la palanca de liberación para
cerrar el separador.
5. Extraiga el separador de la toracotomía.
7 Renuncia de responsabilidad (global)
AUNQUE EL PRODUCTO HA SIDO DISEÑADO, FABRICADO Y PROBADO EN
CONDICIONES CUIDADOSAMENTE CONTROLADAS ANTES DE PONERLO
A LA VENTA, EL PRODUCTO PUEDE NO CUMPLIR SUS FUNCIONES
SATISFACTORIAMENTE POR VARIAS RAZONES. MEDTRONIC NO TIENE
CONTROL SOBRE LAS CONDICIONES BAJO LAS QUE SE UTILIZA ESTE
51
Español
Page 52

PRODUCTO. LAS ADVERTENCIAS QUE CONTIENE LA DOCUMENTACIÓN
DEL PRODUCTO PROPORCIONAN INFORMACIÓN MÁS DETALLADA Y SE
CONSIDERAN COMO PARTE INTEGRANTE DE ESTA RENUNCIA DE
RESPONSABILIDAD. POR TANTO, MEDTRONIC NIEGA TODA GARANTÍA,
TANTO EXPRESA COMO IMPLÍCITA, CON RESPECTO AL PRODUCTO,
INCLUIDA ENTRE OTRAS TODA GARANTÍA IMPLÍCITA DE
COMERCIABILIDAD O IDONEIDAD PARA UN FIN PARTICULAR. MEDTRONIC
NO SERÁ RESPONSABLE ANTE NINGUNA PERSONA O ENTIDAD POR LOS
GASTOS MÉDICOS O DAÑOS DIRECTOS, INDIRECTOS O RESULTANTES
CAUSADOS POR EL USO, DEFECTO, FALLO O MAL FUNCIONAMIENTO DEL
PRODUCTO AUN CUANDO LA RECLAMACIÓN SE BASE EN UNA
GARANTÍA, CONTRATO, RESPONSABILIDAD EXTRACONTRACTUAL U
OTRO FUNDAMENTO LEGAL. SALVO QUE PERSONAL AUTORIZADO DE
MEDTRONIC HAYA ACORDADO LO CONTRARIO POR ESCRITO, NINGUNA
PERSONA TIENE AUTORIDAD PARA VINCULAR A MEDTRONIC CON
NINGUNA DECLARACIÓN O GARANTÍA EN RELACIÓN CON EL PRODUCTO.
Las exclusiones y limitaciones detalladas anteriormente no pretenden contravenir
las disposiciones obligatorias establecidas por la legislación vigente ni deben
interpretarse de dicha forma. En el supuesto de que cualquier parte o término de la
presente Renuncia de responsabilidad fuera declarado por cualquier tribunal
competente como ilegal, inaplicable o contrario a la ley, ello no afectará a la validez
del resto de la Renuncia de responsabilidad, interpretándose y aplicándose
cuantos derechos y obligaciones se contienen en la misma como si la presente
Renuncia de responsabilidad no contuviera la parte o término considerado no
válido.
Español
52
Page 53

1 Toote kirjeldus
Mudel Kirjeldus
28610 Minimaalselt invasiivse südamekirurgia retraktorsüsteem
28611 Retraktsiooniraam
28601 Vasaku arteria thoracica interna (LIMA) labad, standard-
28602 Vasaku arteria thoracica interna (LIMA) labad, sügavad
28603 Pikad torakotoomia labad, standardsed
28604 Pikad torakotoomia labad, sügavad
28604B Pikk alumine pikendatud alusega laba, standardne
28605 Lühikesed torakotoomia labad, standardsed
28606 Lühikesed torakotoomia labad, sügavad
28606B Lühike alumine pikendatud alusega laba, standardne
Märkus. Laba mudelit 28601 kasutatakse kõige sagedamini vasaku arteria
thoracica interna (LIMA) lõikuse korral. Laba mudelit 28605 kasutatakse kõige
sagedamini üldiseks haava laiendamiseks torakotoomia korral. Kõik teised labad
on kasutatavad mitmesuguse anatoomiaga patsientidel.
Märkus. Mudelid 28604B ja 28606B on naistele ning rasvunud patsientidele
mõeldud alumised labad. Kasutage neid labasid koos ülemiste labadega (mudelid
28604 ja 28606).
sed
2 Kasutusnäidustused
Minimaalselt invasiivse südamekirurgia retraktorsüsteem ThoraTrak on mõeldud
kirurgilise juurdepääsu tagamiseks minimaalselt invasiivsete südame- ja
rindkerekirurgia protseduuride korral, sh minimaalselt invasiivne koronaararteri
šunteerimine ja vasaku arteria thoracica interna lõikus, tõmmates pehmet ning
luulist kude tagasi.
3 Ettevaatusabinõud
Õigete kirurgiliste protseduuride ja tehnika järgimine on meditsiinitöötaja
vastutusel. Kirurgid peavad mistahes protseduuri sobivust ja õigustatust hindama
oma meditsiinialase väljaõppe ning kogemuste põhjal.
4 Kõrvaltoimed
Teadaolevad kõrvaltoimed puuduvad.
5 Töötlemine ja korduv töötlemine
Ettevõte Medtronic on kinnitanud järgmised juhised selle meditsiiniseadme
korduvaks kasutamiseks ettevalmistamiseks. Töötleja vastutus on tagada, et
tegelik töötlus, mida tehakse töötlusasutuse seadmete, materjalide ja personali
abil, annab soovitud tulemuse. Töötlemine nõuab kinnitust ja rutiinset jälgimist.
Samuti tuleks kõiki töötleja kõrvalekaldeid järgmistest juhistest põhjalikult
efektiivsuse ja võimalike ebasoodsate tagajärgede suhtes uurida. Puhastada võib
käsitsi või vastavalt nendele juhistele automaatselt või võrdväärse kinnitatud
meetodiga.
5.1 Puhastamine
Hoiatus! Puhastage seadet enne steriliseerimist põhjalikult, et eemaldada mustus.
53
Eesti
Page 54

Hoiatus! Ärge kasutage lahustil põhinevaid puhastusvahendeid (nt atsetoon või
tolueen).
• Ärge laske saastunud seadmetel enne puhastamist kuivada.
• Töödelge seadmeid 2 tunni jooksul pärast kasutamist. Kui transport
töötlemisalasse viibib, asetage seade kuivamise vältimiseks suletud
mahutisse, mis sisaldab ensümaatilist puhastusvahendit.
• Kui seade koosneb mitmest osast, võtke need enne kasutusjuhiste järgi
puhastamist täielikult lahti.
• Kontrollige seadet enne kasutamist mõranemise ja lagunemise suhtes. Ärge
kasutage ühtegi mõranenud või lagunenud osadega seadet.
• Termodesinfitseerimine ei ole vajalik, kuna seadmed on lõplikult steriliseeritud.
5.1.1 Käsitsi puhastamine
Ettevõte Medtronic on kehtestanud järgmise käsitsi puhastamise protseduuri, vt
tabel 1. Need etapid tuleb teostada maksimaalselt 2 tunni jooksul pärast
kasutamist.
Märkus. Kui seadmel on liikuvad osad, veenduge, et kõik pinnad on põhjalikult
puhastatud.
Tabel 1. Juhised käsitsi puhastamiseks
Etapp Toiming Temperatuur Puhastamise juhised
1 Loputa-
2 Sukelda-
3 Ultraheli-
puhastus
4 Loputa-
5 Kuivata-
6 Kontrolli-
5.1.2 Automatiseeritud puhastamine
Ettevõte Medtronic on kehtestanud järgmise automatiseeritud puhastamise
protseduuri. Teostage tabel 2 toodud etapid maksimaalselt 2 tunni jooksul pärast
kasutamist.
> 27 °C (> 81 °F) Eemaldage suurem mustus voolava
mine
> 28 °C (> 82 °F) Sukeldage seade täielikult vähemalt
mine
> 27 °C (> 81 °F) Sukeldage seade täielikult ultrahelipu-
> 27 °C (> 81 °F)
mine
Ei rakendu
mine
Ei rakendu Kontrollige visuaalselt kõiki seadmeid
mine
vee all 1 min jooksul. Puhastage seade
põhjalikult pehme harjaga (nt nailonharjastega hambahari).
5 min puhastuslahusesse, mis koosneb veega lahjendatud ensümaatilisest puhastusvahendist (nt ENZOL™)
kontsentratsiooniga 15,6 mL/1 L (või 2
untsi/1 galloni kohta). Eemaldage nähtav mustus pehme harjaga.
hastisse (nt Bransonic™), kuhu on lisatud 7,8 mL/1 L (või 1 unts/1 galloni
kohta) ensümaatilist puhastusvahendit
(nt ENZOL) ja vett. Töödelge ultraheliga 10 min.
Loputage seadet voolava vee all 1 min.
Kuivatage puhta kiuvaba lapiga.
allesjäänud mustuse või niiskuse suhtes. Kui mustus püsib, korrake protsessi.
Eesti
54
Page 55

Märkus. Kui seadmel või komponendil on liikuvad osad, veenduge, et kõik pinnad
on põhjalikult puhastatud.
Tabel 2. Töötlemiseelsed juhised
Etapp Toiming Veetemperatuur Puhastamise juhised
1 Loputa-
mine
2 Sukelda-
mine
3 Loputa-
mine
4 Kontrolli-
mine
Ettevõte Medtronic kasutas automaatpesu protsessi kinnitamiseks Prolystica™
tooterühma puhastusvahendeid vastavalt tootja soovitustele. Töötleja peab
tagama, et töötlus toimuks vastavalt kinnitatud meetodile. Kõiki töötleja
kõrvalekaldeid nendest soovitustest tuleks uurida.
1. Asetage seade automaatpesumasinasse (nt Steris Reliance™ Genfore™
pesumasin/desinfitseerija).
Märkus. Vältige pesumasina täitmisel seadmete kokkupuudet.
2. Seadistage automaatpesumasin tabel 3 toodud parameetritele ja laske
automaatpesumasinal pesutsükkel läbida.
Tabel 3. Automaatpesumasina parameetrid
Töötlus
Ensümaatiline
pesu
Pesu 02:00 ≥ 60 °C
Loputus 02:00 ≥ 60 °C
Kuivatus 15:00 ≥ 82 °C
Kontrollimine Ei
> 25 °C (> 77 °F) Eemaldage suurem mustus voolava
> 25 °C (> 77 °F) Sukeldage seade täielikult vähe-
> 25 °C (> 77 °F) Loputage seadet vähemalt 2 min.
Ei rakendu Kontrollige visuaalselt seadet alles-
Aeg
(min) Temperatuur Puhastusvahend
04:00 ≥ 60 °C
(≥ 140 °F)
(≥ 140 °F)
(≥ 140 °F)
(≥ 180 °F)
Ei rakendu Kontrollige visuaalselt kõiki seadmeid
rakendu
kraaniveega.
malt 1 min puhastuslahusesse, mis
koosneb veega lahjendatud ensümaatilisest puhastusvahendist (nt
ENZOL) kontsentratsiooniga
7,8 mL/1 L (või 1 unts/1 galloni
kohta). Eemaldage nähtav mustus
pehme harjaga (nt nailonharjastega
hambahari).
jäänud mustuse suhtes. Vajadusel
korrake protsessi.
Ensümaatilise puhastusvahendi
Steris Prolystica™ Ultra Concentrate
Enzymatic Cleaner lahus kontsentratsiooniga 1,0 mL/1 L (või 0,125 untsi/1
galloni kohta).
Ensümaatilise puhastusvahendi
Steris Prolystica™ Ultra Concentrate
Neutral Detergent lahus kontsentratsiooniga 1,0 mL/1 L (või 0,125 untsi/1
galloni kohta).
Ei rakendu
Ei rakendu
allesjäänud mustuse või niiskuse
suhtes. Kui mustus püsib, korrake
protsessi. Kuivatage seade vajaduse
55 Eesti
Page 56

Tabel 3. Automaatpesumasina parameetrid (jätkub)
Aeg
Töötlus
(min) Temperatuur Puhastusvahend
korral filtreeritud suruõhuga või kiuvaba lapiga.
5.2 Auruga steriliseerimine/resteriliseerimine
• Kasutage standardset pakkematerjali. Veenduge, et seade mahub pakendisse
tihendeid rõhumata. Ettevõte Medtronic kasutas steriliseerimisprotsesside
kinnitamisel iga seadme puhul sobivat lisatarvikute alust.
• Ettevõte Medtronic kinnitas auruga steriliseerimise tsüklid, kui seadmed olid
pakitud keskse steriliseerimisosakonna pakendisse. Siiski võib auruga
steriliseerida ka siis, kui seadmed on pakendamata või pakitud auruga
steriliseerimiseks kõlbliku materjaliga.
• Kui te steriliseerite 1 autoklaavitsükliga mitut seadet, ärge ületage sterilisaatori
maksimaalset laadungit.
• Kontrollige seadet enne kasutamist mõranemise ja lagunemise suhtes. Ärge
kasutage mõranenud või lagunenud osadega seadet.
• Teatavad USA-välised tervishoiuasutused soovitavad kasutada selliseid
steriliseerimistsükli parameetreid, mis minimeerivad Creutzfeldti-Jakobi tõve
(CJD) edasikandumise potentsiaalset riski. See soovitus on eriti oluline
kirurgiliste instrumentide puhul, mis võivad kokku puutuda
kesknärvisüsteemiga.
Tabel 4. Steriliseerimistsükli parameetrid
Tsükli tüüp
Temperatuur 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Kokkupuute-
aeg
Kuivatusaeg
a
Ettevõte Medtronic soovitab tuhastada seadmed, mis on puutunud vahetult kokku
patsientidega, kellel on transmissiivse spongiformse entsefalopaatia (TSE)/CJD diagnoos või
selle kahtlus. NHS Estates HTM 2010 Parts 4 & 6: Appendix 2, Items contaminated with TSE
Agents ja WHO Infection Control Guidelines for Transmissible Spongiform Encephalopathies
sisaldavad viidet TSE dekontaminatsioonitsüklile, milles kasutatakse aurautoklaavi
temperatuuril 134 °C kuni 137 °C (273 °F kuni 279 °F) ühe 18 min tsükli jooksul või mitme tsükli
jooksul, mille kogupikkus on 18 min (nt kuus 3 min tsüklit).
b
Minimaalsete kuivatamisaegade kinnitamiseks kasutati vaakumkuivatuse võimalusega
sterilisaatoreid. Atmosfäärirõhuga kuivatamistsüklite puhul võib kuivatamisaeg kujuneda
pikemaks. Vt sterilisaatori tootja soovitusi.
Eelvaakum
(dünaamiline
õhu eemalda-
mine)
Eelvaakum
(dünaamiline
õhu eemalda-
mine)
4 min 3 min 18 min
b
20 min 16 min 30 min
Eelvaakum (dünaami-
line õhu eemaldamine)
CJD puhul
a
6 Kasutusjuhend
Märkus. Labad on tähistatud numbritega, mis vastavad mudeli numbri viimasele
numbrile. Nt 28603 on tähisega „3“; 28606B on tähisega „6B“. Iga laba on tähistatud
unikaalse seerianumbriga.
Eesti
56
Page 57

6.1 Laba kinnitamine
1. Kinnitage labad retraktsiooniraami külge, lükates laba aluse
retraktsiooniraami õlas olevasse pesasse.
2. Eemaldage labad retraktsiooniraami küljest, tõmmates laba aluse
retraktsiooniraami õlas olevast pesast välja.
6.2 Vasaku arteria thoracica interna (LIMA) lõikus
1. Asetage retraktor (mille külge on kinnitatud vasaku arteria thoracica interna
labad) torakotoomia haavale. Suur vasaku arteria thoracica interna laba, mille
ühes otsas on auk, tuleb paigutada väiksemast labast kraniaalsemale.
2. Keerake retraktori nuppu, et retraktor avada, ja laiendage torakotoomia haava.
3. Avaldage suurele vasaku arteria thoracica interna labale selle otsmise augu
juures ülespidist survet, et kallutada retraktor ülespoole. See toiming
võimaldab juurdepääsu vasakule arteria thoracica internale ja selle lõikust.
Märkus. Retraktor ühildub retraktorsüsteemiga Rultract™, et avaldada
suurele vasaku arteria thoracica interna labale ülespidist survet. Ülespidist
survet võib ka teiste võtete või meetoditega avaldada.
4. Kui vasaku arteria thoracica interna lõikus on lõpetatud, vabastage suur
vasaku arteria thoracica interna laba ülespidise surve alt.
5. Vajutage vabastushoovale, et retraktor sulgeda.
6. Eemaldage retraktor torakotoomia haavast.
6.3 Üldine haava laiendamine torakotoomia korral
1. Kinnitage torakotoomia labad retraktori külge.
2. Asetage retraktor torakotoomia haavale.
3. Keerake retraktori nuppu, et retraktor avada, ja laiendage torakotoomia haava.
4. Pärast protseduuri lõpetamist vajutage vabastushoovale, et retraktor sulgeda.
5. Eemaldage retraktor torakotoomia haavast.
7 Garantiist lahtiütlemine (kõikides riikides)
KUIGI TOODE ON VÄLJA TÖÖTATUD, TOODETUD JA ENNE MÜÜKI
TESTITUD HOOLIKALT KONTROLLITUD TINGIMUSTES, VÕIB TOOTE
ETTENÄHTUD FUNKTSIOONI TÄITMINE MITMESUGUSTEL PÕHJUSTEL
EBAÕNNESTUDA. ETTEVÕTTEL MEDTRONIC EI OLE KONTROLLI
TINGIMUSTE ÜLE, MILLISTES SEDA TOODET KASUTATAKSE. TOOTE
SILTIDEL TOODUD HOIATUSED ANNAVAD ÜKSIKASJALIKUMAT TEAVET
NING NEID LOETAKSE KÄESOLEVA GARANTIIST LAHTIÜTLEMISE
LAHUTAMATUKS OSAKS. SEETÕTTU LOOBUB MEDTRONIC KÕIKIDEST, NII
OTSESTEST KUI KAUDSETEST, GARANTIIDEST TOOTE OSAS,
SEALHULGAS, KUID MITTE AINULT, KÕIKIDEST KAUDSETEST
GARANTIIDEST TURUSTATAVUSE VÕI KONKREETSEKS OTSTARBEKS
SOBIVUSE KOHTA. MEDTRONIC EI VASTUTA ÜHEGI INIMESE EGA ISIKU
MEDITSIINIKULUDE EGA ÜHEGI OTSESE, JUHUSLIKU VÕI PÕHJUSLIKU
KAHJU EEST, MIDA PÕHJUSTAB SEADME MISTAHES KASUTAMINE,
DEFEKT, TÕRGE VÕI TALITLUSHÄIRE, SÕLTUMATA SELLEST, KAS
KAHJUNÕUE PÕHINEB GARANTIIL, LEPINGUL, LEPINGUVÄLISEL KAHJUL
VÕI MUUL. VÄLJA ARVATUD JUHUL, KUI ETTEVÕTTE MEDTRONIC
VOLITATUD TÖÖTAJAGA ON TEISITI KIRJALIKULT KOKKU LEPITUD, EI OLE
ÜHELGI ISIKUL VOLITUSI ETTEVÕTTE MEDTRONIC SIDUMISEKS MINGITE
TOOTEGA SEOTUD AVALDUSTE VÕI GARANTIIDEGA.
Ülaltoodud välistamised ja piirangud pole mõeldud kohaldatavate seaduste
kohustuslike sätetega vastuollu sattuma ja neid ei tohiks sellisena käsitada. Kui
57
Eesti
Page 58

mistahes pädeva jurisdiktsiooni kohus peab selle garantiist lahtiütlemise mistahes
osa või tingimust ebaseaduslikuks, jõustamatuks või kohaldatavate seadustega
vastuolus olevaks, ei mõjuta see garantiist lahtiütlemise ülejäänud osade kehtivust
ning kõiki õigusi ja kohustusi tuleb mõista ja rakendada nii, nagu poleks garantiist
lahtiütlemine kehtetuks kuulutatud osa või tingimust sisaldanud.
58Eesti
Page 59

1 Tuotteen kuvaus
Malli Kuvaus
28610 MICS-levitinjärjestelmä
28611 Levitinrunko
28601 LIMA-lavat, vakiot
28602 LIMA-lavat, syvät
28603 Pitkät torakotomialavat, vakiot
28604 Pitkät torakotomialavat, syvät
28604B Pitkällä kiinnikkeellä varustettu pitkä alempi lapa, vakio
28605 Lyhyet torakotomialavat, vakiot
28606 Lyhyet torakotomialavat, syvät
28606B Pitkällä kiinnikkeellä varustettu lyhyt alempi lapa, vakio
Huomautus: Malli 28601 on lapa, jota käytetään yleisimmin rintakehän vasemman
sisävaltimon (LIMA) siirteen irrottamiseen. Malli 28605 on lapa, jota käytetään
yleisimmin yleiseen torakotomiaviillon levittämiseen. Kaikki muut lavat on
suunniteltu potilaiden erilaisen anatomian mukaisiksi.
Huomautus: Mallit 28604B ja 28606B ovat alempia lapoja, jotka on suunniteltu
naisille ja lihaville potilaille. Käytä näitä alempia lapoja ylempien lapojen
(mallien 28604 ja 28606) kanssa.
2 Käyttöaiheet
Mini-invasiivisessa sydänkirurgiassa (MICS) käytettävä
ThoraTrak-levitinjärjestelmä on tarkoitettu pehmyt- ja luukudoksen levittämiseen
mini-invasiivisissa sydän- ja rintaelintoimenpiteissä, kuten mini-invasiivisessa
sepelvaltimoiden ohitusleikkauksessa (CABG) ja rintakehän vasemman
sisävaltimon (LIMA) siirteen irrottamisessa.
3 Varotoimet
Oikeiden kirurgisten toimenpiteiden ja tekniikoiden käyttö on lääkärin vastuulla.
Kirurgien tulee arvioida minkä tahansa toimenpiteen soveltuvuus oman
lääketieteellisen koulutuksensa ja kokemuksensa perusteella.
4 Haittavaikutukset
Ei tunneta.
5 Käsittely ja uudelleenkäsittely
Medtronic on validoinut seuraavat ohjeet tämän lääkinnällisen laitteen valmisteluun
uudelleenkäyttöä varten. Käsittelijän vastuulla on varmistaa, että haluttu tulos
saavutetaan niillä käsittelevän laitoksen laitteilla ja materiaaleilla ja sillä
henkilökunnalla, joita käsittelyssä todellisuudessa käytetään. Käsittely edellyttää
validointia ja rutiininomaista seurantaa. Samoin jos käsittelijä poikkeaa seuraavista
ohjeista, poikkeavan menettelyn tehokkuus ja mahdolliset haitalliset seuraukset on
arvioitava asianmukaisesti. Puhdistuksessa voidaan käyttää näiden
käyttöohjeiden mukaista manuaalista tai automaattista menetelmää tai vastaavaa
validoitua menetelmää.
5.1 Puhdistus
Vaara: Puhdista laitteesta perusteellisesti kaikki lika ennen sterilointia.
59
Suomi
Page 60

Vaara: Älä käytä liuotepohjaisia puhdistusaineita (kuten asetonia tai tolueenia).
• Älä anna kontaminoituneiden laitteiden kuivua ennen puhdistustoimenpiteiden
aloittamista.
• Käsittele laitteet kahden tunnin kuluessa käytön jälkeen. Jos siirto
käsittelyalueelle viivästyy, estä laitteen kuivuminen asettamalla se peitettyyn
astiaan, jossa on entsyymipesuainetta.
• Jos laitteessa on useita osia, pura osat kokonaan ja puhdista ne sitten näiden
käyttöohjeiden mukaisesti.
• Tarkista ennen käyttöä, ettei laitteessa ole halkeamia tai vaurioita. Älä käytä
laitetta, jos sen osissa on merkkejä halkeamista tai vaurioista.
• Lämpödesinfiointia ei tarvita, koska laitteet on steriloitu terminaalisesti.
5.1.1 Manuaalinen puhdistus
Medtronic on vahvistanut seuraavan manuaalisen puhdistusmenettelyn
(Taulukko 1). Nämä toimenpiteet on tehtävä kahden tunnin kuluessa käytön
jälkeen.
Huomautus: Jos laitteessa on liikkuvia osia, varmista, että kaikki pinnat on
puhdistettu perusteellisesti.
Taulukko 1. Manuaalisen puhdistuksen ohjeet
Vaihe Prosessi Lämpötila Puhdistusohjeet
1 Huuhtelu > 27 °C (> 81 °F) Poista karkea lika käyttämällä juokse-
2 Liotus > 28 °C (> 82 °F) Upota laite kokonaan vähintään 5 min
3 Ultraääni-
puhdistus
4 Huuhtelu > 27 °C (> 81 °F) Huuhtele laitetta juoksevalla vedellä
5 Kuivaus – Kuivaa puhtaalla, nukkaamattomalla lii-
6 Tarkastus – Tarkista silmämääräisesti, ettei mis-
5.1.2 Automaattinen puhdistus
Medtronic on vahvistanut seuraavan automaattisen puhdistusmenettelyn.
Seuraavassa taulukossa (Taulukko 2) kuvatut toimenpiteet on tehtävä kahden
tunnin kuluessa käytön jälkeen.
Huomautus: Jos laitteessa tai osassa on liikkuvia osia, varmista, että kaikki pinnat
on puhdistettu perusteellisesti.
> 27 °C (> 81 °F) Upota laite kokonaan ultraäänipesuriin
vaa vettä 1 min ajan. Puhdista laite
perusteellisesti pehmeäharjaksisella
harjalla (kuten nailonhammasharjalla).
ajaksi liuokseen, jossa on vettä ja entsyymipesuainetta (kuten ENZOL™)
15,6 mL / 1 L (tai 2 unssia / 1 gallona).
Poista näkyvä lika pehmeäharjaksisella harjalla.
(kuten Bransonic™), jossa on vettä ja
entsyymipesuainetta (kuten ENZOL)
7,8 mL / 1 L (tai 1 unssi / 1 gallona).
Käytä ultraäänipesuria 10 min ajan.
1 min ajan.
nalla.
sään laitteessa ole likaa tai kosteutta.
Jos likaa jää, toista prosessi.
Suomi
60
Page 61

Taulukko 2. Esikäsittelyohjeet
Vaihe Prosessi Veden lämpötila Puhdistusohjeet
1 Huuhtelu > 25 °C (> 77 °F) Poista karkea lika käyttämällä juok-
2 Liotus > 25 °C (> 77 °F) Upota laite kokonaan vähintään
3 Huuhtelu > 25 °C (> 77 °F) Huuhtele laitetta vähintään 2 min
4 Tarkastus – Tarkista silmämääräisesti, onko lait-
Medtronic validoi automaattisen puhdistusprosessin käyttämällä
Prolystica™-sarjan pesukoneita valmistajan suositusten mukaisesti. Käsittelijän
vastuulla on varmistaa, että käsittelyssä käytetään validoitua menetelmää. Jos
käsittelijä poikkeaa näistä suosituksista, poikkeava menettely on arvioitava.
1. Aseta laite automaattipesukoneeseen (kuten Steris Reliance™
Genfore™ -pesu- ja desinfiointilaitteeseen).
Huomautus: Vältä laitteiden välistä kosketusta, kun täytät pesukonetta.
2. Ohjelmoi automaattipesukoneeseen seuraavassa taulukossa (Taulukko 3)
annetut parametrit ja anna automaattipesukoneen suorittaa pesujakso
loppuun.
Taulukko 3. Automaattipesukoneen puhdistusparametrit
Käsittely
Entsyymipesu 04:00 ≥ 60 °C
Pesu 02:00 ≥ 60 °C
Huuhtelu 02:00 ≥ 60 °C
Kuivaus 15:00 ≥ 82 °C
Tarkastus – – Tarkista silmämääräisesti, ettei mis-
Aika
(min) Lämpötila Puhdistusaine
(≥ 140 °F)
(≥ 140 °F)
(≥ 140 °F)
(≥ 180 °F)
sevaa vesijohtovettä.
1 min ajaksi liuokseen, jossa on
vettä ja entsyymipesuainetta (kuten
ENZOL) 7,8 mL / 1 L (tai
1 unssi / 1 gallona). Poista näkyvä
lika pehmeäharjaksisella harjalla
(kuten nailonhammasharjalla).
ajan.
teessa vielä likaa. Toista prosessi
tarvittaessa.
Steris Prolystica™ Ultra Concentrate
Enzymatic Cleaner, joka on laimennettu pitoisuuteen 1,0 mL / 1 L (tai
0,125 unssia / 1 gallona).
Steris Prolystica™ Ultra Concentrate
Neutral Detergent, joka on laimennettu pitoisuuteen 1,0 mL / 1 L (tai
0,125 unssia / 1 gallona).
–
–
sään laitteessa ole likaa tai kosteutta.
Jos likaa jää, toista prosessi. Kuivaa
tarvittaessa laite suodatetulla paineilmalla tai nukkaamattomalla liinalla.
5.2 Höyrysterilointi ja uudelleensterilointi
• Käytä vakiopakkausmateriaalia. Varmista, että pakkaus on riittävän iso, jotta
laite mahtuu siihen rasittamatta tiivisteitä. Medtronic käytti sterilointiprosessien
validoinnissa kunkin laitteen asianmukaista lisävarustetarjotinta.
61
Suomi
Page 62

• Medtronic validoi höyrysterilointijaksot, kun laitteet oli kääritty CSR (Central
Supply Room) -kääreeseen. Höyrysterilointiprosessi voidaan kuitenkin tehdä
myös laitteille, joita ei ole kääritty tai jotka on kääritty höyrysterilointiin
soveltuvilla materiaaleilla.
• Kun steriloit useita laitteita yhdellä autoklaavijaksolla, älä ylitä sterilointilaitteen
maksimikuormaa.
• Tarkista ennen käyttöä, ettei laitteessa ole halkeamia tai vaurioita. Älä käytä
laitetta, jos sen osissa on merkkejä halkeamista tai vaurioista.
• Yhdysvaltojen ulkopuolella jotkin terveysviranomaiset suosittelevat
sterilointijakson parametreja, jotka minimoivat Creutzfeldt–Jakobin taudin
(CJD:n) mahdollisen leviämisriskin. Tämä suositus koskee erityisesti kirurgisia
instrumentteja, jotka voivat joutua kosketuksiin keskushermoston kanssa.
Taulukko 4. Sterilointijakson parametrit
Jakson tyyppi
Esityhjiö
(dynaaminen
ilmanpoisto)
Esityhjiö
(dynaaminen
ilmanpoisto)
Esityhjiö (dynaaminen
ilmanpoisto) CJD:n
varalta
a
Lämpötila 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Altistusaika 4 min 3 min 18 min
Kuivausaika
a
Medtronic suosittelee laitteiden polttamista, jos ne ovat olleet suorassa kosketuksessa
potilaisiin, joilla epäillään tai on vahvistettu olevan tarttuva spongiforminen enkefalopatia (TSE,
Transmissible Spongiform Encephalopathy) tai CJD. Lähteissä NHS Estates HTM 2010 Parts
4 & 6: Appendix 2, Items contaminated with TSE Agents (TSE:n taudinaiheuttajien
kontaminoimat tuotteet) ja WHO Infection Control Guidelines for Transmissible Spongiform
Encephalopathies (WHO:n infektiontorjuntaohjeet liittyen tarttuviin spongiformisiin
enkefalopatioihin) viitataan TSE-dekontaminaatiojaksoon, jossa käytetään höyryautoklaavia
lämpötilassa 134 °C–137 °C (273 °F–279 °F) yhden 18 minuutin jakson ajan tai useiden,
yhteensä 18 minuuttia kestävien jaksojen ajan (esimerkiksi kuuden 3 minuutin jakson ajan).
b
Vähimmäiskuivausajat on validoitu sterilointilaitteilla, joissa on tyhjiökuivausominaisuus.
Ympäristön ilmanpaineessa toimivia kuivausjaksoja käytettäessä kuivausajat voivat olla
pitempiä. Noudata sterilointilaitteen valmistajan suosituksia.
b
20 min 16 min 30 min
6 Käyttöohjeet
Huomautus: Lavat on merkitty numerolla, joka vastaa mallinumeron viimeistä
numeroa. Esimerkiksi mallin 28603 merkintä on ”3”; mallin 28606B merkintä
on ”6B”. Jokaiseen lapaan on merkitty yksilöllinen sarjanumero.
6.1 Lavan kiinnitys
1. Kiinnitä lavat levitinrunkoon liu’uttamalla lapakiinnike levitinrungon varteen.
2. Irrota lavat liu’uttamalla lapakiinnike pois levitinrungon varresta.
6.2 Rintakehän vasemman sisävaltimon (LIMA) siirteen irrotus
1. Aseta torakotomiaviiltoon levitin, johon on kiinnitetty LIMA-lavat. Suuri
LIMA-lapa, jonka päässä on reikä, on asetettava pään suuntaan pieneen
lapaan nähden.
2. Avaa levitin kääntämällä sen nuppia ja levitä torakotomiaviiltoa.
3. Kallista levitintä ylöspäin vetämällä suurta LIMA-lapaa ylöspäin sen päässä
olevasta reiästä. Näin saat näkyviin rintakehän vasemman sisävaltimon ja
pystyt irrottamaan siirteen.
Huomautus: Levitin on suunniteltu yhteensopivaksi
Rultract™-levitinjärjestelmän kanssa, joten tätä järjestelmää voi käyttää
Suomi
62
Page 63

suuren LIMA-lavan vetämiseen ylöspäin. Myös muita välineitä tai menetelmiä
voidaan käyttää lavan vetämiseen ylöspäin.
4. Kun rintakehän vasemman sisävaltimon siirre on irrotettu, lopeta suuren
LIMA-lavan vetäminen ylöspäin.
5. Sulje levitin painamalla vapautusvipua.
6. Poista levitin torakotomiaviillosta.
6.3 Yleinen torakotomiaviillon levitys
1. Kiinnitä torakotomialavat levittimeen.
2. Aseta levitin torakotomiaviiltoon.
3. Avaa levitin kääntämällä sen nuppia ja levitä torakotomiaviiltoa.
4. Toimenpiteen lopussa sulje levitin painamalla vapautusvipua.
5. Poista levitin torakotomiaviillosta.
7 Takuuta koskeva vastuuvapauslauseke (maailmanlaajuinen)
VAIKKA TUOTE ON SUUNNITELTU, VALMISTETTU JA TESTATTU ENNEN
MYYNTIÄ HUOLELLISESTI VALVOTUISSA OLOSUHTEISSA, USEISTA ERI
SYISTÄ SAATTAA JOHTUA, ETTÄ TUOTE EI TOIMI TARKOITETULLA
TAVALLA. MEDTRONIC EI PYSTY VALVOMAAN OLOSUHTEITA, JOISSA
TÄTÄ TUOTETTA KÄYTETÄÄN. TUOTTEEN MERKINNÖISSÄ OLEVAT
VAROITUKSET SISÄLTÄVÄT TARKEMPIA LISÄTIETOJA JA KUULUVAT
OLENNAISENA OSANA TÄHÄN TAKUUTA KOSKEVAAN
VASTUUVAPAUSLAUSEKKEESEEN. MEDTRONIC SANOUTUU SITEN IRTI
KAIKISTA TUOTTEESEEN LIITTYVISTÄ NIMENOMAISISTA JA
KONKLUDENTTISISTA TAKUISTA, MUKAAN LUKIEN, MUTTA NIIHIN
RAJOITTUMATTA, KONKLUDENTTISET TAKUUT SOVELTUVUUDESTA
KAUPANKÄYNNIN KOHTEEKSI TAI TIETTYYN TARKOITUKSEEN.
MEDTRONIC EI OLE VASTUUSSA KENENKÄÄN HENKILÖN TAI TAHON
HOITOKULUISTA TAI MISTÄÄN SUORASTA, SATUNNAISESTA TAI
VÄLILLISESTÄ VAHINGOSTA, JOKA ON AIHEUTUNUT TUOTTEEN
KÄYTÖSTÄ, VIASTA, TOIMINNAN LAKKAAMISESTA TAI VIRHEELLISESTÄ
TOIMINNASTA, RIIPPUMATTA SIITÄ, PERUSTUUKO VAATIMUS
TAKUUSEEN, SOPIMUKSEEN, OIKEUDENLOUKKAUKSEEN TAI MUUHUN
SEIKKAAN. KENELLÄKÄÄN EI OLE VALTUUKSIA SITOA
MEDTRONIC-YHTIÖTÄ MIHINKÄÄN TUOTETTA KOSKEVIIN ILMOITUKSIIN
TAI TAKUISIIN, PAITSI SILLOIN, KUN MEDTRONIC-YHTIÖN VALTUUTETTU
HENKILÖKUNTA ON ANTANUT SIIHEN KIRJALLISEN SUOSTUMUKSEN.
Yllä mainittuja rajoituksia ei ole tarkoitettu voimassa olevan pakottavan
lainsäädännön vastaisiksi, eikä niitä pidä tällä tavoin tulkita. Mikäli toimivaltainen
tuomioistuin katsoo, että jokin tämän takuuta koskevan vastuuvapauslausekkeen
osa tai ehto on laiton, täytäntöönpanokelvoton tai ristiriidassa tapaukseen
sovellettavan lainsäädännön kanssa, takuuta koskeva vastuuvapauslauseke säilyy
kuitenkin muilta osin voimassa, ja kaikkia oikeuksia ja velvollisuuksia on tulkittava ja
pantava täytäntöön ikään kuin tämä takuuta koskeva vastuuvapauslauseke ei
sisältäisi sitä erityistä osaa tai ehtoa, joka katsotaan pätemättömäksi.
63
Suomi
Page 64

1 Description du produit
Modèle Description
28610 Kit écarteur MICS
28611 Crémaillère de l’écarteur
28601 Valves AMIG, standard
28602 Valves AMIG, profondes
28603 Valves de thoracotomie longues, standard
28604 Valves de thoracotomie longues, profondes
28604B Valve inférieure de fixation, rallongée, longue, standard
28605 Valves de thoracotomie courtes, standard
28606 Valves de thoracotomie courtes, profondes
28606B Valve inférieure de fixation, rallongée, courte, standard
Remarque : La valve Modèle 28601 est la plus couramment utilisée pour le
prélèvement de l’artère mammaire interne gauche (AMIG). La valve Modèle 28605
est la plus couramment utilisée pour l’écartement général de la thoracotomie.
Toutes les autres valves ont été conçues pour répondre aux différentes anatomies.
Remarque : Les valves Modèles 28604B et 28606B sont des valves inférieures
destinées aux femmes et aux patients obèses. Ces valves inférieures doivent être
utilisées avec les valves supérieures (Modèles 28604 et 28606).
2 Indications d’utilisation
Le kit écarteur ThoraTrak pour interventions cardiaques mini-invasives (MICS) est
conçu pour fournir un accès chirurgical lors des interventions cardiothoraciques
mini-invasives, y compris le pontage par greffe coronarienne (CABG) et le
prélèvement AMIG, en écartant les tissus mous et osseux.
3 Précautions
L’utilisation de procédures et de techniques chirurgicales appropriées relève de la
responsabilité du médecin. Le chirurgien doit évaluer l’adéquation de l’intervention
en fonction de sa propre formation et de sa propre expérience médicales.
4 Effets secondaires
Aucun connu.
5 Traitement et retraitement
Les instructions suivantes ont été validées par Medtronic pour la préparation de cet
appareil médical en vue de sa réutilisation. Il incombe à l’établissement de s’assurer
que le traitement, tel qu’il est effectivement exécuté par le personnel à l’aide des
équipements et des matériels du service de traitement, permet d’obtenir le résultat
souhaité. Le traitement doit faire l’objet d’une validation et d’une surveillance de
routine. De même, toute déviation de la part de l’établissement par rapport aux
instructions suivantes doit être correctement évaluée en termes d’efficacité et de
conséquences secondaires potentielles. Le nettoyage peut être effectué
manuellement ou être automatique conformément au présent mode d’emploi ou à
une méthode validée équivalente.
5.1 Nettoyage
Avertissement : Nettoyer soigneusement l’appareil pour éliminer toute trace de
salissure avant la stérilisation.
Français
64
Page 65

Avertissement : Ne pas utiliser de produits nettoyants à base de solvant (par
exemple, acétone ou toluène).
• Ne pas laisser sécher les appareils contaminés avant de mettre en œuvre toute
procédure de nettoyage.
• Retraiter les appareils dans les 2 heures suivant l’utilisation. Si le transfert vers
la zone de traitement est susceptible d’être retardé, placer l’appareil dans un
conteneur muni d’un couvercle et contenant un détergent enzymatique pour
éviter la dessiccation.
• Si l’appareil contient plusieurs composants, démonter complètement les
composants avant d’effectuer le nettoyage conformément au présent mode
d’emploi.
• Examiner l’appareil avant l’utilisation pour vérifier l’absence de craquelure ou
de dégradation. Ne pas utiliser l’appareil si des composants présentent des
signes de craquelure ou de dégradation.
• Une désinfection thermique n’est pas nécessaire, car les appareils sont
stérilisés en fin de procédure.
5.1.1 Nettoyage manuel
Medtronic a établi la procédure de nettoyage manuel suivante dans le Tableau 1.
Ces étapes doivent impérativement être réalisées dans les 2 heures suivant
l’utilisation.
Remarque : Si l’appareil comprend des pièces mobiles, vérifier que toutes les
parties en surface ont été soigneusement nettoyées.
Tableau 1. Instructions de nettoyage manuel
Étape
Proces-
1 Rinçage > 27 °C (> 81 °F) Éliminer toute salissure visible à l’eau
2 Trempage > 28 °C (> 82 °F) Immerger complètement l’appareil
3 Nettoyage
4 Rinçage > 27 °C (> 81 °F) Rincer l’appareil à l’eau courante pen-
5 Séchage S/O Sécher avec un chiffon propre non
6 Inspection S/O Inspecter chaque appareil pour déceler
sus Température Instructions de nettoyage
courante pendant 1 min. Utiliser une
brosse à poils souples (par exemple,
une brosse à dents en nylon) pour nettoyer soigneusement l’appareil.
pendant au moins 5 min dans un
mélange de 15,6 mL/1 L (ou 2 onces/1
gallon) de détergent enzymatique (par
exemple, ENZOL™) et d’eau. Retirer
toute salissure visible à l’aide d’une
par ultra-
> 27 °C (> 81 °F) Immerger complètement l’appareil
sons
brosse à poils souples.
dans un nettoyeur par ultrasons (par
exemple, Bransonic™) dans un
mélange de 7,8 mL/1 L (ou 1 once/1
gallon) de détergent enzymatique (par
exemple, ENZOL) et d’eau. Procéder à
une sonication pendant 10 min.
dant 1 min.
pelucheux.
d’éventuels restes de salissure ou
65 Français
Page 66

Tableau 1. Instructions de nettoyage manuel (suite)
Étape
5.1.2 Nettoyage automatique
Medtronic a établi la procédure de nettoyage automatique suivante. Les étapes
décrites dans le Tableau 2 doivent impérativement être réalisées dans les 2 heures
suivant l’utilisation.
Remarque : Si l’appareil ou le composant comprend des pièces mobiles, vérifier
que toutes les parties en surface ont été soigneusement nettoyées.
Tableau 2. Instructions de prétraitement
Étape
Medtronic a utilisé la gamme de nettoyants Prolystica™ conformément aux
recommandations du fabricant pour valider le processus de nettoyage
automatique. Il incombe à l’établissement de s’assurer que le traitement est réalisé
conformément à une méthode validée. Toute déviation de la part de l’établissement
par rapport aux présentes recommandations doit être évaluée.
1. Placer l’appareil dans un laveur automatique (par exemple, le
2. Régler le laveur automatique selon les paramètres indiqués dans le Tableau 3
Tableau 3. Paramètres de nettoyage du laveur automatique
Traitement
Lavage enzy-
Proces-
sus Température Instructions de nettoyage
Proces-
sus
1 Rinçage > 25 °C (> 77 °F) Éliminer toute salissure visible à
2 Trempage > 25 °C (> 77 °F) Immerger complètement l’appareil
3 Rinçage > 25 °C (> 77 °F) Rincer l’appareil pendant au moins
4 Inspection S/O Inspecter l’appareil pour déceler
laveur-désinfecteur Steris Reliance™ Genfore™).
Remarque : Éviter tout contact entre les appareils lors du chargement dans le
laveur.
et le laisser terminer le cycle de lavage.
matique
Température de
l’eau Instructions de nettoyage
Durée
(min) Température Agent nettoyant
04:00 ≥ 60 °C
(≥ 140 °F)
d’humidité. S’il reste des salissures,
répéter le processus.
l’eau courante du robinet.
pendant au moins 1 min dans un
mélange de 7,8 mL/1 L (ou 1 once/1
gallon) de détergent enzymatique
(par exemple, ENZOL) et d’eau.
Retirer toute salissure visible à l’aide
d’une brosse à poils souples (par
exemple, une brosse à dents en
nylon).
2 min.
d’éventuels restes de salissure.
Répéter le processus si nécessaire.
Nettoyant enzymatique ultra concentré Steris Prolystica™ Ultra Concen-
66Français
Page 67

Tableau 3. Paramètres de nettoyage du laveur automatique (suite)
Durée
Traitement
(min) Température Agent nettoyant
trate Enzymatic Cleaner dilué à
1,0 mL/1 L (ou 0,125 once/1 gallon).
Lavage 02:00 ≥ 60 °C
(≥ 140 °F)
Détergent neutre ultra concentré
Steris Prolystica™ Ultra Concentrate
Neutral Detergent dilué à 1,0 mL/1 L
(ou 0,125 once/1 gallon).
Rinçage 02:00 ≥ 60 °C
S/O
(≥ 140 °F)
Séchage 15:00 ≥ 82 °C
S/O
(≥ 180 °F)
Inspection S/O S/O Inspecter chaque appareil pour déce-
ler d’éventuels restes de salissure ou
d’humidité. S’il reste des salissures,
répéter le processus. Si nécessaire,
sécher l’appareil à l’air comprimé filtré
ou à l’aide d’un chiffon non pelucheux.
5.2 Stérilisation et restérilisation à la vapeur
• Utiliser un emballage standard. Vérifier que l’emballage est suffisamment large
pour contenir l’appareil sans exercer de contrainte sur les joints. Au cours de la
validation des processus de stérilisation, Medtronic a utilisé le plateau
d’accessoires approprié pour chaque appareil.
• Medtronic a validé les cycles de stérilisation à la vapeur lorsque les appareils
ont été emballés à l’aide d’un film CSR (Central Supply Room). Toutefois, le
processus de stérilisation à la vapeur peut être réalisé lorsque les appareils
sont déballés ou emballés à l’aide de matériaux compatibles avec la
stérilisation à la vapeur.
• Lors de la stérilisation de plusieurs appareils dans 1 cycle autoclave, ne pas
dépasser la charge maximale du stérilisateur.
• Examiner l’appareil avant l’utilisation pour vérifier l’absence de craquelure ou
de dégradation. Ne pas utiliser l’appareil si les composants présentent des
signes de craquelure ou de dégradation.
• Certaines autorités sanitaires non américaines recommandent des paramètres
du cycle de stérilisation qui réduisent au maximum le risque potentiel de
transmission de la maladie de Creutzfeldt-Jakob (MCJ). Cette
recommandation est particulièrement importante pour les instruments
chirurgicaux qui pourraient entrer en contact avec le système nerveux central.
Tableau 4. Paramètres du cycle de stérilisation
Type de cycle
Température 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Durée d’expo-
sition
Durée de
séchage
a
Medtronic recommande d’incinérer les appareils qui ont été en contact direct avec les patients
dont le diagnostic d’encéphalopathie spongiforme transmissible (EST)/MCJ est envisagé ou
Prévide (éva-
cuation dyna-
mique de l’air)
b
Prévide (éva-
cuation dynami-
que de l’air)
Prévide (évacuation
dynamique de l’air)
pour la MCJ
4 min 3 min 18 min
20 min 16 min 30 min
a
67
Français
Page 68

établi. NHS Estates HTM 2010 Parties 4 et 6 : Annexe 2, Éléments contaminés par les agents
de l’EST (NHS Estates HTM 2010 Parts 4 & 6: Appendix 2, Items contaminated with TSE
Agents) et les Directives de contrôle des infections de l’OMS pour les encéphalopathies
spongiformes transmissibles (WHO Infection Control Guidelines for Transmissible Spongiform
Encephalopathies) font référence à un cycle de décontamination des EST à l’aide d’un
autoclave à vapeur à une température comprise entre 134 °C et 137 °C (273 °F et 279 °F)
pendant un cycle unique de 18 min ou plusieurs cycles d’une durée totale de 18 min (par
exemple, six cycles de 3 min chacun).
b
Les durées de séchage minimales ont été validées en utilisant des stérilisateurs dotés de
fonctions de séchage à vide. Les cycles de séchage utilisant la pression atmosphérique
ambiante peuvent durer plus longtemps. Se reporter aux recommandations du fabricant du
stérilisateur.
6 Mode d’emploi
Remarque : Les valves comportent un numéro qui correspond au dernier chiffre du
numéro du modèle. Par exemple, la valve 28603 porte le numéro "3" et la
valve 28606B le numéro "6B". Chaque valve comporte un numéro de série unique.
6.1 Fixation de la valve
1. Fixer les valves à la crémaillère de l’écarteur en glissant le porte-valves dans
le bras de la crémaillère.
2. Retirer les valves en faisant glisser le porte-valves hors du bras de la
crémaillère.
6.2 Prélèvement de l’AMIG
1. Placer l’écarteur, auquel sont fixées les valves AMIG, dans la thoracotomie. La
grande valve AMIG munie d’un orifice à son extrémité doit être orientée vers la
tête du patient par rapport à la valve plus petite.
2. Tourner le bouton de l’écarteur afin d’ouvrir ce dernier et d’agrandir la
thoracotomie.
3. Appliquer sur la grande valve AMIG une tension vers le haut au niveau de
l’orifice situé à l’extrémité de la valve pour faire basculer l’écarteur vers le haut.
Cette action permet d’accéder à l’AMIG et d’effectuer le prélèvement.
Remarque : L’écarteur a été conçu pour fonctionner avec le kit écarteur
Rultract™ de manière à appliquer sur la grande valve AMIG une tension vers
le haut. D’autres moyens ou méthodes peuvent être utilisés pour appliquer la
tension vers le haut.
4. Une fois le prélèvement de l’AMIG terminé, relâcher la tension vers le haut de
la grande valve AMIG.
5. Appuyer sur le levier de dégagement pour fermer l’écarteur.
6. Retirer l’écarteur de la thoracotomie.
6.3 Écartement général de la thoracotomie
1. Fixer les valves de thoracotomie sur l’écarteur.
2. Placer l’écarteur dans la thoracotomie.
3. Tourner le bouton de l’écarteur afin d’ouvrir ce dernier et d’agrandir la
thoracotomie.
4. À la fin de l’intervention, appuyer sur le levier de dégagement pour fermer
l’écarteur.
5. Retirer l’écarteur de la thoracotomie.
Français
68
Page 69

7 Déni de garantie (global)
BIEN QUE LE PRODUIT AIT ÉTÉ CONÇU, FABRIQUÉ ET TESTÉ AVANT SA
MISE EN VENTE À L’AIDE DE CONTRÔLES RIGOUREUX, LE PRODUIT PEUT,
POUR DIVERSES RAISONS, CONNAÎTRE DES DÉFAILLANCES.
MEDTRONIC N’A AUCUN CONTRÔLE SUR LES CONDITIONS DANS
LESQUELLES CE PRODUIT EST UTILISÉ. LES AVERTISSEMENTS
FIGURANT SUR LES ÉTIQUETTES DU PRODUIT DONNENT DES
INFORMATIONS PLUS DÉTAILLÉES ET DOIVENT ÊTRE CONSIDÉRÉS
COMME FAISANT PARTIE INTÉGRANTE DU PRÉSENT DÉNI DE GARANTIE.
EN CONSÉQUENCE, MEDTRONIC DÉCLINE TOUTE GARANTIE, EXPRESSE
OU IMPLICITE, RELATIVE AU PRODUIT, DONT, ENTRE AUTRES, TOUTE
GARANTIE IMPLICITE DE QUALITÉ MARCHANDE OU D’ADÉQUATION À UN
USAGE PARTICULIER. MEDTRONIC NE POURRA EN AUCUN CAS ÊTRE
TENUE POUR RESPONSABLE, ENVERS AUCUNE PERSONNE OU ENTITÉ,
DES FRAIS MÉDICAUX OU DES DOMMAGES DIRECTS, FORTUITS OU
INDIRECTS QUI SERAIENT PROVOQUÉS PAR TOUS USAGES,
DÉFECTUOSITÉS, DÉFAILLANCES OU DYSFONCTIONNEMENTS DU
PRODUIT, ET CE QUE LA PLAINTE SOIT FONDÉE SUR UNE GARANTIE, UNE
RESPONSABILITÉ CONTRACTUELLE, DÉLICTUEUSE OU AUTRE. SAUF
DISPOSITION CONTRAIRE MENTIONNÉE PAR ÉCRIT PAR LE PERSONNEL
AUTORISÉ DE MEDTRONIC, NUL N’EST HABILITÉ À LIER MEDTRONIC À
QUELQUE GARANTIE OU RESPONSABILITÉ QUE CE SOIT CONCERNANT
LE PRODUIT.
Les exclusions et les limitations mentionnées ci-dessus ne sont pas, et ne doivent
pas être, interprétées comme contraires aux dispositions obligatoires des lois
applicables. Si une partie ou une disposition du présent Déni de garantie devait être
considérée comme illégale, non applicable ou contraire à la loi en vigueur par un
tribunal compétent, la validité des autres dispositions du présent Déni de garantie
n’en sera pas affectée et tous les droits et obligations seront interprétés et appliqués
comme si le présent Déni de garantie ne contenait pas la partie ou la disposition
considérée comme non valide.
69
Français
Page 70

1 Opis proizvoda
Model Opis
28610 Sustav retraktora MICS
28611 Postolje retraktora
28601 Oštrice za lijevu unutarnju mamarnu arteriju, standardne
28602 Oštrice za lijevu unutarnju mamarnu arteriju, duboke
28603 Duge oštrice za torakotomiju, standardne
28604 Duge oštrice za torakotomiju, duboke
28604B Duga oštrica za produženu donju montažu, standardna
28605 Kratke oštrice za torakotomiju, standardne
28606 Kratke oštrice za torakotomiju, duboke
28606B Kratka oštrica za produženu donju montažu, standardna
Napomena: model 28601 oštrica je koja se najčešće upotrebljava za uzimanje
uzorka lijeve unutarnje mamarne arterije (LIMA). Model 28605 oštrica je koja se
najčešće upotrebljava za opću retrakciju torakotomije. Sve ostale oštrice izrađene
su kako bi se prilagodile različitim anatomskim obilježjima bolesnika.
Napomena: modeli 28604B i 28606B donje su oštrice izrađene za žene i za pretile
bolesnike. Upotrijebite te donje oštrice zajedno s gornjim oštricama (modeli 28604
i 28606).
2 Indikacije za upotrebu
Sustav minimalno invazivnih retraktora (MICS) za kardiokirurgiju ThoraTrak
namijenjen je za kirurški pristup retrakcijom mekog i koštanog tkiva za minimalno
invazivne kardiotorakalne zahvate, uključujući minimalno invazivno presađivanje
premosnice koronarne arterije (CABG) i uzimanje uzorka lijeve unutarnje mamarne
arterije.
3 Mjere opreza
Za odabir odgovarajućih zahvata i tehnika odgovorno je medicinsko osoblje. Nužno
je da kirurzi procijene prikladnost bilo kojeg zahvata na temelju svojega vlastitog
medicinskog znanja i iskustva.
4 Nuspojave
Nisu poznate.
5 Obrada i ponovna primjena
Tvrtka Medtronic potvrdila je da su sljedeće upute valjane za pripremu ovoga
medicinskog uređaja za ponovnu upotrebu. Odgovornost je osobe koja obavlja
obradu osigurati da se obradom, koja se vrši pomoću opreme, materijala i osoblja
u postrojenju za obradu, postigne željeni rezultat. Za obradu su potrebni provjera
valjanosti i rutinski nadzor. Svako odstupanje od sljedećih uputa potrebno je
ispravno procijeniti s aspekta djelotvornosti i mogućih neželjenih posljedica.
Čišćenje može biti ručno ili automatsko u skladu s ovim uputama za upotrebu ili
jednako vrijednom provjerenom metodom.
5.1 Čišćenje
Upozorenje: prije sterilizacije temeljito očistite uređaj da biste uklonili nečistoću.
Hrvatski
70
Page 71

Upozorenje: nemojte upotrebljavati sredstva za čišćenje na bazi otapala
(primjerice aceton ili toluen).
• Kontaminirani se uređaji ne smiju osušiti prije čišćenja.
• Uređaje ponovno obradite u roku od 2 sata nakon upotrebe. Ako će prijevoz do
područja obrade kasniti, uređaj smjestite u prekriveni spremnik s deterdžentom
na bazi enzima da biste spriječili isušivanje.
• Ako se uređaj sastoji od više komponenti, potpuno ih rastavite prije čišćenja u
skladu s ovim uputama za upotrebu.
• Prije upotrebe pregledajte ima li na uređaju znakova pucanja ili oštećenja.
Nemojte upotrebljavati uređaj ako na njegovim komponentama uočite pukotine
ili oštećenja.
• Termička dezinfekcija nije potrebna jer su uređaji terminalno sterilizirani.
5.1.1 Ručno čišćenje
Tvrtka Medtronic utvrdila je sljedeći postupak ručnog čišćenja u odjeljku tabl. 1. Te
je korake potrebno provesti najkasnije 2 sata nakon upotrebe.
Napomena: ako se na uređaju nalaze uklonjivi dijelovi, provjerite da su sve
površine temeljito očišćene.
Tabl. 1. Upute za ručno čišćenje
Korak Postupak Temperatura Upute za čišćenje
1 Ispiranje >27 °C (>81 °F) Jaču prljavštinu uklonite tekućom
2 Namakanje>28 °C (>82 °F) Uređaj najmanje 5 min potpuno uronite
3 Ultrazvučn
o čišćenje
4 Ispiranje >27 °C (>81 °F) Isperite uređaj pod tekućom vodom
5 Sušenje Nije dostupno Osušite čistom krpom bez dlačica.
6 Provjera Nije dostupno Vizualno pregledajte svaki uređaj da
5.1.2 Automatsko čišćenje
Tvrtka Medtronic utvrdila je sljedeći postupak automatskog čišćenja. Korake u
odjeljku tabl. 2 potrebno je provesti u roku od 2 sata nakon upotrebe.
Napomena: Ako se na uređaju ili komponenti nalaze uklonjivi dijelovi, provjerite da
su sve površine temeljito očišćene.
>27 °C (>81 °F) Uređaj potpuno uronite u ultrazvučni
vodom tijekom 1 min. Za temeljito
čišćenje uređaja upotrijebite meku
četkicu (primjerice najlonsku četkicu za
zube).
u mješavinu deterdženta na bazi
enzima (primjerice ENZOL™) i vode u
omjeru 15,6 mL/1 L (ili 2 unce/1 galon).
Vidljivu nečistoću uklonite mekom
četkicom.
uređaj za čišćenje (primjerice
Bransonic™) s mješavinom deterdženta na bazi enzima (primjerice
ENZOL) i vode u omjeru 7,8 mL/1 L (ili 1
unca/1 galon). Primjenjujte ultrazvuk
10 min.
1 min.
biste vidjeli je li na njima preostalo nečistoća ili vlage. Ako ima nečistoća,
ponovite postupak.
71
Hrvatski
Page 72

Tabl. 2. Upute prije obrade
Korak Postupak Temperatura vode Upute za čišćenje
1 Ispiranje >25 °C (>77 °F) Jaču prljavštinu uklonite tekućom
2 Namakanje>25 °C (>77 °F) Uređaj najmanje 1 min potpuno uro-
3 Ispiranje >25 °C (>77 °F) Ispirite uređaj najmanje 2 min.
4 Provjera Nije dostupno Vizualno pregledajte ima li još neči-
Medtronic upotrebljava liniju uređaja za čišćenje Prolystica™ u skladu s
preporukama proizvođača radi provjere valjanosti automatskog čišćenja. Osoba
koja obavlja obradu zadužena je za provedbu u skladu s provjerenom metodom.
Svako odstupanje od tih preporuka potrebno je procijeniti.
1. Umetnite uređaj u automatski uređaj za pranje (primjerice uređaj za
pranje/dezinfekciju Steris Reliance™ Genfore™).
Napomena: pazite da ne dođe do kontakta između uređaja prilikom punjenja
uređaja za pranje.
2. Postavite automatski uređaj za pranje tako da pokreće parametre navedene u
odjeljku tabl. 3 te omogućite uređaju za pranje da dovrši ciklus pranja.
Tabl. 3. Parametri za čišćenje automatskog uređaja za čišćenje
Obrada
Pranje na bazi
enzima
Pranje 02:00 ≥60 °C
Ispiranje 02:00 ≥60 °C
Sušenje 15:00 ≥82 °C
Provjera Nije
Vrijeme
(min) Temperatura Sredstvo za čišćenje
04:00 ≥60 °C
(≥140 °F)
(≥140 °F)
(≥140 °F)
(≥180 °F)
Nije dostupno Vizualno pregledajte svaki uređaj da
dostupn
o
vodom iz slavine.
nite u mješavinu deterdženta na
bazi enzima (primjerice ENZOL) i
vode u omjeru 7,8 mL/1 L (ili 1
uncu/1 galon). Vidljivu nečistoću
uklonite mekom četkicom
(primjerice najlonskom četkicom za
zube).
stoća na uređaju. Prema potrebi
ponovite postupak.
Ultra koncentrirano sredstvo za
čišćenje na bazi enzima Steris
Prolystica™ razrijeđeno kao
1,0 mL/1 L (ili 0,125 unca/1 galon).
Ultra koncentrirani neutralni deterdžent Steris Prolystica™ razrijeđen
kao 1,0 mL/1 L (ili 0,125 unca/1
galon).
Nije dostupno
Nije dostupno
biste vidjeli je li na njima preostalo
nečistoća ili vlage. Ako ima nečistoća,
ponovite postupak. Uređaj po potrebi
osušite filtriranim, komprimiranim
zrakom ili krpom koja ne pušta
dlačice.
72Hrvatski
Page 73

5.2 Sterilizacija / ponovna sterilizacija parom
• Upotrebljavajte standardni materijal za pakiranje. Provjerite je li pakiranje
dovoljno veliko da uređaj ne ošteti izolaciju. Pri provjeri postupaka sterilizacije
tvrtka Medtronic upotrijebila je odgovarajuću ladicu za dodatnu opremu uz
svaki uređaj.
• Medtronic je provjerio cikluse parenja kada su uređaji bili omotani oblogom iz
središnje nabavne jedinice (CSR). No postupak sterilizacije parom može se
dovršiti kada je uređaj odmotan ili umotan u materijale prilagođene sterilizaciji
parom.
• Kada sterilizirate veći broj uređaja u 1 ciklusu autoklaviranja, nemojte
prekoračiti maksimalno opterećenje uređaja za sterilizaciju.
• Prije upotrebe pregledajte ima li na uređaju znakova pucanja ili oštećenja.
Nemojte upotrebljavati uređaj ako na komponentama uočite pukotine ili
oštećenja.
• Neke zdravstvene ustanove izvan Sjedinjenih Američkih Država preporučuju
sterilizaciju prema parametrima ciklusa koji će smanjiti moguće opasnosti od
prijenosa Creutzfeldt-Jakobljeve bolesti (CJD). Ova je preporuka osobito važna
za kirurške instrumente koji mogu doći u doticaj sa središnjim živčanim
sustavom.
Tabl. 4. Parametri ciklusa sterilizacije
Vrsta ciklusa
Temperatura 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Vrijeme
izlaganja
Vrijeme
sušenja
a
Tvrtka Medtronic preporučuje spaljivanje uređaja koji su bili u izravnom kontaktu s bolesnicima
u kojih se sumnja na dijagnozu prijenosne spongiformne encefalopatije (TSE)/CJD ili je ona
potvrđena. NHS Estates HTM 2010 Parts 4 & 6: Appendix 2, Items contaminated with TSE
Agents i WHO Infection Control Guidelines for Transmissible Spongiform Encephalopathies
odnose se na ciklus dekontaminacije za TSE parnim autoklavom na temperaturama od 134 °C
do 137 °C (273 °F do 279 °F) u jednom ciklusu u trajanju od 18 min ili u više ciklusa ukupnog
trajanja 18 min (npr. šest ciklusa od 3 min).
b
Minimalno vrijeme sušenja potvrđeno je pomoću sterilizatora sa značajkom vakuumskog
sušenja. Ciklusi sušenja u kojima se upotrebljava zrak iz okoline pod atmosferskim tlakom
mogu biti dulji. Pogledajte preporuke proizvođača sterilizatora.
b
Predvakuumir
anje
(dinamičko
uklanjanje
zraka)
Predvakuumira
nje (dinamičko
uklanjanje
zraka)
Predvakuumiranje
(dinamičko uklanjanje
zraka) za CJD
4 min 3 min 18 min
20 min 16 min 30 min
a
6 Upute za upotrebu
Napomena: oštrice su označene brojem koji odgovara posljednjoj znamenci broja
modela. Primjerice 28603 označen je s “3”; 28606B označen je sa “6B”. Svaka
oštrica označena je jedinstvenim serijskim brojem.
6.1 Pričvršćivanje oštrice
1. Pričvrstite oštrice na postolje retraktora pomicanjem postolja oštrice u držač
postolja retraktora.
2. Uklonite oštrice pomicanjem postolja oštrice iz držača postolja retraktora.
73
Hrvatski
Page 74

6.2 Uzimanje uzorka lijeve unutarnje mamarne arterije
1. Retraktor na kojem su pričvršćene oštrice za lijevu unutarnju mamarnu arteriju
postavite u torakotomiju. Velika oštrica za lijevu unutarnju mamarnu arteriju s
otvorom na kraju treba se usmjeriti kranijalno prema manjoj oštrici.
2. Okrenite gumb retraktora da biste otvorili retraktor i proširili torakotomiju.
3. Promijenite pritisak prema gore na veliku oštricu za lijevu unutarnju mamarnu
arteriju na otvor na kraju oštrice da biste nagnuli retraktor prema gore. Ovom
se radnjom omogućuje pristup lijevoj unutarnjoj mamarnoj arteriji i uzimanje
uzorka.
Napomena: retraktor je izrađen za rad sa sustavom retraktora Rultract™ kako
bi se primijenio pritisak prema gore na veliku oštricu za lijevu unutarnju
mamarnu arteriju. Mogu se upotrijebiti druga sredstva ili načini za primjenu
pritiska prema gore.
4. Nakon dovršetka uzimanja uzorka lijeve unutarnje mamarne arterije, otpustite
pritisak prema gore s velike oštrice za lijevu unutarnju mamarnu arteriju.
5. Pritisnite polugu za otpuštanje da biste zatvorili retraktor.
6. Izvadite retraktor iz torakotomije.
6.3 Generalna retrakcija torakotomije
1. Pričvrstite oštrice torakotomije na retraktor.
2. Umetnite retraktor u torakotomiju.
3. Okrenite gumb retraktora da biste otvorili retraktor i proširili torakotomiju.
4. Nakon dovršetka postupka pritisnite polugu za otpuštanje da biste zatvorili
retraktor.
5. Izvadite retraktor iz torakotomije.
7 Isključenje jamstva (globalno)
IAKO JE PROIZVOD PAŽLJIVO OSMIŠLJEN, PROIZVEDEN I TESTIRAN
PRIJE PRODAJE U PAŽLJIVO KONTROLIRANIM UVJETIMA, MOŽE SE
DOGODITI DA IZ NIZA RAZLOGA NE FUNKCIONIRA NA ZADOVOLJAVAJUĆI
NAČIN. MEDTRONIC NEMA KONTROLE NAD UVJETIMA POD KOJIMA SE
OVAJ PROIZVOD UPOTREBLJAVA. UPOZORENJA NA OZNACI PROIZVODA
SADRŽE DETALJNIJE INFORMACIJE I SMATRAJU SE SASTAVNIM DIJELOM
OVOG ISKLJUČENJA JAMSTVA. MEDTRONIC SE STOGA ODRIČE SVIH
JAMSTAVA, IZRIČITIH I PODRAZUMIJEVANIH, U ODNOSU NA PROIZVOD,
UKLJUČUJUĆI IZMEĐU OSTALOGA SVA PODRAZUMIJEVANA JAMSTVA O
MOGUĆNOSTIMA PRODAJE ILI PRIKLADNOSTI ZA ODREĐENU SVRHU.
MEDTRONIC NIJE ODGOVORAN NI JEDNOJ PRIVATNOJ ILI PRAVNOJ
OSOBI NI ZA KAKVE MEDICINSKE TROŠKOVE NI IZRAVNE, SLUČAJNE ILI
POSLJEDIČNE ŠTETE NASTALE USLIJED UPOTREBE, NEDOSTATKA,
KVARA ILI NEISPRAVNE FUNKCIJE PROIZVODA, NEOVISNO O TOME
TEMELJI LI SE ZAHTJEV NA JAMSTVU, UGOVORU, KAZNENOM DJELU ILI
NEKOJ DRUGOJ OSNOVI. OSIM AKO JE DRUGAČIJE DOGOVORENO U
PISANOM OBLIKU OD STRANE OVLAŠTENOG OSOBLJA TVRTKE
MEDTRONIC, NIJEDNA OSOBA NEMA PRAVO OBVEZATI MEDTRONIC NI NA
KAKVA ZASTUPANJA ILI JAMSTVA VEZANA UZ PROIZVOD.
Gore opisana izuzeća i ograničenja nisu zamišljena kao opreka obveznim
odredbama mjerodavnog zakonodavstva te ih tako ne treba tumačiti. Ako bilo koji
dio ovog isključenja jamstva nadležni sud proglasi nezakonitim, neprovedivim ili u
sukobu s mjerodavnim zakonodavstvom, to neće utjecati na valjanost preostalih
dijelova ovog isključenja jamstva te će se sva prava i obveze tumačiti i provoditi kao
da ovo isključenje jamstva ne sadrži opisani dio ili uvjet koji se smatra nezakonitim.
Hrvatski
74
Page 75

1 A termék leírása
Típus Leírás
28610 MICS mellkasterpesz-rendszer
28611 A mellkasterpesz állványa
28601 Standard, bal oldali artéria mammaria interna lapocok
28602 Mély, bal oldali artéria mammaria interna lapocok
28603 Hosszú, standard thoracotomiás lapocok
28604 Hosszú, mély thoracotomiás lapocok
28604B Hosszú, standard, nyújtott karú inferior lapoc
28605 Rövid, standard thoracotomiás lapocok
28606 Rövid, mély thoracotomiás lapocok
28606B Rövid, standard, nyújtott karú inferior lapoc
Megjegyzés: A 28601-es típusú lapocot használják a leggyakrabban a bal oldali
artéria mammaria interna nyeréséhez. A 28605-ös típusú lapocot használják a
leggyakrabban az általános thoracotomiás feltáráshoz. Az összes többi lapoc úgy
lett kialakítva, hogy alkalmazkodjanak a páciensek eltérő anatómiai viszonyaihoz.
Megjegyzés: A 28604B és 28606B típusú inferior lapocok nők és túlsúlyos betegek
számára készültek. Ezeket az inferior lapocokat superior lapocokkal (28604-es és
a 28606-os típus) kell használni.
2 Alkalmazási terület
A ThoraTrak minimálisan invazív szívsebészeti (MICS) mellkasterpesz-rendszer
minimálisan invazív ér- és mellkassebészeti beavatkozásokhoz – például
minimálisan invazív koszorúér bypass műtéthez (CABG) és a bal oldali artéria
mammaria interna (LIMA) nyeréséhez – biztosít sebészi feltárást a lágyszövetek és
csontok elhúzásával.
3 Előírások
A megfelelő sebészeti eljárások és módszerek alkalmazása a szakorvos
felelőssége. A sebész felelőssége az is, hogy képzettségének és tapasztalatának
megfelelően mérlegelje bármely eljárás alkalmazhatóságát.
4 Szövődmények
Nem ismeretesek.
5 Feldolgozás és újrafeldolgozás
A Medtronic a következő útmutatásokat hitelesítette az orvostechnikai eszközök
újrahasználathoz való előkészítésére. Továbbra is a feldolgozást végzők
felelőssége annak biztosítása, hogy a feldolgozás – ahogyan azt ténylegesen
elvégzik a feldolgozási helyen alkalmazott berendezésekkel, anyagokkal és
személyzettel – elérje a kívánt eredményt. Az újrafeldolgozáshoz a folyamatot
validálni szükséges, és rutinszerűen figyelemmel kell kísérni. Továbbá, ha a
feldolgozást végző bármiben eltérne a következő utasításoktól, azt az
eredményesség és a lehetséges nem kívánt következmények tekintetében
megfelelően értékelni kell. A tisztítás ezen használati útmutató szerinti végezhető
manuálisan vagy automatizált művelettel, illetve azzal egyenértékű, validált
módszerrel.
75
Magyar
Page 76

5.1 Tisztítás
Vigyázat! Sterilizálás előtt alaposan tisztítsa meg az eszközt, hogy ne maradjon
rajta szennyeződés.
Vigyázat! Nem szabad oldószeres (pl. acetonos vagy toluolos) tisztítószereket
használni.
• Tisztítóeljárások végzése előtt ne engedje a szennyeződött eszközöket
megszáradni!
• A használatot követő két órán belül sort kell keríteni eszközök
újrafeldolgozására. Ha a feldolgozási területre való szállításra később kerül sor,
akkor a kiszáradás megelőzése érdekében helyezze az eszközt enzimes
mosószert tartalmazó, fedett tárolóba.
• Ha az eszköz több részegységből áll, akkor tisztítás előtt a használati
útmutatónak megfelelően szerelje szét teljesen részegységeire.
• Használat előtt vizsgálja át az eszközt, nincs-e rajta valamilyen repedés vagy
minőségromlás. Nem szabad az eszközt használni, ha bármely részegységen
repedésére vagy minőségromlására utaló jelet talál.
• Az eszközök terminális sterilizálása miatt hővel való fertőtlenítés nem
szükséges.
5.1.1 Manuális tisztítás
A Medtronic a következő kézi tisztítási eljárást dolgozta ki, és rögzítette az
1. táblázat keretében. Ezeket a lépéseket a használatot követően legfeljebb két
órán belül el kell végezni.
Megjegyzés: Ha az eszköznek mozgó részei vannak, ellenőrizze, hogy minden
felületet alaposan megtisztított-e.
1. táblázat. Kézi tisztítási utasítások Lépés Folyamat Hőmérséklet Tisztítási utasítások
1. Öblítés >27 °C (>81 °F) 1 min folyóvízben történő öblítéssel
2. Áztatás >28 °C (>82 °F) Az eszközt legalább 5 min időtartamra
3. Ultrahangos tisztí-
4. Öblítés >27 °C (>81 °F) Öblítse le az eszközt folyó víz alatt,
5. Szárítás N/A Tiszta, nem foszló törlővel törölje szá-
6. Szemrevé-
telezés
>27 °C (>81 °F) Ultrahangos tisztítóberendezésben
tás
N/A Szemrevételezéssel vizsgálja át mind-
távolítsa el a nagyobb szennyeződéseket. Puha sörtéjű kefével (például nylon
fogkefével) tisztítsa meg alaposan az
eszközt.
teljesen merítse bele enzimes mosószer (például ENZOL™)
15,6 mL/1 L-es (vagy 2 uncia/1 gallonos) vizes oldatába. A látható szenynyeződéseket puha sörtéjű kefével
távolítsa el.
(például Bransonic™) teljesen merítse
bele az eszközt enzimes mosószer
(például ENZOL) 7,8 mL/1 L-es (vagy 1
uncia/1 gallonos) vizes oldatába. Szonikálja 10 min időtartamon keresztül.
1 min időtartamon keresztül.
razra.
egyik eszközt, nem maradt-e rajtuk
76Magyar
Page 77

1. táblázat. Kézi tisztítási utasítások (folytatás)
Lépés Folyamat Hőmérséklet Tisztítási utasítások
5.1.2 Automatizált tisztítás
A Medtronic a következő automatikus tisztítási eljárást dolgozta ki. A 2. táblázat
keretében jelzett lépéseket a használatot követően legfeljebb két órán belül el kell
végezni.
Megjegyzés: Ha az eszköznek vagy részegységnek mozgó részei vannak,
ellenőrizze, hogy minden felületet alaposan megtisztított-e.
2. táblázat. Előkezelési utasítások Lépés Folyamat Víz hőmérséklete Tisztítási utasítások
1. Öblítés >25 °C (>77 °F) Folyó csapvíz alatti öblítéssel távo-
2. Áztatás >25 °C (>77 °F) Az eszközt legalább 1 min időtar-
3. Öblítés >25 °C (>77 °F) Öblítse az eszközt legalább 2 min
4. Szemrevételezés
Az automatizált tisztítási folyamat validálására a gyártó ajánlása szerint a Medtronic
a Prolystica™ tisztítócsaládot használta. A feldolgozást végzőnek kell ügyelnie
arra, hogy a feldolgozást a validált módszer szerint végezzék. Ha a feldolgozást
végző bármiben eltérne ezen ajánlásoktól, azt megfelelően értékelni kell.
1. Helyezze az eszközt automatizált mosóberendezésbe (például Steris
Reliance™ Genfore™ mosó/fertőtlenítő).
Megjegyzés: A mosó megtöltésekor az eszközök ne érintkezzenek
egymással.
2. Az automatizált mosóberendezést a 3. táblázat keretében rögzített
paramétereknek megfelelően futassa, és hagyja, hogy az automatizált
mosóberendezés elvégezze a mosási ciklust.
3. táblázat. Az automatizált mosóberendezés tisztítási paraméterei
Kezelés
Enzimatikus
mosás
Idő
(min) Hőmérséklet Tisztítószer
04:00 ≥60 °C
N/A Szemrevételezéssel vizsgálja át az
(≥140 °F)
szennyeződés vagy nedvesség. Ha
szennyeződés marad, ismételje meg a
folyamatot.
lítsa el a nagyobb szennyeződéseket.
tamra teljesen merítse bele enzimes
mosószer (például ENZOL)
7,8 mL/1 L-es (vagy 1 uncia/1 gallonos) vizes oldatába. A látható
szennyeződéseket puha sörtéjű
kefével (például nylon fogkefe) távolítsa el.
időtartamig.
eszközt, nem maradt-e rajta szenynyeződés. Szükség szerint ismételje meg a folyamatot.
Steris Prolystica™ ultrakoncentrált
enzimes tisztítószer 1,0 mL/1 L-es
77 Magyar
Page 78

3. táblázat. Az automatizált mosóberendezés tisztítási paraméterei (folytatás)
Idő
Kezelés
(min) Hőmérséklet Tisztítószer
(vagy 0,125 uncia/1 gallonos) hígításban.
Mosás 02:00 ≥60 °C
(≥140 °F)
Steris Prolystica™ ultrakoncentrált
semleges tisztítószer 1,0 mL/1 L-es
(vagy 0,125 uncia/1 gallonos) hígításban.
Öblítés 02:00 ≥60 °C
N/A
(≥140 °F)
Szárítás 15:00 ≥82 °C
N/A
(≥180 °F)
Szemrevétele-
zés
N/A N/A Szemrevételezéssel vizsgálja át
mindegyik eszközt, nem maradt-e rajtuk szennyeződés vagy nedvesség.
Ha szennyeződés marad, ismételje
meg a folyamatot. Szükség szerint az
eszközöket szűrt, sűrített levegővel
vagy nem foszló kendővel szárítsa.
5.2 Gőzsterilizálás és újrasterilizálás
• Szokványos csomagolóanyagot használjon. Ügyeljen arra, hogy a csomag
elég nagy legyen, és elférjen benne az eszköz úgy, hogy ne feszítse a
zárásokat. A sterilizálási folyamatok validálására a Medtronic minden egyes
eszközhöz megfelelő tartozéktálcát használt.
• A Medtronic akkor validálta a gőzölési ciklusokat, amikor az eszközök a
központi sterilizáló által használt csomagolóanyagba voltak csomagolva. Ezzel
szemben a gőzsterilizálás folyamata egyaránt elvégezhető akkor is, amikor az
eszközök nincsenek csomagolva, vagy a gőzsterilizálás szempontjából
kompatibilis anyagokba vannak csomagolva.
• Amikor több eszközt sterilizál egyetlen autoklávciklusban, ne lépje túl a
sterilizáló maximális terhelését.
• Használat előtt vizsgálja át az eszközt, nincs-e rajta valamilyen repedés vagy
minőségromlás. Nem szabad az eszközt használni, ha a részegységeken
repedésére vagy minőségromlására utaló jelet talál.
• Néhány nem egyesült államokbeli egészségügyi hatóság olyan paramétereket
ajánl a sterilizálási ciklushoz, melyek minimálisra csökkentik a
Creutzfeld-Jakob kór (CJD) átvitelének potenciális kockázatát. Ez az ajánlás
különösen fontos az olyan sebészi eszközök esetében, amelyek érintkezésbe
kerülhetnek a központi idegrendszerrel.
4. táblázat. A sterilizálási ciklus paraméterei
Ciklus típusa
Hőmérséklet 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Expozíciós idő 4 min 3 min 18 min
Száradási idő
a
A Medtronic ajánlása szerint az olyan eszközöket el kell égetni, amelyek közvetlen kapcsolatba
kerültek feltételezhetően vagy igazoltan fertőző szivacsos agyvelőbántalmakkal
(TSE)/Creutzfeld-Jakob kórral diagnosztizált betegekkel. Az NHS Estates HTM 2010 Parts 4 &
Elővákuum
(dinamikus
levegő-eltávo-
lítás)
b
20 min 16 min 30 min
Elővákuum
(dinamikus
levegő-eltávolí-
tás)
Elővákuum (dinamikus
levegő-eltávolítás)
Creutzfeld-Jakob kór
esetében
a
Magyar
78
Page 79

6: Appendix 2, Items contaminated with TSE Agents (Az Egyesült Királyság Állami
Egészségügyi Szolgálatának 2010-es állapotelemző, egészségügyi szakmai
előterjesztésének 4. és 6. rész: 2. melléklete: TSE-ágensekkel fertőzött elemek), valamint
a WHO Infection Control Guidelines for Transmissible Spongiform Encephalopathies (Az
Egészségügyi Világszervezet fertőző szivacsos agyvelőbántalmakra vonatkozó
fertőzésellenőrzési irányelvei) a TSE dekontaminációs ciklust gőzsterilizáló autokláv
alkalmazása mellett határozza meg a következő paraméterekkel: 134 °C és 137 °C (273 °F és
279 °F) közötti hőmérséklet egyetlen, 18 min tartamú ciklusra, illetve több, összesen 18 min
időtartamot kitevő ciklusra (pl. hat 3 min hosszúságú ciklus).
b
A minimális száradási időket vákuumszárításos sterilizátorokkal validálták. A környezeti,
légköri nyomást használó szárítási ciklusok esetén több időre lehet szükség. Lásd a sterilizátor
gyártójának ajánlásait.
6 Használati utasítás
Megjegyzés: A lapocokon feltüntetett szám a típusszám utolsó számjegyének felel
meg. Például a 28603 jelzése „3”; a 28606B jelzése „6B.” Minden lapoc egyedi
sorozatszámmal rendelkezik.
6.1 A lapoc felerősítése
1. Erősítse fel a lapocokat a mellkasterpesz állványára úgy, hogy rácsúsztatja a
lapocrögzítőt a mellkasterpeszállvány-karra.
2. A lapocrögzítő mellkasterpeszállvány-karról történő lecsúsztatásával távolítsa
el a lapocokat.
6.2 Bal oldali artéria mammaria interna nyerése
1. Helyezze a bal oldali artéria mammaria interna lapocokkal felszerelt
mellkasterpeszt a thoracotomiás nyílásba. A nagyméretű, a végén lyukkal
rendelkező bal oldali artéria mammaria interna lapocnak a kisebb lapochoz
képest cephalikus irányban kell elhelyezkednie.
2. Forgassa a mellkasterpesz forgógombját a mellkasterpesz kinyitásához, és a
thoracotomiás nyílás kiterjesztéséhez.
3. A mellkasterpesz felfelé dönthető a nagyméretű bal oldali artéria mammaria
interna lapoc végénél található lyukra kifejtett, felfelé irányuló nyomással. Ez a
művelet hozzáférést biztosít a bal oldali artéria mammaria internához, és
lehetővé teszi az érnyerést.
Megjegyzés: A mellkasterpeszt a Rultract™ mellkasterpesz-rendszerrel való
használatra tervezték, így biztosítható a nagyméretű bal oldali artéria
mammaria interna lapocra gyakorolt, felfelé irányuló nyomás. Más módon és
módszerrel is lehetséges a felfelé irányuló nyomás biztosítása.
4. A bal oldali artéria mammaria interna nyerésének befejezése után szüntesse
meg a nagyméretű bal oldali mammaria interna lapocra gyakorolt, felfelé
irányuló nyomást.
5. A mellkasterpesz bezárásához nyomja meg a kioldó emelőt.
6. Vegye ki a mellkasterpeszt a thoracotomiás nyílásból.
6.3 Általános thoracotomiás feltárás
1. Erősítse fel a thoracotomiás lapocokat a mellkasterpeszre.
2. Helyezze a mellkasterpeszt a thoracotomiás nyílásba.
3. Forgassa a mellkasterpesz forgógombját a mellkasterpesz kinyitásához, és a
thoracotomiás nyílás kiterjesztéséhez.
79
Magyar
Page 80

4. Az eljárás befejezésekor nyomja meg az kioldó emelőt a mellkasterpesz
zárásához.
5. Vegye ki a mellkasterpeszt a thoracotomiás nyílásból.
7 Szavatossági nyilatkozat (globális érvényű)
BÁR A TERMÉK TERVEZÉSE, GYÁRTÁSA ÉS ÉRTÉKESÍTÉS ELŐTTI
ELLENŐRZÉSE KÖRÜLTEKINTŐEN SZABÁLYOZOTT FELTÉTELEK
MELLETT TÖRTÉNT, ELŐFORDULHAT, HOGY A TERMÉK KÜLÖNBÖZŐ
OKOKBÓL ESETLEG NEM LÁTJA EL FELADATÁT. A MEDTRONIC NEM
TUDJA FELÜGYELNI A TERMÉK FELHASZNÁLÁSÁNAK KÖRÜLMÉNYEIT. A
TERMÉK CÍMKÉIN FELTÜNTETETT FIGYELMEZTETÉSEK TOVÁBBI
INFORMÁCIÓKKAL SZOLGÁLNAK, ÉS JELEN SZAVATOSSÁGI
NYILATKOZAT SZERVES RÉSZÉNEK TEKINTENDŐEK. A MEDTRONIC
ENNEK MEGFELELŐEN A TERMÉKKEL KAPCSOLATBAN SEMMINEMŰ
KIFEJEZETT VAGY TÖRVÉNYI FELELŐSSÉGET NEM VÁLLAL, TÖBBEK
KÖZÖTT ARRA SEM, HOGY A TERMÉK FORGALOMKÉPES, ÉS EGY ADOTT
CÉLRA MEGFELEL. A MEDTRONIC SEMMILYEN TERMÉSZETES VAGY JOGI
SZEMÉLYNEK NEM FELEL A TERMÉK HASZNÁLATÁBÓL,
MŰKÖDÉSKÉPTELENSÉGÉBŐL VAGY HIBÁS MŰKÖDÉSÉBŐL EREDŐ
ORVOSI KÖLTSÉGÉRT, SEM KÖZVETLEN, VÉLETLEN VAGY
KÖVETKEZMÉNYES KÁRÉRT, LEGYEN AZ IGÉNY ALAPJA AKÁR
SZAVATOSSÁG, AKÁR SZERZŐDÉS, AKÁR SZERZŐDÉSEN KÍVÜLI
KÁROKOZÁS, AKÁR VALAMI EGYÉB DOLOG. AMENNYIBEN ABBA A
MEDTRONIC JOGOSÍTOTT SZEMÉLYZETE ÍRÁSBAN MÁSKÉPPEN BELE
NEM EGYEZIK, SENKI SEM JOGOSULT KÖTELEZNI A MEDTRONIC
VÁLLALATOT SEMMILYEN NYILATKOZATTÉTELRE VAGY
SZAVATOSSÁGVÁLLALÁSRA A TERMÉKKEL KAPCSOLATBAN.
A fenti kizárásoknak és korlátozásoknak nem célja a vonatkozó jogszabályok
kötelező előírásait megkerülni, és olyan értelmezésnek nincs helye. Ha a jelen
Szavatossági nyilatkozat bármely részét vagy feltételét illetékes bíróság
jogellenesnek, érvényesíthetetlennek vagy a vonatkozó jogszabályokkal
ellentétesnek mondja ki, az a Szavatossági nyilatkozat fennmaradó részének
érvényességét nem érinti; minden jog és kötelezettség úgy értelmezendő és
érvényesítendő, mintha a jelen Szavatossági nyilatkozat nem tartalmazná az
érvénytelennek minősített részt vagy feltételt.
Magyar
80
Page 81

1 Descrizione del prodotto
Modello Descrizione
28610 Sistema di divaricazione per cardiochirurgia mininvasiva
28611 Binario del divaricatore
28601 Lame per arteria mammaria interna sinistra, standard
28602 Lame per arteria mammaria interna sinistra, profonde
28603 Lame per toracotomia lunghe standard
28604 Lame per toracotomia lunghe profonde
28604B Lama per toracotomia inferiore lunga, standard, con
28605 Lame per toracotomia corte standard
28606 Lame per toracotomia corte profonde
28606B Lama per toracotomia inferiore corta, standard, con
Nota: il modello 28601 è il tipo di lame più comunemente utilizzato per l’isolamento
dell’arteria mammaria interna sinistra. Il modello 28605 è il tipo di lame più
comunemente utilizzato per la divaricazione generale della toracotomia. Gli altri
modelli di lame vengono utilizzati in base all’anatomia specifica del paziente.
Nota: i modelli 28604B e 28606B sono lame inferiori progettate per l’uso sui
pazienti di sesso femminile e sui pazienti obesi. Utilizzare queste lame inferiori con
le lame superiori (modelli 28604 e 28606).
(MICS)
attacco esteso
attacco esteso
2 Indicazioni per l’uso
Il sistema di divaricazione per cardiochirurgia mininvasiva (MICS) Thoratrak è
progettato per consentire l’accesso chirurgico durante le procedure
cardiotoraciche mininvasive, quali le procedure chirurgiche mininvasive di innesto
di bypass aortocoronarico (CABG) e di isolamento dell’arteria mammaria interna
sinistra, mediante retrazione dei tessuti molli e ossei.
3 Precauzioni
È responsabilità del medico adottare procedure e tecniche chirurgiche adeguate. I
chirurghi devono valutare l’adeguatezza di ogni procedura in base alla propria
formazione ed esperienza medica.
4 Effetti indesiderati
Nessun effetto indesiderato noto.
5 Condizionamento e ricondizionamento
Le seguenti istruzioni sono state convalidate da Medtronic per la preparazione di
questo dispositivo medico al riutilizzo. È responsabilità dell’autore del
condizionamento garantire che tale processo venga svolto da personale
qualificato, mediante le apparecchiature e i materiali appropriati, nonché in
un’apposita struttura, in modo da raggiungere il risultato previsto. Il
condizionamento richiede la convalida e il monitoraggio di routine. Allo stesso
modo, ogni deviazione dalle istruzioni seguenti da parte dell’autore del
condizionamento dovrà essere valutata in modo adeguato riguardo all’efficacia ed
alle eventuali conseguenze avverse. Il metodo di pulizia utilizzato potrà essere
81
Italiano
Page 82

manuale o automatico, in base alle presenti istruzioni per l’uso, oppure un metodo
convalidato equivalente.
5.1 Pulizia
Avvertenza: pulire accuratamente il dispositivo per eliminare le impurità prima
della sterilizzazione.
Avvertenza: non utilizzare detergenti a base di solventi (ad esempio, acetone o
toluene).
• Non lasciare che i dispositivi contaminati si asciughino prima di eseguire le
procedure di pulizia.
• Ricondizionare il dispositivo entro 2 ore dall’utilizzo. Se si prevede un ritardo nel
trasporto verso l’area di condizionamento, collocare il dispositivo in un
contenitore coperto e riempito con un detergente enzimatico per mantenerlo
umido.
• Se il dispositivo contiene più componenti, smontarli completamente prima di
effettuare la pulizia in base alle presenti istruzioni per l’uso.
• Prima dell’uso, ispezionare il dispositivo per escludere la presenza di
incrinature o segni di deterioramento. Non utilizzare il dispositivo in caso di
incrinature o segni di deterioramento dei componenti.
• La disinfezione termica non è necessaria, in quanto i dispositivi sono già stati
sottoposti a sterilizzazione terminale.
5.1.1 Pulizia manuale
La procedura di pulizia manuale stabilita da Medtronic è la seguente, come indicato
nella Tabella 1. Tale procedura deve essere svolta entro un massimo di 2 ore
dall’utilizzo.
Nota: se il dispositivo comprende delle parti mobili, assicurarsi che tutte le superfici
siano state pulite a fondo.
Tabella 1. Istruzioni per la pulizia manuale
Fase Processo Temperatura Istruzioni per la pulizia
1 Risciac-
2 Immer-
sione
3 Pulizia a
ultrasuoni
4 Risciac-
>27 °C (>81 °F) Rimuovere le impurità più grossolane
quo
>28 °C (>82 °F) Immergere completamente il disposi-
>27 °C (>81 °F) Immergere completamente il disposi-
>27 °C (>81 °F) Risciacquare il dispositivo con acqua
quo
utilizzando acqua corrente per 1 min.
Pulire accuratamente il dispositivo con
uno spazzolino a setole morbide (ad
esempio, uno spazzolino a setole di
nylon).
tivo per almeno 5 min con 15,6 mL/1 L
(o 2 once/1 gallone) di detergente enzimatico (ad esempio, ENZOL™) e
acqua. Rimuovere tutte le impurità visibili con uno spazzolino a setole morbide.
tivo in un pulitore a ultrasuoni (ad esempio, Bransonic™) con 7,8 mL/1 L (o
1 oncia/1 gallone) di detergente enzimatico (ad esempio, ENZOL) e acqua.
Sottoporre a ultrasuoni per 10 min.
corrente per 1 min.
82Italiano
Page 83

Tabella 1. Istruzioni per la pulizia manuale (continua)
Fase Processo Temperatura Istruzioni per la pulizia
5 Asciuga-
tura
6 Ispezione N/A Controllare visivamente ogni disposi-
5.1.2 Pulizia automatica
La procedura di pulizia automatica è stata stabilita da Medtronic nel modo
seguente. La procedura illustrata nella Tabella 2 deve essere svolta entro un
massimo di 2 ore dall’utilizzo.
Nota: se il dispositivo o il componente comprende delle parti mobili, assicurarsi che
tutte le superfici siano state pulite a fondo.
Tabella 2. Istruzioni di pretrattamento
Fase Processo
1 Risciac-
quo
2 Immer-
sione
3 Risciac-
quo
4 Ispezione N/A Controllare visivamente il disposi-
Per convalidare il processo di pulizia automatica, Medtronic ha utilizzato la famiglia
di detergenti Prolystica™, seguendo le raccomandazioni del produttore. È
responsabilità dell’autore del condizionamento garantire che tale processo venga
svolto in base a un metodo convalidato. Ogni deviazione da queste
raccomandazioni da parte dell’autore del condizionamento dovrà essere valutata
con attenzione.
1. Collocare il dispositivo in una lavatrice automatica (ad esempio, sistema di
lavaggio e disinfezione Steris Reliance™ Genfore™).
Nota: quando si carica la lavatrice, evitare il contatto fra i dispositivi.
2. Impostare la lavatrice automatica in modo che esegua i parametri indicati nella
Tabella 3 e completi il ciclo di lavaggio.
N/A Asciugare con un panno pulito che non
rilascia fibre.
tivo per escludere la presenza di impurità o umidità. Se dovessero rimanere
delle impurità, ripetere la procedura di
pulizia.
Temperatura
dell’acqua Istruzioni per la pulizia
>25 °C (>77 °F) Rimuovere le impurità più grosso-
lane utilizzando acqua corrente di
rubinetto.
>25 °C (>77 °F) Immergere completamente il dispo-
sitivo per almeno 1 min con
7,8 mL/1 L (o 1 oncia/1 gallone) di
detergente enzimatico (ad esempio,
ENZOL) e acqua. Rimuovere tutte le
impurità visibili con uno spazzolino a
setole morbide (ad esempio, uno
spazzolino a setole di nylon).
>25 °C (>77 °F) Risciacquare il dispositivo per
almeno 2 min.
tivo per escludere la presenza di
impurità. Se necessario, ripetere la
procedura di pulizia.
83
Italiano
Page 84

Tabella 3. Parametri di pulizia della lavatrice automatica
Trattamento
Lavaggio enzi-
matico
Lavaggio 02:00 ≥60 °C
Risciacquo 02:00 ≥60 °C
Asciugatura 15:00 ≥82 °C
Ispezione N/A N/A Controllare visivamente ogni disposi-
Tempo
(min) Temperatura Detergente
04:00 ≥60 °C
(≥140 °F)
(≥140 °F)
(≥140 °F)
(≥180 °F)
Detergente enzimatico ultraconcentrato Steris Prolystica™ diluito
1,0 mL/1 L (o 0,125 once/1 gallone).
Detergente neutro ultraconcentrato
Steris Prolystica™ diluito 1,0 mL/1 L
(o 0,125 once/1 gallone).
N/A
N/A
tivo per escludere la presenza di
impurità o umidità. Se dovessero
rimanere delle impurità, ripetere la
procedura di pulizia. Se necessario,
asciugare il dispositivo con aria compressa filtrata o con un panno che non
rilascia fibre.
5.2 Sterilizzazione e risterilizzazione a vapore
• Utilizzare il materiale da imballaggio standard. Assicurarsi che la confezione sia
abbastanza grande da poter contenere il dispositivo senza esercitare tensione
sui sigilli. Durante la procedura di convalida dei processi di sterilizzazione,
Medtronic ha utilizzato il vassoio per accessori appropriato per ciascun
dispositivo.
• Medtronic ha convalidato i cicli di vapore con dispositivi avvolti in telo chirurgico
sterile (CSR). Tuttavia, il processo di sterilizzazione a vapore può essere
completato quando i dispositivi non sono avvolti o sono avvolti in materiali
compatibili con la sterilizzazione a vapore.
• Quando si sterilizzano più dispositivi in 1 ciclo di autoclave, non superare il
carico massimo dello sterilizzatore.
• Prima dell’uso, ispezionare il dispositivo per escludere la presenza di
incrinature o segni di deterioramento. Non utilizzare il dispositivo in caso di
incrinature o segni di deterioramento dei componenti.
• Alcuni enti sanitari non statunitensi raccomandano la sterilizzazione in
conformità con parametri che permettono di minimizzare il rischio di
trasmissione della malattia di Creutzfeldt-Jakob (MCJ). Tale raccomandazione
è di particolare importanza nel caso di strumenti chirurgici che possono entrare
in contatto con il sistema nervoso centrale.
Italiano
84
Page 85

Tabella 4. Parametri del ciclo di sterilizzazione
Pre-vuoto
Tipo di ciclo
(rimozione
dinamica
dell’aria)
Pre-vuoto (rimo-
zione dinamica
dell’aria)
Pre-vuoto (rimozione
dinamica dell’aria) per
MCJ
a
Temperatura 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Tempo di espo-
4 min 3 min 18 min
sizione
Tempo di asciu-
a
b
b
gatura
Medtronic raccomanda l’incenerimento dei dispositivi che sono entrati in contatto diretto con
pazienti con diagnosi sospetta o accertata di encefalopatie spongiformi trasmissibili
(TSE)/malattia di Creutzfeldt-Jacob. Le pubblicazioni NHS Estates HTM 2010 Parts 4 & 6:
Appendix 2, Items contaminated with TSE Agents e WHO Infection Control Guidelines for
Transmissible Spongiform Encephalopathies fanno riferimento a un ciclo di decontaminazione
per le TSE con vapore in autoclave a una temperatura da 134 °C a 137 °C (da 273 °F a 279 °F)
per un ciclo singolo di 18 min o per cicli multipli della durata complessiva di 18 min (ad esempio,
6 cicli da 3 min ciascuno).
I tempi di asciugatura minimi sono stati convalidati utilizzando sterilizzatori dotati di asciugatura
a vuoto. I cicli di asciugatura tramite pressione atmosferica ambientale possono richiedere
tempi di asciugatura maggiori. Fare riferimento alle raccomandazioni del fabbricante dello
sterilizzatore.
20 min 16 min 30 min
6 Istruzioni per l’uso
Nota: le lame sono contrassegnate con il numero corrispondente all’ultima cifra del
numero di modello. Ad esempio, il modello 28603 è contrassegnato con il numero
"3"; il modello 28606B è invece contrassegnato con il numero "6B". Ogni lama è
contrassegnata con un numero di serie univoco.
6.1 Montaggio delle lame
1. Montare le lame al binario del divaricatore facendo scorrere l’attacco delle
lame nel braccio del binario.
2. Rimuovere le lame facendole scorrere fuori dal braccio del binario del
divaricatore.
6.2 Isolamento dell’arteria mammaria interna sinistra
1. Posizionare il divaricatore nella toracotomia con le lame per arteria mammaria
interna sinistra montate. La lama per arteria mammaria interna sinistra più
grande con l’estremità dotata di foro deve presentare un orientamento cefalico
rispetto alla lama più piccola.
2. Ruotare la manopola del divaricatore per aprirlo ed estendere la toracotomia.
3. Esercitare una tensione verso l’alto sulla lama per arteria mammaria interna
sinistra più grande in corrispondenza del foro dell’estremità della lama in modo
da inclinare il divaricatore verso l’alto. Questa azione consente di accedere
all’arteria mammaria interna sinistra e di eseguirne l’isolamento.
Nota: il divaricatore è stato progettato per essere utilizzato insieme al sistema
di divaricazione Rultract™ per l’applicazione della tensione verso l’alto sulla
lama per arteria mammaria interna sinistra più grande. È possibile utilizzare
altri mezzi o metodi di applicazione della tensione verso l’alto.
4. Al termine dell’isolamento dell’arteria mammaria interna sinistra, rilasciare la
tensione verso l’alto esercitata sulla lama per arteria mammaria interna sinistra
più grande.
85
Italiano
Page 86

5. Premere la leva per chiudere il divaricatore.
6. Estrarre il divaricatore dalla toracotomia.
6.3 Divaricazione generale della toracotomia
1. Fissare le lame per toracotomia al divaricatore.
2. Posizionare il divaricatore nella toracotomia.
3. Ruotare la manopola del divaricatore per aprirlo ed estendere la toracotomia.
4. Al completamento della procedura, premere la leva per chiudere il
divaricatore.
5. Estrarre il divaricatore dalla toracotomia.
7 Esclusione dalla garanzia (globale)
SEBBENE IL PRODOTTO SIA STATO ACCURATAMENTE PROGETTATO,
REALIZZATO E TESTATO PRIMA DI ESSERE COMMERCIALIZZATO, IN
CONDIZIONI ATTENTAMENTE CONTROLLATE, IL PRODOTTO POTREBBE
NON FUNZIONARE IN MODO SODDISFACENTE PER DIVERSE RAGIONI.
MEDTRONIC NON ESERCITA ALCUN CONTROLLO SULLE MODALITÀ DI
IMPIEGO DEL PRODOTTO. LE AVVERTENZE INDICATE SULLE ETICHETTE
DEL PRODOTTO FORNISCONO INFORMAZIONI PIÙ DETTAGLIATE A TALE
RIGUARDO E SONO DA CONSIDERARSI PARTE INTEGRANTE DELLA
PRESENTE ESCLUSIONE DALLA GARANZIA. DI CONSEGUENZA,
MEDTRONIC NON RILASCIA ALCUNA GARANZIA, NÉ ESPRESSA NÉ
TACITA, IN MERITO AL PRODOTTO COMPRESA, TRA L’ALTRO, QUALSIASI
GARANZIA IMPLICITA DI COMMERCIABILITÀ O DI IDONEITÀ A
DETERMINATI SCOPI. MEDTRONIC NON PUÒ IN ALCUN CASO ESSERE
RITENUTA RESPONSABILE NEI CONFRONTI DI ALCUN SOGGETTO O
ENTITÀ, PER SPESE MEDICHE, DANNI DIRETTI, INCIDENTALI O
CONSEQUENZIALI CAUSATI DALL’USO, DAI DIFETTI O DAL
MALFUNZIONAMENTO DEL PRODOTTO, INDIPENDENTEMENTE DAL
FATTO CHE LA RICHIESTA DI RISARCIMENTO DI TALI DANNI SIA BASATA
SU GARANZIA, CONTRATTO, FATTO ILLECITO O ALTRO. SALVO DIVERSO
ACCORDO SOTTOSCRITTO DA PERSONALE AUTORIZZATO MEDTRONIC,
NESSUN SOGGETTO HA L’AUTORITÀ DI VINCOLARE MEDTRONIC A
QUALSIASI RAPPRESENTAZIONE O GARANZIA IN MERITO AL PRODOTTO.
Le esclusioni e le restrizioni di cui sopra non sono intese, né devono essere
interpretate, come contravvenenti a norme ritenute inderogabili dalla legislazione
vigente. Nel caso in cui una parte od un termine della presente Esclusione dalla
Garanzia venga giudicato illegale, inefficace od in conflitto con la legge vigente, la
validità delle rimanenti parti della presente Esclusione dalla Garanzia non verrà
compromessa e tutti i diritti e gli obblighi verranno interpretati ed applicati come se
la presente Esclusione dalla Garanzia non contenesse la parte od i termini ritenuti
non validi.
Italiano
86
Page 87

1 Gaminio aprašymas
Modelis Apibūdinimas
28610 MICS retraktoriaus sistema
28611 Retraktorius
28601 LIMA mentelės, standartinės
28602 LIMA mentelės, giliosios
28603 Ilgos torakotomijos mentelės, standartinės
28604 Ilgos torakotomijos mentelės, giliosios
28604B Ilga pailginto tvirtinimo papildoma mentelė, standartinė
28605 Trumpos torakotomijos mentelės, standartinės
28606 Trumpos torakotomijos mentelės, giliosios
28606B Trumpa pailginto tvirtinimo papildoma mentelė, standar-
Pastaba. 28601 modelio mentelė dažniausiai naudojama kairiosios vidinės
krūtinės arterijos (LIMA) parinkimo procedūroms. 28605 modelio mentelė
dažniausiai naudojama bendrosios torakotomijos retrakcijai. Visos kitos mentelės
sukonstruotos pritaikant jas įvairioms paciento anatomijoms.
Pastaba. 28604B ir 28606B modeliai yra papildomos mentelės, skirtos moterims ir
nutukusiems pacientams. Naudokite šias papildomas menteles su pagrindinėmis
mentelėmis (28604 ir 28606 modeliais).
tinė
2 Naudojimo indikacijos
„ThoraTrak“ minimalios invazijos širdies chirurgijos (MICS) retraktoriaus sistema
yra skirta chirurginei prieigai užtikrinti atliekant minimalios invazijos širdies-krūtinės
ląstos procedūras, įskaitant minimalios invazijos vainikinių arterijų šuntavimo
(CABG) operaciją ir LIMA parinkimą, atitraukiant minkštuosius ir kaulinius audinius.
3 Atsargumo priemonės
Už tinkamas chirurgines procedūras ir būdus atsako medicinos specialistai.
Remdamasis medicininiu išsilavinimu bei patirtimi chirurgas privalo įvertinti
procedūrų tinkamumą.
4 Nepageidaujami poveikiai
Nežinomi.
5 Apdorojimas ir pakartotinis apdorojimas
„Medtronic“ patvirtinto, kad šios instrukcijos tinka ruošiant medicininį prietaisą
naudoti pakartotinai. Už apdorojimą atsakingas asmuo turi užtikrinti, kad realiai
atliekamu apdorojimu, naudojant įrangą, medžiagas ir dalyvaujant darbuotojams
apdorojimo vietoje, būtų pasiektas pageidaujamas rezultatas. Apdorojant būtinas
tinkamumo įvertinimas ir nuolatinis stebėjimas. Taip pat reikia tinkamai įvertinti bet
kokį apdorojimą atliekančio asmens įvykdytą nuokrypį nuo šių instrukcijų,
atsižvelgiant į efektyvumą ir galimas nepageidaujamas pasekmes. Valymą galima
atlikti rankiniu būdu arba tai galima atlikti automatiškai, kaip nurodyta šiose
naudojimo instrukcijose, arba panašiu patvirtintu metodu.
5.1 Valymas
Įspėjimas. Prieš sterilizuodami kruopščiai nuvalykite prietaisą, kad pašalintumėte
nešvarumus.
87
Lietuviškai
Page 88

Įspėjimas. Nenaudokite iš tirpiklių pagamintų valiklių (pavyzdžiui, acetono arba
toluolo).
• Prieš atlikdami bet kokią valymo procedūrą, neleiskite nešvarumams ant
prietaiso išdžiūti.
• Pakartotinai apdorokite prietaisus per 2 valandas po naudojimo. Jei perkėlimas
į valymo vietą bus atliekamas vėliau, įdėkite prietaisą į uždarą indą, kuriame yra
fermentinio detergento, kad apsaugotumėte nuo išdžiūvimo.
• Jei prietaisą sudaro keli komponentai, prieš valydami visiškai išrinkite
komponentus, laikydamiesi šiose naudojimo instrukcijose pateiktų nurodymų.
• Prieš naudodami patikrinkite, ar prietaisas neįtrūkęs ir nesusidėvėjęs.
Nenaudokite prietaiso, jei pastebėjote kokių nors įtrūkimų ar susidėvėjimo
požymių.
• Nebūtina dezinfekuoti terminiu būdu, nes atliekamas galutinis prietaisų
sterilizavimas.
5.1.1 Rankinis valymas
„Medtronic“ nustatė 1 lent. aprašytą rankinio valymo procedūrą. Šiuos veiksmus
reikia atlikti pradėjus ne daugiau nei 2 valandoms po naudojimo.
Pastaba. Jeigu prietaise yra judančių dalių, užtikrinkite, kad visos paviršiaus sritys
būtų gerai nuvalytos.
1 lentelė. Rankinio valymo instrukcijos
Veiks-
mas Procesas Temperatūra Valymo instrukcijos
1 Skalavi-
2 Mirkymas >28 °C (>82 °F) Visiškai panardinkite prietaisą į
3 Ultragarsi-
nis valy-
4 Skalavi-
5 Džiovini-
6 Tikrinimas Nėra Apžiūrėkite kiekvieną prietaisą, ar ant
>27 °C (>81 °F) Pašalinkite stambius nešvarumus ska-
mas
>27 °C (>81 °F) Visiškai panardinkite prietaisą į ultra-
mas
>27 °C (>81 °F) Praskalaukite prietaisą tekančiu van-
mas
Nėra Nusausinkite švariu nesipūkuojančiu
mas
laudami tekančiu vandeniu 1 min. Prietaisą kruopščiai nuvalykite šepetėliu
minkštais šereliais (pvz., nailoniniu
dantų šepetėliu).
15,6 mL : 1 L (arba 2 uncijų : 1 galone)
santykio fermentinio detergento
(pavyzdžiui, ENZOL™) ir vandens tirpalą ir palaikykite mažiausiai 5 min.
Matomus nešvarumus pašalinkite
šepetėliu minkštais šereliais.
garsinio valymo įtaisą (pavyzdžiui,
„Bransonic™“), kuriame yra 7,8 mL : 1 L
(arba 1 uncijos 1 galone) santykio fermentinio detergento (pavyzdžiui,
ENZOL) ir vandens tirpalas. Apdorokite
ultragarsu 10 min.
deniu 1 min.
audeklu.
jo neliko nešvarumų ar skysčio. Jei
pastebėjote likusių nešvarumų, pakartokite procedūrą.
88Lietuviškai
Page 89

5.1.2 Automatinis valymas
„Medtronic“ nustatė tokią rankinio valymo procedūrą. Veiksmai, nurodyti 2 lent., turi
būti atliekami praėjus ne daugiau nei 2 valandoms po naudojimo.
Pastaba. Jeigu prietaise arba komponente yra judančių dalių, užtikrinkite, kad
visos paviršiaus sritys būtų gerai nuvalytos.
2 lentelė. Pirminio apdorojimo instrukcijos
Veiks-
mas Procesas
1 Skalavi-
2 Mirkymas >25 °C (>77 °F) Visiškai panardinkite prietaisą į
3 Skalavi-
4 Tikrinimas Nėra Apžiūrėkite prietaisą, ar neliko
„Medtronic“ patvirtino automatinio valymo procedūrą pagal gamintojo
rekomendacijas naudodama „Prolystica™“ valiklius. Apdorojimą atliekantis asmuo
privalo užtikrinti, kad jis būtų atliekamas laikantis patvirtintos metodikos. Būtina
įvertinti bet kokį apdorojimą atliekančio asmens įvykdytą nuokrypį nuo šių
rekomendacijų.
1. Įdėkite prietaisą į automatinį plovimo įrenginį (pavyzdžiui, „Steris Reliance™
Genfore™“ plovimo / dezinfekavimo įtaisą).
Pastaba. Saugokite, kad prietaisai, dedant į plovimo įrenginį, nesiliestų.
2. Nustatykite automatinio plovimo įrenginio parametrus, nurodytus 3 lent., ir
paleiskite automatinį plovimo įrenginį, kad atliktų visą plovimo ciklą.
3 lentelė. Automatinio plovimo įrenginio plovimo parametrai
Apdorojimas
Fermentinis
plovimas
Plovimas 02:00 ≥60 °C
Skalavimas 02:00 ≥60 °C
Džiovinimas 15:00 ≥82 °C
Tikrinimas Nėra Nėra Apžiūrėkite kiekvieną prietaisą, ar ant
Vandens tempera-
tūra Valymo instrukcijos
mas
mas
>25 °C (>77 °F) Pašalinkite stambius nešvarumus
>25 °C (>77 °F) Skalaukite prietaisą mažiausiai
Laikas
(min) Temperatūra Valymo priemonė
04:00 ≥60 °C
(≥140 °F)
(≥140 °F)
(≥140 °F)
(≥180 °F)
tekančiu vandeniu.
7,8 mL : 1 L (arba 1 uncijos 1 galonui) santykio fermentinio detergento
(pavyzdžiui, ENZOL) ir vandens ir
palaikykite mažiausiai 1 min. Matomus nešvarumus pašalinkite šepetėliu minkštais šereliais (pvz., nailoniniu dantų šepetėliu).
2 min.
nešvarumų. Jei reikia, pakartokite
procedūrą.
„Steris Prolystica™ Ultra“ koncentruotas fermentinis ploviklis atskiestas
santykiu 1,0 mL : 1 L (arba 0,125 uncijos 1 galone).
„Steris Prolystica™ Ultra“ koncentruotas neutralus ploviklis, atskiestas
santykiu 1,0 mL : 1 L (arba 0,125 uncijos 1 galone).
Nėra
Nėra
jo neliko nešvarumų ar skysčio. Jei
89 Lietuviškai
Page 90

3 lentelė. Automatinio plovimo įrenginio plovimo parametrai (tęsinys)
Laikas
Apdorojimas
(min) Temperatūra Valymo priemonė
pastebėjote likusių nešvarumų,
pakartokite procedūrą. Jei reikia,
išdžiovinkite prietaisą filtruotu
suspaustu oru arba nusausinkite
nesipūkuojančiu audeklu.
5.2 Sterilizavimas / pakartotinis sterilizavimas garais
• Naudokite standartinę pakavimo medžiagą. Įsitikinkite, ar pakuotė pakankamai
didelė, kad joje tilptų prietaisas ir neįsitemptų sandarinamosios dalys.
Sterilizavimo procedūrai tikrinti „Medtronic“ kiekvienam prietaisui naudojo
atitinkamą priedų dėklą.
• „Medtronic“ tikrinant garų ciklų tinkamumą, prietaisai buvo suvynioti į CSR
(„Central Supply Room“) vyniojimo medžiagą. Tačiau sterilizavimo garais
procedūrą galima atlikti prietaiso nesuvyniojus arba suvyniojus į sterilizavimui
garais tinkamas medžiagas.
• Jei 1 autoklavavimo ciklo metu sterilizuojate kelis prietaisus, neviršykite
didžiausios leistinos sterilizatoriaus įkrovos.
• Prieš naudodami patikrinkite, ar prietaisas neįtrūkęs ir nesusidėvėjęs.
Nenaudokite prietaiso, jei pastebėjote įtrūkimų ar susidėvėjimo požymių.
• Kai kurios ne JAV sveikatos priežiūros valdymo institucijos rekomenduoja
sterilizavimo ciklą atlikti pagal parametrus, kurie sumažintų galimą
Creutzfeldto-Jakobo ligos (CJD) plitimą. Šios rekomendacijos labai svarbios
chirurginiams instrumentams, kurie gali turėti sąlytį su centrine nervų sistema.
4 lentelė. Sterilizavimo ciklo parametrai
Ciklo tipas
Temperatūra 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Poveikio
trukmė
Džiovinimo
trukmė
a
„Medtronic“ rekomenduoja sudeginti prietaisus, turėjusius tiesioginį sąlytį su pacientais,
kuriems įtariama arba patvirtinta užkrečiamos spongiforminės encefalopatijos (USE) / CJD
diagnozė. NHS Estates HTM 2010 Parts 4 & 6: Appendix 2, Items contaminated with TSE
Agents ir WHO Infection Control Guidelines for Transmissible Spongiform Encephalopaties
rekomenduoja USE kenksmingumo pašalinimo ciklą naudojant garų autoklavą nuo 134 °C iki
137 °C (nuo 273 °F iki 279 °F) temperatūroje vienu 18 min ciklu arba keliais ciklais, kurių bendra
trukmė 18 min (pvz., šešiais 3 min ciklais).
b
Minimali džiovinimo trukmė patvirtinta naudojant sterilizatorius su vakuuminio džiovinimo
funkcijomis. Jei džiovinimo ciklo metu slėgis yra toks pat kaip aplinkos atmosferos, gali tekti
pailginti džiovinimo trukmę. Žr. sterilizatoriaus gamintojo rekomendacijas.
(dinaminis oro
b
Vakuuminis
pašalinimas)
Vakuuminis
(dinaminis oro
pašalinimas)
Vakuuminis (dinaminis
oro pašalinimas) esant
4 min 3 min 18 min
20 min 16 min 30 min
CJD
a
6 Naudojimo instrukcijos
Pastaba. Mentelės yra pažymėtos numeriais, kurie atitinka paskutinį modelio
numerio skaitmenį. Pavyzdžiui, 28603 pažymėtas „3“; 28606B pažymėtas „6B“.
Kiekviena mentelė pažymėta unikaliu serijos numeriu.
Lietuviškai
90
Page 91

6.1 Mentelės tvirtinimas
1. Pritvirtinkite menteles prie retraktoriaus įstumdami mentelės laikiklį į
retraktoriaus svirtį.
2. Išimkite menteles ištraukdami mentelės laikiklį iš retraktoriaus svirties.
6.2 LIMA parinkimas
1. Įstatykite retraktorių su uždėtomis LIMA mentelėmis į torakotomiją. Didelė
LIMA mentelė su kiauryme gale turi būti nukreipta cefaline kryptimi į mažesnę
mentelę.
2. Sukdami retraktoriaus rankenėlę atsidarykite retraktorių ir išskėskite
torakotomiją.
3. Kelkite LIMA mentelę aukštyn už kiaurymės mentelės gale, kad pakreiptumėte
retraktorių aukštyn. Atlikus šį veiksmą, atsidengs prieiga prie LIMA ir bus
galima atlikti parinkimo procedūrą.
Pastaba. Retraktorius yra skirtas dirbti su „Rultract™“ retraktoriaus sistema
didelės LIMA mentelės įtempimui aukštyn užtikrinti. Galima naudoti ir kitus
įtempimo aukštyn būdus.
4. Kai LIMA parinkimas baigtas, atlaisvinkite didelės LIMA mentelės įtempimą
aukštyn.
5. Paspauskite atlaisvinimo svirtį, kad retraktorius užsidarytų.
6. Išimkite retraktorių iš torakotomijos.
6.3 Bendra torakotomijos atitraukimo procedūra
1. Prijunkite torakotomijos menteles prie retraktoriaus.
2. Įstatykite retraktorių į torakotomiją.
3. Sukdami retraktoriaus rankenėlę atsidarykite retraktorių ir išskėskite
torakotomiją.
4. Atlikę procedūrą, paspauskite atlaisvinimo svirtį, kad retraktorius užsidarytų.
5. Išimkite retraktorių iš torakotomijos.
7 Atsisakymas suteikti garantiją (globalus)
NORS GAMINYS BUVO SUKONSTRUOTAS, PAGAMINTAS IR PATIKRINTAS
PRIEŠ PARDUODANT ATIDŽIAI KONTROLIUOJAMOMIS SĄLYGOMIS,
GAMINYS DĖL ĮVAIRIŲ PRIEŽASČIŲ GALI TINKAMAI NEATLIKTI NUMATYTŲ
FUNKCIJŲ. „MEDTRONIC” NEGALI KONTROLIUOTI ŠIO GAMINIO
NAUDOJIMO SĄLYGŲ. GAMINIO ETIKETĖSE NURODYTUOSE
ĮSPĖJIMUOSE PATEIKIAMA DAUGIAU INFORMACIJOS IR JIE YRA LAIKOMI
SUDĖTINE ŠIO ATSISAKYMO SUTEIKTI GARANTIJĄ DALIMI. TODĖL
„MEDTRONIC“ NEPRISIIMA ATSAKOMYBĖS UŽ VISAS AIŠKIAI IŠREIKŠTAS
AR NUMANOMAS GARANTIJAS, SUSIJUSIAS SU ŠIUO GAMINIU,
ĮSKAITANT BET KOKIĄ NUMANOMĄ GARANTIJĄ DĖL PERKAMUMO AR
TINKAMUMO KONKREČIAM TIKSLUI, BET TUO NEAPSIRIBOJANT.
„MEDTRONIC“ NĖRA ATSAKINGA ASMENIMS AR ĮMONĖMS UŽ
MEDICININES IŠLAIDAS, TIESIOGINIUS, ATSITIKTINIUS AR PASEKMINIUS
GEDIMUS, ATSIRADUSIUS DĖL GAMINIO NAUDOJIMO, DEFEKTŲ,
NEVEIKIMO AR SUTRIKIMO, NEATSIŽVELGIANT Į TAI, AR PRETENZIJOS
PAREMTOS GARANTIJA, SUTARTIMI, CIVILINĖS TEISĖS PAŽEIDIMU AR KT.
JEIGU KITAIP NENURODYTA RAŠTU ĮGALIOTŲ
„MEDTRONIC“ DARBUOTOJŲ, JOKS ASMUO NETURI ĮGALIOJIMŲ
ĮPAREIGOTI „MEDTRONIC“ TAIKYTI GARANTIJAS AR PRISIIMTI
ATSAKOMYBĘ DĖL ŠIO GAMINIO.
91
Lietuviškai
Page 92

Aukščiau išdėstytos išimtys bei apribojimai nėra ir nelaikytini prieštaraujančiais
privalomosioms taikomo įstatymo nuostatoms. Jei kurią nors šio atsisakymo
suteikti garantiją dalį arba sąlygą kompetentingos jurisdikcijos teismas paskelbtų
neteisėta, neįgyvendinama arba prieštaraujančia galiojantiems įstatymams, tai
neturės poveikio likusių šio atsisakymo suteikti garantiją dalių galiojimui, o visos
teisės ir įsipareigojimai bus aiškinami ir įgyvendinami taip, lyg šiame atsisakyme
suteikti garantiją nebūtų negaliojančia paskelbtos dalies arba sąlygos.
92Lietuviškai
Page 93

1 Izstrādājuma apraksts
Modelis Apraksts
28610 MICS atvilcēja sistēma
28611 Atvilcēja statne
28601 LIMA lāpstiņas, standarta
28602 LIMA lāpstiņas, apakšējās
28603 Garas torakotomijas lāpstiņas, standarta
28604 Garas torakotomijas lāpstiņas, apakšējās
28604B Gara pagarināma stiprinājuma iekšējā lāpstiņa, standarta
28605 Īsās torakotomijas lāpstiņas, standarta
28606 Īsās torakotomijas lāpstiņas, apakšējās
28606B Īsa pagarināma stiprinājuma iekšējā lāpstiņa, standarta
Piezīme: 28601. modelis ir lāpstiņa, ko visbiežāk izmanto kreisās iekšējās krūšu
artērijas (LIMA — Left internal mammary artery) materiālam. 28605. modelis ir
lāpstiņa, ko visbiežāk izmanto vispārējai torakotomijas retrakcijai. Pārējās lāpstiņas
paredzētas dažādām pacienta ķermeņa daļām.
Piezīme: 28604B modelis un 28606B modelis ir iekšējās lāpstiņas, kas paredzētas
pacientēm sievietēm un tukliem pacientiem. Izmantojiet šīs iekšējās lāpstiņas kopā
ar augšējām lāpstiņām (28604. modelis un 28606. modelis).
2 Lietošanas indikācijas
Minimāli invazīvās sirds ķirurģijas (MICS — Minimally invasive cardiac surgery)
atvilcēja sistēma ThoraTrak nodrošina minimāli invazīvas kardiotorakālas
procedūras, tostarp minimāli invazīvu koronāro artēriju šuntēšanu (CABG —
Coronary artery bypass grafting), kā arī LIMA materiāla iegūšanu, atvelkot mīkstos
un kaulu audus.
3 Piesardzības pasākumi
Par pareizu ķirurģiskās procedūras veikšanu un metodes izvēli atbildīgs ir
medicīnas speciālists. Ķirurgiem jānovērtē ikvienas procedūras piemērotība
atbilstoši savām medicīniskajām zināšanām un pieredzei, kā arī ķirurģiskās
procedūras veidam.
4 Blakusparādības
Nav zināmas.
5 Apstrāde un atkārtota apstrāde
Uzņēmums Medtronic ir apstiprinājis tālāk minētos norādījumus par šīs medicīnas
ierīces sagatavošanu atkārtotai lietošanai. Apstrādātāja pienākums ir nodrošināt,
ka ar apstrādi, kas tiek veikta, izmantojot aprīkojumu, materiālus un personālu
apstrādes iestādē, tiek sasniegts vēlamais rezultāts. Apstrādes veikšanai
nepieciešama apstiprināšana un regulāra uzraudzība. Jebkura neatbilstība tālāk
sniegtajiem norādījumiem procesa gaitā ir attiecīgi jāizvērtē, ņemot vērā efektivitāti
un iespējamās nevēlamās blakusparādības. Saskaņā ar šiem lietošanas
norādījumiem tīrīšanu var veikt manuāli vai automatizēt vai izmantot līdzvērtīgu
apstiprinātu paņēmienu.
5.1 Tīrīšana
Brīdinājums! Pirms sterilizācijas rūpīgi notīriet no ierīces netīrumus.
93
Latviski
Page 94

Brīdinājums! Neizmantojiet tīrītājus uz šķīdinātāja bāzes (piemēram, acetonu vai
toluolu).
• Pirms jebkāda veida tīrīšanas piesārņotās ierīces nedrīkst nožūt.
• Atkārtoti apstrādājiet ierīces divu stundu laikā pēc to lietošanas. Ja
pārvietošana uz apstrādes vietu aizkavēsies, ievietojiet ierīci slēgtā konteinerā
ar fermentu tīrīšanas līdzekli, lai ierīce neizžūtu.
• Ja ierīcei ir vairākas sastāvdaļas, pirms tās tīrīšanas saskaņā ar šiem lietošanas
norādījumiem, pilnībā atvienojiet sastāvdaļas.
• Pirms lietošanas pārbaudiet, vai ierīcei nav plaisu vai bojājumu. Ja sastāvdaļām
ir redzamas plaisas vai bojājumi, nelietojiet ierīci.
• Tā kā ierīces tiek termiski sterilizētas, termiskā dezinfekcija nav nepieciešama.
5.1.1 Manuāla tīrīšana
Uzņēmums Medtronic sadaļā 1. tabulu ir noteicis tālāk aprakstīto manuālās
tīrīšanas procedūru. Šīs darbības ir jāveic ne vēlāk kā divu stundu laikā pēc
lietošanas.
Piezīme: Ja ierīcei ir kustīgas detaļas, gādājiet, lai visas virsmas tiktu kārtīgi
notīrītas.
1. tabula. Manuālās tīrīšanas norādījumi Dar-
bība Process Temperatūra Tīrīšanas norādījumi
1 Skalošana >27 °C (>81 °F) Notīriet lielākos netīrumus, skalojot ar
2 Mērcē-
šana
3 Tīrīšana ar
ultraskaņu
4 Skalošana >27 °C (>81 °F) 1 min skalojiet ierīci ar tekošu ūdeni.
5 Žāvēšana Nav attiecināms Nosusiniet ar tīru bezplūksnu drānu.
6 Pārbaude Nav attiecināms Apskatot pārbaudiet katru ierīci, vai uz
5.1.2 Automātiskā tīrīšana
Uzņēmums Medtronic ir noteicis tālāk aprakstīto automātiskās tīrīšanas procedūru.
Šīs darbības 2. tabulu jāveic ne vēlāk kā divas stundas pēc lietošanas.
Piezīme: Ja ierīcei vai komponentam ir noņemamas sastāvdaļas, gādājiet, lai visas
virsmas tiktu kārtīgi notīrītas.
>28 °C (>82 °F) Pilnībā iegremdējiet ierīci vismaz 5 min
>27 °C (>81 °F) Pilnībā iegremdējiet ierīci ultraskaņas
tekošu ūdeni 1 min. Izmantojiet suku ar
mīkstiem sariem (piemēram, zobu birsti ar neilona sariem), lai rūpīgi notīrītu
ierīci.
15,6 mL/1 L (vai 2 unces/1 galonu) fermentu mazgāšanas līdzekļa (piemēram, ENZOL™) un ūdens šķīdumā. Ar
mīkstu saru suku notīriet redzamos
netīrumus.
tīrītājā (piemēram, Bransonic™),
izmantojot 7,8 mL/1 L (vai 1 unci/1
galonu) fermentu mazgāšanas līdzekļa
(piemēram, ENZOL) un ūdens šķīdumu. 10 min apstrādājiet ar ultraskaņu.
tās nav palikuši netīrumi vai mitrums. Ja
ir redzami netīrumi, atkārtojiet procesu.
Latviski
94
Page 95

2. tabula. Norādījumi pirms procedūras Dar-
bība Process
1 Skalošana >25 °C (>77 °F) Notīriet lielāko netīrumu daļu,
2 Mērcē-
šana
3 Skalošana >25 °C (>77 °F) Skalojiet ierīci vismaz 2 min.
4 Pārbaude Nav attiecināms Apskatiet, vai uz ierīces nav palikuši
Automatizētās tīrīšanās procesa pārbaudē uzņēmums Medtronic izmantoja
Prolystica™ tīrītājus, ievērojot ražotāja norādījumus. Apstrādātājs ir atbildīgs, lai
apstrāde tiktu veikta saskaņā ar apstiprināto metodi. Jebkāda apstrādātāja darbību
novire no tālāk norādītajām instrukcijām ir jāizvērtē.
1. Ievietojiet ierīci automātiskajā mazgātājā (piemēram, Steris Reliance™
Genfore™ mazgātājs/dezinficētājs).
Piezīme: Ievietojot ierīces mazgāšanas ierīcē, nepieļaujiet, ka ierīces
saskaras.
2. Iestatiet, lai automātiskais mazgātājs darbojas ar parametriem, kas noteikti
3. tabulu, un ļaujiet mazgātājam veikt mazgāšanas ciklu.
3. tabula. Automātiskā mazgātāja tīrīšanas parametri
Apstrāde
Enzīmu mazgāšanas līdz-
eklis
Mazgāšana 02:00 ≥60 °C
Skalošana 02:00 ≥60 °C
Žāvēšana 15:00 ≥82 °C
Pārbaude Nav
Ūdens tempera-
tūra Tīrīšanas norādījumi
>25 °C (>77 °F) Vismaz 1 min pilnībā iegremdējiet
Laiks
(min) Temperatūra Tīrīšanas līdzeklis
04:00 ≥60 °C
attieci-
nāms
(≥140 °F)
(≥140 °F)
(≥140 °F)
(≥180 °F)
Nav attieci-
nāms
izmantojot tekošu krāna ūdeni.
ierīci 7,8 mL/1 L (vai 1 unci/1 galona)
fermentu mazgāšanas līdzekļa (piemēram, ENZOL) un ūdens šķīdumā.
Ar mīkstu saru suku (piemēram, ar
neilona zobu birsti), notīriet redzamos netīrumus.
netīrumi. Ja nepieciešams, atkārtojiet procesu.
Koncentrēts fermentu mazgāšanas
līdzeklis Steris Prolystica™ Ultra
Concentrate, kas atšķaidīts attiecībā
1,0 mL/1 L (vai 0,125 unces/1
galons).
Koncentrēts neitrāls mazgāšanas
līdzeklis Steris Prolystica™ Ultra
Concentrate, kas atšķaidīts attiecībā
1,0 mL/1 L (vai 0,125 unces/1
galons).
Nav attiecināms
Nav attiecināms
Apskatot pārbaudiet katru ierīci, vai
uz tās nav palikuši netīrumi vai
mitrums. Ja ir redzami netīrumi, atkārtojiet procesu. Ja nepieciešams,
nožāvējiet ierīci ar filtrētu, saspiestu
gaisu vai bezplūksnu drānu.
95 Latviski
Page 96

5.2 Sterilizēšana ar tvaiku un atkārtota sterilizēšana
• Lietojiet parasto iepakojuma materiālu. Nodrošiniet, ka iepakojums būtu
pietiekami liels ierīces ievietošanai, nenospriegojot blīvējumu. Pārbaudot
sterilizēšanas procesu, Medtronic katrai ierīcei izmantoja atbilstošu piederumu
paplāti.
• Medtronic pārbaudīja tvaika ciklus, ierīces ietinot CSR (Central Supply
Room — centrālā apgādes telpa) ietinamajā materiālā. Taču sterilizēšanu ar
tvaiku var veikt gan neiepakotām ierīcēm, gan tādām, kas ietītas tvaika
sterilizēšanai piemērotos materiālos.
• Ja autoklāva apstrādes 1 ciklā tiek sterilizētas vairākas ierīces, nepārsniedziet
sterilizatora maksimālo slodzi.
• Pirms lietošanas pārbaudiet, vai ierīcei nav plaisu vai bojājumu. Ja sastāvdaļām
ir redzamas plaisas vai bojājumi, nelietojiet ierīci.
• Dažas veselības aizsardzības iestādes ārpus ASV iesaka sterilizācijas cikla
parametrus, kas samazina iespējamo Kreicfelda-Jakoba slimības izplatīšanas
risku. Tas īpaši attiecas uz ķirurģiskajiem instrumentiem, kas var nonākt
saskarē ar centrālo nervu sistēmu.
4. tabula. Sterilizācijas cikla parametri
Cikla veids
Temperatūra 132 °C (270 °F) 135 °C (275 °F) 134 °C (273 °F)
Apstrādes laiks 4 min 3 min 18 min
Žāvēšanas
ilgums
a
Uzņēmums Medtronic iesaka sadedzināt ierīces, kas bijušas tiešā saskarē ar pacientiem ar
apstiprinātu transmisīvās sūkļveida encefalopātijas (TSE)/Kreicfelda-Jakoba slimības
diagnozi vai tādiem, kam tā varētu tikt apstiprināta. NHS Estates HTM 2010 Parts 4 & 6:
Appendix 2, Items contaminated with TSE Agents un WHO Infection Control Guidelines for
Transmissible Spongiform Encephalopathies attiecas uz TSE dekontaminācijas ciklu,
izmantojot viena 18 min cikla vai vairāku ciklu ar kopumā 18 min (piemēram, sešu 3 min ciklu)
apstrādi tvaika autoklāvā ar temperatūru no 134 °C līdz 137 °C (no 273 °F līdz 279 °F) .
b
Minimālie žāvēšanas laiki tika apstiprināti, izmantojot sterilizatorus ar vakuuma žāvēšanas
funkcionalitāti. Žāvēšanas cikli, izmantojot apkārtējās vides atmosfēras spiedienu, var prasīt
ilgāku žāvēšanas laiku. Ievērojiet sterilizatora ražotāja ieteikumus.
b
Iepriekšēja
apstrāde ar
vakuumu
(dinamiska
gaisa izvadī-
šana)
Iepriekšēja
apstrāde ar
vakuumu (dina-
miska gaisa
izvadīšana)
Iepriekšēja apstrāde ar
vakuumu (dinamiska
gaisa izvadīšana)
Kreicfelda-Jakoba sli-
mības gadījumā
20 min 16 min 30 min
a
6 Lietošanas norādījumi
Piezīme: Lāpstiņas ir apzīmētas ar numuru, kas atbilst modeļa numura pēdējam
ciparam. Piemēram: 28603 apzīmē kā “3”; 28606B — kā “6B”. Katra lāpstiņa ir
apzīmēta ar unikālu sērijas numuru.
6.1 Lāpstiņas palīgierīce
1. Piestipriniet lāpstiņas atvilcēja statnei, iebīdot lāpstiņas stiprinājumu atvilcēja
statnes svirā.
2. Noņemiet lāpstiņas, izbīdot lāpstiņas stiprinājumu no atvilcēja statnes sviras.
Latviski
96
Page 97

6.2 LIMA materiāla ieguve
1. Ievietojiet atvilcēju ar pievienotajām LIMA lāpstiņām torakotomijā. Lielajai
LIMA lāpstiņai ar atveri galā jābūt vērstai pret mazās lāpstiņas galvgali.
2. Grieziet atvilcēja rokturi, lai atvērtu atvilcēju un paplašinātu torakotomiju.
3. Pielieciet lielās LIMA lāpstiņas gala atverei augšupvērstu spēku, lai sasvērtu
atvilcēju uz augšu. Šī darbība nodrošinās piekļuvi LIMA un ļaus iegūt
materiālu.
Piezīme: Atvilcējs ir paredzēts atvilcēju sistēmas Rultract™ lietošanai ar
augšupvērstu spriegojumu uz lielo LIMA lāpstiņu. Var tikt izmantoti arī citi
augšupvērsta spriegojuma spēka pielikšanas līdzekļi un paņēmieni.
4. Kad LIMA materiāla ieguve pabeigta, atlaidiet augšupvērsto lielās LIMA
lāpstiņas spriegojumu.
5. Nospiediet atlaišanas sviru, lai aizvērtu atvilcēju.
6. Izņemiet atvilcēju no torakotomijas.
6.3 Vispārēja torakotomijas atvilkšana
1. Piestipriniet torakotomijas lāpstiņas atvilcējam.
2. Ievietojiet atvilcēju torakotomijā.
3. Grieziet atvilcēja rokturi, lai atvērtu atvilcēju un paplašinātu torakotomiju.
4. Pēc procedūras pabeigšanas nospiediet atlaišanas sviru, lai aizvērtu atvilcēju.
5. Izņemiet atvilcēju no torakotomijas.
7 Garantijas atruna (globālā)
LAI ARĪ IZSTRĀDĀJUMS IR KONSTRUĒTS, RAŽOTS UN PIRMS
PĀRDOŠANAS PĀRBAUDĪTS RŪPĪGI UZRAUDZĪTOS APSTĀKĻOS, ŠIS
IZSTRĀDĀJUMS VAR NEPILDĪT PAREDZĒTO FUNKCIJU DAŽĀDU IEMESLU
DĒĻ. MEDTRONIC NEVAR IETEKMĒT APSTĀKĻUS, KĀDOS ŠIS
IZSTRĀDĀJUMS TIEK LIETOTS. BRĪDINĀJUMI UZ IZSTRĀDĀJUMA
ETIĶETES IETVER PLAŠĀKU INFORMĀCIJU UN IR UZSKATĀMI PAR ŠĪS
GARANTIJAS ATRUNAS NEATŅEMAMU DAĻU. TĀDĒĻ MEDTRONIC
ATSAUC VISAS AR IZSTRĀDĀJUMU SAISTĪTĀS GAN TIEŠĀS, GAN
NETIEŠĀS GARANTIJAS, TOSTARP, BET NE TIKAI, VISAS NETIEŠĀS
GARANTIJAS PAR IERĪCES DERĪGUMU PĀRDOŠANAI VAI PIEMĒROTĪBU
KONKRĒTAM MĒRĶIM. UZŅĒMUMS MEDTRONIC NAV ATBILDĪGS PAR
FIZISKU VAI JURIDISKU PERSONU MEDICĪNISKIEM IZDEVUMIEM VAI PAR
TIEŠIEM, NETIEŠIEM VAI IZRIETOŠIEM ZAUDĒJUMIEM, KAS RADUŠIES
IZSTRĀDĀJUMA LIETOŠANAS LAIKĀ, DEFEKTA, KĻŪMES VAI
DISFUNKCIJAS DĒĻ, NEATKARĪGI NO TĀ, VAI PRASĪBA PAR ŠĀDIEM
ZAUDĒJUMIEM IR IZVIRZĪTA, PAMATOJOTIES UZ GARANTIJU, LĪGUMA
NOTEIKUMIEM, TIESĪBU AKTU NORMĀM VAI CITIEM APSTĀKĻIEM. JA VIEN
PAR TO NAV NOSLĒGTA RAKSTISKA VIENOŠANĀS AR PILNVAROTIEM
MEDTRONIC DARBINIEKIEM, NEVIENAI PERSONAI NAV TIESĪBU SAISTĪT
MEDTRONIC AR JEBKĀDU PĀRSTĀVNIECĪBU VAI GARANTIJU ATTIECĪBĀ
UZ ŠO IZSTRĀDĀJUMU.
Iepriekš izklāstītie izņēmumi un ierobežojumi ir obligāti interpretējami spēkā esošo
tiesību aktu obligāto normu ietvaros. Ja kādas kompetentas jurisdikcijas tiesa
nosaka, ka šīs garantijas atrunas kāda daļa vai nosacījums ir pretlikumīgs,
nepiemērojams vai pretrunā ar spēkā esošu likumu, pārējo garantijas atrunas daļu
spēkā esamība netiek ietekmēta un visas tiesības un pienākumi jāinterpretē un
jāpiemēro tā, it kā šī garantijas atruna neietvertu attiecīgo daļu vai nosacījumu, kurš
tika atzīts par spēkā neesošu.
97
Latviski
Page 98

1 Productbeschrijving
Model Beschrijving
28610 MICS-wondspreidingssysteem
28611 Wondspreider
28601 LIMA-bladen, standaard
28602 LIMA-bladen, diep
28603 Lange thoracotomiebladen, standaard
28604 Lange thoracotomiebladen, diep
28604B Laag-grijpend, lang blad met verlengd montagestuk, stan-
28605 Korte thoracotomiebladen, standaard
28606 Korte thoracotomiebladen, diep
28606B Laag-grijpend, kort blad met verlengd montagestuk, stan-
Opmerking: Model 28601 is het meest gebruikelijke blad voor LIMA (left internal
mammary artery) -preparatie. Model 28605 is het meest gebruikelijke blad voor
algemene thoracotomiespreiding. Alle andere bladen zijn ontworpen voor diverse
patiëntanatomieën.
Opmerking: Modellen 28604B en 28606B zijn laag-grijpende bladen ontworpen
voor vrouwen en patiënten met overgewicht. Deze dienen te worden gebruikt met
de hoog-grijpende bladen (Modellen 28604 en 28606).
daard
daard
2 Indicaties voor gebruik
Met het ThoraTrak minimaal invasieve cardiochirurgie
(MICS) -wondspreidingssysteem kunt u t.b.v. minimaal invasieve cardiothoracale
ingrepen, inclusief minimaal invasieve coronaire-bypassgraftingprocedures
(CABG) en preparatie van de LIMA, zowel zacht als benig weefsel spreiden om
toegang te krijgen tot het operatiegebied.
3 Voorzorgsmaatregelen
De juiste chirurgische procedures en technieken vallen onder de
verantwoordelijkheid van de arts. De chirurg dient de geschiktheid van procedures
te evalueren op basis van zijn of haar medische opleiding en ervaring.
4 Bijwerkingen
Geen bekend.
5 Verwerking en herverwerking
Medtronic heeft de volgende instructies voor het voorbereiden van dit medische
product voor hergebruik gevalideerd. Het blijft de verantwoordelijkheid van de
verwerker om ervoor te zorgen dat het uitgevoerde proces het gewenste resultaat
bewerkstelligt met de apparatuur, materialen en personeel in de
verwerkingsfaciliteit. Bij verwerking is validatie en standaardbewaking vereist. Elke
afwijking van de volgende instructies door de verwerker dient op toepasselijke wijze
te worden geëvalueerd op effectiviteit en mogelijke nadelige gevolgen. Reiniging
kan handmatig of automatisch worden uitgevoerd volgens deze
gebruiksaanwijzing, of een equivalente gevalideerde methode.
Nederlands
98
Page 99

5.1 Reiniging
Waarschuwing: Reinig het product grondig om vuil vóór de sterilisatie te
verwijderen.
Waarschuwing: Gebruik geen op oplosmiddel gebaseerde reinigingsmiddelen
(bijv. aceton of tolueen).
• Laat gecontamineerde producten niet opdrogen voordat er een
reinigingsprocedure wordt toegepast.
• Reinig de producten binnen 2 uur na gebruik. Als het transport naar het
verwerkingsgebied vermoedelijk vertraagd is, plaatst u de producten in een
afgedekte container met een enzymatisch reinigingsmiddel om te voorkomen
dat ze opdrogen.
• Als het product uit meerdere onderdelen bestaat, moeten deze onderdelen
voorafgaand aan de reiniging volgens deze gebruiksaanwijzing volledig
worden gedemonteerd.
• Inspecteer het product vóór gebruik op barsten of aantasting. Gebruik het
product niet bij zichtbare barsten of aantasting van een van de onderdelen.
• Thermische desinfectie is niet vereist aangezien de producten in de
eindverpakking gesteriliseerd zijn.
5.1.1 Handmatige reiniging
Medtronic heeft de volgende procedure voor handmatige reiniging in Tabel 1
opgesteld. Deze stappen moeten binnen maximaal 2 uur na gebruik worden
uitgevoerd.
Opmerking: Als het product beweegbare delen heeft, zorg er dan voor dat alle
oppervlakken grondig zijn gereinigd.
Tabel 1. Instructies voor handmatige reiniging
Stap Proces Temperatuur Reinigingsinstructies
1 Spoelen > 27 °C (> 81 °F) Spoel ernstig vuil gedurende 1 min af
2 Weken > 28 °C (> 82 °F) Dompel het product minimaal 5 min vol-
3 Ultrasone
reiniging
4 Spoelen > 27 °C (> 81 °F) Spoel het product gedurende 1 min met
> 27 °C (> 81 °F) Dompel het product volledig onder in
met stromend leidingwater. Gebruik
een zachte borstel (bijvoorbeeld een
nylon tandenborstel) om het product
grondig te reinigen.
ledig onder in een enzymatisch reinigingsmiddel (bijv. ENZOL™) en water
in de verhouding 15,6 mL/1 L (of 2
oz/1 gallon). Verwijder zichtbaar vuil
met een zachte borstel.
een ultrasone reiniger (bijv. de
Bransonic™) met een enzymatisch reinigingsmiddel (bijv. ENZOL) en water
in de verhouding 7,8 mL/1 L (of 1
oz/1 gallon). Pas gedurende 10 min
sonicatie toe.
stromend water.
99 Nederlands
Page 100

Tabel 1. Instructies voor handmatige reiniging (vervolg)
Stap Proces Temperatuur Reinigingsinstructies
5 Drogen N.v.t. Afdrogen met een schone, pluisvrije
6 Controle N.v.t. Controleer elk product visueel op even-
5.1.2 Automatisch reinigen
Medtronic heeft de volgende procedure voor automatische reiniging opgesteld. De
stappen in Tabel 2 moeten binnen maximaal 2 uur na gebruik worden uitgevoerd.
Opmerking: Als het product of onderdeel beweegbare delen heeft, zorg er dan
voor dat alle oppervlakken grondig zijn gereinigd.
Tabel 2. Voorbehandelingsinstructies
Stap Proces Watertemperatuur Reinigingsinstructies
1 Spoelen > 25 °C (> 77 °F) Verwijder ernstig vuil met stromend
2 Weken > 25 °C (> 77 °F) Dompel het product minimaal 1 min
3 Spoelen > 25 °C (> 77 °F) Spoel het product gedurende mini-
4 Controle N.v.t. Controleer het product visueel op
Medtronic gebruikte de reinigingsapparaten uit de Prolystica™-serie volgens de
aanbevelingen van de fabrikant om het automatische reinigingsproces te valideren.
Het is de verantwoordelijkheid van de verwerker om ervoor te zorgen dat de
verwerking ten behoeve van hergebruik volgens een gevalideerde methode wordt
uitgevoerd. Elke afwijking van deze aanbevelingen door de verwerker dient te
worden geëvalueerd.
1. Plaats de producten in een automatische wasautomaat (bijv. de Steris
Reliance™ Genfore™-wasautomaat/desinfector).
Opmerking: Vermijd contact tussen de producten wanneer u de wasautomaat
vult.
2. Stel de automatische wasmachine in volgens de parameters in Tabel 3 en laat
het apparaat de wascyclus volledig voltooien.
doek.
tuele resten vuil of vocht. Bij zichtbaar
vuil herhaalt u het proces.
kraanwater.
volledig onder in een enzymatisch
reinigingsmiddel (bijv. ENZOL) en
water in de verhouding 7,8 mL/1 L
(of 1 oz/1 gallon). Verwijder zichtbaar vuil met een zachte borstel (bijvoorbeeld een nylon tandenborstel).
maal 2 min.
eventuele resten vuil. Herhaal zo
nodig het proces.
Nederlands
100
 Loading...
Loading...