
N.º
Número de catálogo
Especs.
1
CG2701
1 teste por kit
2
CG2705
5 testes por kit
3
CG2710
10 testes por kit
4
CG2725
25 testes por kit
5
CG2750
50 testes por kit
Especs.
Aplicação:
Informações sobre o
descartável:
4,7 mm
Cotonete nasal
Solução de tratamento
amostral
Opção A
Opção B
1 teste / kit
1 test 1 300 μL ×1
300 μL ×1
1 peça
5 testes / kit
5 tests 1 1 mL ×1
300 μL ×5
5 peças
300 μL
×10
300 μL
×25
300 μL
×50
Remova a camada de cobertura do
Insira a cabeça do cotonete dentro da
tratamento de amostra.
Vire a área esquerda de cabeça para
cronometrar.
Aguarde o aparecimento de uma faixa
minutos.
SARS-CoV-2 Kit de teste rápido de antígeno
(Imunocromatografia de Ouro Coloidal)
PT
[Especificações de embalagem]
1 teste por kit, 5 testes por kit, 10 testes por kit, 25 testes por kit, 50 testes por kit
[Nome do Produto]
Nome genérico: SARS-CoV-2 Kit de teste rápido de antígeno (Imunocromatografia
de ouro coloidal)
[Uso pretendido]
Este produto é usado para detectar qualitativamente os antígenos do novo
coronavírus (SARS-CoV-2) em amostras clínicas (cotonetes nasais e cotonetes
nasofaríngeos).
[Introdução] O coronavírus, como uma ampla família de vírus, é um vírus de vertente única mais
RNA com um envelope. O vírus é conhecido por causar grandes doenças como
resfriado, Síndrome Respiratória do Oriente Médio (MERS) e Síndrome
Respiratória Aguda Grave (SRAG). A proteína do núcleo de SARS-CoV-2 é a
proteína de N (Nucleocapsídeo), que é um componente proteico dentro do vírus. É
relativamente conservador entre β-coronavírus e é usado geralmente como uma
ferramenta diagnóstica para o coronavírus. Como receptor-chave para
SARS-CoV-2 entrar nas células, o ACE2 é significativo para o estudo de
mecanismos de infecção viral.
[Princípio]
O kit de teste atual baseia-se em reação específica de anticorpos-antígenos e na
técnica de imunoensaio. O cartão de teste contém um anticorpo monoclonal com
proteína N do novo coronavírus com rótulo dourado, pré-revestido na almofada de
ligação e um anticorpo monoclonal com proteína N do novo coronavírus
emparelhado, fixado na linha de teste (T) e anticorpos correspondentes na linha de
controle de qualidade (C).
Durante o teste, a proteína N na amostra se liga ao novo anticorpo da proteína N do
coronavírus marcado com um dourado pré-revestido na almofada de ligação e o
conjugado se move para cima sob o efeito capilar e, em seguida, é capturado pelo
conjugado do anticorpo monoclonal da proteína N fixada na Linha de Teste (T).
Quanto maior o teor de proteína N na amostra, mais conjugados são capturados e
mais escura é a cor da Linha de Teste (T). Caso não haja o novo coronavírus na
amostra ou o conteúdo do vírus esteja abaixo do limite de detecção, não aparece
nenhuma cor na Linha de Teste (T). Uma faixa vermelho arroxeada na Linha de
Controle (C), independentemente de haver ou não vírus na amostra. A faixa
vermelho arroxeada que aparece na Linha de Controle (C) é o critério para
determinar se há ou não amostra suficiente e se o processo de cromatografia está
normal.
[Componentes Principais]
O produto inclui cartões, manual de instruções, cotonetes e solução de tratamento de amostra Cada kit reagente contém 1 cartão de teste de antígeno do novo coronavírus (SARS-CoV-2) e uma bolsa de dessecante.
Informações sobre o cotonete esterilizado descartável:
O cotonete nasal ou o cotonete nasofaríngeo podem ser fornecidos com base na
necessidade do cliente.
cotonete esterilizado
3,0 mm Cotonete Nasofaríngeo
0123 MDD 93/42/EEC Fabricante 1: Zhejiang Gongdong Medical Technology Co., Ltd. Área Industrial de Beicheng 318020 Huangyan China
0197 MDD 93/42/EEC Fabricante 2: Jiangsu Changfeng Medical Industry Co., Ltd. Cidade de Touqiao,Distrito de Guangling, Yangzhou 225109 Jiangsu China
0197 MDD 93/42/EEC Fabricante 3: Shenzhen KangDaAn Biological Technology Co., Ltd. Zona industrial de Liuxiandong, Rua Xili, Distrito de Nanshan, Shenzhen 518055 Guangdong China
0413 MDD 93/42/EEC Fabricante 4: Medico Technology Co., Ltd. Parque Industrial de Zhangbei, Rua Longcheng, Distrito de Longgang, Shenzhen, 518100 Guangdong, China
0197 MDD 93/42/EEC Fabricante 5: Goodwood Medical Care Ltd. 1º-2º Andar, 3-919, Rua Yongzheng, Distrito de Jinzhou, Dalian 116100 Liaoning, China
Especificação.
10 testes / kit 10 tests 1 2 mL ×1
25 testes / kit 25 tests 1 3 mL ×2
50 testes / kit 50 tests 1 5 mL ×2
Cartão
de teste
Manual
O cartão de teste consiste em uma almofada rotulada com ouro (pulverizada com
ouro coloidal anticorpo monoclonal de proteína N coloidal SARS-CoV-2),
almofada da amostra, membrana de nitrocelulose (T revestida com anticorpo
monoclonal de proteína N SARS-CoV-2 N; Linha C revestida com anticorpo de
anti-cabra e anti-rato), papel absorvente e cartão rígido hidrofóbico.
[Condições de armazenamento e período de validade]
Armazenado em local seco e escuro com temperatura ambiente de 4-30°C, válido
por 18 meses.
O prazo de validade do cartão de teste (1 teste) é de 1 hora após a abertura do pacote
interno.
Veja no rótulo da embalagem a data de fabricação e validade do material.
[Espécime Requisitos]
Este kit de teste é adequado para testar amostras de cotonete nasal humanas ou
amostras de cotonete nasofaríngeo:
1 / 2
Cotonetes
10 peças
25 peças
50 peças
Coleta de amostras: Durante o processo de coleta, o pessoal relevante deve estar
bem protegido para evitar contato direto com a amostra. Em caso de contato
acidental, deve ser realizada desinfecção oportuna e devem ser tomadas medidas
necessárias.
Coleta de amostras do cotonete nasal: Durante a amostragem, a cabeça do cotonete
nasal deve ser totalmente inserida na cavidade nasal e girada suavemente 5 vezes.
Quando for removido, a amostra deve ser levada da mesma forma na outra
cavidade nasal para garantir a coleta de amostras suficientes.
Coleta de espécimes do cotonete nasofaríngeo: Durante a amostragem, incline a
cabeça do paciente ligeiramente para trás cerca de 45-70 graus. A cabeça do
cotonete nasofaríngeo deve ser inserida a partir da narina, atingir uma profundidade
igual à distância das narinas até a abertura externa da orelha, girada suavemente 5
vezes e mantenha o cotonete no local por 3 segundos para absorver as secreções.
Após a amostragem, remova lentamente o cotonete enquanto o gira.
Preservação da amostra: Depois que a amostra for coletada, por favor, complete o
teste dentro de 1 hora.
A amostra deve ser testada após o retorno à temperatura ambiente.
[Método de Teste]
Você deve ler o manual de instruções completamente antes de realizar
qualquer teste, e usar os reagentes e espécimes depois de retornar à
temperatura ambiente.
1. Consulte o procedimento padrão de coleta de espécimes em cotonete nasal ou
nasofaríngeo para coletar a amostra.
2. Remova a camada de cobertura do adesivo de dupla face para evitar o respingo
do líquido antes de adicionar o líquido ao kit de teste.
3. Insira a cabeça do cotonete dentro da cavidade A a partir do fundo da cavidade
B, adicione 6 gotas da solução de tratamento de amostra e gire-a em sentido
horário e anti-horário duas vezes na solução de tratamento de amostra.
4. No processo de testagem, o cartão de teste deve ser colocado em uma mesa
horizontal, e não deve ser movido.
5. Vire a área esquerda de cabeça para baixo para que ambos os lados se encaixem
completamente, comece a cronometrar e aguarde pelo aparecimento da faixa
vermelho-púrpura. Os resultados dos testes devem ser lidos dentro de 15-20
minutos.
adesivo de dupla face para evitar o
respingo do líquido.
cavidade A a partir do fundo da
cavidade B, adicione 6 gotas da
solução de tratamento de amostra e
gire-a em sentido horário e
anti-horário duas vezes na solução de
baixo para que ambos os lados se
encaixem completamente, comece a
vermelho-púrpura. Os resultados dos
testes devem ser lidos dentro de 15-20
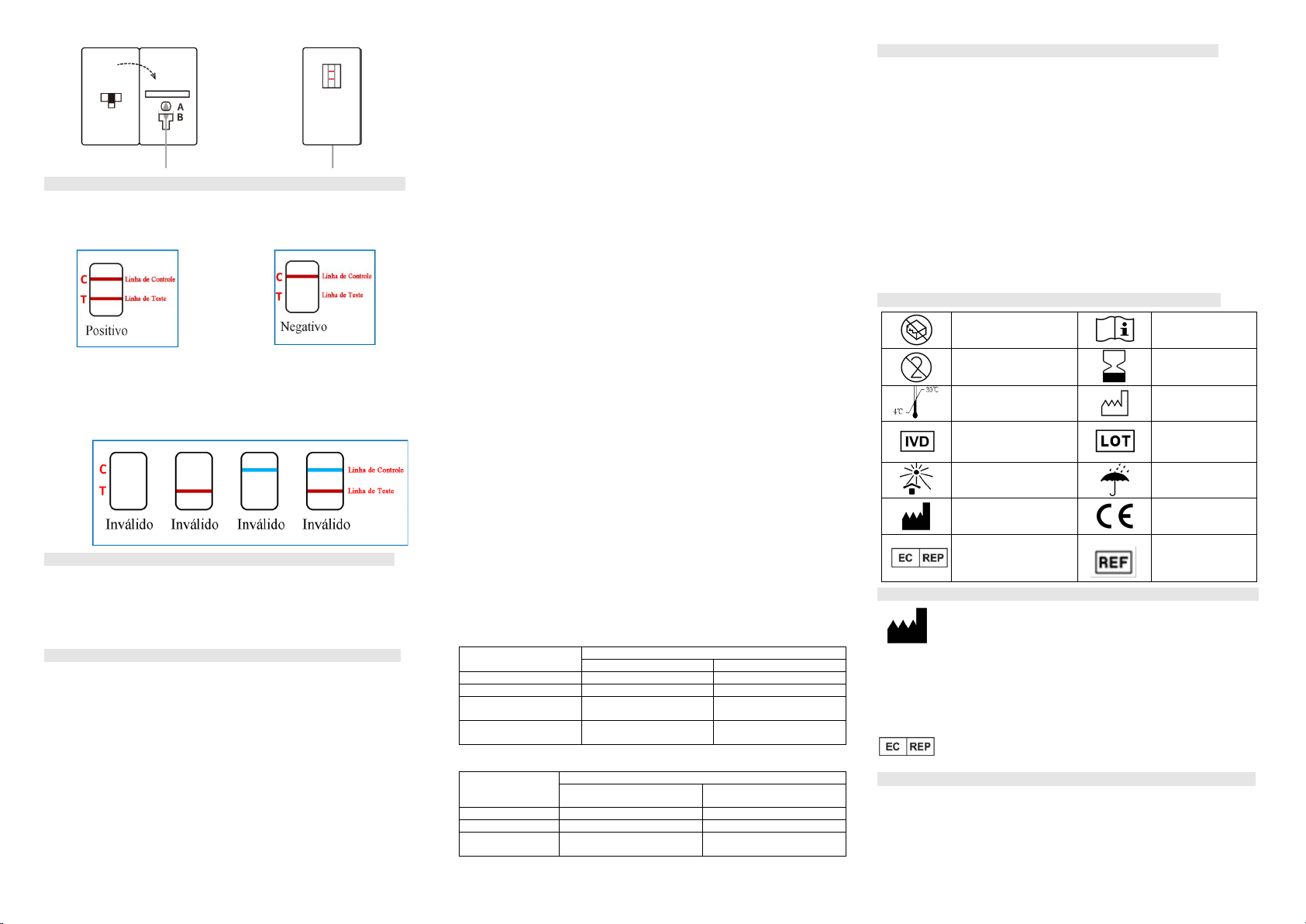
[Explicação dos Resultados dos Testes]
Positivo (+): Uma faixa
de Teste (T).
Negativo (-): Apenas a Linha de Controle
púrpura.
aparece na Linha de Teste (T).
SARS-CoV-2- kit de teste
rápido de antígeno
Ensaio de ácido nucleico (PCR)
Positivo
Negativo
Positivo
231
1
Negativo
12
264
95,06%
(IC95%: 91,57%~97,15%)
99,62%
(IC95%: 97,89%~99,93%)
SARS-CoV-2- kit de
antígeno
Ensaio de ácido nucleico (PCR)
Positivo
227
202
Negativo 8 3
96,60%
(IC95%: 93,43%~98,27%)
98,54%
(IC95%: 95,79% ~ 99,50%)
NÃO UTILIZE SE
DANIFICADO
CONSULTAR
USO
DISPOSITIVO PARA
VITRO
REPRESENTANTE
EUROPEIA
vermelho-púrpura aparece na
Linha de Controle (C) e na Linha
(C) mostra uma faixa vermelhoNenhuma faixa vermelho-púrpura
Inválido: Se "nenhuma faixa vermelho-púrpura aparecer na Linha de Controle
(C)" e "uma faixa azul aparecer na Linha de Controle (C)", isso indica que o
processo de operação está incorreto ou o papel de teste foi danificado. Neste
caso, leia cuidadosamente o manual de instruções novamente e teste novamente
com um novo papel de teste. Se o problema persistir, pare de usar este lote de
produtos imediatamente e entre em contato com seu fornecedor local.
[Limitações do método de teste]
1. Os resultados de teste deste produto devem ser combinados com outras
informações clínicas e avaliada de forma abrangente por médicos, e não
devem ser usados como único critério.
2. Este produto é usado apenas para determinar o novo coronavírus
(SARS-CoV-2) antígeno na amostra.
[Índice de Desempenho do Produto]
1. Descrição
1.1 Aparência
O cartão de teste deve estar limpo e completo, livre de saliências, danos e contaminação; o material deve ser firmemente anexado; o rótulo deve ser legível e sem danos. O tampão de amostra deve ser claro e transparente, livre de impurezas e flóculos.
1.2 Velocidade de migração líquida
A velocidade de migração líquida não deve ser inferior a 10 mm/min.
1.3 Largura da tira de película
A largura da tira de película do cartão de teste é de ≥ 2,5 mm.
1.4 Volume da solução de tratamento de amostra
O volume da solução de tratamento de amostra não é inferior ao valor da etiqueta.
2. Limite de Detecção
2.1 Determinação do Limite de Detecção
Através da diluição gradiente da proteína N recombinante SARS-CoV-2, o
resultado mostrou que a taxa positiva estava entre 90% e 95% abaixo de 1/ (2×10
de condição de diluição, assim, a razão de diluição do menor limite de detecção foi
finalmente determinada como sendo 1/ (2×10
6
), e a concentração de proteína N
recombinante correspondente de SARS-CoV-2 foi de cerca de 1ng/ml através do
cálculo. A concentração do vírus LOD é de 200TCID50/ml.
2.2 Verificação do Limite de Detecção
Detectar a substância de referência de sensibilidade e a taxa positiva não deve ser inferior a 90%.
3. Taxa de conformidade da substância de referência negativa
Teste a substância de referência negativa da empresa e a taxa negativa deve ser de 100%.
4. Taxa de conformidade da substância de referência positiva
Teste a substância de referência positiva da empresa e a taxa positiva deve ser de 100%.
5. Repetição
Teste as substâncias de referência repetíveis da empresa, e os resultados devem ser todos positivos e de cor uniforme.
6. Análise da especificidade
6.1 Reação cruzada: Este produto não apresenta reação cruzada com coronavírus
humano endêmico OC43, coronavírus humano endêmico HKU1, coronavírus
humano endêmico NL63, coronavírus humano endêmico 229E,vírus influenza A,
vírus influenza B, vírus sincicial respiratório, adenovírus, vírus Epstein-Barr, vírus
do sarampo, citomegalovírus, rotavírus, norovírus, vírus da caxumba, vírus
varicela-zoster, micoplasma pneumoniae, metapneumovírus, staphylococcus
aureus, staphylococcus epidermidis, pseudomonas aeruginosa, estreptococosa
pneumoniae e alta concentração de proteína N.
6.2 Substâncias interferentes: Quando a concentração de mucina é ≤5mg/mL e
sangue inteiro humano ≤2%, não haverá interferência nos resultados do teste deste
produto; os seguintes medicamentos não têm efeito nos resultados do teste deste
produto sob a concentração da verificação, incluindo o quinino, zanamivir,
ribavirina, oseltamivir, peramivir, lopinavir, ritonavir, arbidol, acetaminofeno,
ácido acetilsalicílico, ibuprofeno, levofloxacina, azithromicina, ceftromicina,
meropenem, tobramicina, cloridrato de histamina, fenilefrina, oximetazolina,
cloreto de sódio (que contêm conservantes), beclometasona, dexametasona,
flunisolida, acetonido de triancinolona, budesonida, mometasona, fluticasona,
Strepsils (flurbiprofeno 8.75mg), e Lozenges (menta).
7. Desempenho clínico
Foram coletadas 508 amostras clínicas baseadas em ensaio de ácido nucleico
(PCR), incluindo 243 amostras positivas e 265 amostras negativas. Após a
comparação deste produto com o ensaio nucleico ácido (PCR) através das amostras
clínicas coletadas, os resultados são resumidos da seguinte forma:
Análise de sensibilidade
Análise da especificidade /
/
Desempenho em relação ao método do comparador - por contagens iniciais de
ciclo.
teste rápido de
Sensibilidade
Positivo (Ct≤32) Positivo (Ct≤25)
[Precauções]
6
)
1. Este cartão de teste só é adequado para profissionais como um auxílio
diagnóstico in vitro. Não utilize produtos vencidos.
2. Não refrigerar ou usar após a data de validade (consulte a embalagem para
verificar a data de validade).
3. Deve-se evitar a temperatura e a umidade do ambiente experimental sejam muito
altas, a temperatura de reação deve ser de 15-30°C e a umidade deve ficar abaixo de
70%.
4. A embalagem contém dessecante, não o use.
5. Ao testar, use roupas de proteção, luvas e óculos.
6. Por favor, não use o cartão de teste com embalagem danificada da sacola do
cartão, marcação incerta ou fora da data de validade.
7. Descarte amostras usadas, cartões de teste e outros resíduos de acordo com as
leis e regulamentos locais relevantes.
8. Um cartão de teste deve ser usado dentro de 1 hora após ser retirado do saco de
papel alumínio.
9. Os usuários devem colher amostras de acordo com o manual de instruções.
10. Remova a camada de cobertura do adesivo de dupla face para evitar o respingo
do líquido antes do teste.
11. Não pingue a solução de tratamento de amostra na cavidade errada
12. No processo de teste, o cartão de teste deve ser colocado em uma mesa
horizontal, e não deve ser movido.
[Explicação dos Símbolos]
O PACOTE ESTIVER
NÃO REUTILIZAR
LIMITE DE
TEMPERATURA
DIAGNÓSTICO IN
MANTER AFASTADO
DA LUZ SOLAR
FABRICANTE:
AUTORIZADO NA
COMUNIDADE
INSTRUÇÕES DE
FABRICANTE
CÓDIGO DO LOTE
LOCAL SECO
MARCAÇÃO CE
[Informação Básica]
Beijing Lepu Medical Technology Co., Ltd.
Andar 3 Edifício 7-1, Nº 37, Estrada Chaoqian, Distrito de Changping,
Pequim, 102200, P.R. China
Andar 5 Edifício 7-1, Nº 37, Estrada Chaoqian, Distrito de Changping,
Pequim, 102200, P.R. China
Tel: +86-10-80123964
E-mail: lepuservice@lepumedical.com
Web: en.lepumedical.com
Lepu Medical (Europa) Cooperatief U.A.
Abe Lenstra Boulevard 36, 8448 JB, Heerenveen, Holanda
Tel: +31-515-573399 Fax: +31-515-760020
[Data de Aprovação e Revisão do Manual]
Aprovado em 24 de agosto de 2021;
Número de versão: CE-CG27-In01-A08
PRAZO DE
VALIDADE
DATA DO
MANTER EM
NÚMERO DE
CATÁLOGO
2 / 2
 Loading...
Loading...